第七单元燃料及其利用测试卷-2021-2022学年九年级化学人教版上册(word 含解析)
文档属性
| 名称 | 第七单元燃料及其利用测试卷-2021-2022学年九年级化学人教版上册(word 含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 88.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-10-28 00:00:00 | ||
图片预览


文档简介
第七单元《燃料及其利用》测试卷
一、单选题(共15小题)
1.下列属于温室气体的是( )
A. H2
B. N2
C. O2
D. CO2
2.两份质量相等的碳,一份与足量的氧气完全反应生成二氧化碳,另一份与氧气反应全部生成一氧化碳,则前者与后者消耗的氧气的质量比为( )
A. 3:4
B. 3:8
C. 2:1
D. 1:2
3.下列关于一氧化碳的说法正确的是( )
A. 一氧化碳既有可燃性,又有还原性
B. 在炉子上放一盆水可以避免一氧化碳中毒
C. 一氧化碳和二氧化碳的化学性质相似
D. 一氧化碳是有刺激性气味的毒气
4.下列不属于二氧化碳用途的是( )
A. 供给呼吸
B. 用于灭火
C. 用作气体肥料
D. 生产碳酸饮料
5.实验室制取CO2有以下步骤:①连接好装置;②向试管中小心放入几小块石灰石;③向试管中小心注入适量稀盐酸;④检查装置的气密性;⑤收集产生的气体;⑥用燃烧的木条检验集气瓶是否收集满CO2,以上操作按由先至后的顺序排列正确的是( )
A. ①②③④⑤⑥
B. ①④②③⑤⑥
C. ①③②④⑤⑥
D. ③①②④⑤⑥
6.臭氧层空洞、酸雨和温室效应是人类所面临的三大环境问题。其中温室效应是因为人类活动的加剧,从而向环境排放了大量的什么气体造成的( )
A. 二氧化硫
B. 二氧化碳
C. 臭氧
D. 一氧化碳
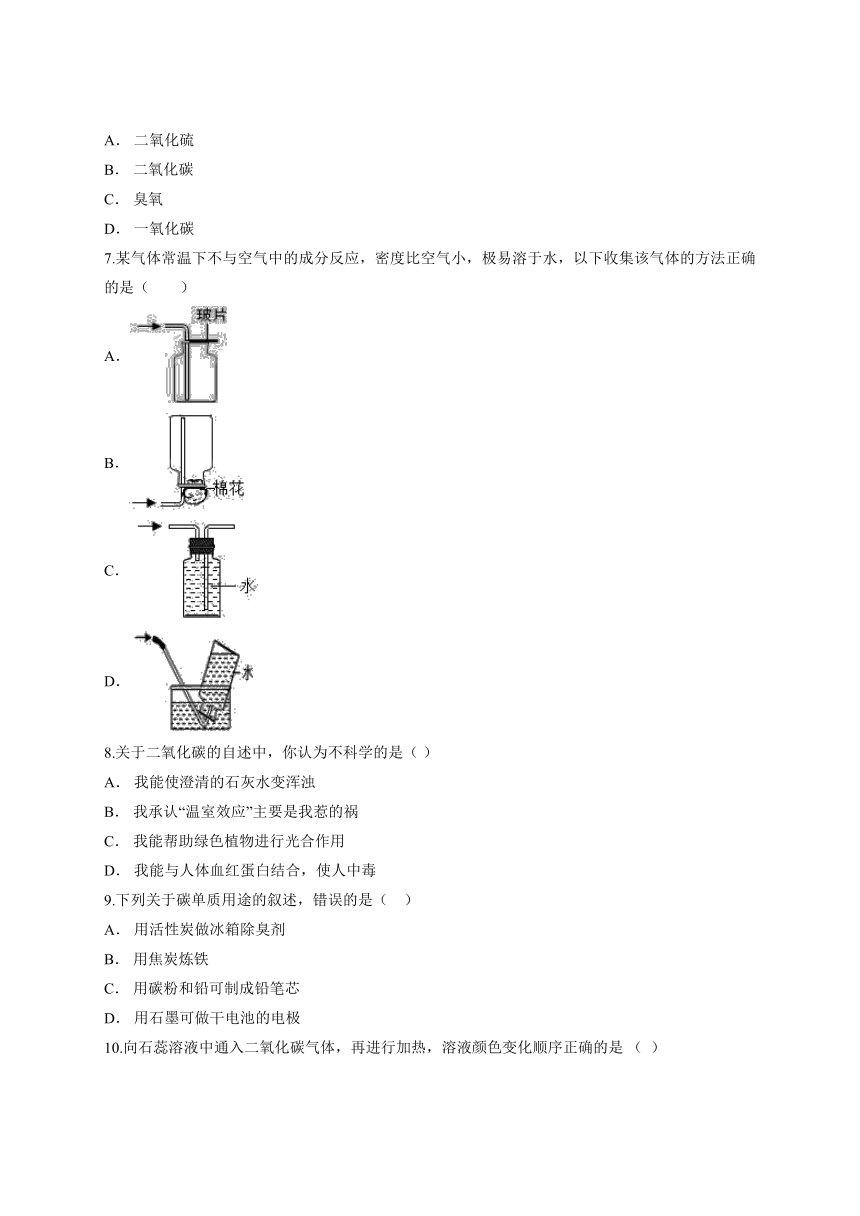
7.某气体常温下不与空气中的成分反应,密度比空气小,极易溶于水,以下收集该气体的方法正确的是( )
A.
B.
C.
D.
8.关于二氧化碳的自述中,你认为不科学的是( )
A. 我能使澄清的石灰水变浑浊
B. 我承认“温室效应”主要是我惹的祸
C. 我能帮助绿色植物进行光合作用
D. 我能与人体血红蛋白结合,使人中毒
9.下列关于碳单质用途的叙述,错误的是( )
A. 用活性炭做冰箱除臭剂
B. 用焦炭炼铁
C. 用碳粉和铅可制成铅笔芯
D. 用石墨可做干电池的电极
10.向石蕊溶液中通入二氧化碳气体,再进行加热,溶液颜色变化顺序正确的是 ( )
A. 红色—紫色—红色
B. 紫色—红色—紫色
C. 红色—紫色—蓝色
D. 红色—无色—红色
11.硅(Si)是现代电子工业的基础。工业上用碳在高温下还原二氧化硅的方法可制得硅,同时还有一氧化碳生成。下列说法正确的是( )
A. 上述反应的化学方程式为SiO2+2CSi+2CO↑
B. 碳发生了还原反应
C. 碳表现氧化性
D. 二氧化硅是还原剂
12.我国“辽宁号”航母甲板上涂有耐高温、耐磨的碳化硅(SiC)涂层,碳化硅的结构类似于金刚石的结构,则构成碳化硅的粒子是( )
A. 分子
B. 原子
C. 离子
D. 中子
13.二氧化碳占空气总体积的0.03%,正常情况下能维持这个含量基本不变是因为自然界存在如图所示的循环过程,图中A处不包括下列哪项( )
A. 发展和利用太阳能
B. 植物的呼吸作用
C. 人和动物的呼吸
D. 含碳燃料的燃烧
14.某班同学在对CO2进行功与过的讨论时,列举的以下事实既可以体现CO2的功,又可以体现CO2的过的是( )
A. CO2可以使人窒息
B. CO2可以作气体肥料
C. CO2可以产生温室效应
D. 固体CO2可用于人工降雨
15.化学家创造出一种物质“干水”,其每个颗粒含水95%,外层是SiO2,干水吸收二氧化碳的能力比普通清水高三倍。下列有关说法正确的是( )
A. 干水和干冰是同一种物质
B. 干水中的水分子不再运动
C. 用干水吸收CO2有助于减缓温室效应
D. 干水吸收CO2的过程只发生物理变化
二、填空题(共3小题)
16.碳在过量氧气中充分燃烧的化学方程式______________,该反应属于_____(填“放热”或“吸热”)反应。
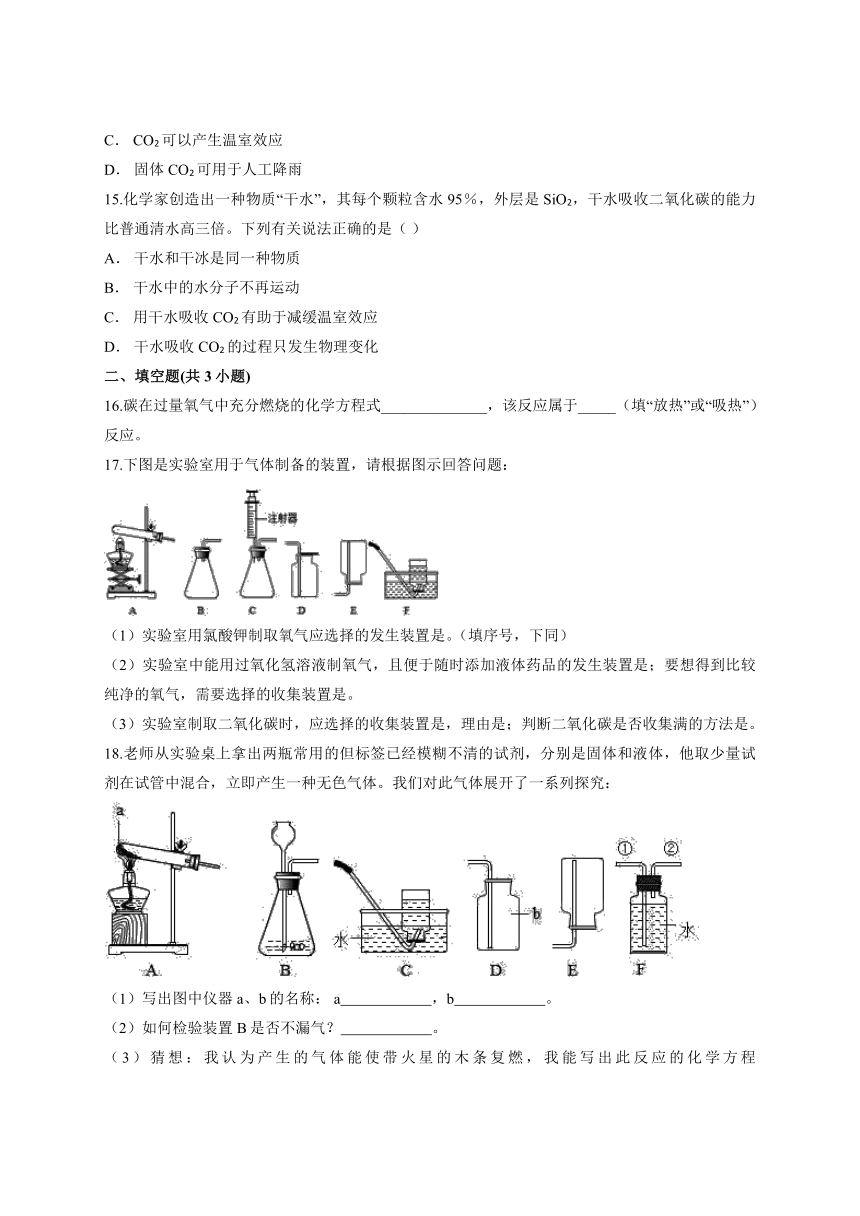
17.下图是实验室用于气体制备的装置,请根据图示回答问题:
(1)实验室用氯酸钾制取氧气应选择的发生装置是。(填序号,下同)
(2)实验室中能用过氧化氢溶液制氧气,且便于随时添加液体药品的发生装置是;要想得到比较纯净的氧气,需要选择的收集装置是。
(3)实验室制取二氧化碳时,应选择的收集装置是,理由是;判断二氧化碳是否收集满的方法是。
18.老师从实验桌上拿出两瓶常用的但标签已经模糊不清的试剂,分别是固体和液体,他取少量试剂在试管中混合,立即产生一种无色气体。我们对此气体展开了一系列探究:
(1)写出图中仪器a、b的名称: a ,b 。
(2)如何检验装置B是否不漏气? 。
(3)猜想:我认为产生的气体能使带火星的木条复燃,我能写出此反应的化学方程式: ,我知道它的反应类型是 。
(4)我想制取该气体,发生装置将选取图中的 (填序号,以下同),收集装置选取
。
(5)如果用如图中的F装置收集该气体,我认为气体应从 端(填“①”或“②”)导入。
(6)我猜想无色气体还可能是另外一种气体,产生它的化学方程式是 。收集装置可选取上图中的 〔填序号〕。
(7)甲烷是一种无色、无味、难溶于水的气体,实验室用加热无水醋酸钠和碱石灰的固体混合物的方法制取甲烷,则实验室制取并收集甲烷应选择的装置组合是 。
三、实验与探究(共3小题)
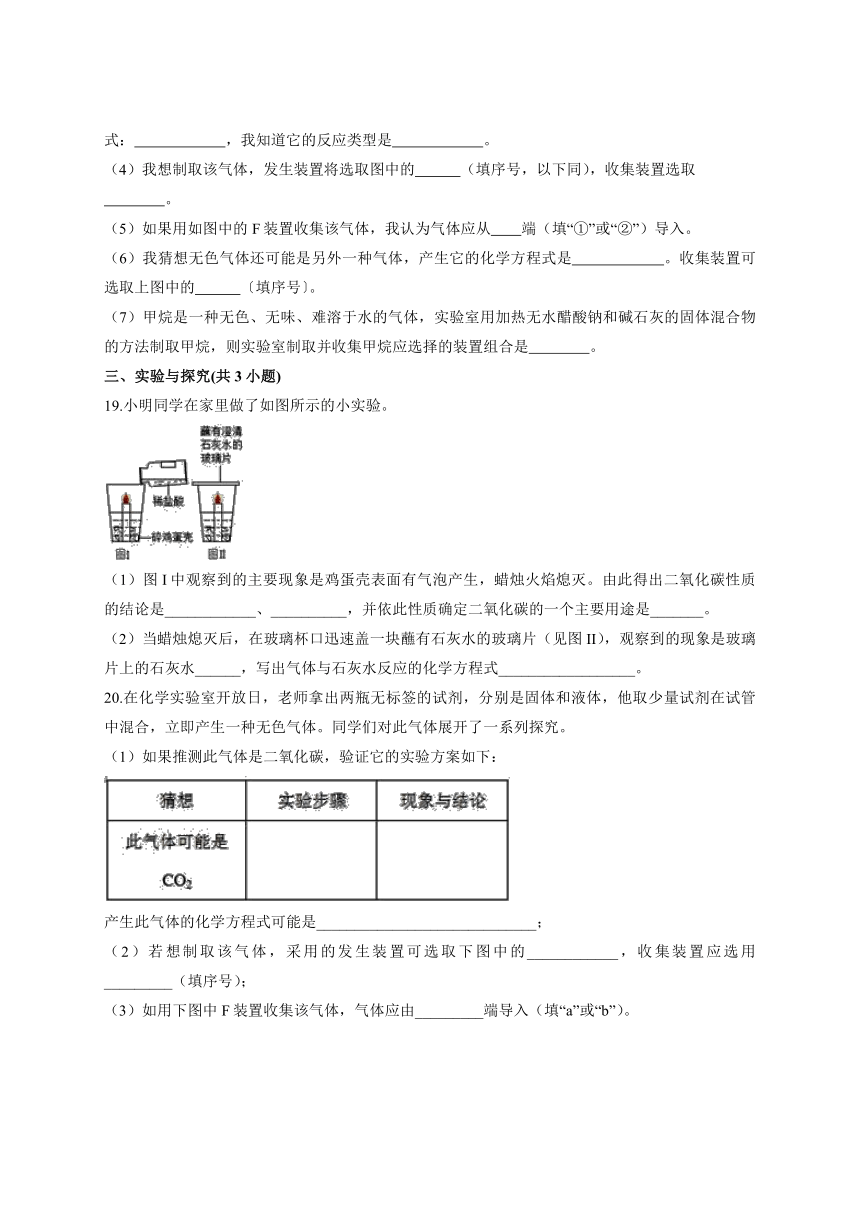
19.小明同学在家里做了如图所示的小实验。
(1)图I中观察到的主要现象是鸡蛋壳表面有气泡产生,蜡烛火焰熄灭。由此得出二氧化碳性质的结论是____________、__________,并依此性质确定二氧化碳的一个主要用途是_______。
(2)当蜡烛熄灭后,在玻璃杯口迅速盖一块蘸有石灰水的玻璃片(见图II),观察到的现象是玻璃片上的石灰水______,写出气体与石灰水反应的化学方程式__________________。
20.在化学实验室开放日,老师拿出两瓶无标签的试剂,分别是固体和液体,他取少量试剂在试管中混合,立即产生一种无色气体。同学们对此气体展开了一系列探究。
(1)如果推测此气体是二氧化碳,验证它的实验方案如下:
产生此气体的化学方程式可能是_____________________________;
(2)若想制取该气体,采用的发生装置可选取下图中的____________,收集装置应选用_________(填序号);
(3)如用下图中F装置收集该气体,气体应由_________端导入(填“a”或“b”)。
21.下图是实验室用碳酸钙与稀盐酸反应制取二氧化碳并验证其性质的的实验装置图,试根据题目要求回答下列问题:
(1)仪器a的名称是;仪器b的名称是;
(2)实验室制取气体时,仪器组装后,加入试剂前必不可少的一项操作是 。装置A中的反应方程式;装置B中的反应化学方程式;装置C中观察到的现象是。装置A还可以制取氧气,化学方程式为。
(3)装置D中观察到的现象是____________,说明二氧化碳的密度比空气大,它不能燃烧,也不能支持燃烧。由此可知,二氧化碳在生活中可用于__________。
(4)实验室用装置E来收集二氧化碳时,二氧化碳应从(填“c端”或“d端”)通入。
答案解析
1.【答案】D
【解析】化石燃料的过度燃烧产生大量的二氧化碳气体排放到空气中形成了温室效应,与氢气、氮气、氧气等无关。
2.【答案】C
【解析】根据碳燃烧的化学方程式可以判断生成二氧化碳消耗的氧气是生成一氧化碳消耗氧气的2倍,其质量比为2:1。
3.【答案】A
【解析】一氧化碳既有可燃性,又有还原性,A说法正确;一氧化碳难溶于水,B说法不正确;一氧化碳和二氧化碳的化学性质不同,C说法不正确;一氧化碳是无色、无味的气体,D说法不正确。
4.【答案】A
【解析】本题主要考查二氧化碳的用途。供给呼吸是氧气的用途,二氧化碳不能供给呼吸。
5.【答案】B
【解析】制取二氧化碳的操作步骤是:连(连接仪器、组装实验装置)→查(检查装置的气密性)→加(加入固体药品)→倒(倒入液体药品)→定(用铁架台固定仪器装置)→收集(用向上排空气法收集)。故正确的操作顺序为:①④②③⑤⑥。
6.【答案】B
【解析】二氧化碳可以防止地表热量辐射到太空中,具有调节地球气温的功能,而温室效应就是由于大气中二氧化碳等气体的含量增加,使全球气温升高的现象。
7.【答案】B
【解析】气体常温下不与空气中的成分反应,密度比空气小,可以采用向下排空气法进行收集,极易溶于水,不能采用排水法进行收集。
8.【答案】D
【解析】二氧化碳无毒,不能与人体的血红蛋白结合,D的自述不正确,其他各项的叙述都是正确的。
9.【答案】C
【解析】活性炭具有吸附性,可用活性炭做冰箱除臭剂;焦炭具有还原性,可以用焦炭冶炼金属;用碳粉和泥土可制成铅笔芯,而不是铅;石墨易导电,可以用石墨做干电池的电极。
10.【答案】B
【解析】二氧化碳能溶于水并与水生成碳酸,使紫色石蕊试液变成红色,碳酸不稳定,加热后分解成二氧化碳与水,试液又由红色变成紫色。
11.【答案】A
【解析】根据提示信息可以判断该反应的化学方程式为SiO2+2CSi+2CO↑,在反应中,碳能夺取二氧化硅中的氧具有还原性,碳是还原剂,发生了氧化反应,所以只有A正确。
12.【答案】B
【解析】金刚石是由碳原子直接构成的,碳化硅的结构类似于金刚石的结构,因此其构成微粒为原子。
13.【答案】A
【解析】由题中图示显示,A处应是消耗氧气,产生二氧化碳,B、C、D都符合这一要求。而发展和利用太阳能既不产生二氧化碳也不消耗氧气。
14.【答案】C
【解析】CO2不支持呼吸,故可以使人窒息,体现了CO2的过;CO2是光合作用的原料,可以作气体肥料,体现了CO2的功;而温室效应可以使全球变暖,使气候反常,这是过,也可提高大棚内的温度,有利于大棚蔬菜的培育,这是功;固体CO2可用于人工降雨,体现了CO2的功。
15.【答案】C
【解析】干冰是固体二氧化碳,由题目信息看出干水是混合物,故两者不是同一种物质;分子都是不停地运动的;干水吸收二氧化碳的能力比普通清水高三倍,故用干水吸收二氧化碳有助于减缓温室效应;由二氧化碳的性质可知,二氧化碳溶于水且部分与水反应生成碳酸,故干水吸收二氧化碳的过程不只发生物理变化。
16.【答案】C + O2CO2放热
【解析】碳在过量氧气中充分燃烧生成二氧化碳,该反应放出大量的热,属于放热反应。
17.【答案】(1)A (2)C F (3)D 二氧化碳能溶于水,密度大于空气 将燃着的木条放在瓶口,木条火焰熄灭,证明已满
【解析】(1)实验室用氯酸钾制取氧气的反应是固体加热,故应用的发生装置是固体加热型装置A。(2)实验室用过氧化氢制取氧气需用固液不加热型装置,同时要控制反应的发生和停止,故选用C装置做发生装置;要制得纯净氧气,需要用排水法收集。(3)实验室制取二氧化碳,因为二氧化碳能溶于水,密度大于空气,故用向上排空气法收集,验满的方法是将燃着的木条放在瓶口,木条熄灭,证明已满。
18.【答案】(1)试管 集气瓶
(2)加水形成液封,先把导管的一端浸入水中,然后两手紧握锥形瓶的外壁,观察导管口有气泡冒出,证明不漏气
(3) 2H2O22H2O+O2↑ 分解反应
(4)B D或C
(5)②
(6)CaCO3+2HCl=CaCl2+H2O+CO2↑ D (合理即可)
(7)AC或AE
【解析】结合实验装置图可以确定a是试管,b是集气瓶;检验装置B气密性的方法是:加水形成液封,先把导管的一端浸入水中,然后两手紧握锥形瓶的外壁,观察导管口有气泡冒出,证明不漏气;用固体与液体制取氧气,是过氧化氢在二氧化锰的催化作用下生成水与氧气,属于分解反应,发生装置选用B装置,可用排水法或向上排空气法收集;实验室制取二氧化碳,是在常温下用大理石或石灰石和稀盐酸制取的,二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;实验室用加热无水醋酸钠和碱石灰的固体混合物的方法制取甲烷,因此需要加热,甲烷是一种无色、无味、难溶于水、密度比空气小的气体,因此能用排水法和向下排空气法收集。
19.【答案】(1)二氧化碳不燃烧也不支持燃烧 密度比空气大 灭火
(2)变浑浊 Ca(OH)2+CO2═CaCO3↓+H2O
【解析】(1)鸡蛋壳的主要成分是碳酸钙,可以与盐酸反应生成二氧化碳气体,而二氧化碳的密度比空气大,二氧化碳不能燃烧也不能支持燃烧,随着反应的进行,二氧化碳逐渐增多,淹没蜡烛,会看到蜡烛熄灭,因此二氧化碳可以用于灭火。(2)生成的二氧化碳气体能与澄清的石灰水反应生成碳酸钙沉淀与水,澄清石灰水变浑浊。
20.【答案】(1)
CaCO3+ 2HCl = CaCl2+ H2O + CO2↑ (2)B E (3)a
【解析】检验二氧化碳的方法是通入澄清的石灰水,如果石灰水变浑浊,可以证明是二氧化碳气体;固体和液体常温下反应生成二氧化碳气体,是石灰石与稀盐酸的反应,发生装置应该选用固液不加热型,应选用B装置,由于二氧化碳能溶于水,且密度比空气大,所以应该选用向上排空气法收集;如果用F装置收集气体,根据二氧化碳的密度大于空气,所以应该从长导管通入。
21.【答案】(1)长颈漏斗 烧杯
(2)检查装置的气密性 CaCO3+2HCl=CaCl2+H2O+CO2↑
Ca(OH)2+CO2=CaCO3↓+H2O 紫色的石蕊试液变红
2H2O22H2O+O2↑
(3)下面的蜡烛比上面的蜡烛先熄灭 灭火
(4)c端
【解析】结合装置图可以判断a是长颈漏斗,b是烧杯;(2)实验室制取气体时,仪器组装后,加入试剂前应先检查装置的气密性,装置A中是碳酸钙与盐酸反应生成氯化钙、水与二氧化碳,装置B中是氢氧化钙与二氧化碳反应生成碳酸钙沉淀与水,生成的二氧化碳通入C中,紫色的石蕊试液变红,用装置A制取氧气时,应该用过氧化氢与二氧化锰;(3)装置D中观察到的现象是下面的蜡烛比上面的蜡烛先熄灭,二氧化碳不燃烧也不支持燃烧,生活中常用于灭火;(4)收集二氧化碳时应该用向上排空气法收集,应该从c通入。
一、单选题(共15小题)
1.下列属于温室气体的是( )
A. H2
B. N2
C. O2
D. CO2
2.两份质量相等的碳,一份与足量的氧气完全反应生成二氧化碳,另一份与氧气反应全部生成一氧化碳,则前者与后者消耗的氧气的质量比为( )
A. 3:4
B. 3:8
C. 2:1
D. 1:2
3.下列关于一氧化碳的说法正确的是( )
A. 一氧化碳既有可燃性,又有还原性
B. 在炉子上放一盆水可以避免一氧化碳中毒
C. 一氧化碳和二氧化碳的化学性质相似
D. 一氧化碳是有刺激性气味的毒气
4.下列不属于二氧化碳用途的是( )
A. 供给呼吸
B. 用于灭火
C. 用作气体肥料
D. 生产碳酸饮料
5.实验室制取CO2有以下步骤:①连接好装置;②向试管中小心放入几小块石灰石;③向试管中小心注入适量稀盐酸;④检查装置的气密性;⑤收集产生的气体;⑥用燃烧的木条检验集气瓶是否收集满CO2,以上操作按由先至后的顺序排列正确的是( )
A. ①②③④⑤⑥
B. ①④②③⑤⑥
C. ①③②④⑤⑥
D. ③①②④⑤⑥
6.臭氧层空洞、酸雨和温室效应是人类所面临的三大环境问题。其中温室效应是因为人类活动的加剧,从而向环境排放了大量的什么气体造成的( )
A. 二氧化硫
B. 二氧化碳
C. 臭氧
D. 一氧化碳
7.某气体常温下不与空气中的成分反应,密度比空气小,极易溶于水,以下收集该气体的方法正确的是( )
A.
B.
C.
D.
8.关于二氧化碳的自述中,你认为不科学的是( )
A. 我能使澄清的石灰水变浑浊
B. 我承认“温室效应”主要是我惹的祸
C. 我能帮助绿色植物进行光合作用
D. 我能与人体血红蛋白结合,使人中毒
9.下列关于碳单质用途的叙述,错误的是( )
A. 用活性炭做冰箱除臭剂
B. 用焦炭炼铁
C. 用碳粉和铅可制成铅笔芯
D. 用石墨可做干电池的电极
10.向石蕊溶液中通入二氧化碳气体,再进行加热,溶液颜色变化顺序正确的是 ( )
A. 红色—紫色—红色
B. 紫色—红色—紫色
C. 红色—紫色—蓝色
D. 红色—无色—红色
11.硅(Si)是现代电子工业的基础。工业上用碳在高温下还原二氧化硅的方法可制得硅,同时还有一氧化碳生成。下列说法正确的是( )
A. 上述反应的化学方程式为SiO2+2CSi+2CO↑
B. 碳发生了还原反应
C. 碳表现氧化性
D. 二氧化硅是还原剂
12.我国“辽宁号”航母甲板上涂有耐高温、耐磨的碳化硅(SiC)涂层,碳化硅的结构类似于金刚石的结构,则构成碳化硅的粒子是( )
A. 分子
B. 原子
C. 离子
D. 中子
13.二氧化碳占空气总体积的0.03%,正常情况下能维持这个含量基本不变是因为自然界存在如图所示的循环过程,图中A处不包括下列哪项( )
A. 发展和利用太阳能
B. 植物的呼吸作用
C. 人和动物的呼吸
D. 含碳燃料的燃烧
14.某班同学在对CO2进行功与过的讨论时,列举的以下事实既可以体现CO2的功,又可以体现CO2的过的是( )
A. CO2可以使人窒息
B. CO2可以作气体肥料
C. CO2可以产生温室效应
D. 固体CO2可用于人工降雨
15.化学家创造出一种物质“干水”,其每个颗粒含水95%,外层是SiO2,干水吸收二氧化碳的能力比普通清水高三倍。下列有关说法正确的是( )
A. 干水和干冰是同一种物质
B. 干水中的水分子不再运动
C. 用干水吸收CO2有助于减缓温室效应
D. 干水吸收CO2的过程只发生物理变化
二、填空题(共3小题)
16.碳在过量氧气中充分燃烧的化学方程式______________,该反应属于_____(填“放热”或“吸热”)反应。
17.下图是实验室用于气体制备的装置,请根据图示回答问题:
(1)实验室用氯酸钾制取氧气应选择的发生装置是。(填序号,下同)
(2)实验室中能用过氧化氢溶液制氧气,且便于随时添加液体药品的发生装置是;要想得到比较纯净的氧气,需要选择的收集装置是。
(3)实验室制取二氧化碳时,应选择的收集装置是,理由是;判断二氧化碳是否收集满的方法是。
18.老师从实验桌上拿出两瓶常用的但标签已经模糊不清的试剂,分别是固体和液体,他取少量试剂在试管中混合,立即产生一种无色气体。我们对此气体展开了一系列探究:
(1)写出图中仪器a、b的名称: a ,b 。
(2)如何检验装置B是否不漏气? 。
(3)猜想:我认为产生的气体能使带火星的木条复燃,我能写出此反应的化学方程式: ,我知道它的反应类型是 。
(4)我想制取该气体,发生装置将选取图中的 (填序号,以下同),收集装置选取
。
(5)如果用如图中的F装置收集该气体,我认为气体应从 端(填“①”或“②”)导入。
(6)我猜想无色气体还可能是另外一种气体,产生它的化学方程式是 。收集装置可选取上图中的 〔填序号〕。
(7)甲烷是一种无色、无味、难溶于水的气体,实验室用加热无水醋酸钠和碱石灰的固体混合物的方法制取甲烷,则实验室制取并收集甲烷应选择的装置组合是 。
三、实验与探究(共3小题)
19.小明同学在家里做了如图所示的小实验。
(1)图I中观察到的主要现象是鸡蛋壳表面有气泡产生,蜡烛火焰熄灭。由此得出二氧化碳性质的结论是____________、__________,并依此性质确定二氧化碳的一个主要用途是_______。
(2)当蜡烛熄灭后,在玻璃杯口迅速盖一块蘸有石灰水的玻璃片(见图II),观察到的现象是玻璃片上的石灰水______,写出气体与石灰水反应的化学方程式__________________。
20.在化学实验室开放日,老师拿出两瓶无标签的试剂,分别是固体和液体,他取少量试剂在试管中混合,立即产生一种无色气体。同学们对此气体展开了一系列探究。
(1)如果推测此气体是二氧化碳,验证它的实验方案如下:
产生此气体的化学方程式可能是_____________________________;
(2)若想制取该气体,采用的发生装置可选取下图中的____________,收集装置应选用_________(填序号);
(3)如用下图中F装置收集该气体,气体应由_________端导入(填“a”或“b”)。
21.下图是实验室用碳酸钙与稀盐酸反应制取二氧化碳并验证其性质的的实验装置图,试根据题目要求回答下列问题:
(1)仪器a的名称是;仪器b的名称是;
(2)实验室制取气体时,仪器组装后,加入试剂前必不可少的一项操作是 。装置A中的反应方程式;装置B中的反应化学方程式;装置C中观察到的现象是。装置A还可以制取氧气,化学方程式为。
(3)装置D中观察到的现象是____________,说明二氧化碳的密度比空气大,它不能燃烧,也不能支持燃烧。由此可知,二氧化碳在生活中可用于__________。
(4)实验室用装置E来收集二氧化碳时,二氧化碳应从(填“c端”或“d端”)通入。
答案解析
1.【答案】D
【解析】化石燃料的过度燃烧产生大量的二氧化碳气体排放到空气中形成了温室效应,与氢气、氮气、氧气等无关。
2.【答案】C
【解析】根据碳燃烧的化学方程式可以判断生成二氧化碳消耗的氧气是生成一氧化碳消耗氧气的2倍,其质量比为2:1。
3.【答案】A
【解析】一氧化碳既有可燃性,又有还原性,A说法正确;一氧化碳难溶于水,B说法不正确;一氧化碳和二氧化碳的化学性质不同,C说法不正确;一氧化碳是无色、无味的气体,D说法不正确。
4.【答案】A
【解析】本题主要考查二氧化碳的用途。供给呼吸是氧气的用途,二氧化碳不能供给呼吸。
5.【答案】B
【解析】制取二氧化碳的操作步骤是:连(连接仪器、组装实验装置)→查(检查装置的气密性)→加(加入固体药品)→倒(倒入液体药品)→定(用铁架台固定仪器装置)→收集(用向上排空气法收集)。故正确的操作顺序为:①④②③⑤⑥。
6.【答案】B
【解析】二氧化碳可以防止地表热量辐射到太空中,具有调节地球气温的功能,而温室效应就是由于大气中二氧化碳等气体的含量增加,使全球气温升高的现象。
7.【答案】B
【解析】气体常温下不与空气中的成分反应,密度比空气小,可以采用向下排空气法进行收集,极易溶于水,不能采用排水法进行收集。
8.【答案】D
【解析】二氧化碳无毒,不能与人体的血红蛋白结合,D的自述不正确,其他各项的叙述都是正确的。
9.【答案】C
【解析】活性炭具有吸附性,可用活性炭做冰箱除臭剂;焦炭具有还原性,可以用焦炭冶炼金属;用碳粉和泥土可制成铅笔芯,而不是铅;石墨易导电,可以用石墨做干电池的电极。
10.【答案】B
【解析】二氧化碳能溶于水并与水生成碳酸,使紫色石蕊试液变成红色,碳酸不稳定,加热后分解成二氧化碳与水,试液又由红色变成紫色。
11.【答案】A
【解析】根据提示信息可以判断该反应的化学方程式为SiO2+2CSi+2CO↑,在反应中,碳能夺取二氧化硅中的氧具有还原性,碳是还原剂,发生了氧化反应,所以只有A正确。
12.【答案】B
【解析】金刚石是由碳原子直接构成的,碳化硅的结构类似于金刚石的结构,因此其构成微粒为原子。
13.【答案】A
【解析】由题中图示显示,A处应是消耗氧气,产生二氧化碳,B、C、D都符合这一要求。而发展和利用太阳能既不产生二氧化碳也不消耗氧气。
14.【答案】C
【解析】CO2不支持呼吸,故可以使人窒息,体现了CO2的过;CO2是光合作用的原料,可以作气体肥料,体现了CO2的功;而温室效应可以使全球变暖,使气候反常,这是过,也可提高大棚内的温度,有利于大棚蔬菜的培育,这是功;固体CO2可用于人工降雨,体现了CO2的功。
15.【答案】C
【解析】干冰是固体二氧化碳,由题目信息看出干水是混合物,故两者不是同一种物质;分子都是不停地运动的;干水吸收二氧化碳的能力比普通清水高三倍,故用干水吸收二氧化碳有助于减缓温室效应;由二氧化碳的性质可知,二氧化碳溶于水且部分与水反应生成碳酸,故干水吸收二氧化碳的过程不只发生物理变化。
16.【答案】C + O2CO2放热
【解析】碳在过量氧气中充分燃烧生成二氧化碳,该反应放出大量的热,属于放热反应。
17.【答案】(1)A (2)C F (3)D 二氧化碳能溶于水,密度大于空气 将燃着的木条放在瓶口,木条火焰熄灭,证明已满
【解析】(1)实验室用氯酸钾制取氧气的反应是固体加热,故应用的发生装置是固体加热型装置A。(2)实验室用过氧化氢制取氧气需用固液不加热型装置,同时要控制反应的发生和停止,故选用C装置做发生装置;要制得纯净氧气,需要用排水法收集。(3)实验室制取二氧化碳,因为二氧化碳能溶于水,密度大于空气,故用向上排空气法收集,验满的方法是将燃着的木条放在瓶口,木条熄灭,证明已满。
18.【答案】(1)试管 集气瓶
(2)加水形成液封,先把导管的一端浸入水中,然后两手紧握锥形瓶的外壁,观察导管口有气泡冒出,证明不漏气
(3) 2H2O22H2O+O2↑ 分解反应
(4)B D或C
(5)②
(6)CaCO3+2HCl=CaCl2+H2O+CO2↑ D (合理即可)
(7)AC或AE
【解析】结合实验装置图可以确定a是试管,b是集气瓶;检验装置B气密性的方法是:加水形成液封,先把导管的一端浸入水中,然后两手紧握锥形瓶的外壁,观察导管口有气泡冒出,证明不漏气;用固体与液体制取氧气,是过氧化氢在二氧化锰的催化作用下生成水与氧气,属于分解反应,发生装置选用B装置,可用排水法或向上排空气法收集;实验室制取二氧化碳,是在常温下用大理石或石灰石和稀盐酸制取的,二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;实验室用加热无水醋酸钠和碱石灰的固体混合物的方法制取甲烷,因此需要加热,甲烷是一种无色、无味、难溶于水、密度比空气小的气体,因此能用排水法和向下排空气法收集。
19.【答案】(1)二氧化碳不燃烧也不支持燃烧 密度比空气大 灭火
(2)变浑浊 Ca(OH)2+CO2═CaCO3↓+H2O
【解析】(1)鸡蛋壳的主要成分是碳酸钙,可以与盐酸反应生成二氧化碳气体,而二氧化碳的密度比空气大,二氧化碳不能燃烧也不能支持燃烧,随着反应的进行,二氧化碳逐渐增多,淹没蜡烛,会看到蜡烛熄灭,因此二氧化碳可以用于灭火。(2)生成的二氧化碳气体能与澄清的石灰水反应生成碳酸钙沉淀与水,澄清石灰水变浑浊。
20.【答案】(1)
CaCO3+ 2HCl = CaCl2+ H2O + CO2↑ (2)B E (3)a
【解析】检验二氧化碳的方法是通入澄清的石灰水,如果石灰水变浑浊,可以证明是二氧化碳气体;固体和液体常温下反应生成二氧化碳气体,是石灰石与稀盐酸的反应,发生装置应该选用固液不加热型,应选用B装置,由于二氧化碳能溶于水,且密度比空气大,所以应该选用向上排空气法收集;如果用F装置收集气体,根据二氧化碳的密度大于空气,所以应该从长导管通入。
21.【答案】(1)长颈漏斗 烧杯
(2)检查装置的气密性 CaCO3+2HCl=CaCl2+H2O+CO2↑
Ca(OH)2+CO2=CaCO3↓+H2O 紫色的石蕊试液变红
2H2O22H2O+O2↑
(3)下面的蜡烛比上面的蜡烛先熄灭 灭火
(4)c端
【解析】结合装置图可以判断a是长颈漏斗,b是烧杯;(2)实验室制取气体时,仪器组装后,加入试剂前应先检查装置的气密性,装置A中是碳酸钙与盐酸反应生成氯化钙、水与二氧化碳,装置B中是氢氧化钙与二氧化碳反应生成碳酸钙沉淀与水,生成的二氧化碳通入C中,紫色的石蕊试液变红,用装置A制取氧气时,应该用过氧化氢与二氧化锰;(3)装置D中观察到的现象是下面的蜡烛比上面的蜡烛先熄灭,二氧化碳不燃烧也不支持燃烧,生活中常用于灭火;(4)收集二氧化碳时应该用向上排空气法收集,应该从c通入。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
