1.2 溶液组成的定量表示 同步课件(18张PPT)
文档属性
| 名称 | 1.2 溶液组成的定量表示 同步课件(18张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-10-29 00:00:00 | ||
图片预览





文档简介
(共18张PPT)
第二节 溶液组成的定量表示
第一单元 溶液
鲁教版(五四制) 化学 九年级
溶液组成的表示方法
01
1.称取8g蔗糖加到烧杯中。再加入40mL水,搅拌,使蔗糖溶解。
2.称取10g蔗糖加到另一烧杯中。再加入50mL水,搅拌,使蔗糖溶解。
思考:
1.你能知道哪杯水更甜吗?你判断的依据是什么?
2.如果你的结论是通过计算获得的,你列出的算式是怎样的?
活动天地
1、溶质的质量分数定义:
2、溶质质量分数的表达式:
溶质的质量分数
溶质质量
溶液质量
×100%
溶质质量
溶质质量+溶剂质量
×100%
溶质质量与溶液质量之比。
溶液组成的表示方法
溶质的质量分数
溶质质量
溶液质量
×100%
溶质的质量=
溶液的质量=
溶质的质量
溶质的质量分数
溶液的质量×溶质的质量分数
关系式变形:
溶液组成的表示方法
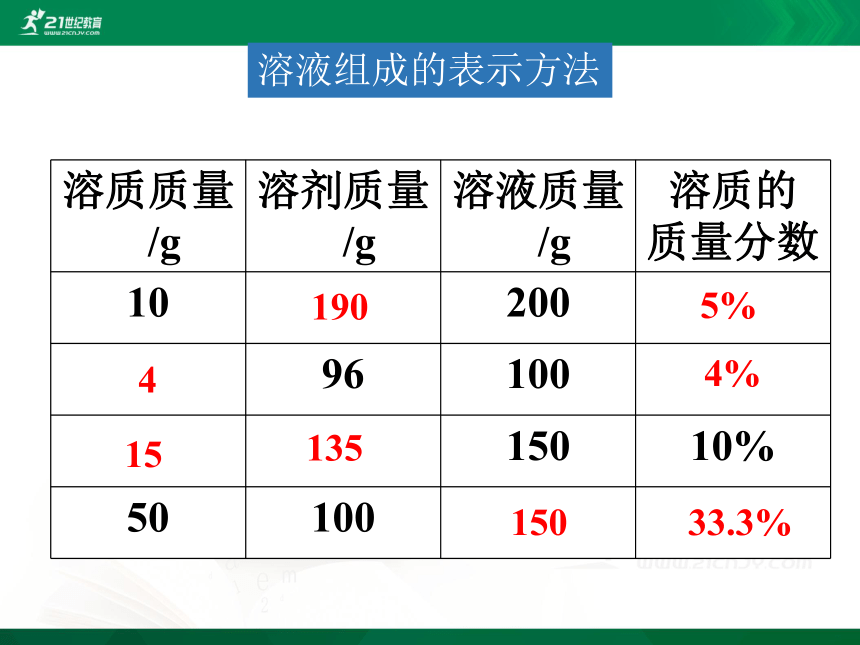
溶质质量/g 溶剂质量/g 溶液质量/g 溶质的
质量分数
10 200
96 100
150 10%
50 100
190
5%
4%
15
135
150
33.3%
4
溶液组成的表示方法
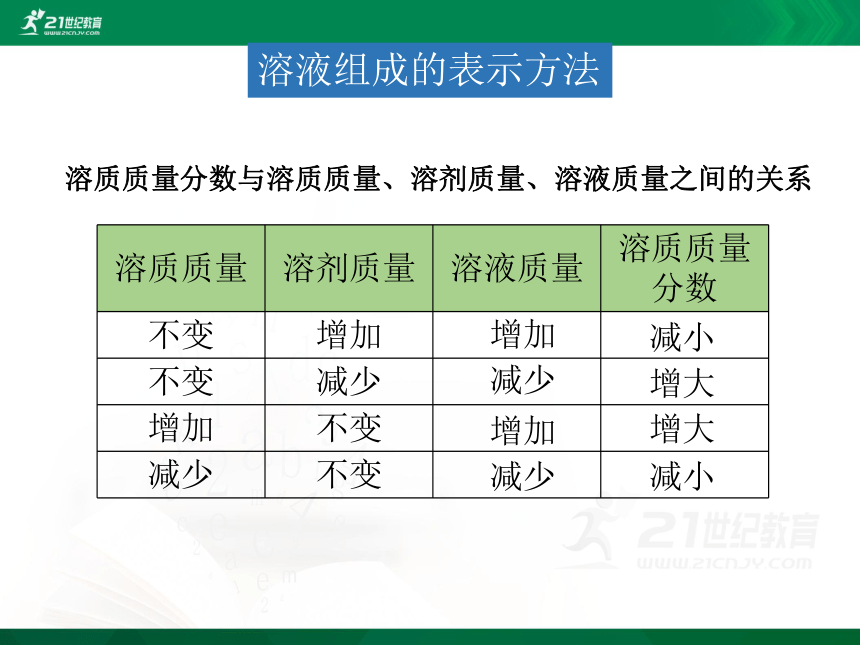
溶质质量分数与溶质质量、溶剂质量、溶液质量之间的关系
溶质质量 溶剂质量 溶液质量 溶质质量分数
不变 增加
不变 减少
增加 不变
减少 不变
减小
减小
增大
增大
增加
减少
增加
减少
溶液组成的表示方法
有关溶液中溶质的质量分数的计算类型
1、溶质的质量、溶液的质量(或溶剂的质量)、溶质的质量分数之间的换算,直接应用公式。
2、溶液去水浓缩或加水稀释的计算,解此类题目抓住一点即可:浓缩或稀释前后溶液中溶质的质量不变。
溶液组成的表示方法
3、一定质量的溶液中进行溶质的质量分数的计算时,涉及溶液的体积、密度的计算,应先根据公式m=ρV(即溶液的质量=溶液的密度×溶液的体积)进行换算,或先计算质量,再利用公式进行换算。
4、不同质量分数的同种溶质的溶液混合的计算。
m1·a1%+m2·a2%=(m1+m2)·a%
溶液组成的表示方法
白酒的“度数”指的是白酒中酒精的含量。这里的含量不是指质量分数,而是体积分数。例如,52度(52°)的酒表示100 mL酒中含有52 mL酒精(通常为20 ℃时的测量值)。体积分数也是一种表示溶液组成的方法。
课外延伸
白酒的“度数”
溶液的配制
02
二、溶液的配制
1、实验目的:配制50 g 16%的氯化钠溶液。
2、实验过程:
(1)计算:配制50 g 16%的氯化钠溶液。
①需氯化钠的质量是______________。
②需水的质量为______________,
体积为___________________。
50 g×16%=8 g
50 g-8 g=42 g
探究
溶液的配制
(2)称量。
①称量固体氯化钠选用的仪器是_________。
②量取水选用的仪器是______的量筒。
(3)溶解:为加速溶解,你采用的方法是_____________。
(4)装瓶存放:把配制好的溶液装入试剂瓶中,盖好瓶盖,贴上标
签(注明_________和_______________),放入_______中。
托盘天平
50 mL
用玻璃棒搅拌
药品名称
溶质的质量分数
试剂柜
溶液的配制
探究
(1)计算:要准确。
(2)称量:①托盘天平:左物右码。
②量筒:视线与凹液面最低处相平。
(3)溶解:用玻璃棒搅拌时不可碰触烧杯壁和烧杯底。
(4)装瓶存放:标签内容应填写如下两项:
a.药品名称 b.溶质质量分数
注意事项
(1)导致溶液的溶质质量分数偏小的原因可能有:
①天平使用不正确,如药品和砝码位置放反,且使用了游码;
②用量筒量取水时,仰视读数;
③称取食盐前,天平未调平衡,天平指针偏左;
误差分析
④将食盐倒入烧杯时,有少量食盐洒落;
⑤配制所用的烧杯不干燥。
(2)导致溶液的溶质质量分数偏大的原因可能有:
①称取食盐前,天平未调平衡,指针偏右;
②用量筒量取水时,俯视读数;
③将量筒内的水倒入烧杯时,有水洒出。
误差分析
谢谢聆听
第二节 溶液组成的定量表示
第一单元 溶液
鲁教版(五四制) 化学 九年级
溶液组成的表示方法
01
1.称取8g蔗糖加到烧杯中。再加入40mL水,搅拌,使蔗糖溶解。
2.称取10g蔗糖加到另一烧杯中。再加入50mL水,搅拌,使蔗糖溶解。
思考:
1.你能知道哪杯水更甜吗?你判断的依据是什么?
2.如果你的结论是通过计算获得的,你列出的算式是怎样的?
活动天地
1、溶质的质量分数定义:
2、溶质质量分数的表达式:
溶质的质量分数
溶质质量
溶液质量
×100%
溶质质量
溶质质量+溶剂质量
×100%
溶质质量与溶液质量之比。
溶液组成的表示方法
溶质的质量分数
溶质质量
溶液质量
×100%
溶质的质量=
溶液的质量=
溶质的质量
溶质的质量分数
溶液的质量×溶质的质量分数
关系式变形:
溶液组成的表示方法
溶质质量/g 溶剂质量/g 溶液质量/g 溶质的
质量分数
10 200
96 100
150 10%
50 100
190
5%
4%
15
135
150
33.3%
4
溶液组成的表示方法
溶质质量分数与溶质质量、溶剂质量、溶液质量之间的关系
溶质质量 溶剂质量 溶液质量 溶质质量分数
不变 增加
不变 减少
增加 不变
减少 不变
减小
减小
增大
增大
增加
减少
增加
减少
溶液组成的表示方法
有关溶液中溶质的质量分数的计算类型
1、溶质的质量、溶液的质量(或溶剂的质量)、溶质的质量分数之间的换算,直接应用公式。
2、溶液去水浓缩或加水稀释的计算,解此类题目抓住一点即可:浓缩或稀释前后溶液中溶质的质量不变。
溶液组成的表示方法
3、一定质量的溶液中进行溶质的质量分数的计算时,涉及溶液的体积、密度的计算,应先根据公式m=ρV(即溶液的质量=溶液的密度×溶液的体积)进行换算,或先计算质量,再利用公式进行换算。
4、不同质量分数的同种溶质的溶液混合的计算。
m1·a1%+m2·a2%=(m1+m2)·a%
溶液组成的表示方法
白酒的“度数”指的是白酒中酒精的含量。这里的含量不是指质量分数,而是体积分数。例如,52度(52°)的酒表示100 mL酒中含有52 mL酒精(通常为20 ℃时的测量值)。体积分数也是一种表示溶液组成的方法。
课外延伸
白酒的“度数”
溶液的配制
02
二、溶液的配制
1、实验目的:配制50 g 16%的氯化钠溶液。
2、实验过程:
(1)计算:配制50 g 16%的氯化钠溶液。
①需氯化钠的质量是______________。
②需水的质量为______________,
体积为___________________。
50 g×16%=8 g
50 g-8 g=42 g
探究
溶液的配制
(2)称量。
①称量固体氯化钠选用的仪器是_________。
②量取水选用的仪器是______的量筒。
(3)溶解:为加速溶解,你采用的方法是_____________。
(4)装瓶存放:把配制好的溶液装入试剂瓶中,盖好瓶盖,贴上标
签(注明_________和_______________),放入_______中。
托盘天平
50 mL
用玻璃棒搅拌
药品名称
溶质的质量分数
试剂柜
溶液的配制
探究
(1)计算:要准确。
(2)称量:①托盘天平:左物右码。
②量筒:视线与凹液面最低处相平。
(3)溶解:用玻璃棒搅拌时不可碰触烧杯壁和烧杯底。
(4)装瓶存放:标签内容应填写如下两项:
a.药品名称 b.溶质质量分数
注意事项
(1)导致溶液的溶质质量分数偏小的原因可能有:
①天平使用不正确,如药品和砝码位置放反,且使用了游码;
②用量筒量取水时,仰视读数;
③称取食盐前,天平未调平衡,天平指针偏左;
误差分析
④将食盐倒入烧杯时,有少量食盐洒落;
⑤配制所用的烧杯不干燥。
(2)导致溶液的溶质质量分数偏大的原因可能有:
①称取食盐前,天平未调平衡,指针偏右;
②用量筒量取水时,俯视读数;
③将量筒内的水倒入烧杯时,有水洒出。
误差分析
谢谢聆听
同课章节目录
- 第一单元 溶液
- 1 溶液的形成
- 2 溶液组成的定量表示
- 3物质的溶解性
- 到实验室去:配制一定溶质质量分数的溶液
- 第二单元 常见的酸和碱
- 1 酸及其性质
- 2 碱及其性质
- 3 溶液的酸碱性
- 4 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 到图书馆去:分子变成离子
- 第三单元 海水中的化学
- 1 海洋化学资源
- 2 海水“晒盐”
- 3 海水“制碱”
- 到实验室去:粗盐中难溶性杂质的去除
- 第四单元 金属
- 1 常见的金属材料
- 2 金属的化学性质
- 3 钢铁的锈蚀与防护
- 到实验室去:探究金属的性质
- 第五单元 化学与健康
- 1 食物中的有机物
- 2 化学元素与人体健康
- 3 远离有毒物质
- 第六单元 化学与社会发展
- 1 化学与能源开发
- 2 化学与材料研制
- 3 化学与农业生产
- 4 化学与环境保护
