人教版九年级化学 第三单元 物质构成的奥秘 阶段性优测卷(含答案)
文档属性
| 名称 | 人教版九年级化学 第三单元 物质构成的奥秘 阶段性优测卷(含答案) |  | |
| 格式 | docx | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-10-29 21:16:17 | ||
图片预览




文档简介
中小学教育资源及组卷应用平台
第三单元 物质构成的奥秘
(说明:本试卷为闭卷笔答,答题时间70分钟,满分70分)
题号 一 二 三 四 五 六 总分
得分
第Ⅰ卷 选择题(共20分)
一、选择题(本大题共10个小题,每小题2分,共20分。在每小题给出的四个选项中,只有一项符合题目要求,请选出填在下表中。)
1.分子是构成物质的粒子之一。下列物质中,含有氧分子的是 ( )
A.氧气 B.过氧化氢 C.二氧化硫 D.二氧化氮
2.从微观的角度分析,下列解释错误的是 ( )
A.在水中加入白糖后水变甜,是由于分子永不停息地做无规则运动
B.1L细沙与1L水混合后总体积小于2L,是由于分子间有间隔
C.体温计内汞柱液面上升,是由于汞原子间的间隔变大
D.氧气和二氧化碳化学性质不同,是因为其分子构成不同
3.氧化铈抛光粉具有抛光速度快、光洁度高和使用寿命长的优点广泛用于照相机、摄影机镜头、电视显像管、眼镜片等的抛光。已知铈原子的原子核内有58个质子和82个中子,该原子的核外电子数为 ( )
A.24 B.58 C.82 D.140
4.科学研究表明:海洋生物可利用氮的多寡是影响海洋生产力的重要因素,且氮的生物地球化学循环会产生大量温室效应气体。因而,氮循环的波动对全球气候变化有着重要影响。上述有关表述中的“氮”指的是 ( )
A.原子 B.分子 C.元素 D.物质
5.如图,向两支试管中分别加入等量清水和红墨水,使其有较明显的分界面,将其中一支试管放入盛有热水的烧杯中,观察到浸在热水中的试管里的两种液体分界面模糊得更快些。该对比实验主要说明构成物质的微粒 ( )
A.体积小、质量小 B.在不断运动 C.相互之间有间隔 D.随温度升高运动速率加快
6.下图是分子结构模型示意图(图中“〇”“●”表示两种不同的原子),其中表示混合物的是 ( )
7.下列对分子、原子、离子的认识正确的是 ( )
A.同种分子排列方式不同,化学性质不同 B.在干冰(固态二氧化碳)中,分子因相互作用而静止不动
C.同种原子按不同方式结合,可以构成不同的物质 D.原子得失电子形成离子后,原子核发生了变化
8.下列关于元素符号“O”表示的含义的说法中,正确的是 ( )
①表示氧元素 ②表示氧气 ③表示1个氧原子 ④表示1个氧分子
A.①② B.②③ C.①③ D.②④
9.下列结构示意图所表示的粒子在化学反应中容易得到电子的是 ( )
10.如图是钙、铬元素在元素周期表中的单元格,下列说法错误的是 ( )
A.钙和铬都属于金属元素 B.铬比钙原子的核电荷数多4
C.钙和铬原子的核外电子数之比为5:6 D.钙和铬的相对原子质量之和是92.08g
第Ⅱ卷 非选择题(共50分)
二、生活、生产应用题(本大题共5个小题。每空1分,共16空,共16分。)
【关注生活现象】
11.“智能加热器”是液体蚊香的好搭档,可以定时加热,自动停止,减少蚊香液的浪费。从微观角度看,蚊香液逐渐减少的原因是________________________,据此推测影响微粒运动快慢的可能因素是_____________________
____________________________________________________________。
12.我国“化学”一词最早出于《化学鉴原》(1871年),该书把一种元素翻译为“矽”(xī)在地壳里,“矽”的含量在所有元素含量中居第二位。请回答:
(1)“矽”元素现在的名称为________________,属于________(填“金属”或“非金属”)元素。
(2)在地壳里,排在“矽”元素后面的元素的化学符号为________。
13.地球大气中存在氧气(O2)和臭氧(O3)两种含氧元素的单质,其中臭氧虽然能减弱高能量紫外线对地球表面的辐射,但是近地面臭氧污染却对人体健康和生态系统有很大损害。2020年4月后,氧已悄然取代PM2成为深圳目前大气的首要污染物。我省也于当年3月由省生态环境厅组织省生态环境研究中心专家开设了“云课堂”来提升全省臭氧污染治理水平。
(1)氧气分子和臭氧分子都由________________构成。
(2)氧气(O2)和臭氧(O3)化学性质不同的原因为________________
(3)下列说法正确的是________(填字母)。
A.组成元素相同的物质不一定是同种物质 B.由同一种元素组成的物质一定是纯净物
C.元素组成相同,物质的用途可能不同
14.家庭装修中用的涂料、地板等人造板材,除了含有甲醛、甲苯、二甲苯等有害物质外,还有许多其他挥发性有机物,都会对人体造成很大的危害。如某些花岗岩石材中就含有放射性元素氡,如图是氡在元素周期表中的一格及氡原子的结构示意图。请回答下列问题:
(1)氡的相对原子质量为________,中子数为________
(2)氡的化学性质________(填“稳定”或“不稳定”)
【关注生产实际】
15.如图为模拟工业制氧气的微观示意图。已知同温同压下,气体体积比等于分子个数比。请回答下列问题:
(1)空气属于________(填“纯净物”或“混合物”),从微观角度解释原因为________________________
(2)空气加压、降温转化为液态空气的过程中,________________________发生改变,该变化属于________(填“物理变化”或“化学变化”)。
(3)“”表示的是________(填“氧分子”或“氮分子”)。
三、科普阅读题(本大题共1个小题。每空1分,共7空,共7分。)
16.阅读下面科普短文,回答下列问题。
征服原子-揭开原子的神秘面纱
伟大的科学家费曼说:“假如只允许把人类的科学史压缩成一句话,它就会是一切东西都是由原子构成”。人类在探索物质是由什么构成的历史长河中,充满了智慧。
1803年,近代化学之父,英国科学家道尔顿(Dalt0n)在前人研究的基础上,提出“道尔顿原子论”:一切物质都由原子构成,原子很小,呈圆球状,是一个实心球体,不可再分…但由于受当时实验条件限制,道尔顿无法用事实证明自己的观点。
1811年,意大利化学家阿伏加德罗提出:有些物质也是由分子构成,原子的基本工作形式是分子。
1897年,汤姆生在原子内部发现了电子,进一步发展了原子、分子论。1911年,卢瑟福又通过实验,推测原子是由原子核和核外电子构成,并提出了沿用至今的现代原子结构理论。
1913年,玻尔提出他的原子模型:电子在原子核外空间的一定轨道上绕核做高速的圆周运动。
(1)道尔顿的原子论,不是事实的归纳,而是思维的产物,体现了直觉和想象在科学创造中的作用。你认为道尔顿的原子论存在的缺陷或错误是____________________、____________________、______________________。
(2)汤姆生主要是纠正了“道尔顿原子论”中的________________________________________观点。
(3)请运用所学知识对玻尔的原子模型作出判断,并说明理由。________(填“正确”或“错误”),理由是
________________________________________________________________________________。
(4)原子是一种看不见、摸不着的微粒,为了帮助人们理解原子的结构,这几位科学家都运用了________来表达他们的理论成果。
四、物质组成与变化分析题(本大题共1个小题。文字表达式每空2分,其余每空1分,共5空,共6分。)
17.A 、B、C、D四种元素,A元素的一种原子核内无中子;B是地壳中含量第二多的金属元素;只含有C元素的物质在只含有D元素的物质中燃烧,发出蓝紫色火焰,生成有刺激性气味的气体。
(1)写出A、B、D三种元素的符号:A_________;B.________;D________。
(2)写出B元素组成的金属在氧气中燃烧的现象:________________________________________________。
(3)写出只含C元素的物质在只含D元素的物质中燃烧的文字表达式:________________________________
____________________________________________________________。
五、实验探究题(本大题共2个小题。每空分,共15空,共15分。)
【基本实验】
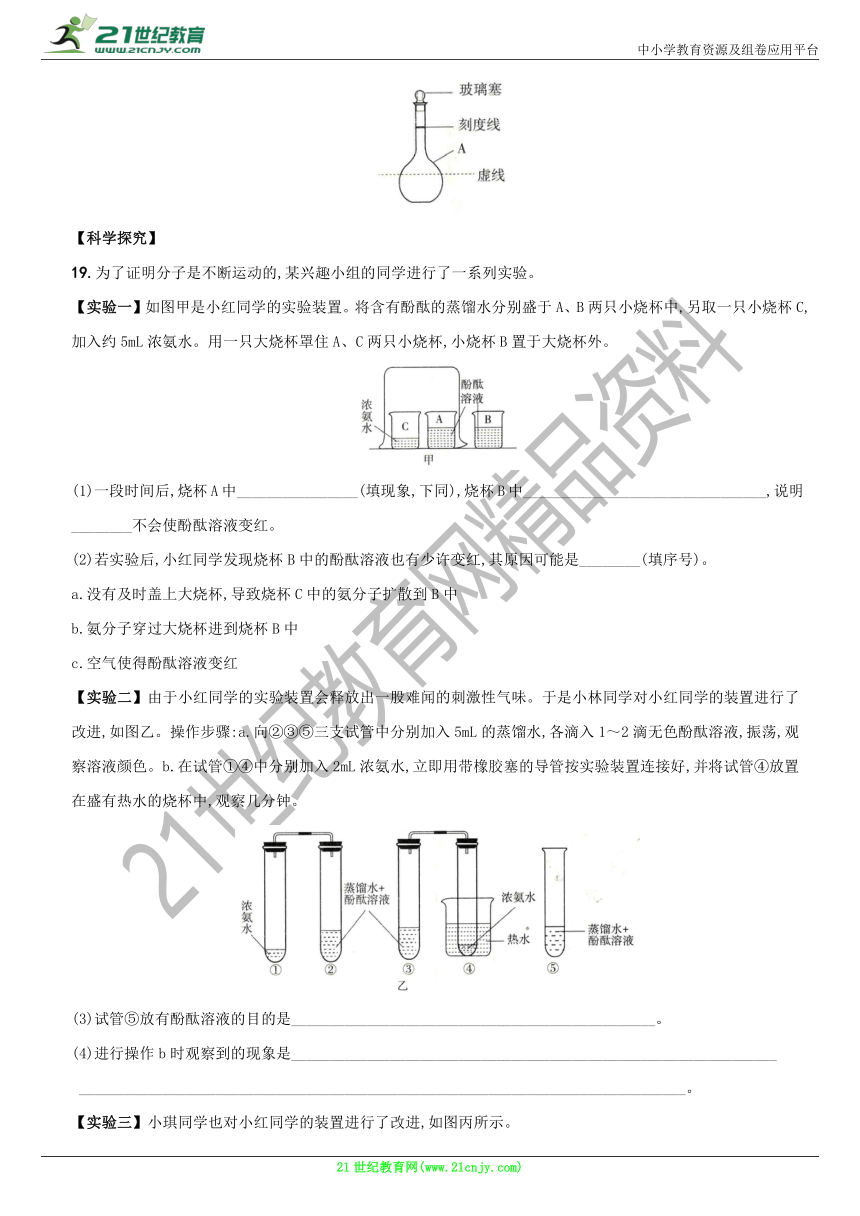
18.向容积为250mL的细颈玻璃仪器A中加水至虚线处,再滴几滴红墨水,一段时间后,A中的现象是________________,说明________________________________。继续向A中加酒精至凹液面最低处正好与刻度线相切。塞紧玻璃塞,将A中液体倒转摇匀,重复2次。静置一段时间后,A中的现象为________________________________________,说明________________________________________。仪器A细颈部的作用是________________________________________
【科学探究】
19.为了证明分子是不断运动的,某兴趣小组的同学进行了一系列实验。
【实验一】如图甲是小红同学的实验装置。将含有酚酞的蒸馏水分别盛于A、B两只小烧杯中,另取一只小烧杯C,加入约5mL浓氨水。用一只大烧杯罩住A、C两只小烧杯,小烧杯B置于大烧杯外。
(1)一段时间后,烧杯A中________________(填现象,下同),烧杯B中________________________________,说明________不会使酚酞溶液变红。
(2)若实验后,小红同学发现烧杯B中的酚酞溶液也有少许变红,其原因可能是________(填序号)。
a.没有及时盖上大烧杯,导致烧杯C中的氨分子扩散到B中
b.氨分子穿过大烧杯进到烧杯B中
c.空气使得酚酞溶液变红
【实验二】由于小红同学的实验装置会释放出一股难闻的刺激性气味。于是小林同学对小红同学的装置进行了改进,如图乙。操作步骤:a.向②③⑤三支试管中分别加入5mL的蒸馏水,各滴入1~2滴无色酚酞溶液,振荡,观察溶液颜色。b.在试管①④中分别加入2mL浓氨水,立即用带橡胶塞的导管按实验装置连接好,并将试管④放置在盛有热水的烧杯中,观察几分钟。
(3)试管⑤放有酚酞溶液的目的是________________________________________________。
(4)进行操作b时观察到的现象是________________________________________________________________
________________________________________________________________________________。
【实验三】小琪同学也对小红同学的装置进行了改进,如图丙所示。
在T形三通管的粗玻璃管里,固定一根用酚酞润湿的纱布条。用胶头滴管吸取少许浓氨水,将其滴入T形三通管的细弯管处,然后用橡皮帽封闭管口。
(5)一段时间后,可观察到________(填“ba”或“bc”)段纱布条先变成红色。
(6)若将图丙中装有浓氨水的细弯管处浸入冰水中,可观察到纱布条变红的速率变________(填“快”或“慢”),请从微观角度进行解释:__________________________________________________________________。
(7)与图甲装置相比,图丙装置的优点是____________________________________________________________
________________________________________________________________________________。
六、定量分析题(本大题共1个小题,共6分。)
20.已知一个碳12原子的质量为m kg,另一个原子的质量为n kg,且其中有a个质子。
(1)A原子中的中子数是_________。
(2)A2+和B2-的核外电子数相同,B原子的质子数为__________________。
《参考答案及解析》
第三单元 物质构成的奥秘
1.A
[解析]氧气由氧分子构成,因此氧气中含有氧分子,故A正确;过氧化氢由过氧化氢分子构成,二氧化硫由二氧化硫分子构成,二氧化氮由二氧化氮分子构成,因此B、、D中均没有氧分子。
2.B
[解析]细沙与水是宏观物质,1L细沙与1L水混合后总体积小于2L,不能说明分子间有间隔。
3.B
[解析]在原子中,质子数=核外电子数。
4.C
[解析]这里的“氮”指的是元素,与具体形态无关。
5.D
[解析]两组实验对比,变量是温度。温度高的试管中液体混合快,证明温度高时分子运动快。
6.D
[解析]宏观上,混合物由两种或两种以上物质组成;微观上,混合物由不同种分子或原子构成。观察四个选项:A、B、C均由同种分子构成,属于纯净物;D由两种不同分子构成,因此属于混合物。
7.C
[解析]同种分子排列方式不同,但分子的种类不变,化学性质相同,故A错误;分子总是在不断地运动着故B错误;同种原子按不同方式结合,可以构成不同的物质,如水和过氧化氢,故C正确;原子得失电子形成离子后,原子核没有发生变化,只是核外电子数发生改变,故D错误。
8.C
[解析]“O”是氧元素的符号,表示氧元素和1个氧原子。
9.D
[解析]最外层电子数与元素的化学性质密切相关。A粒子最外层达到8个电子的稳定结构,不易得失电子;B、C粒子最外层电子数少于4个,易失去电子;D粒子最外层有7个电子,非常容易得到1个电子,达到最外层为8个电子的稳定结构。
10.D
[解析]相对原子质量的单位为“1,通常省略不写,钙和铬的相对原子质量之和是92.08。
11.分子不断运动到空气中了 温度
[解析]题干中提到“加热”,据此推测温度影响微粒运动的快慢。
12.
(1)硅 非金属
(2)Al
[解析]
(1)在地壳里,硅元素的含量居第二位,硅带有“石字旁,属于非金属元素。
(2)排在硅元素后面的元素是铝,其化学符号为Al
13.
(1)氧原子
(2)分子构成不同
(3)AC
[解析]氧气(O2)和臭氧(O3)都由氧元素组成,说明同种元素可以组成不同的物质,由同一种元素组成的物质不一定是纯净物,可能是混合物。
14.
(1)222 136
(2)稳定
[解析]
(1)由氡在元素周期表中的一格可知,氡的相对原子质量为222,中子数=222-86=136。
(2)由氡的原子结构示意图可知,氡原子的最外层电子数为8,达到相对稳定结构,既不易失去电子,也不易得到电子,化学性质稳定。
15.
(1)混合物 空气由不同种分子构成
(2)分子间的间隔 物理变化
(3)氧分子
[解析]
(1)空气中含有不同种分子,属于混合物。
(2)空气加压、降温的过程中分子间的间隔变小,分子种类不变该变化属于物理变化。
(3)空气中氮气的体积分数约为78%,氧气的体积分数约为21%,已知同温同压下,气体体积比等于分子个数比。因此,分子个数少的为氧分子,多的为氮分子,则“”表示的是氧分子。
16.
(1)一切物质都由原子构成原子不可再分原子是实心球体
(2)原子不可再分
(3)错误原子核外有很大的空间,电子就在这个空间做高速的运动,但不是做圆周运动,不存在确切的轨道
(4)模型
[解析]
(1)物质由分子、原子、离子构成。在化学反应中,原子不可再分,但原子并不是不可分割的实心球体
(2)汤姆生在原子内部发现了电子,说明原子并不是不可再分。
(3)原子核外有很大的空间,电子就在这个空间做高速的运动。
(4)为了帮助人们理解原子的结构,这几位科学家都运用了模型进行演示。
17.
(1)H Fe O
(2)剧烈燃烧,火星四射,放出热量,生成一种黑色固体
(3)硫+氧气二氧化硫
[解析]有一种氢元素的原子核内没有中子;铁是地壳中含量第二多的金属元素;根据燃烧时发出蓝紫色火焰,生成有刺激性气味的气体,可以判断是硫在氧气中燃烧。
18.瓶中水变红 分子在不断地运动 液面低于刻度线且距离较远分子间存在间隔便于观察液面变化
[解析]构成红色物质的分子不断运动到水中,使整瓶水变红。酒精分子运动到水分子间隔中,导致液体总体积变小。
19.
(1)液体变红 没有明显现象 空气
(2)a
(3)作对照
(4)③、②试管中的酚酞溶液先后变成红色
(5)ba
(6)慢 温度越低,分子运动速率越慢
(7)节省药品,防止污染空气等(合理即可)
[解析]
(1)实验一中,由于浓氨水具有挥发性,所以一段时间后,烧杯C中氨分子进入烧杯A中,使得烧杯A中液体变红。烧杯B放在空气中,没有现象,说明空气不会使酚酞溶液变红。
(2)若实验后发现烧杯B中的酚酞溶液也有少许变红,说明有氨分子进入烧杯B中,则a选项正确。
(3)试管⑤放有酚酞溶液的目的是对比,通过对比可知,空气中的物质不能使酚酞溶液变红色。
(4)由于温度越高,分子运动速率越快,所以④中氨分子运动快,③中的酚酞溶液先变红色。
(5)实验三中用胶头滴管吸取少许浓氨水,将其滴入T形三通管的细弯管处,然后用橡皮帽封闭管口。由于氨气的密度比空气的小,所以一段时间后会观察到ba段纱布条先变成红色。
(6)若将图丙中装有浓氨水的细弯管处浸入冰水中,可观察到纱布条变红的速率变慢,这是因为温度越低,分子运动速率越慢。
(7)对比图甲装置,图丙装置的药品用量少,而且对环境污染小。
20.
(1) -a(3分)
(2)a-4(3分)
[解析]
(1)A原子的相对原子质量为,相对原子质量近似等于质子数与中子数之和,A原子中的中子数= -a。
(2)A原子的质子数为a,失去两个电子形成A2+,则A2+的核外电子数为a-2。设B原子的质子数为b,B原子得到两个电子形成B2-,则B2-的核外电子数为b+2。a-2=b+2,则b=a-4。
21世纪教育网(www.21cnjy.com)
第三单元 物质构成的奥秘
(说明:本试卷为闭卷笔答,答题时间70分钟,满分70分)
题号 一 二 三 四 五 六 总分
得分
第Ⅰ卷 选择题(共20分)
一、选择题(本大题共10个小题,每小题2分,共20分。在每小题给出的四个选项中,只有一项符合题目要求,请选出填在下表中。)
1.分子是构成物质的粒子之一。下列物质中,含有氧分子的是 ( )
A.氧气 B.过氧化氢 C.二氧化硫 D.二氧化氮
2.从微观的角度分析,下列解释错误的是 ( )
A.在水中加入白糖后水变甜,是由于分子永不停息地做无规则运动
B.1L细沙与1L水混合后总体积小于2L,是由于分子间有间隔
C.体温计内汞柱液面上升,是由于汞原子间的间隔变大
D.氧气和二氧化碳化学性质不同,是因为其分子构成不同
3.氧化铈抛光粉具有抛光速度快、光洁度高和使用寿命长的优点广泛用于照相机、摄影机镜头、电视显像管、眼镜片等的抛光。已知铈原子的原子核内有58个质子和82个中子,该原子的核外电子数为 ( )
A.24 B.58 C.82 D.140
4.科学研究表明:海洋生物可利用氮的多寡是影响海洋生产力的重要因素,且氮的生物地球化学循环会产生大量温室效应气体。因而,氮循环的波动对全球气候变化有着重要影响。上述有关表述中的“氮”指的是 ( )
A.原子 B.分子 C.元素 D.物质
5.如图,向两支试管中分别加入等量清水和红墨水,使其有较明显的分界面,将其中一支试管放入盛有热水的烧杯中,观察到浸在热水中的试管里的两种液体分界面模糊得更快些。该对比实验主要说明构成物质的微粒 ( )
A.体积小、质量小 B.在不断运动 C.相互之间有间隔 D.随温度升高运动速率加快
6.下图是分子结构模型示意图(图中“〇”“●”表示两种不同的原子),其中表示混合物的是 ( )
7.下列对分子、原子、离子的认识正确的是 ( )
A.同种分子排列方式不同,化学性质不同 B.在干冰(固态二氧化碳)中,分子因相互作用而静止不动
C.同种原子按不同方式结合,可以构成不同的物质 D.原子得失电子形成离子后,原子核发生了变化
8.下列关于元素符号“O”表示的含义的说法中,正确的是 ( )
①表示氧元素 ②表示氧气 ③表示1个氧原子 ④表示1个氧分子
A.①② B.②③ C.①③ D.②④
9.下列结构示意图所表示的粒子在化学反应中容易得到电子的是 ( )
10.如图是钙、铬元素在元素周期表中的单元格,下列说法错误的是 ( )
A.钙和铬都属于金属元素 B.铬比钙原子的核电荷数多4
C.钙和铬原子的核外电子数之比为5:6 D.钙和铬的相对原子质量之和是92.08g
第Ⅱ卷 非选择题(共50分)
二、生活、生产应用题(本大题共5个小题。每空1分,共16空,共16分。)
【关注生活现象】
11.“智能加热器”是液体蚊香的好搭档,可以定时加热,自动停止,减少蚊香液的浪费。从微观角度看,蚊香液逐渐减少的原因是________________________,据此推测影响微粒运动快慢的可能因素是_____________________
____________________________________________________________。
12.我国“化学”一词最早出于《化学鉴原》(1871年),该书把一种元素翻译为“矽”(xī)在地壳里,“矽”的含量在所有元素含量中居第二位。请回答:
(1)“矽”元素现在的名称为________________,属于________(填“金属”或“非金属”)元素。
(2)在地壳里,排在“矽”元素后面的元素的化学符号为________。
13.地球大气中存在氧气(O2)和臭氧(O3)两种含氧元素的单质,其中臭氧虽然能减弱高能量紫外线对地球表面的辐射,但是近地面臭氧污染却对人体健康和生态系统有很大损害。2020年4月后,氧已悄然取代PM2成为深圳目前大气的首要污染物。我省也于当年3月由省生态环境厅组织省生态环境研究中心专家开设了“云课堂”来提升全省臭氧污染治理水平。
(1)氧气分子和臭氧分子都由________________构成。
(2)氧气(O2)和臭氧(O3)化学性质不同的原因为________________
(3)下列说法正确的是________(填字母)。
A.组成元素相同的物质不一定是同种物质 B.由同一种元素组成的物质一定是纯净物
C.元素组成相同,物质的用途可能不同
14.家庭装修中用的涂料、地板等人造板材,除了含有甲醛、甲苯、二甲苯等有害物质外,还有许多其他挥发性有机物,都会对人体造成很大的危害。如某些花岗岩石材中就含有放射性元素氡,如图是氡在元素周期表中的一格及氡原子的结构示意图。请回答下列问题:
(1)氡的相对原子质量为________,中子数为________
(2)氡的化学性质________(填“稳定”或“不稳定”)
【关注生产实际】
15.如图为模拟工业制氧气的微观示意图。已知同温同压下,气体体积比等于分子个数比。请回答下列问题:
(1)空气属于________(填“纯净物”或“混合物”),从微观角度解释原因为________________________
(2)空气加压、降温转化为液态空气的过程中,________________________发生改变,该变化属于________(填“物理变化”或“化学变化”)。
(3)“”表示的是________(填“氧分子”或“氮分子”)。
三、科普阅读题(本大题共1个小题。每空1分,共7空,共7分。)
16.阅读下面科普短文,回答下列问题。
征服原子-揭开原子的神秘面纱
伟大的科学家费曼说:“假如只允许把人类的科学史压缩成一句话,它就会是一切东西都是由原子构成”。人类在探索物质是由什么构成的历史长河中,充满了智慧。
1803年,近代化学之父,英国科学家道尔顿(Dalt0n)在前人研究的基础上,提出“道尔顿原子论”:一切物质都由原子构成,原子很小,呈圆球状,是一个实心球体,不可再分…但由于受当时实验条件限制,道尔顿无法用事实证明自己的观点。
1811年,意大利化学家阿伏加德罗提出:有些物质也是由分子构成,原子的基本工作形式是分子。
1897年,汤姆生在原子内部发现了电子,进一步发展了原子、分子论。1911年,卢瑟福又通过实验,推测原子是由原子核和核外电子构成,并提出了沿用至今的现代原子结构理论。
1913年,玻尔提出他的原子模型:电子在原子核外空间的一定轨道上绕核做高速的圆周运动。
(1)道尔顿的原子论,不是事实的归纳,而是思维的产物,体现了直觉和想象在科学创造中的作用。你认为道尔顿的原子论存在的缺陷或错误是____________________、____________________、______________________。
(2)汤姆生主要是纠正了“道尔顿原子论”中的________________________________________观点。
(3)请运用所学知识对玻尔的原子模型作出判断,并说明理由。________(填“正确”或“错误”),理由是
________________________________________________________________________________。
(4)原子是一种看不见、摸不着的微粒,为了帮助人们理解原子的结构,这几位科学家都运用了________来表达他们的理论成果。
四、物质组成与变化分析题(本大题共1个小题。文字表达式每空2分,其余每空1分,共5空,共6分。)
17.A 、B、C、D四种元素,A元素的一种原子核内无中子;B是地壳中含量第二多的金属元素;只含有C元素的物质在只含有D元素的物质中燃烧,发出蓝紫色火焰,生成有刺激性气味的气体。
(1)写出A、B、D三种元素的符号:A_________;B.________;D________。
(2)写出B元素组成的金属在氧气中燃烧的现象:________________________________________________。
(3)写出只含C元素的物质在只含D元素的物质中燃烧的文字表达式:________________________________
____________________________________________________________。
五、实验探究题(本大题共2个小题。每空分,共15空,共15分。)
【基本实验】
18.向容积为250mL的细颈玻璃仪器A中加水至虚线处,再滴几滴红墨水,一段时间后,A中的现象是________________,说明________________________________。继续向A中加酒精至凹液面最低处正好与刻度线相切。塞紧玻璃塞,将A中液体倒转摇匀,重复2次。静置一段时间后,A中的现象为________________________________________,说明________________________________________。仪器A细颈部的作用是________________________________________
【科学探究】
19.为了证明分子是不断运动的,某兴趣小组的同学进行了一系列实验。
【实验一】如图甲是小红同学的实验装置。将含有酚酞的蒸馏水分别盛于A、B两只小烧杯中,另取一只小烧杯C,加入约5mL浓氨水。用一只大烧杯罩住A、C两只小烧杯,小烧杯B置于大烧杯外。
(1)一段时间后,烧杯A中________________(填现象,下同),烧杯B中________________________________,说明________不会使酚酞溶液变红。
(2)若实验后,小红同学发现烧杯B中的酚酞溶液也有少许变红,其原因可能是________(填序号)。
a.没有及时盖上大烧杯,导致烧杯C中的氨分子扩散到B中
b.氨分子穿过大烧杯进到烧杯B中
c.空气使得酚酞溶液变红
【实验二】由于小红同学的实验装置会释放出一股难闻的刺激性气味。于是小林同学对小红同学的装置进行了改进,如图乙。操作步骤:a.向②③⑤三支试管中分别加入5mL的蒸馏水,各滴入1~2滴无色酚酞溶液,振荡,观察溶液颜色。b.在试管①④中分别加入2mL浓氨水,立即用带橡胶塞的导管按实验装置连接好,并将试管④放置在盛有热水的烧杯中,观察几分钟。
(3)试管⑤放有酚酞溶液的目的是________________________________________________。
(4)进行操作b时观察到的现象是________________________________________________________________
________________________________________________________________________________。
【实验三】小琪同学也对小红同学的装置进行了改进,如图丙所示。
在T形三通管的粗玻璃管里,固定一根用酚酞润湿的纱布条。用胶头滴管吸取少许浓氨水,将其滴入T形三通管的细弯管处,然后用橡皮帽封闭管口。
(5)一段时间后,可观察到________(填“ba”或“bc”)段纱布条先变成红色。
(6)若将图丙中装有浓氨水的细弯管处浸入冰水中,可观察到纱布条变红的速率变________(填“快”或“慢”),请从微观角度进行解释:__________________________________________________________________。
(7)与图甲装置相比,图丙装置的优点是____________________________________________________________
________________________________________________________________________________。
六、定量分析题(本大题共1个小题,共6分。)
20.已知一个碳12原子的质量为m kg,另一个原子的质量为n kg,且其中有a个质子。
(1)A原子中的中子数是_________。
(2)A2+和B2-的核外电子数相同,B原子的质子数为__________________。
《参考答案及解析》
第三单元 物质构成的奥秘
1.A
[解析]氧气由氧分子构成,因此氧气中含有氧分子,故A正确;过氧化氢由过氧化氢分子构成,二氧化硫由二氧化硫分子构成,二氧化氮由二氧化氮分子构成,因此B、、D中均没有氧分子。
2.B
[解析]细沙与水是宏观物质,1L细沙与1L水混合后总体积小于2L,不能说明分子间有间隔。
3.B
[解析]在原子中,质子数=核外电子数。
4.C
[解析]这里的“氮”指的是元素,与具体形态无关。
5.D
[解析]两组实验对比,变量是温度。温度高的试管中液体混合快,证明温度高时分子运动快。
6.D
[解析]宏观上,混合物由两种或两种以上物质组成;微观上,混合物由不同种分子或原子构成。观察四个选项:A、B、C均由同种分子构成,属于纯净物;D由两种不同分子构成,因此属于混合物。
7.C
[解析]同种分子排列方式不同,但分子的种类不变,化学性质相同,故A错误;分子总是在不断地运动着故B错误;同种原子按不同方式结合,可以构成不同的物质,如水和过氧化氢,故C正确;原子得失电子形成离子后,原子核没有发生变化,只是核外电子数发生改变,故D错误。
8.C
[解析]“O”是氧元素的符号,表示氧元素和1个氧原子。
9.D
[解析]最外层电子数与元素的化学性质密切相关。A粒子最外层达到8个电子的稳定结构,不易得失电子;B、C粒子最外层电子数少于4个,易失去电子;D粒子最外层有7个电子,非常容易得到1个电子,达到最外层为8个电子的稳定结构。
10.D
[解析]相对原子质量的单位为“1,通常省略不写,钙和铬的相对原子质量之和是92.08。
11.分子不断运动到空气中了 温度
[解析]题干中提到“加热”,据此推测温度影响微粒运动的快慢。
12.
(1)硅 非金属
(2)Al
[解析]
(1)在地壳里,硅元素的含量居第二位,硅带有“石字旁,属于非金属元素。
(2)排在硅元素后面的元素是铝,其化学符号为Al
13.
(1)氧原子
(2)分子构成不同
(3)AC
[解析]氧气(O2)和臭氧(O3)都由氧元素组成,说明同种元素可以组成不同的物质,由同一种元素组成的物质不一定是纯净物,可能是混合物。
14.
(1)222 136
(2)稳定
[解析]
(1)由氡在元素周期表中的一格可知,氡的相对原子质量为222,中子数=222-86=136。
(2)由氡的原子结构示意图可知,氡原子的最外层电子数为8,达到相对稳定结构,既不易失去电子,也不易得到电子,化学性质稳定。
15.
(1)混合物 空气由不同种分子构成
(2)分子间的间隔 物理变化
(3)氧分子
[解析]
(1)空气中含有不同种分子,属于混合物。
(2)空气加压、降温的过程中分子间的间隔变小,分子种类不变该变化属于物理变化。
(3)空气中氮气的体积分数约为78%,氧气的体积分数约为21%,已知同温同压下,气体体积比等于分子个数比。因此,分子个数少的为氧分子,多的为氮分子,则“”表示的是氧分子。
16.
(1)一切物质都由原子构成原子不可再分原子是实心球体
(2)原子不可再分
(3)错误原子核外有很大的空间,电子就在这个空间做高速的运动,但不是做圆周运动,不存在确切的轨道
(4)模型
[解析]
(1)物质由分子、原子、离子构成。在化学反应中,原子不可再分,但原子并不是不可分割的实心球体
(2)汤姆生在原子内部发现了电子,说明原子并不是不可再分。
(3)原子核外有很大的空间,电子就在这个空间做高速的运动。
(4)为了帮助人们理解原子的结构,这几位科学家都运用了模型进行演示。
17.
(1)H Fe O
(2)剧烈燃烧,火星四射,放出热量,生成一种黑色固体
(3)硫+氧气二氧化硫
[解析]有一种氢元素的原子核内没有中子;铁是地壳中含量第二多的金属元素;根据燃烧时发出蓝紫色火焰,生成有刺激性气味的气体,可以判断是硫在氧气中燃烧。
18.瓶中水变红 分子在不断地运动 液面低于刻度线且距离较远分子间存在间隔便于观察液面变化
[解析]构成红色物质的分子不断运动到水中,使整瓶水变红。酒精分子运动到水分子间隔中,导致液体总体积变小。
19.
(1)液体变红 没有明显现象 空气
(2)a
(3)作对照
(4)③、②试管中的酚酞溶液先后变成红色
(5)ba
(6)慢 温度越低,分子运动速率越慢
(7)节省药品,防止污染空气等(合理即可)
[解析]
(1)实验一中,由于浓氨水具有挥发性,所以一段时间后,烧杯C中氨分子进入烧杯A中,使得烧杯A中液体变红。烧杯B放在空气中,没有现象,说明空气不会使酚酞溶液变红。
(2)若实验后发现烧杯B中的酚酞溶液也有少许变红,说明有氨分子进入烧杯B中,则a选项正确。
(3)试管⑤放有酚酞溶液的目的是对比,通过对比可知,空气中的物质不能使酚酞溶液变红色。
(4)由于温度越高,分子运动速率越快,所以④中氨分子运动快,③中的酚酞溶液先变红色。
(5)实验三中用胶头滴管吸取少许浓氨水,将其滴入T形三通管的细弯管处,然后用橡皮帽封闭管口。由于氨气的密度比空气的小,所以一段时间后会观察到ba段纱布条先变成红色。
(6)若将图丙中装有浓氨水的细弯管处浸入冰水中,可观察到纱布条变红的速率变慢,这是因为温度越低,分子运动速率越慢。
(7)对比图甲装置,图丙装置的药品用量少,而且对环境污染小。
20.
(1) -a(3分)
(2)a-4(3分)
[解析]
(1)A原子的相对原子质量为,相对原子质量近似等于质子数与中子数之和,A原子中的中子数= -a。
(2)A原子的质子数为a,失去两个电子形成A2+,则A2+的核外电子数为a-2。设B原子的质子数为b,B原子得到两个电子形成B2-,则B2-的核外电子数为b+2。a-2=b+2,则b=a-4。
21世纪教育网(www.21cnjy.com)
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
