无机非金属材料的主角——硅最终版
文档属性
| 名称 | 无机非金属材料的主角——硅最终版 |

|
|
| 格式 | zip | ||
| 文件大小 | 2.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2012-09-04 00:00:00 | ||
图片预览










文档简介
(共32张PPT)
美国的硅谷——“斯坦福科研工业区”是美国电子和计算机工业中心,位于美国西海岸加利福尼亚州北部旧金山南郊,圣克拉拉县和圣胡安两城之间的一条长48公里,宽16公里的长条形地带上。由于它集中了全世界90%以上的著名半导体公司,如思科、英特尔、惠普、朗讯、苹果等大公司,而半导体的基本元件是硅片,所以该地区被称为“硅谷”。
硅谷 silicon valley
美国的硅谷——“斯坦福科研工业区”是美国电子和计算机工业中心,位于美国西海岸加利福尼亚州北部旧金山南郊,圣克拉拉县和圣胡安两城之间的一条长48公里,宽16公里的长条形地带上。由于它集中了全世界90%以上的著名半导体公司,而半导体的基本元件是硅片,所以该地区被称为“硅谷”。
硅谷 silicon valley
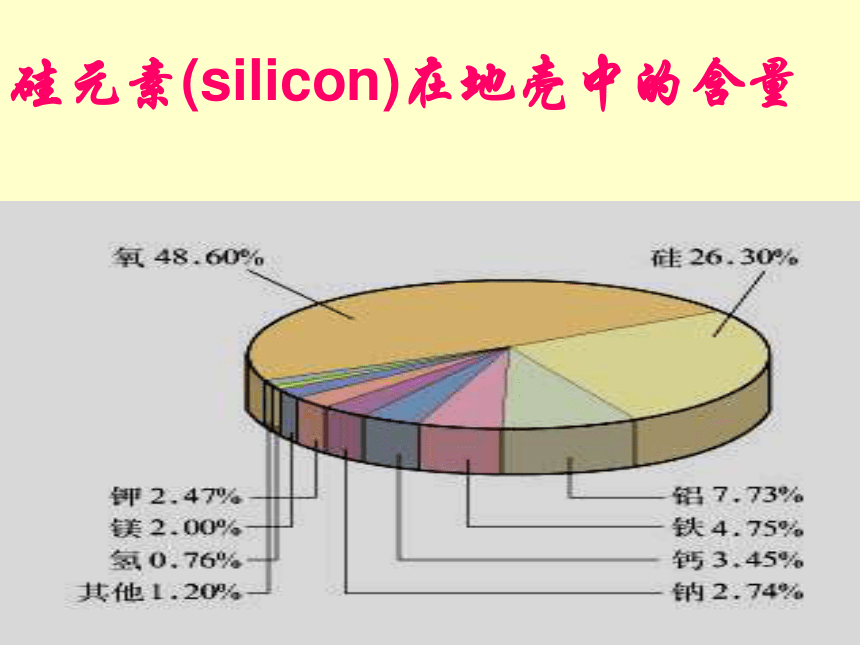
硅元素(silicon)在地壳中的含量
主要成分都是硅及其化合物
硅的氧化物及硅酸盐构成了地壳中大部分的岩石、沙子和土壤、约占地壳总量的90%以上。
第一节 无机非金属材料的主角________硅
Si
最外层电子数是4,碳也是。
思考2:碳、硅原子主要显几价?
正四价(+4价)
思考3:阅读《资料卡片》,比较碳、硅亲合氧的能力。
① 碳、硅都是亲氧元素。硅的亲氧性强于碳的亲氧性。
②因此硅元素在自然界都是与氧的化合物的形态存在。
思考1:硅原子最外层电子数是多少?我们很熟悉的哪种元素最外层电子数与它相同?
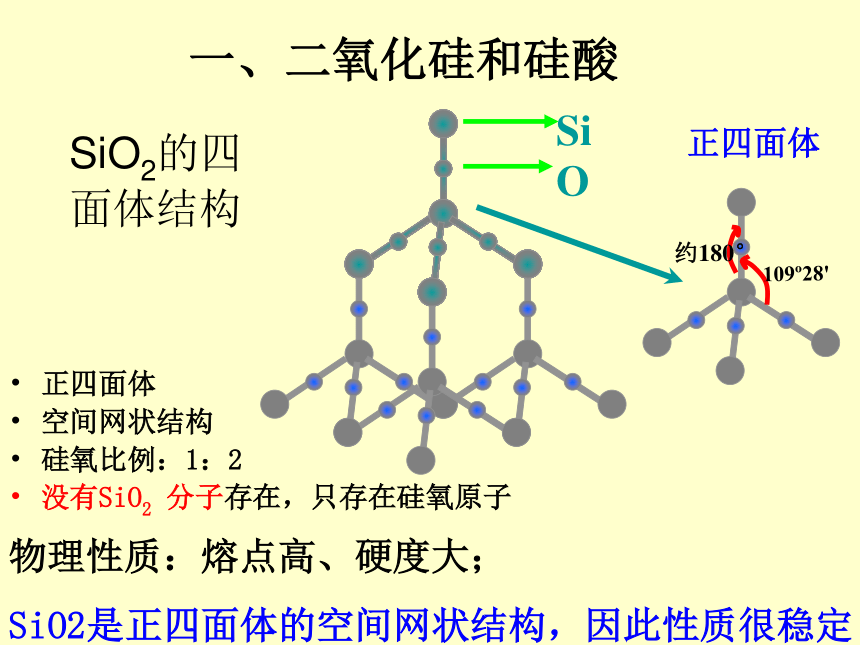
SiO2的四
面体结构
正四面体
空间网状结构
硅氧比例:1:2
没有SiO2 分子存在,只存在硅氧原子
物理性质:熔点高、硬度大;
SiO2是正四面体的空间网状结构,因此性质很稳定
109 28'
约180°
Si
O
正四面体
一、二氧化硅和硅酸
二氧化硅(SiO2)
二氧化硅广泛存在于自然界中,与其他矿物共同构成了岩石。天然二氧化硅也叫硅石,是一种坚硬难熔的固体。
硅石
硅矿山
天
然
的
SiO2
硅
石
有结晶形(石英晶体)
无定形——硅藻土
{
水晶
玛瑙
1、二氧化硅( SiO2 )
玛瑙
水晶
晶体二氧化硅
硅藻土
中国硅藻土资源丰富。全国10个省(区)
有硅藻土矿产出。探明储量的矿区有
354处,总保有储量矿石3.85亿吨。
仅次于美国,居世界第2位。在地区分
布上,以吉林最多,占全国储量的54.8%,
云南、福建、河北等地次之。矿床类型
主要为火山物源沉积型矿床(吉林长白、
山东临胸、浙江嵊州市硅藻土矿等)和
陆源沉积型(云南寻甸、四川米易硅藻
土矿等)矿床。成矿时代集中在第三纪
和第四纪,以第三纪为主。
无定形二氧化硅
一、二氧化硅(silicon dioxide)
水晶
玛瑙
透过图片思考:二氧化硅具有哪些物理性质 化学稳定性如何 你的根据是什么 SiO2的这些性质是由什么决定的?
坚硬难熔的固体,熔沸点比较高,不溶于水,硬度比较大。
1.物理性质:
一、二氧化硅(silicon dioxide)
实验室盛装NaOH溶液的试剂瓶用橡皮塞而不用玻璃塞,你知道为什么吗?
防止玻璃中的SiO2与NaOH溶液反应生成粘稠的Na2SiO3,使瓶塞和瓶口粘在一起
2.化学性质
②不能与水反应
SiO2 + CaO === CaSiO3
SiO2 + 2NaOH == Na2SiO3 + H2O
高温
① 是酸性氧化物
④不与酸反应(除氢氟酸以外)
SiO2 + 4HF == SiF4 + 2H2O
③在高温下与碳酸盐的反应
SiO2 + Na2CO3 == CO2 + Na2SiO3
高温
SiO2 + CaCO3 == CO2 + CaSiO3
高温
你知道吗?
玻璃花雕刻工艺和我们化学有什么深厚的合作关系?
2.化学性质
⑤弱氧化性
SiO2 +2C === Si + 2CO
高温
工业上用此反应制备粗硅,这就是“从沙滩到用户”!
2.化学性质
练一练:指出下列反应中SiO2所表现的化学性质或作用,在A-E选项中选择正确答案填入括号内。
①SiO2+2NaOH==Na2SiO3+H2O ( )
②SiO2+Na2CO3=高温=Na2SiO3+CO2 ( )
③SiO2+2C=高温=Si+2CO ( )
④ SiO2+4HF==SiF4 +2H2O ( )
A、作为玻璃的成分被消耗而使玻璃被腐蚀
B、弱氧化性 C、酸性氧化物的通性
D、将挥发性的酸酐从其盐中置换出来
C
D
B
A
3、二氧化硅的用途
由于SiO2具有优良的物理化学性能,加上SiO2在自然界的广泛存在,因此从古到今都被人类广泛地应用。
光学纤维胃镜
1.SiO2是制造光导纤维的主要原料
石 英 制 品
2.石英玻璃(结晶的二氧化硅)
用水晶,玛瑙制作的精美饰品,工艺品
3.用水晶,玛瑙制作的精美饰品,工艺品
CO2+H2O=H2CO3 ,但是SiO2不能与水直接化合成H2SiO3,这是一个特性。
刚才讲到SiO2不溶于水,不能直接和水化合成H2SiO3,那怎样制备H2SiO3呢?
提示:强酸制备弱酸!
二、硅酸(H2SiO3)
实验1:向饱和Na2SiO3溶液中,滴入酚酞,再滴入稀盐酸
现象
结论
方程式
滴入酚酞溶液呈红色,滴入盐酸有有白色胶状沉淀产生
Na2SiO3呈碱性,硅酸难溶于水
探究1:怎样由石英(SiO2)制取硅酸?
Na2SiO3+2HCl=2NaCl+H2SiO3↓
H2SiO3==H2O+SiO2
加热
硅酸的酸性比盐酸弱,那么硅酸酸性与碳酸相比较如何呢?请你设计一个实验论证你的推断。
实验探究2:
实验2:将CO2通入Na2SiO3溶液中
现象:透明的硅酸凝胶生成
方程式:
Na2SiO3+H2O+CO2==H2SiO3 ↓ +Na2CO3
你的结论:
硅酸是一种很弱的酸,
酸性:硅酸<碳酸<盐酸
硅酸凝胶经干燥脱水就形成干胶,称为“硅胶”。
硅胶多孔,吸附水份能力强,常用作实验室和袋装食品,瓶装药品等的干燥剂,也可以用作催化剂的载体。
1、下列各组物质有关性质关系的比较,正确的是( )
A.溶解性:CO2 H2CO3
C.熔点:SiO2 > CO2(干冰) D.硬度: SiO22、下列物质中,不能用玻璃瓶来盛装的是( )
A.烧碱溶液 B.浓硫酸 C.氢氟酸 D.碳酸钠溶液
3、要除去SiO2中的CaO杂质,最适宜的试剂是( )
A.纯碱溶液 B 盐酸 C 硫酸 D 苛性钠溶液
C
C
B
课堂回顾练习:
课堂练习
下列说法正确的是( )
A.SiO2是酸性氧化物,所以可以和碱反应,
不和任何酸反应。
B.CO2通入硅酸钠溶液中可以制得硅酸
C.SiO2对应的酸有不同的组成
D.SiO2跟水反应可得硅酸
BC
谢谢!
美国的硅谷——“斯坦福科研工业区”是美国电子和计算机工业中心,位于美国西海岸加利福尼亚州北部旧金山南郊,圣克拉拉县和圣胡安两城之间的一条长48公里,宽16公里的长条形地带上。由于它集中了全世界90%以上的著名半导体公司,如思科、英特尔、惠普、朗讯、苹果等大公司,而半导体的基本元件是硅片,所以该地区被称为“硅谷”。
硅谷 silicon valley
美国的硅谷——“斯坦福科研工业区”是美国电子和计算机工业中心,位于美国西海岸加利福尼亚州北部旧金山南郊,圣克拉拉县和圣胡安两城之间的一条长48公里,宽16公里的长条形地带上。由于它集中了全世界90%以上的著名半导体公司,而半导体的基本元件是硅片,所以该地区被称为“硅谷”。
硅谷 silicon valley
硅元素(silicon)在地壳中的含量
主要成分都是硅及其化合物
硅的氧化物及硅酸盐构成了地壳中大部分的岩石、沙子和土壤、约占地壳总量的90%以上。
第一节 无机非金属材料的主角________硅
Si
最外层电子数是4,碳也是。
思考2:碳、硅原子主要显几价?
正四价(+4价)
思考3:阅读《资料卡片》,比较碳、硅亲合氧的能力。
① 碳、硅都是亲氧元素。硅的亲氧性强于碳的亲氧性。
②因此硅元素在自然界都是与氧的化合物的形态存在。
思考1:硅原子最外层电子数是多少?我们很熟悉的哪种元素最外层电子数与它相同?
SiO2的四
面体结构
正四面体
空间网状结构
硅氧比例:1:2
没有SiO2 分子存在,只存在硅氧原子
物理性质:熔点高、硬度大;
SiO2是正四面体的空间网状结构,因此性质很稳定
109 28'
约180°
Si
O
正四面体
一、二氧化硅和硅酸
二氧化硅(SiO2)
二氧化硅广泛存在于自然界中,与其他矿物共同构成了岩石。天然二氧化硅也叫硅石,是一种坚硬难熔的固体。
硅石
硅矿山
天
然
的
SiO2
硅
石
有结晶形(石英晶体)
无定形——硅藻土
{
水晶
玛瑙
1、二氧化硅( SiO2 )
玛瑙
水晶
晶体二氧化硅
硅藻土
中国硅藻土资源丰富。全国10个省(区)
有硅藻土矿产出。探明储量的矿区有
354处,总保有储量矿石3.85亿吨。
仅次于美国,居世界第2位。在地区分
布上,以吉林最多,占全国储量的54.8%,
云南、福建、河北等地次之。矿床类型
主要为火山物源沉积型矿床(吉林长白、
山东临胸、浙江嵊州市硅藻土矿等)和
陆源沉积型(云南寻甸、四川米易硅藻
土矿等)矿床。成矿时代集中在第三纪
和第四纪,以第三纪为主。
无定形二氧化硅
一、二氧化硅(silicon dioxide)
水晶
玛瑙
透过图片思考:二氧化硅具有哪些物理性质 化学稳定性如何 你的根据是什么 SiO2的这些性质是由什么决定的?
坚硬难熔的固体,熔沸点比较高,不溶于水,硬度比较大。
1.物理性质:
一、二氧化硅(silicon dioxide)
实验室盛装NaOH溶液的试剂瓶用橡皮塞而不用玻璃塞,你知道为什么吗?
防止玻璃中的SiO2与NaOH溶液反应生成粘稠的Na2SiO3,使瓶塞和瓶口粘在一起
2.化学性质
②不能与水反应
SiO2 + CaO === CaSiO3
SiO2 + 2NaOH == Na2SiO3 + H2O
高温
① 是酸性氧化物
④不与酸反应(除氢氟酸以外)
SiO2 + 4HF == SiF4 + 2H2O
③在高温下与碳酸盐的反应
SiO2 + Na2CO3 == CO2 + Na2SiO3
高温
SiO2 + CaCO3 == CO2 + CaSiO3
高温
你知道吗?
玻璃花雕刻工艺和我们化学有什么深厚的合作关系?
2.化学性质
⑤弱氧化性
SiO2 +2C === Si + 2CO
高温
工业上用此反应制备粗硅,这就是“从沙滩到用户”!
2.化学性质
练一练:指出下列反应中SiO2所表现的化学性质或作用,在A-E选项中选择正确答案填入括号内。
①SiO2+2NaOH==Na2SiO3+H2O ( )
②SiO2+Na2CO3=高温=Na2SiO3+CO2 ( )
③SiO2+2C=高温=Si+2CO ( )
④ SiO2+4HF==SiF4 +2H2O ( )
A、作为玻璃的成分被消耗而使玻璃被腐蚀
B、弱氧化性 C、酸性氧化物的通性
D、将挥发性的酸酐从其盐中置换出来
C
D
B
A
3、二氧化硅的用途
由于SiO2具有优良的物理化学性能,加上SiO2在自然界的广泛存在,因此从古到今都被人类广泛地应用。
光学纤维胃镜
1.SiO2是制造光导纤维的主要原料
石 英 制 品
2.石英玻璃(结晶的二氧化硅)
用水晶,玛瑙制作的精美饰品,工艺品
3.用水晶,玛瑙制作的精美饰品,工艺品
CO2+H2O=H2CO3 ,但是SiO2不能与水直接化合成H2SiO3,这是一个特性。
刚才讲到SiO2不溶于水,不能直接和水化合成H2SiO3,那怎样制备H2SiO3呢?
提示:强酸制备弱酸!
二、硅酸(H2SiO3)
实验1:向饱和Na2SiO3溶液中,滴入酚酞,再滴入稀盐酸
现象
结论
方程式
滴入酚酞溶液呈红色,滴入盐酸有有白色胶状沉淀产生
Na2SiO3呈碱性,硅酸难溶于水
探究1:怎样由石英(SiO2)制取硅酸?
Na2SiO3+2HCl=2NaCl+H2SiO3↓
H2SiO3==H2O+SiO2
加热
硅酸的酸性比盐酸弱,那么硅酸酸性与碳酸相比较如何呢?请你设计一个实验论证你的推断。
实验探究2:
实验2:将CO2通入Na2SiO3溶液中
现象:透明的硅酸凝胶生成
方程式:
Na2SiO3+H2O+CO2==H2SiO3 ↓ +Na2CO3
你的结论:
硅酸是一种很弱的酸,
酸性:硅酸<碳酸<盐酸
硅酸凝胶经干燥脱水就形成干胶,称为“硅胶”。
硅胶多孔,吸附水份能力强,常用作实验室和袋装食品,瓶装药品等的干燥剂,也可以用作催化剂的载体。
1、下列各组物质有关性质关系的比较,正确的是( )
A.溶解性:CO2
C.熔点:SiO2 > CO2(干冰) D.硬度: SiO2
A.烧碱溶液 B.浓硫酸 C.氢氟酸 D.碳酸钠溶液
3、要除去SiO2中的CaO杂质,最适宜的试剂是( )
A.纯碱溶液 B 盐酸 C 硫酸 D 苛性钠溶液
C
C
B
课堂回顾练习:
课堂练习
下列说法正确的是( )
A.SiO2是酸性氧化物,所以可以和碱反应,
不和任何酸反应。
B.CO2通入硅酸钠溶液中可以制得硅酸
C.SiO2对应的酸有不同的组成
D.SiO2跟水反应可得硅酸
BC
谢谢!
