鲁教版(五四制)八年级全一册 第四单元 我们周围的空气 复习 课件(共46张PPT)
文档属性
| 名称 | 鲁教版(五四制)八年级全一册 第四单元 我们周围的空气 复习 课件(共46张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-10-30 00:00:00 | ||
图片预览





文档简介
(共46张PPT)
第四单元 我们周围的空气
复习课件
性质
物理性质:
化学性质
氧气
制法
与金属反应
(P、S、C)
(Fe、Mg、Al、Cu)
与非金属反应
检验:
实验室制法
工业制法:
分离液态空气
使带火星的木条复燃
存在:
占空气21%(体积分数)
知识纲要
H2O2分解
加热KMnO4
加热KClO3与MnO2
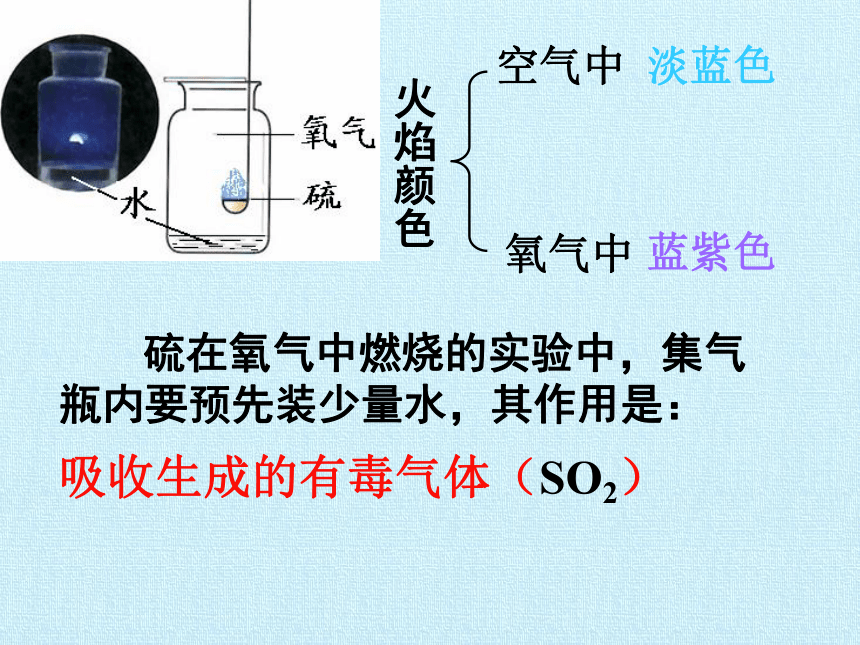
硫在氧气中燃烧的实验中,集气瓶内要预先装少量水,其作用是:
吸收生成的有毒气体(SO2)
火焰颜色
空气中
氧气中
淡蓝色
蓝紫色
细铁丝在氧气中燃烧的实验操作注意事项:
①火柴的作用:
②将铁丝绕成螺旋状:
③待火柴即将燃尽时再将铁丝伸入氧气瓶中:
④预先在集气瓶中装少量水或在瓶底铺一薄层 细沙:
引燃铁丝
增大铁丝的受热面积
防止火柴燃烧消耗过多的氧气而使铁丝不能顺利燃烧。
防止熔化物溅落炸裂集气瓶底。
氧化物
由两种元素组成,其中一种为氧元素的化合物。
化合物
含氧化
合物
氧化物
如:H2O、H2O2、MgO、CuO、MnO2、Fe3O4……
KMnO4是氧化物吗?为什么?
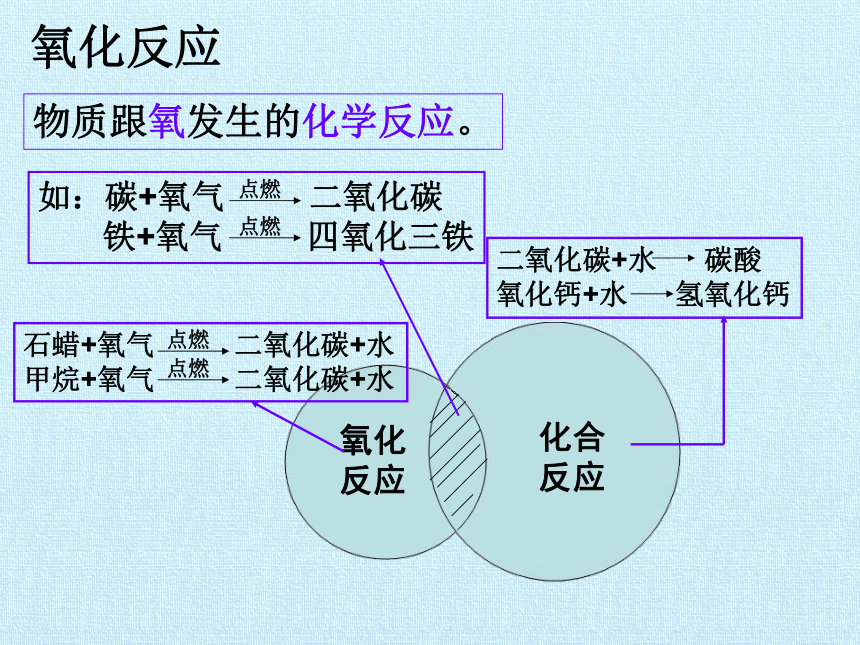
氧化反应
物质跟氧发生的化学反应。
如:碳+氧气 二氧化碳
铁+氧气 四氧化三铁
点燃
氧化
反应
化合
反应
石蜡+氧气 二氧化碳+水
甲烷+氧气 二氧化碳+水
点燃
点燃
二氧化碳+水 碳酸
氧化钙+水 氢氧化钙
点燃
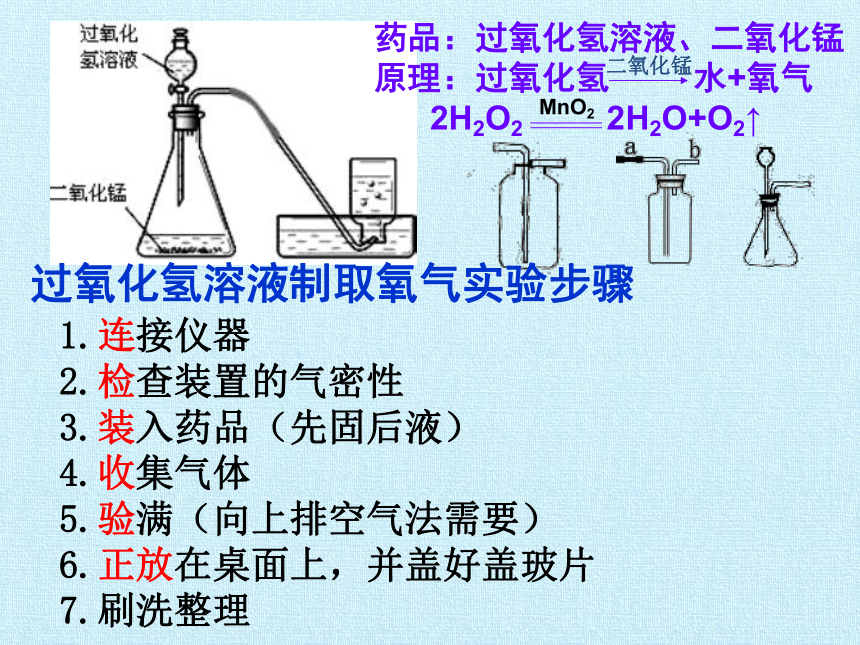
过氧化氢溶液制取氧气实验步骤
1.连接仪器
2.检查装置的气密性
3.装入药品(先固后液)
4.收集气体
5.验满(向上排空气法需要)
6.正放在桌面上,并盖好盖玻片
7.刷洗整理
药品:过氧化氢溶液、二氧化锰
原理:过氧化氢 水+氧气
2H2O2 2H2O+O2↑
二氧化锰
MnO2
催化剂:这种能改变化学反应的速率,而本身的质量和化学性质在反应前后没有发生变化的物质。
一变二不变
改变反应速率
本身质量、化学性质反应前后不变
催化剂在化学反应前后的物理性质可能变也可能不变
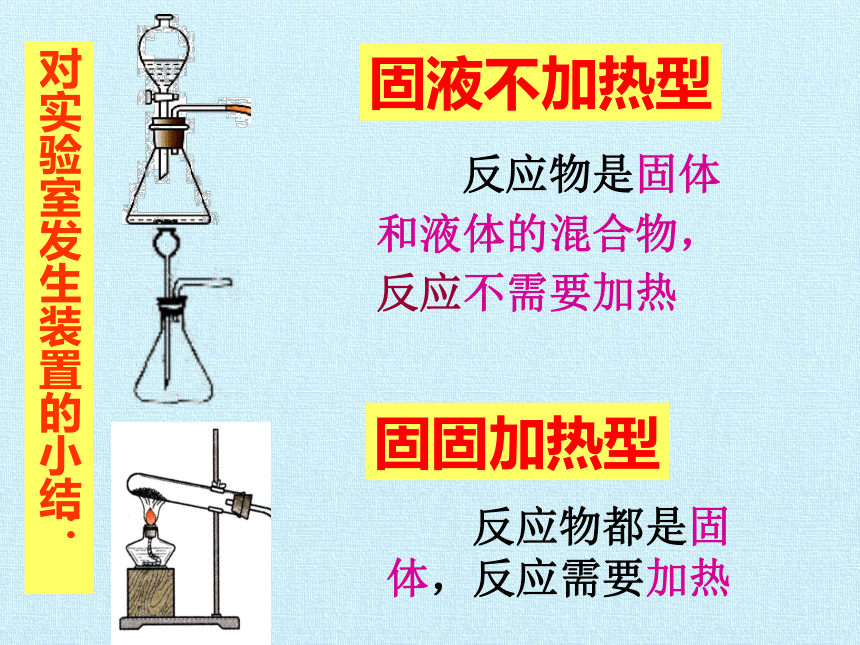
反应物都是固体,反应需要加热
反应物是固体和液体的混合物,反应不需要加热
固液不加热型
固固加热型
对实验室发生装置的小结:
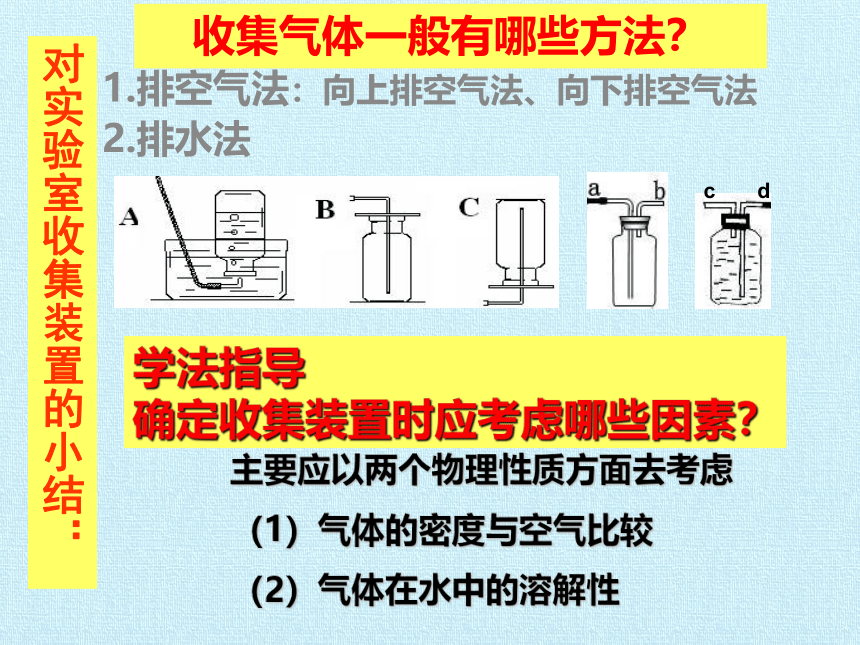
收集气体一般有哪些方法?
1.排空气法:向上排空气法、向下排空气法
2.排水法
学法指导
确定收集装置时应考虑哪些因素?
主要应以两个物理性质方面去考虑
(1)气体的密度与空气比较
(2)气体在水中的溶解性
对实验室收集装置的小结:
c d
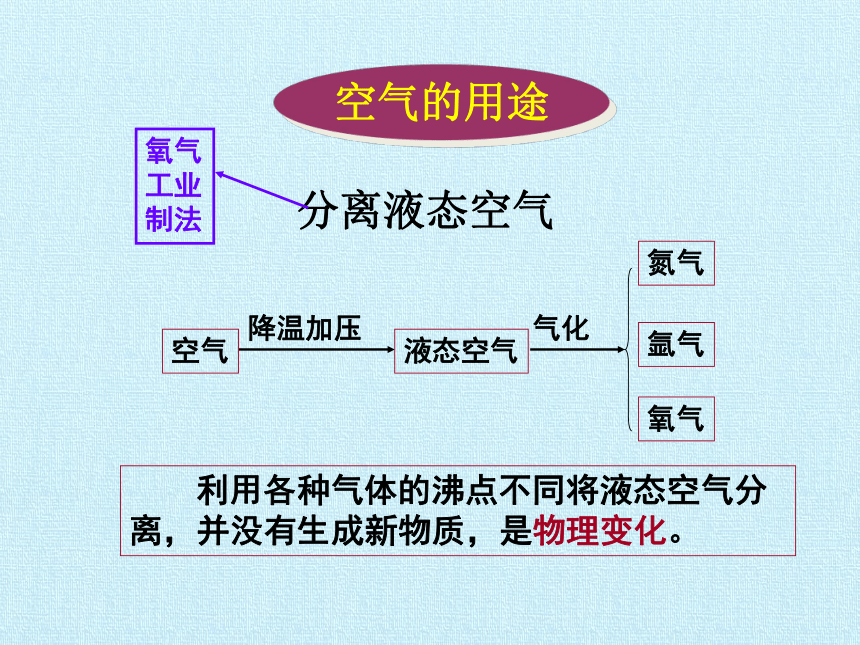
空气的用途
分离液态空气
空气
降温加压
液态空气
气化
氮气
氩气
氧气
利用各种气体的沸点不同将液态空气分离,并没有生成新物质,是物理变化。
氧气
工业
制法
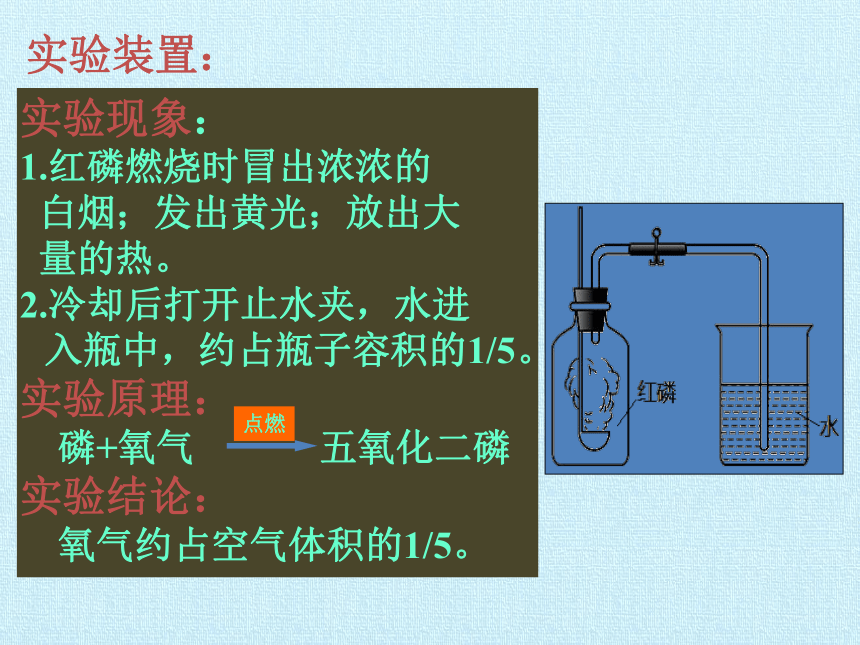
实验现象:
1.红磷燃烧时冒出浓浓的
白烟;发出黄光;放出大
量的热。
2.冷却后打开止水夹,水进
入瓶中,约占瓶子容积的1/5。
实验原理:
磷+氧气 五氧化二磷
实验结论:
氧气约占空气体积的1/5。
点燃
实验装置:
归纳与总结
空
气
1、空气的组成
2、空气是一种宝贵的自然资源
3、空气的污染与防治:
空气成分 氮 气 氧 气 稀有 气体 二氧 化碳 其它气体
和杂质
体积分数 78% 21%
有害气体
烟尘
污染源
二氧化硫SO2
一氧化碳CO
二氧化氮NO2
臭氧O3
可吸入颗粒物
总悬浮颗粒物
空气污染物
粉尘
有害气体
(如沙尘暴)
SO2
CO
NO2
减少使用含硫的化石燃料
植树造林
使燃料充分燃烧
例1:汽车安全气囊内的物质能在碰撞后10毫秒内生成空气中体积分数最大的气体,该气体是( )
A、O2 B、N2 C、CO2 D、稀有气体
B
例2:减少污染,净化空气,“还我一片蓝天”,已成为世界各国人民的共同心声。下列气体会造成空气污染的是( )
A、CO B、CO2 C、O2 D、N2
A
例3:如图所示装置可用于测定空气中氧气的含量。实验前在集气瓶内加入少量的水,并做上记号,下列说法中,不正确的是( )
A、点燃红磷前先用弹簧夹夹紧乳胶管
B、实验时红磷一定要过量
C、红磷熄灭后立即打开止水夹
D、最终进入瓶中水的
体积约为氧气的体积
C
红磷
水
思维拓展
硫粉
请问:将实验中的红磷改为硫粉、木炭或
铁丝实验能进行吗?
[思考]甲广口瓶内水面上升明显小于瓶内空气体积的1/5,乙广口瓶内水面上升明显大于瓶内空气体积的1/5。解释合理的是
甲同学可能使用红磷的量不足,瓶内氧
气没有消耗完
甲同学可能未塞紧瓶塞,红磷熄灭冷却
时外界空气进入瓶内
乙同学可能没夹紧弹簧夹,红磷燃烧时
瓶内部分空气受热从导管逸出
乙同学可能插入燃烧匙太慢,塞紧瓶塞
之前,瓶内部分空气受热逸出
若分解过氧化氢制取氧气,供选用的装置如下:
要得到平稳的氧气流,应选用哪个发生装置
甲
2、右图是某同学组装的验证氧气约占空气总体积1/5实验装置。下列操作不会对实验结果造成影响的是( )
A、弹簧夹没有夹紧
B、没有冷却就打开弹簧夹
C、红磷放过量了
D、燃烧匙内放木炭
1、下列物质在氧气中燃烧,能发出明亮的蓝紫色火焰,并产生刺激性气体的物质是( )
A、镁带 B、红磷 C、硫磺 D、木炭
课堂练习
C
C
3、根据下列仪器,回答:
小林拟选用仪器A、D、E、F、I再设计一套制取氧气的装置,他还需要选用的仪器是__________(填写仪器序号)。
答案参考图
H
4、请结合下图回答:
(1)实验室常用下列三种方法制取氧气
H2O2
O2
KClO3
KMnO4
若用方法甲,则发生装置应选___;甲乙两种方法都要用MnO2,它在反应中起_____作用。用甲方法制取氧气的方程式为_______。
(2)三种方法中,较好的方法是___,理由是:__________________________________________。
甲
乙
丙
B
催化
甲
无需加热,生成物无污染,操作简单
可以用推拉注射器活塞的方法检查下图中装置气密性。当缓慢拉活塞时,如果装置气密性良好,可以观察到的现象是( )
A.长颈漏斗下端口有气泡
B.瓶中液面上升
C.注射器内有液体
D.长颈漏斗内液面上升
我要挑战
A
一、化学式反映物质的组成
H2O、Fe、CuO、NaCl、Cu、CO2
化学式定义:
用元素符号和数字的组合表示纯净物组成的式子
组成元素
微粒个数比
纯净物都有其固定的组成
①任何物质都有化学式吗?
②同种物质可以有不同的化学式吗?
①只有纯净物才能用化学式表示其组成,
②一种物质只能用一个化学式来表示
③化学式可以任意的书写吗?
③化学式的书写必须依据客观事实,不能 主观臆造。
思考
注意:每一种纯净物都只有一种固 定的组成,因此每一种纯净物都只有一个对应的固定的化学式,而混合物没有固定的组成所以混合物没有化学式。
讨论:化学式H2O的含义(宏观和微观方面)
化学式表示的意义:4个
一种物质
该物质的组成元素
该物质的一个分子
该物质的分子构成
微观
宏观
一个原子
一种物质
一种元素
宏观
微观
如:Cu、He等
CO2
二氧化碳
二氧化碳由碳元素和氧元素组成
一个二氧化 碳分子
一个二氧化碳分子由一个碳原子和两个氧原子构成
练习:化学式CO2表示什么意义?
H2O
2
表示2个水分子
表示每个水分子
中有2个氢原子
(1)a表示有a个这样的微粒
(2)b表示一个分子中某种原子的个数.
化学式中数字的意义
aRb
c+
(3)c表示一个离子带c个单位正(负)电荷
思考:2H20中“2”表示的意义
+d
(4)d表示某元素的化合价为正(负)d价
拓展:指出下列化学符号中“2”的意义
①2H2 ②H2 ③ S2- ④2Fe
①表示2个氢气分子
②表示1个氢气分子是由2个氢原子构成
③表示带2个单位负电荷的硫离子
④表示2个铁原子
单质化学式的写法
单质
金属单质
非金属单质
直接用
元素符
号表示
稀有气体
固态
液、气态:
(除I外)
多数为双原子分子如:
氯气、氢气、氧气、氮气、碘
Cl2、H2、O2、N2、I2
练一练
根据以上规则写出下列物质的化学式:
氦气、氖气、氩气
氧气、氮气、氯气
臭氧
金属铝 金属铜 金刚石 固态磷
He
Ne
Ar
O2
N2
Cl2
O3
Al
Cu
C
P
下列符号只表示微观意义的是( )
A、H2 B、Cu C、2I D、O2
C
在下列符号中,既能表示一种元素,又能表示
这种元素的一个原子,还能表示一种物质的是( )
A、 H2 B、Cu C、I D、O
B
通常元素之间化合时,各元素的原子数目是一定的。这一定的数目反映了元素原子在形成化合物时所具有的化合价。
化合价
注:1、化合物中,元素的化合价是由这种元素的一个原子得失电子的数目决定。
2、有些情况下,不同元素之间相互化和是靠各自提供电子、形成共用电子对来实现,这种情况下,化合价的数值就是形成共用电子对的数目。
◆化合物中,通常氢为+1价,氧为-2价,金属元素显正价,非金属元素显负价。
如 :
◆元素的变价:许多元素的原子在不同的条件下可显示不同的化合价。
例:Fe为+2,+3
+1
H
O
-2
◆在化合物里正负化合价的代数和为零。
◆化合价是元素原子在形成化合物时表现出的性质,因此,单质分子中元素的化合价为零。
◆化合价的实质:是元素在形成化合物时表现出
的化学性质。取决于原子最外层电子数。
◆化合价有正价和负价。
化合物的化学式书写
正前、负后、交叉、化简
Al
+3
O
-2
3
Al2O3
依据:客观事实和化合物里各元素正负化合价代数和为0
例1:写出由铝和氧两元素组成化合物的化学式
2
活动与探究
写出下列物质的化学式
锌、氧气、氮气、氩气、硫磺、水银、木炭、白磷、红磷、铁、臭氧
氧化铝、氧化镁、氧化银
硫酸钡、硝酸银、碳酸钠
氯化钠、硫化钾、氯化氢
简单化合物的命名
两种元素组成的的化合物,
读成“某化某”、“某化亚某”。
有酸根原子团的,
读成“某酸某”、“某酸亚某”。
有氢氧根原子团的,
读成“氢氧化某”、“氢氧化亚某”。
活动与探究
读出下列物质的名称
Al2O3、Fe2O3、Fe3O4、FeO、P2O5、HCl
Mg(NO3)2、CuSO4、(NH4)2SO4
NaOH、Al(OH)3
H2O、NH3
Cu、Hg、Al、O2、Ar、H2、N2
物质组成元素的质量比=各原子的相对原子质量×原子个数比
原子个数比=元素的质量比/各原子的相对原子质量
学法指导:在计算相对分子质量时应注意:同种元素的原子可以合并计算。
相对分子质量(Mr):在数值上等于化学式中各原子的相对原子质量的总和。
某元素的质量分数
某元素的总质量
物质的总质量
×100%
=
某元素的相对原子质量×原子个数
相对分子质量
×100%
=
元素的质量=纯物质的质量×元素的质量分数
元素的质量
元素的质量分数
纯物质的质量=
某铁与氧形成的化合物中,铁元素与氧元素的质量比为7:2,试确定该化合物的化学式
设该物质的化学式为FemOn
56m
16n
=
7
2
m
n
=
1
1
故可得化学式为:FeO
逆向运用
则
各成分
用途
分离液
态空气
发现史
污染来源
防治措施
空气质
量报告
元素质
量分数
元素的
质量比
相对分
子质量
意义
书写
读法
记忆
规则
应用
原理
装置
验满
步骤
物理性质
化学性质
谢 谢
第四单元 我们周围的空气
复习课件
性质
物理性质:
化学性质
氧气
制法
与金属反应
(P、S、C)
(Fe、Mg、Al、Cu)
与非金属反应
检验:
实验室制法
工业制法:
分离液态空气
使带火星的木条复燃
存在:
占空气21%(体积分数)
知识纲要
H2O2分解
加热KMnO4
加热KClO3与MnO2
硫在氧气中燃烧的实验中,集气瓶内要预先装少量水,其作用是:
吸收生成的有毒气体(SO2)
火焰颜色
空气中
氧气中
淡蓝色
蓝紫色
细铁丝在氧气中燃烧的实验操作注意事项:
①火柴的作用:
②将铁丝绕成螺旋状:
③待火柴即将燃尽时再将铁丝伸入氧气瓶中:
④预先在集气瓶中装少量水或在瓶底铺一薄层 细沙:
引燃铁丝
增大铁丝的受热面积
防止火柴燃烧消耗过多的氧气而使铁丝不能顺利燃烧。
防止熔化物溅落炸裂集气瓶底。
氧化物
由两种元素组成,其中一种为氧元素的化合物。
化合物
含氧化
合物
氧化物
如:H2O、H2O2、MgO、CuO、MnO2、Fe3O4……
KMnO4是氧化物吗?为什么?
氧化反应
物质跟氧发生的化学反应。
如:碳+氧气 二氧化碳
铁+氧气 四氧化三铁
点燃
氧化
反应
化合
反应
石蜡+氧气 二氧化碳+水
甲烷+氧气 二氧化碳+水
点燃
点燃
二氧化碳+水 碳酸
氧化钙+水 氢氧化钙
点燃
过氧化氢溶液制取氧气实验步骤
1.连接仪器
2.检查装置的气密性
3.装入药品(先固后液)
4.收集气体
5.验满(向上排空气法需要)
6.正放在桌面上,并盖好盖玻片
7.刷洗整理
药品:过氧化氢溶液、二氧化锰
原理:过氧化氢 水+氧气
2H2O2 2H2O+O2↑
二氧化锰
MnO2
催化剂:这种能改变化学反应的速率,而本身的质量和化学性质在反应前后没有发生变化的物质。
一变二不变
改变反应速率
本身质量、化学性质反应前后不变
催化剂在化学反应前后的物理性质可能变也可能不变
反应物都是固体,反应需要加热
反应物是固体和液体的混合物,反应不需要加热
固液不加热型
固固加热型
对实验室发生装置的小结:
收集气体一般有哪些方法?
1.排空气法:向上排空气法、向下排空气法
2.排水法
学法指导
确定收集装置时应考虑哪些因素?
主要应以两个物理性质方面去考虑
(1)气体的密度与空气比较
(2)气体在水中的溶解性
对实验室收集装置的小结:
c d
空气的用途
分离液态空气
空气
降温加压
液态空气
气化
氮气
氩气
氧气
利用各种气体的沸点不同将液态空气分离,并没有生成新物质,是物理变化。
氧气
工业
制法
实验现象:
1.红磷燃烧时冒出浓浓的
白烟;发出黄光;放出大
量的热。
2.冷却后打开止水夹,水进
入瓶中,约占瓶子容积的1/5。
实验原理:
磷+氧气 五氧化二磷
实验结论:
氧气约占空气体积的1/5。
点燃
实验装置:
归纳与总结
空
气
1、空气的组成
2、空气是一种宝贵的自然资源
3、空气的污染与防治:
空气成分 氮 气 氧 气 稀有 气体 二氧 化碳 其它气体
和杂质
体积分数 78% 21%
有害气体
烟尘
污染源
二氧化硫SO2
一氧化碳CO
二氧化氮NO2
臭氧O3
可吸入颗粒物
总悬浮颗粒物
空气污染物
粉尘
有害气体
(如沙尘暴)
SO2
CO
NO2
减少使用含硫的化石燃料
植树造林
使燃料充分燃烧
例1:汽车安全气囊内的物质能在碰撞后10毫秒内生成空气中体积分数最大的气体,该气体是( )
A、O2 B、N2 C、CO2 D、稀有气体
B
例2:减少污染,净化空气,“还我一片蓝天”,已成为世界各国人民的共同心声。下列气体会造成空气污染的是( )
A、CO B、CO2 C、O2 D、N2
A
例3:如图所示装置可用于测定空气中氧气的含量。实验前在集气瓶内加入少量的水,并做上记号,下列说法中,不正确的是( )
A、点燃红磷前先用弹簧夹夹紧乳胶管
B、实验时红磷一定要过量
C、红磷熄灭后立即打开止水夹
D、最终进入瓶中水的
体积约为氧气的体积
C
红磷
水
思维拓展
硫粉
请问:将实验中的红磷改为硫粉、木炭或
铁丝实验能进行吗?
[思考]甲广口瓶内水面上升明显小于瓶内空气体积的1/5,乙广口瓶内水面上升明显大于瓶内空气体积的1/5。解释合理的是
甲同学可能使用红磷的量不足,瓶内氧
气没有消耗完
甲同学可能未塞紧瓶塞,红磷熄灭冷却
时外界空气进入瓶内
乙同学可能没夹紧弹簧夹,红磷燃烧时
瓶内部分空气受热从导管逸出
乙同学可能插入燃烧匙太慢,塞紧瓶塞
之前,瓶内部分空气受热逸出
若分解过氧化氢制取氧气,供选用的装置如下:
要得到平稳的氧气流,应选用哪个发生装置
甲
2、右图是某同学组装的验证氧气约占空气总体积1/5实验装置。下列操作不会对实验结果造成影响的是( )
A、弹簧夹没有夹紧
B、没有冷却就打开弹簧夹
C、红磷放过量了
D、燃烧匙内放木炭
1、下列物质在氧气中燃烧,能发出明亮的蓝紫色火焰,并产生刺激性气体的物质是( )
A、镁带 B、红磷 C、硫磺 D、木炭
课堂练习
C
C
3、根据下列仪器,回答:
小林拟选用仪器A、D、E、F、I再设计一套制取氧气的装置,他还需要选用的仪器是__________(填写仪器序号)。
答案参考图
H
4、请结合下图回答:
(1)实验室常用下列三种方法制取氧气
H2O2
O2
KClO3
KMnO4
若用方法甲,则发生装置应选___;甲乙两种方法都要用MnO2,它在反应中起_____作用。用甲方法制取氧气的方程式为_______。
(2)三种方法中,较好的方法是___,理由是:__________________________________________。
甲
乙
丙
B
催化
甲
无需加热,生成物无污染,操作简单
可以用推拉注射器活塞的方法检查下图中装置气密性。当缓慢拉活塞时,如果装置气密性良好,可以观察到的现象是( )
A.长颈漏斗下端口有气泡
B.瓶中液面上升
C.注射器内有液体
D.长颈漏斗内液面上升
我要挑战
A
一、化学式反映物质的组成
H2O、Fe、CuO、NaCl、Cu、CO2
化学式定义:
用元素符号和数字的组合表示纯净物组成的式子
组成元素
微粒个数比
纯净物都有其固定的组成
①任何物质都有化学式吗?
②同种物质可以有不同的化学式吗?
①只有纯净物才能用化学式表示其组成,
②一种物质只能用一个化学式来表示
③化学式可以任意的书写吗?
③化学式的书写必须依据客观事实,不能 主观臆造。
思考
注意:每一种纯净物都只有一种固 定的组成,因此每一种纯净物都只有一个对应的固定的化学式,而混合物没有固定的组成所以混合物没有化学式。
讨论:化学式H2O的含义(宏观和微观方面)
化学式表示的意义:4个
一种物质
该物质的组成元素
该物质的一个分子
该物质的分子构成
微观
宏观
一个原子
一种物质
一种元素
宏观
微观
如:Cu、He等
CO2
二氧化碳
二氧化碳由碳元素和氧元素组成
一个二氧化 碳分子
一个二氧化碳分子由一个碳原子和两个氧原子构成
练习:化学式CO2表示什么意义?
H2O
2
表示2个水分子
表示每个水分子
中有2个氢原子
(1)a表示有a个这样的微粒
(2)b表示一个分子中某种原子的个数.
化学式中数字的意义
aRb
c+
(3)c表示一个离子带c个单位正(负)电荷
思考:2H20中“2”表示的意义
+d
(4)d表示某元素的化合价为正(负)d价
拓展:指出下列化学符号中“2”的意义
①2H2 ②H2 ③ S2- ④2Fe
①表示2个氢气分子
②表示1个氢气分子是由2个氢原子构成
③表示带2个单位负电荷的硫离子
④表示2个铁原子
单质化学式的写法
单质
金属单质
非金属单质
直接用
元素符
号表示
稀有气体
固态
液、气态:
(除I外)
多数为双原子分子如:
氯气、氢气、氧气、氮气、碘
Cl2、H2、O2、N2、I2
练一练
根据以上规则写出下列物质的化学式:
氦气、氖气、氩气
氧气、氮气、氯气
臭氧
金属铝 金属铜 金刚石 固态磷
He
Ne
Ar
O2
N2
Cl2
O3
Al
Cu
C
P
下列符号只表示微观意义的是( )
A、H2 B、Cu C、2I D、O2
C
在下列符号中,既能表示一种元素,又能表示
这种元素的一个原子,还能表示一种物质的是( )
A、 H2 B、Cu C、I D、O
B
通常元素之间化合时,各元素的原子数目是一定的。这一定的数目反映了元素原子在形成化合物时所具有的化合价。
化合价
注:1、化合物中,元素的化合价是由这种元素的一个原子得失电子的数目决定。
2、有些情况下,不同元素之间相互化和是靠各自提供电子、形成共用电子对来实现,这种情况下,化合价的数值就是形成共用电子对的数目。
◆化合物中,通常氢为+1价,氧为-2价,金属元素显正价,非金属元素显负价。
如 :
◆元素的变价:许多元素的原子在不同的条件下可显示不同的化合价。
例:Fe为+2,+3
+1
H
O
-2
◆在化合物里正负化合价的代数和为零。
◆化合价是元素原子在形成化合物时表现出的性质,因此,单质分子中元素的化合价为零。
◆化合价的实质:是元素在形成化合物时表现出
的化学性质。取决于原子最外层电子数。
◆化合价有正价和负价。
化合物的化学式书写
正前、负后、交叉、化简
Al
+3
O
-2
3
Al2O3
依据:客观事实和化合物里各元素正负化合价代数和为0
例1:写出由铝和氧两元素组成化合物的化学式
2
活动与探究
写出下列物质的化学式
锌、氧气、氮气、氩气、硫磺、水银、木炭、白磷、红磷、铁、臭氧
氧化铝、氧化镁、氧化银
硫酸钡、硝酸银、碳酸钠
氯化钠、硫化钾、氯化氢
简单化合物的命名
两种元素组成的的化合物,
读成“某化某”、“某化亚某”。
有酸根原子团的,
读成“某酸某”、“某酸亚某”。
有氢氧根原子团的,
读成“氢氧化某”、“氢氧化亚某”。
活动与探究
读出下列物质的名称
Al2O3、Fe2O3、Fe3O4、FeO、P2O5、HCl
Mg(NO3)2、CuSO4、(NH4)2SO4
NaOH、Al(OH)3
H2O、NH3
Cu、Hg、Al、O2、Ar、H2、N2
物质组成元素的质量比=各原子的相对原子质量×原子个数比
原子个数比=元素的质量比/各原子的相对原子质量
学法指导:在计算相对分子质量时应注意:同种元素的原子可以合并计算。
相对分子质量(Mr):在数值上等于化学式中各原子的相对原子质量的总和。
某元素的质量分数
某元素的总质量
物质的总质量
×100%
=
某元素的相对原子质量×原子个数
相对分子质量
×100%
=
元素的质量=纯物质的质量×元素的质量分数
元素的质量
元素的质量分数
纯物质的质量=
某铁与氧形成的化合物中,铁元素与氧元素的质量比为7:2,试确定该化合物的化学式
设该物质的化学式为FemOn
56m
16n
=
7
2
m
n
=
1
1
故可得化学式为:FeO
逆向运用
则
各成分
用途
分离液
态空气
发现史
污染来源
防治措施
空气质
量报告
元素质
量分数
元素的
质量比
相对分
子质量
意义
书写
读法
记忆
规则
应用
原理
装置
验满
步骤
物理性质
化学性质
谢 谢
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 自然界中的水
- 第三节 水分子的变化
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 物质构成的奥秘
- 第一节 原子的构成
- 第二节 元素
- 第三节 物质组成的表示
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去 二氧化碳的实验室制取与性质
