鲁教版(五四制)八年级全一册 到实验室去 二氧化碳的实验室制取与性质(1)(课件)(20张PP)
文档属性
| 名称 | 鲁教版(五四制)八年级全一册 到实验室去 二氧化碳的实验室制取与性质(1)(课件)(20张PP) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-10-31 00:00:00 | ||
图片预览





文档简介
(共20张PPT)
到实验室去 二氧化碳的实验室制取与性质
猜一猜?
1750年,英国物理学家布莱克在石灰石煅烧前后分别称其重量,发现煅烧后减轻了44%,他断定这是因为有气体从中放出的缘故。由于这种气体是固定在石灰石中的,他就将它命名为“固定空气”。但是很快他又发现石灰石中加入酸后也会产生这种“固定空气”的气。大家知道这是什么气体吗?
课 题 2
二氧化碳制取的研究
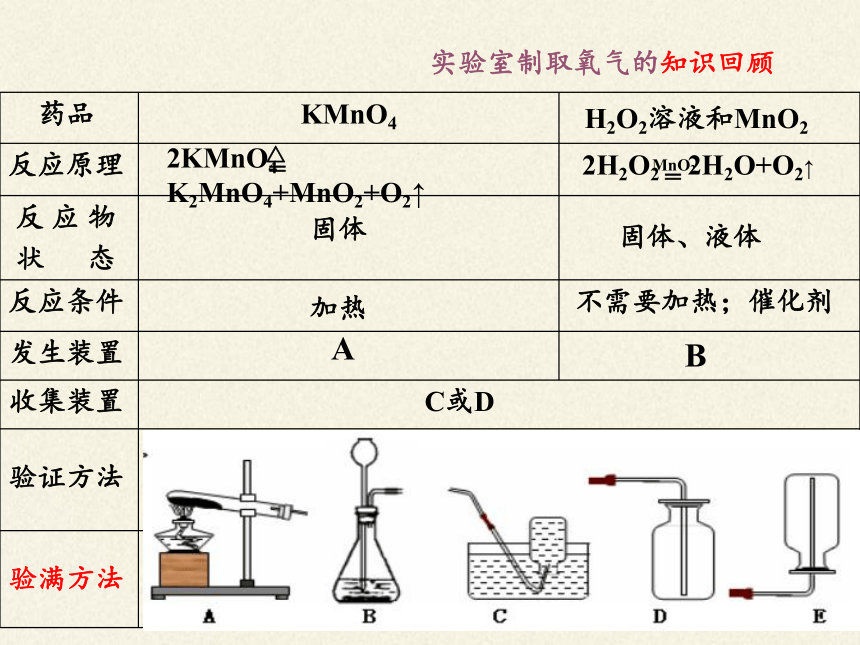
实验室制取氧气的知识回顾
药品 KMnO4 H2O2溶液和MnO2
反应原理
反 应 物 状 态
反应条件
发生装置
收集装置
验证方法
验满方法
A
B
C或D
用带火星的木条伸进瓶内,木条复燃,则该气体是氧气。
用带火星的木条放在瓶口,木条复燃,则氧气已满。
固体
加热
固体、液体
不需要加热;催化剂
2KMnO4 K2MnO4+MnO2+O2↑
2H2O2 2H2O+O2↑
=
=
△
MnO2
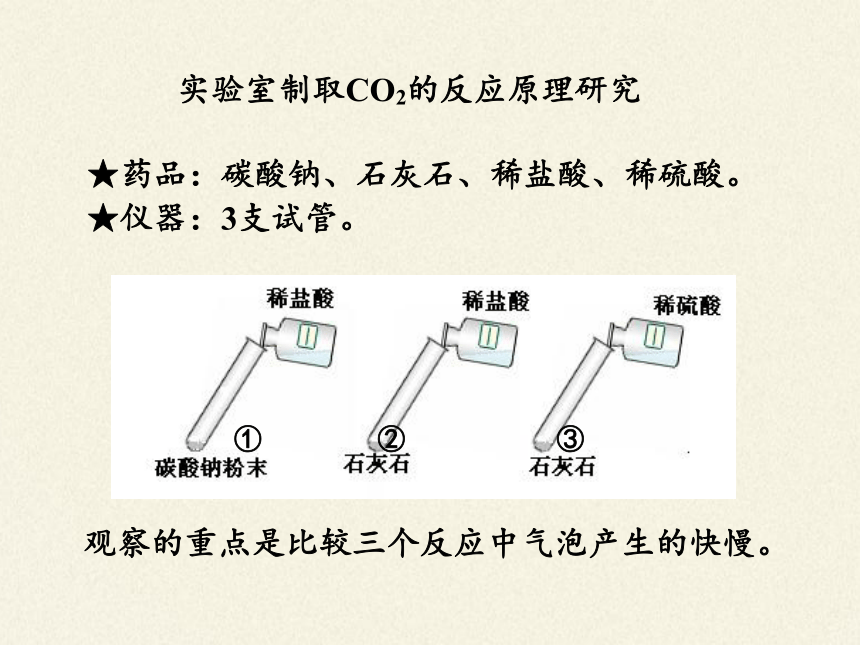
★药品:碳酸钠、石灰石、稀盐酸、稀硫酸。
★仪器:3支试管。
① ② ③
观察的重点是比较三个反应中气泡产生的快慢。
实验室制取CO2的反应原理研究
实验药品 实验现象对比
编号 实验内容 实验现象 实验分析
1 Na2CO3粉末和稀盐酸
2 大理石和稀盐酸
3 大理石和稀硫酸
实验室里制取二氧化碳的最佳反应是 ?
有大量气泡产生,反应剧烈
反应速率太快,不易收集
产生气泡速率比较适中
适合实验室制取二氧化碳气体
刚开始有气泡产生,一段时间后,反应逐渐停止
一段时间后,反应逐渐停止,不适合制取
实验室制取二氧化碳的反应原理
●药 品
●化学方程式
CaCO3+2HCl=CaCl2+H2CO3
H2CO3=H2O+CO2↑
H2CO3
石灰石
(大理石)
稀盐酸
主要成分
主要成分
CaCO3
HCl、H2O
CaCO3+2HCl = CaCl2+
H2O+CO2↑
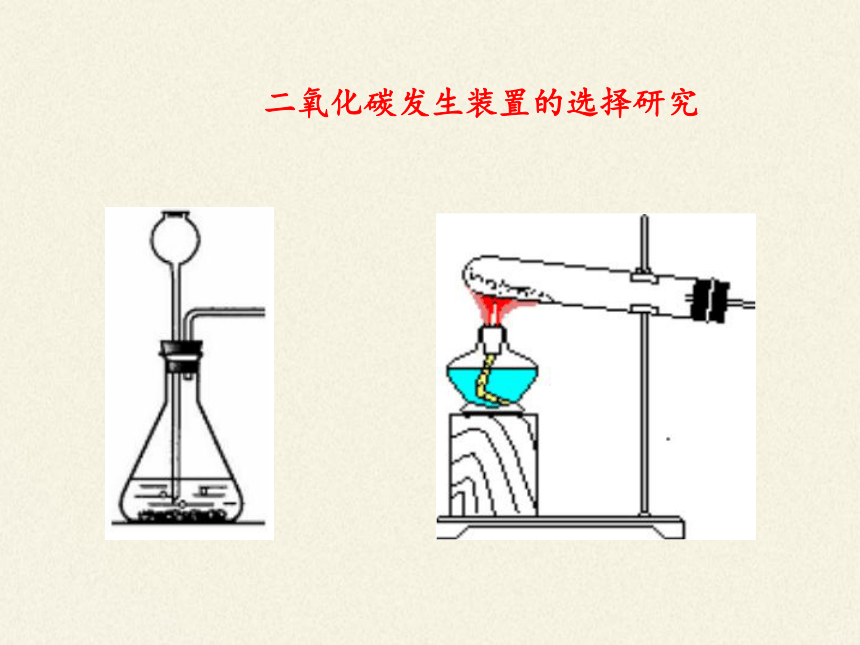
二氧化碳发生装置的选择研究
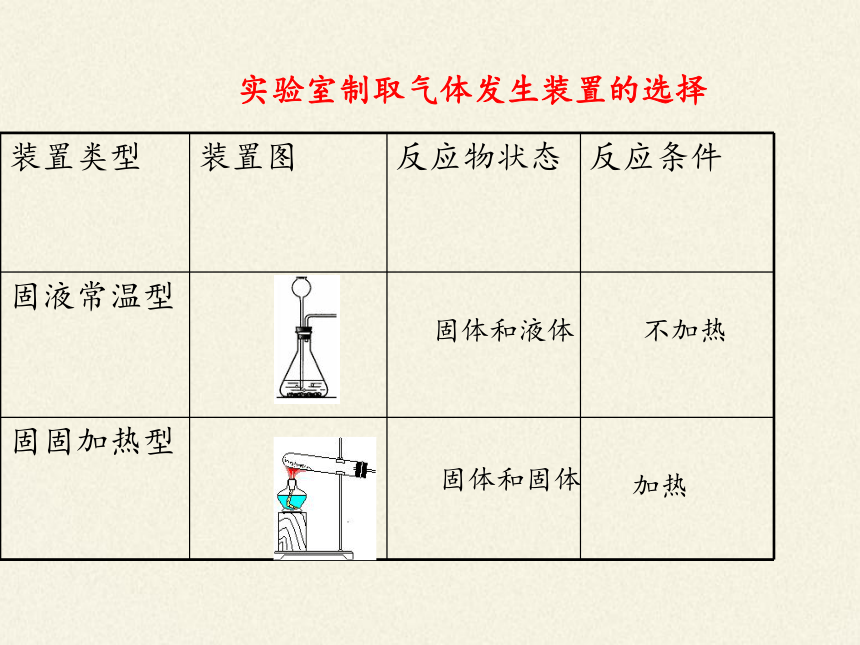
实验室制取气体发生装置的选择
装置类型 装置图 反应物状态 反应条件
固液常温型
固固加热型
固体和液体
固体和固体
不加热
加热
×
×
×
小组合作画装置的组装
以下是设计的部份装置可供参考
1、气体发生装置
A
B
C
D
E
F
G
讨论:用了长颈漏斗的二氧化碳发生装置,如何检查其气密性?
结论:用弹簧夹夹紧胶皮管,向长颈漏斗中加水,形成液封,如果其中的液面保持不变,则说明装置的气密性良好。
气体收集装置的选择研究
排水法
向下排空气法
向上排空气法
气体收集装置
排空气法
排水法
密度比空气大的气体 ----向上排气法
密度比空气小的气体 ----向下排气法
(不易溶于水、不与水反应)
研究CO2的验证方法和验满方法
◆验证二氧化碳气体的方法:
◆验满二氧化碳气体的方法:
将待检验的气体通入澄清的石灰水中,澄清石
灰水变浑浊,证明气体是CO2。
用燃着的木条放在集气瓶口,木条熄灭,说明
CO2已经集满。
检验方法
澄清石灰水
变浑浊
验满方法
实验室制取二氧化碳的步骤:
连、检、装、收、验
发生装置和收集装置
反应物及化学反应的方程式
利用气体的化学性质
实验室制取气体的研究思路
反应原理
制取装置
验证验满方法
实验室用固体氯化铵(NH4Cl)与固体
氢氧化钠在加热的条件下制取氨气(NH3),
化学方程式为
NH4Cl+NaOH====NaCl+NH3↑+H2O,
氨气的密度比空气的密度小,能溶于水
形成氨水。根据以上知识推断:
实验室制取NH3应选用的发生装置
是 ,收集装置是 ;
组合装置是 。
A
E
AE
1、实验室制取CO2最好选用_______________和__________反应。
2、实验室收集CO2的最好方法是____________。
3、实验室制取CO2的化学方程式是______。
4、检验CO2收集满的方法是____________。
5、检验CO2的存在用_______________。
石灰石(或大理石)
稀盐酸
向上排空气法
澄清石灰水
随堂检测:
用燃着的木条伸到集气瓶口,木条熄灭,则证明已经收集满了。
CaCO3+2HCl=CaCl2+H2O+CO2↑
谢 谢
到实验室去 二氧化碳的实验室制取与性质
猜一猜?
1750年,英国物理学家布莱克在石灰石煅烧前后分别称其重量,发现煅烧后减轻了44%,他断定这是因为有气体从中放出的缘故。由于这种气体是固定在石灰石中的,他就将它命名为“固定空气”。但是很快他又发现石灰石中加入酸后也会产生这种“固定空气”的气。大家知道这是什么气体吗?
课 题 2
二氧化碳制取的研究
实验室制取氧气的知识回顾
药品 KMnO4 H2O2溶液和MnO2
反应原理
反 应 物 状 态
反应条件
发生装置
收集装置
验证方法
验满方法
A
B
C或D
用带火星的木条伸进瓶内,木条复燃,则该气体是氧气。
用带火星的木条放在瓶口,木条复燃,则氧气已满。
固体
加热
固体、液体
不需要加热;催化剂
2KMnO4 K2MnO4+MnO2+O2↑
2H2O2 2H2O+O2↑
=
=
△
MnO2
★药品:碳酸钠、石灰石、稀盐酸、稀硫酸。
★仪器:3支试管。
① ② ③
观察的重点是比较三个反应中气泡产生的快慢。
实验室制取CO2的反应原理研究
实验药品 实验现象对比
编号 实验内容 实验现象 实验分析
1 Na2CO3粉末和稀盐酸
2 大理石和稀盐酸
3 大理石和稀硫酸
实验室里制取二氧化碳的最佳反应是 ?
有大量气泡产生,反应剧烈
反应速率太快,不易收集
产生气泡速率比较适中
适合实验室制取二氧化碳气体
刚开始有气泡产生,一段时间后,反应逐渐停止
一段时间后,反应逐渐停止,不适合制取
实验室制取二氧化碳的反应原理
●药 品
●化学方程式
CaCO3+2HCl=CaCl2+H2CO3
H2CO3=H2O+CO2↑
H2CO3
石灰石
(大理石)
稀盐酸
主要成分
主要成分
CaCO3
HCl、H2O
CaCO3+2HCl = CaCl2+
H2O+CO2↑
二氧化碳发生装置的选择研究
实验室制取气体发生装置的选择
装置类型 装置图 反应物状态 反应条件
固液常温型
固固加热型
固体和液体
固体和固体
不加热
加热
×
×
×
小组合作画装置的组装
以下是设计的部份装置可供参考
1、气体发生装置
A
B
C
D
E
F
G
讨论:用了长颈漏斗的二氧化碳发生装置,如何检查其气密性?
结论:用弹簧夹夹紧胶皮管,向长颈漏斗中加水,形成液封,如果其中的液面保持不变,则说明装置的气密性良好。
气体收集装置的选择研究
排水法
向下排空气法
向上排空气法
气体收集装置
排空气法
排水法
密度比空气大的气体 ----向上排气法
密度比空气小的气体 ----向下排气法
(不易溶于水、不与水反应)
研究CO2的验证方法和验满方法
◆验证二氧化碳气体的方法:
◆验满二氧化碳气体的方法:
将待检验的气体通入澄清的石灰水中,澄清石
灰水变浑浊,证明气体是CO2。
用燃着的木条放在集气瓶口,木条熄灭,说明
CO2已经集满。
检验方法
澄清石灰水
变浑浊
验满方法
实验室制取二氧化碳的步骤:
连、检、装、收、验
发生装置和收集装置
反应物及化学反应的方程式
利用气体的化学性质
实验室制取气体的研究思路
反应原理
制取装置
验证验满方法
实验室用固体氯化铵(NH4Cl)与固体
氢氧化钠在加热的条件下制取氨气(NH3),
化学方程式为
NH4Cl+NaOH====NaCl+NH3↑+H2O,
氨气的密度比空气的密度小,能溶于水
形成氨水。根据以上知识推断:
实验室制取NH3应选用的发生装置
是 ,收集装置是 ;
组合装置是 。
A
E
AE
1、实验室制取CO2最好选用_______________和__________反应。
2、实验室收集CO2的最好方法是____________。
3、实验室制取CO2的化学方程式是______。
4、检验CO2收集满的方法是____________。
5、检验CO2的存在用_______________。
石灰石(或大理石)
稀盐酸
向上排空气法
澄清石灰水
随堂检测:
用燃着的木条伸到集气瓶口,木条熄灭,则证明已经收集满了。
CaCO3+2HCl=CaCl2+H2O+CO2↑
谢 谢
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 自然界中的水
- 第三节 水分子的变化
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 物质构成的奥秘
- 第一节 原子的构成
- 第二节 元素
- 第三节 物质组成的表示
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去 二氧化碳的实验室制取与性质
