鲁教版(五四制)八年级全一册 5.1 化学反应中的质量守恒 课件 (共20张PPT)
文档属性
| 名称 | 鲁教版(五四制)八年级全一册 5.1 化学反应中的质量守恒 课件 (共20张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 857.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-10-31 00:00:00 | ||
图片预览





文档简介
(共20张PPT)
化学反应中的质量守恒
学习目标
1、认识质量守恒定律,能够通过实验探究了解化学反应中的质量关系;
2、会用微粒的观点对质量守恒定律作出解释。
【思考】
1、蜡烛燃烧成灰烬,质量如何变化?
2、小树苗长成参天大树,质量如何变化?
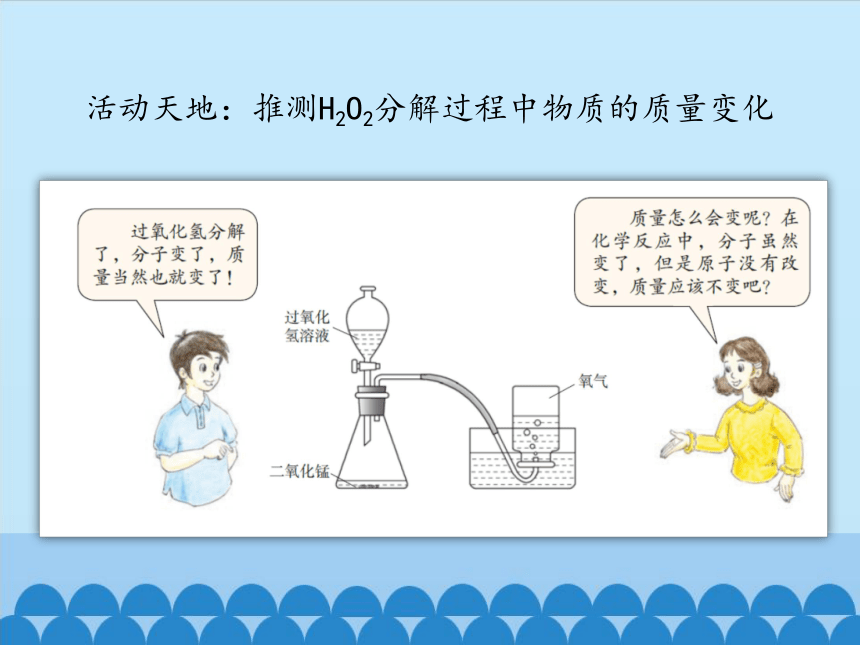
活动天地:推测H2O2分解过程中物质的质量变化
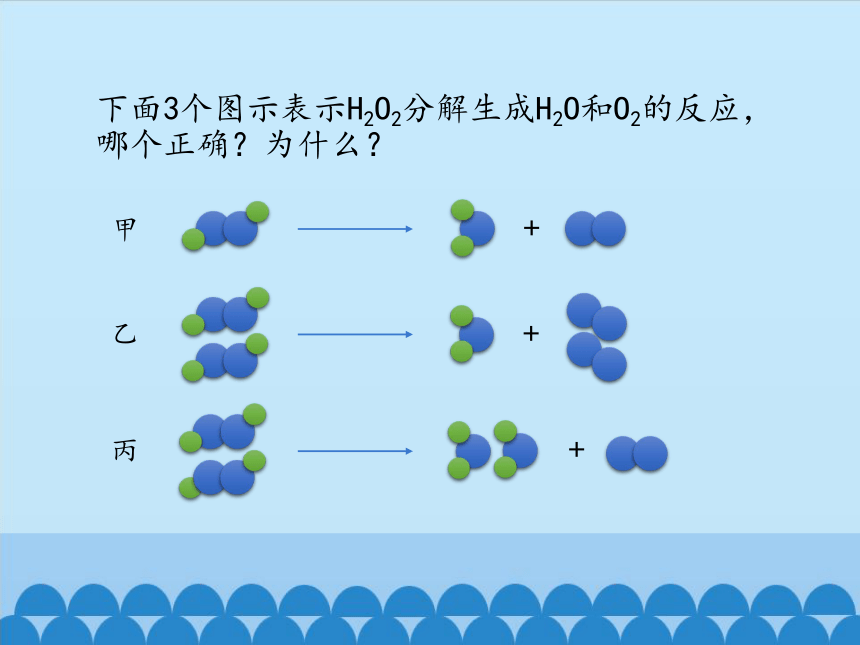
下面3个图示表示H2O2分解生成H2O和O2的反应,哪个正确?为什么?
+
甲
+
乙
+
丙
过氧化氢 水 + 氧气
H2O2 H2O O2
催化剂
【思考】过氧化氢的质量与水和氧气的质量是否相等?
根据你的推测,设计实验来检验你的推测是否正确。
【思考】如何设计实验来检验你的推测是否正确?
(1)首先要确定一个容易发生的化学反应作为研究对象;
(2)其次要考虑怎样测量反应前后的物质质量;
(3)还要考虑怎样使反应发生、在哪里发生,需要哪些仪器、药品等。
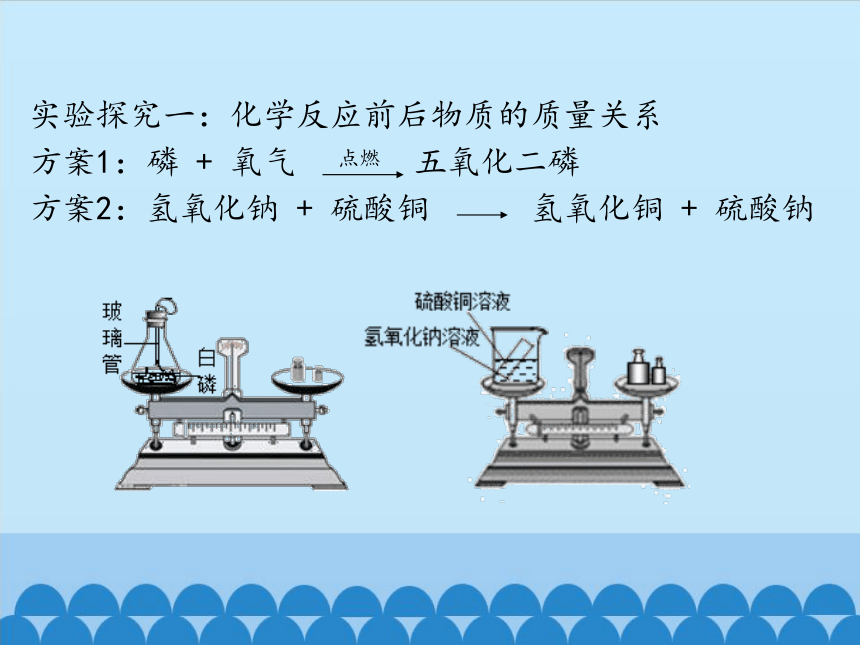
实验探究一:化学反应前后物质的质量关系
方案1:磷 + 氧气 五氧化二磷
方案2:氢氧化钠 + 硫酸铜 氢氧化铜 + 硫酸钠
点燃
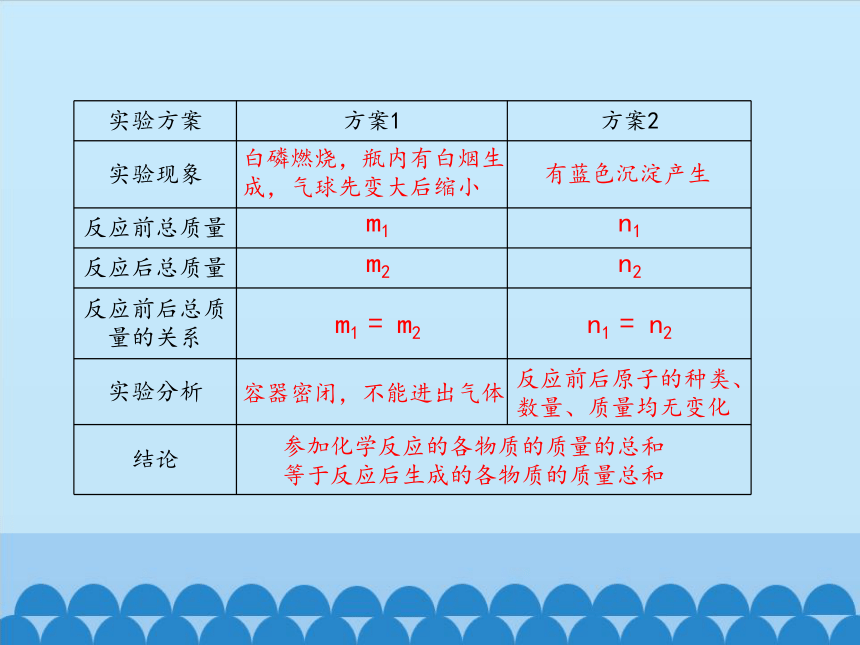
实验方案 方案1 方案2
实验现象
反应前总质量
反应后总质量
反应前后总质量的关系
实验分析
结论
白磷燃烧,瓶内有白烟生成,气球先变大后缩小
有蓝色沉淀产生
m1
n2
m2
n1
m1 = m2
n1 = n2
容器密闭,不能进出气体
反应前后原子的种类、数量、质量均无变化
参加化学反应的各物质的质量的总和等于反应后生成的各物质的质量总和
上述实验证明:参加反应的各物质的质量的总和,等于反应后生成的各物质的质量总和。
这个规律就叫做质量守恒定律。
实验探究二:
实验1:盐酸 + 碳酸钠 氯化钠 + 二氧化碳 + 水
实验2:镁 + 氧气 氧化镁
点燃
你预计这两个反应前后的称量结果是否会有变化?
实验 实验1 实验2
反应前总质量
反应后总质量
反应前后总质量的关系
实验分析
结论
m1
m2
m1 > m2
n2
n1 < n2
n1
生成的二氧化碳气体跑掉,质量减少
镁条燃烧消耗空气中的氧气,质量增加
这两个反应的称量结果都有变化,但仍符合质量守恒定律
质量守恒定律化学变化的实质是:
反应前后原子的种类、数目、质量没有改变。
分子
原子
分解为
新分子
重组
氢气 + 氧气 水
质量守恒定律总结:
1.内容:①适用于化学变化;②“质量”守恒;
③“参加”反应物质。
2.微观本质:
①过程:分子分裂成原子,原子重新组合成新分子;②三不变:原子种类、数目、质量不变;
③一变:分子种类改变。
用质量守恒定律解释生活中的一些现象
蜡烛在空气中燃烧,蜡烛的质量为什么会变小?
铁生锈后,质量为什么会变大?
课堂小结
质量守恒定律
质量守恒定律
微观本质
参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。
化学反应前后,原子的种类、数目和质量都不变。
1.下列现象能用质量守恒定律解释的是( )
A.水结冰前后质量不变
B.1升芝麻和1升大米混合,总体积小于2升
C.在降温加压的条件下,氧气变为淡蓝色液体
D.氧化钙与水反应生成氢氧化钙,反应前后物质的总质量不变
知能训练
D
2.化学反应前后可能发生变化的是( )
A.物质的总质量 B.元素种类
C.原子数目 D.分子数目
D
3.我国计划发射“嫦娥一号”卫星,卫星运载火箭的动力由高氯酸铵(NH4ClO4)分解提供。高氯酸铵分解有可能排入大气的物质是( )
A.H2O B.SO2
C.CO2 D.CO
A
谢 谢
化学反应中的质量守恒
学习目标
1、认识质量守恒定律,能够通过实验探究了解化学反应中的质量关系;
2、会用微粒的观点对质量守恒定律作出解释。
【思考】
1、蜡烛燃烧成灰烬,质量如何变化?
2、小树苗长成参天大树,质量如何变化?
活动天地:推测H2O2分解过程中物质的质量变化
下面3个图示表示H2O2分解生成H2O和O2的反应,哪个正确?为什么?
+
甲
+
乙
+
丙
过氧化氢 水 + 氧气
H2O2 H2O O2
催化剂
【思考】过氧化氢的质量与水和氧气的质量是否相等?
根据你的推测,设计实验来检验你的推测是否正确。
【思考】如何设计实验来检验你的推测是否正确?
(1)首先要确定一个容易发生的化学反应作为研究对象;
(2)其次要考虑怎样测量反应前后的物质质量;
(3)还要考虑怎样使反应发生、在哪里发生,需要哪些仪器、药品等。
实验探究一:化学反应前后物质的质量关系
方案1:磷 + 氧气 五氧化二磷
方案2:氢氧化钠 + 硫酸铜 氢氧化铜 + 硫酸钠
点燃
实验方案 方案1 方案2
实验现象
反应前总质量
反应后总质量
反应前后总质量的关系
实验分析
结论
白磷燃烧,瓶内有白烟生成,气球先变大后缩小
有蓝色沉淀产生
m1
n2
m2
n1
m1 = m2
n1 = n2
容器密闭,不能进出气体
反应前后原子的种类、数量、质量均无变化
参加化学反应的各物质的质量的总和等于反应后生成的各物质的质量总和
上述实验证明:参加反应的各物质的质量的总和,等于反应后生成的各物质的质量总和。
这个规律就叫做质量守恒定律。
实验探究二:
实验1:盐酸 + 碳酸钠 氯化钠 + 二氧化碳 + 水
实验2:镁 + 氧气 氧化镁
点燃
你预计这两个反应前后的称量结果是否会有变化?
实验 实验1 实验2
反应前总质量
反应后总质量
反应前后总质量的关系
实验分析
结论
m1
m2
m1 > m2
n2
n1 < n2
n1
生成的二氧化碳气体跑掉,质量减少
镁条燃烧消耗空气中的氧气,质量增加
这两个反应的称量结果都有变化,但仍符合质量守恒定律
质量守恒定律化学变化的实质是:
反应前后原子的种类、数目、质量没有改变。
分子
原子
分解为
新分子
重组
氢气 + 氧气 水
质量守恒定律总结:
1.内容:①适用于化学变化;②“质量”守恒;
③“参加”反应物质。
2.微观本质:
①过程:分子分裂成原子,原子重新组合成新分子;②三不变:原子种类、数目、质量不变;
③一变:分子种类改变。
用质量守恒定律解释生活中的一些现象
蜡烛在空气中燃烧,蜡烛的质量为什么会变小?
铁生锈后,质量为什么会变大?
课堂小结
质量守恒定律
质量守恒定律
微观本质
参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。
化学反应前后,原子的种类、数目和质量都不变。
1.下列现象能用质量守恒定律解释的是( )
A.水结冰前后质量不变
B.1升芝麻和1升大米混合,总体积小于2升
C.在降温加压的条件下,氧气变为淡蓝色液体
D.氧化钙与水反应生成氢氧化钙,反应前后物质的总质量不变
知能训练
D
2.化学反应前后可能发生变化的是( )
A.物质的总质量 B.元素种类
C.原子数目 D.分子数目
D
3.我国计划发射“嫦娥一号”卫星,卫星运载火箭的动力由高氯酸铵(NH4ClO4)分解提供。高氯酸铵分解有可能排入大气的物质是( )
A.H2O B.SO2
C.CO2 D.CO
A
谢 谢
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 自然界中的水
- 第三节 水分子的变化
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 物质构成的奥秘
- 第一节 原子的构成
- 第二节 元素
- 第三节 物质组成的表示
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去 二氧化碳的实验室制取与性质
