黑龙江省漠河市高级中学2021-2022学年高一上学期第一次月考化学试卷(Word版含答案)
文档属性
| 名称 | 黑龙江省漠河市高级中学2021-2022学年高一上学期第一次月考化学试卷(Word版含答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 201.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-10-31 00:00:00 | ||
图片预览


文档简介
漠河市高级中学2021-2022学年高一上学期第一次月考
化学试题
满分:100分 时间:90分钟
可能用到的相对原子质量:H-1,C-12,N-14,O-16, Na-23,Mg-24,Al-27,S-32,K-39,C1-35.5
一、选择题(20×3分=60分)
1.某试剂瓶标签上的安全标志如图所示,其中的试剂可能是
A.碳酸钠 B.氢氧化钠 C.乙醇 D.氯化钠
2.下列可以进行加热的实验仪器有
①烧杯 ②量筒 ③漏斗 ④蒸发皿 ⑤蒸馏烧瓶 ⑥锥形瓶
A.①③④⑤ B.①②④⑤ C.①④⑤⑥ D.②④⑤⑥
3.初中化学实验中多次使用玻璃棒,下列实验中玻璃棒不是用来搅拌的是
A.稀释浓硫酸 B.蒸发氯化钠溶液
C.过滤泥水 D.溶解蔗糖
4.下列操作能达实验目的且符合实验室安全措施的是
A.稀释浓硫酸,应将水慢慢注入盛有浓硫酸的烧杯中并搅拌
B.酒精灯洒出的酒精万一在桌上着火,应立即用湿抹布扑盖
C.碱溶液沾到皮肤上,应尽快用抹布擦拭干净,再涂上稀盐酸
D.实验室产生的废液可以直接倒入下水道中用水冲走
5.下列叙述正确的是
A.蒸发结束后,用手直接拿走蒸发皿
B.分液漏斗使用前需要检查是否漏液
C.蒸馏时,应从冷凝管的上口通冷却水
D.用四氯化碳萃取碘水中的碘时,可用无水酒精代替四氯化碳
6.下列说法中正确的是
A.H2O的摩尔质量为18g·mol-1 B.1molO2质量为32g·mol-1
C.CO2的相对分子质量为44g D.1mo1OH-的质量为17
7.下列分离和提纯的实验中,所选用的方法或仪器错误的是
选项 A B C D
实验目的 制取蒸馏水 分离水和植物油 分离食盐水与泥沙 从浓食盐水中得到氯化钠晶体
分离方法 蒸馏 分液 萃取 蒸发
选用仪器
8.下列操作中不正确的是
A.过滤时,玻璃棒与三层滤纸的一边接触
B.过滤时,漏斗下端紧贴烧杯内壁
C.制作过滤器时,滤纸边缘应低于漏斗口
D.过滤时,将液体沿玻璃棒注入过滤器,并使液面高于滤纸边缘
9.下列实验操作中正确的是
A.进行蒸发操作时,待混合物中的水分完全蒸干后,及时熄灭酒精灯
B.进行蒸馏操作时,应使温度计水银球伸入液面下
C.进行蒸馏操作时,应弃去达到被提纯液体沸点前蒸出的馏分
D.进行萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
10.在3mL溴水中,加入1mL四氯化碳,振荡、静置后,观察到试管里的分层现象是
A. B. C. D.
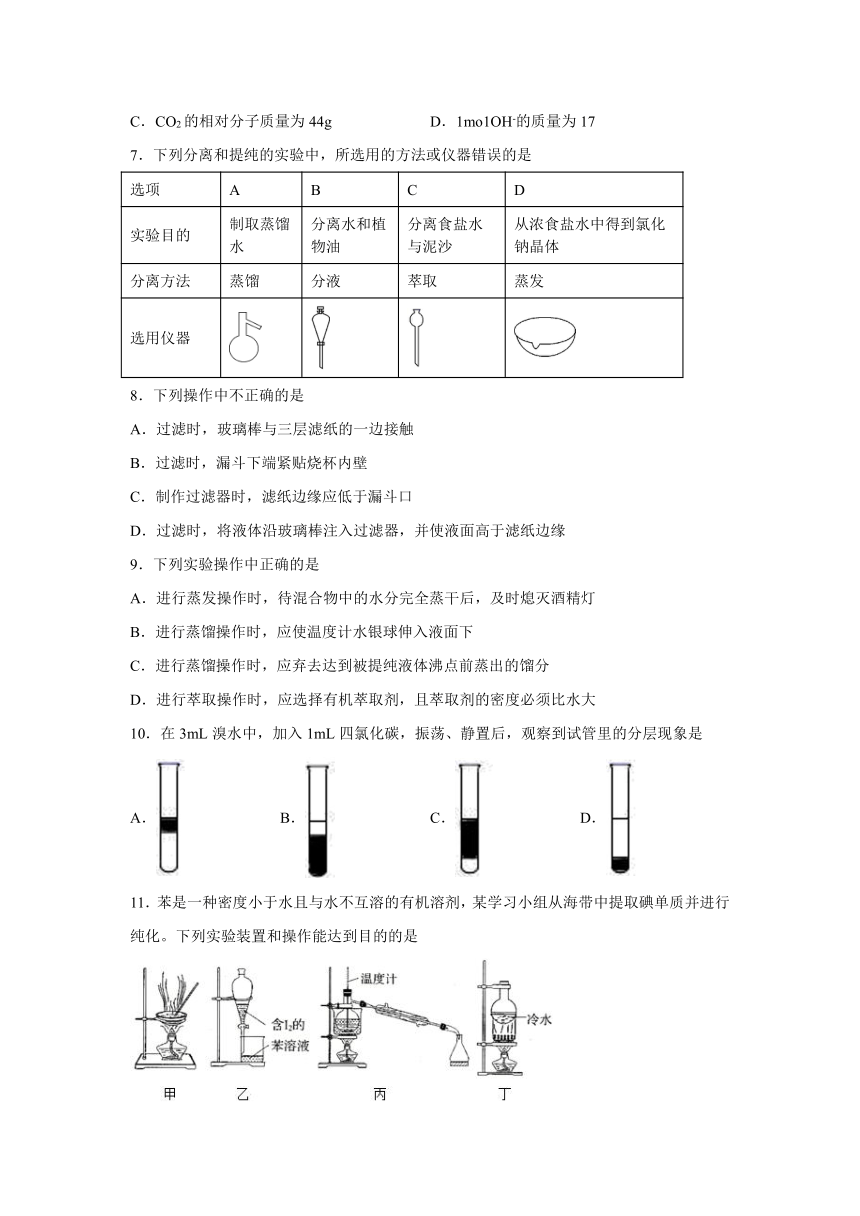
11.苯是一种密度小于水且与水不互溶的有机溶剂,某学习小组从海带中提取碘单质并进行纯化。下列实验装置和操作能达到目的的是
A.装置甲灼烧海带 B.装置乙用苯萃取碘水中的I2
C.装置丙从碘苯溶液中提取I2 D.装置丁精制单质碘
12.在同温同压下,同体积的H2和CH4,它们的原子数之比是
A.2∶5 B.1∶1 C.1∶5 D.1∶8
13.下列说法正确的是
A.1 mol物质的质量就是该物质的摩尔质量
B.12 g 12C中含有碳原子的准确数目为6.02 × 1023
C.常温常压下,1 mol任何物质的体积都约为22. 4L
D.同温同压下,任何气体的体积之比等于其物质的量之比
14.为了除去粗盐中Ca2+、Mg2+、 SO及泥沙,可将粗盐溶于水,然后进行下列五项操作:①过滤②加过量的NaOH溶液③加适量盐酸④加过量Na2CO3溶液⑤加过量BaCl2溶液。其中正确的操作顺序是
A.①④②⑤③ B.④①②⑤③ C.②⑤④①③ D.⑤②④③①
15.设阿伏加德罗常数的值为,下列说法正确的是
A.1mol NH4+中含电子数目为11NA
B.含原子数目为
C.100g 质量分数为98% 的H2SO4溶液中含有氧原子的数目为4NA
D.标准状况下,2.7g Al与足量盐酸充分反应,生成H2的体积为3.36L
16.用NA表示阿伏德罗常数的值,下列叙述正确的是
A.标准状况下,22.4L CCl4含有的分子数为1NA
B.常温常压下,1.06g Na2CO3溶于水,溶液中含Na+离子数为0.02NA
C.25℃,101kPa下,NA个CO2分子占有的体积为22.4L
D.1 mol MgCl2中,含有Cl 数为NA个
17.下列说法正确的是
A.摩尔是国际单位制中七个基本物理量之一
B.2H既可表示2个氢原子,又可表示2mol氢原子
C.当1mol气态物质的体积为22.4L时,该气体一定处于标准状况
D.同温同压下,相同体积的CO和CO2所含的氧原子数目之比为1:2
18.下列叙述中正确的是
A.由同种元素组成的物质一定是单质
B.非金属氧化物不一定是酸性氧化物
C.金属氧化物一定是碱性氧化物
D.CO、NO、CO2均属于不成盐氧化物
19.为了检验某溶液中是否含有硫酸根离子,下列操作最合理的是
A.先加硝酸钡溶液产生白色沉淀,再加盐酸,白色沉淀不溶解则原溶液中含有硫酸根
B.先加硝酸钡溶液产生白色沉淀,再加稀硝酸,白色沉淀不溶解则原溶液中含有硫酸根
C.先用盐酸酸化无明显现象,再加氯化钡溶液,若有白色沉淀则原溶液中含有硫酸根
D.先用硝酸酸化无明显现象,再加氯化钡溶液,若有白色沉淀则原溶液中含有硫酸根
20.由CO2、H2和CO组成的混合气体在同温同压下与氮气的密度相同,则该混合气体中CO2、H2、CO的体积比为
A.29∶8∶13 B.22∶1∶14 C.8∶13∶29 D.26∶16∶57
二、非选择题(每空1分,共40分)
21.(共7分)可用于分离或提纯物质的方法有:a.过滤;b.高温分解;c.蒸发结晶;d.蒸馏;e.萃取;f.分液;g.降温结晶;h.升华,下列各组混合物的分离或提纯应选用上述哪种方法最合适(填字母)
①分离水和汽油的混合物,用_______。
②从溴水里提取溴,用_______。
③除去CaO中的CaCO3,用_______。
④除去NaCl溶液中的泥沙,用_______。
⑤分离乙酸(沸点118℃)与乙醚(沸点34℃)的混合物,用_______。
⑥从含有少量氯化钠的硝酸钾饱和溶液中获取硝酸钾,用_______。
⑦分离氯化钠固体和碘单质的混合物,用_______。
22.(共14分)化学是一门以实验为基础的科学。下列是中学化学中一些常见的实验装置,按要求回答下列问题:
(1)写出仪器名称:A___________、B___________、D___________。
(2)装置①中的错误是___________。
(3)粗盐提纯所需装置为___________和___________。
(4)除去自来水中的Cl 制取蒸馏水可选择的装置为___________,加热前应先加入几粒沸石,目的是___________;如何检验蒸馏得到的水中是否还存在氯离子___________。
23.(共7分)某化学课外小组以海带为原料制取了少量碘水,现用四氯化碳从碘水中萃取碘并用分液漏斗分离两种溶液。其实验步骤为
A.把盛有溶液的分液漏斗放在铁架台的铁圈中;
B.把20 mL碘水和5 mL四氯化碳加入分液漏斗中,并盖好玻璃塞;
C.检验分液漏斗活塞和上口的玻璃塞是否漏液;
D.倒转漏斗振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
E.旋开活塞,用烧杯接收下层溶液;
F.从分液漏斗上口倒出上层溶液;
G.将分液漏斗上口的玻璃塞打开或使塞上的凹槽对准分液漏斗口上的小孔;
H.静置、分层。
就此实验完成下列填空:
(1)实验步骤的顺序为_______→_______→_______→A→H→_______→E→F。
(2)实验结束后,容量瓶内下层溶液的颜色是_______。
(3)上述G步骤操作的目的是___________________________。
(4)能选用四氯化碳从碘水中萃取碘的原因是① ② ③_______。
24.(共12分)根据所学知识填空(NA表示阿伏加德罗常数的值):
(1)0.2molCl2含有______molCl,在标准状况下体积为______L。
(2)1.204×1022个CO2分子,含有C的物质的量为 。
(3)1molOH-中含有_____mol电子,有________个质子。
(4)物质的量相等的SO2和SO3,其质量之比为_______。
(5)等质量的SO2和SO3,其物质的量之比为_______,原子个数之比为 。
(6)有标准状况下的四种气体:①6.72 L CH4,②3.01×1023个H2分子,③3.4 g H2S,④0.2 mol NH3,则分子数按从大到小的顺序为 (填序号,下同),体积按从大到小的顺序为:__________,密度按从大到小的顺序为:__________。
(7)设NA为阿伏加德罗常数的数值,如果ag某未知气体中含有的分子数为b,则该气体的摩尔质量为__________(用a、b、NA的式子表示)。
答案
1、选择题(20×3分=60分)
1-5 BCCBB 6--10 ACDCD 11---15 DADCD 16---20 BDBCD
1、非选择题(共40分)
21. (共7分,每空1分)(应该填小写字母,若填成大写字母,按照错误处理)
①f;②e(f、d)选出e就得分,多选f和d不扣分,若有错选则扣分;
③b;④a;⑤d;⑥g;⑦h
22.(共14分)
(1)A蒸馏烧瓶(2分) B直形冷凝管(2分) D分液漏斗(2分)
(2)冷却水流向错,应下进上出;(2分)
(3)③(1分);④(1分)
(4)①(1分);防止暴沸(1分)取少量待测液于试管中,滴加稀硝酸酸化的硝酸银溶液,若无白色沉淀生成,则不含氯离子。(2分)
23.(共7分)
(1)C B D G (2分)
(2)紫红色 (1分)
(3)使分液漏斗内外空气相通,以保证进行E操作时漏斗里的液体顺利流出 (1分)
(4)①四氯化碳与水和碘都不反应;(1分)②四氯化碳与水不互溶;(1分)
③碘在四氯化碳中的溶解度比在水中大得多(1分)
24. (共12分,每空1分)
(1)0.4; 8.96
(2)0.02mol
(3)10; 9NA或5.418×1024
(4)4:5
(5)5:4; 15:16
(6)②①④③; ②①④③; ④①③②
(6) g/mol
化学试题
满分:100分 时间:90分钟
可能用到的相对原子质量:H-1,C-12,N-14,O-16, Na-23,Mg-24,Al-27,S-32,K-39,C1-35.5
一、选择题(20×3分=60分)
1.某试剂瓶标签上的安全标志如图所示,其中的试剂可能是
A.碳酸钠 B.氢氧化钠 C.乙醇 D.氯化钠
2.下列可以进行加热的实验仪器有
①烧杯 ②量筒 ③漏斗 ④蒸发皿 ⑤蒸馏烧瓶 ⑥锥形瓶
A.①③④⑤ B.①②④⑤ C.①④⑤⑥ D.②④⑤⑥
3.初中化学实验中多次使用玻璃棒,下列实验中玻璃棒不是用来搅拌的是
A.稀释浓硫酸 B.蒸发氯化钠溶液
C.过滤泥水 D.溶解蔗糖
4.下列操作能达实验目的且符合实验室安全措施的是
A.稀释浓硫酸,应将水慢慢注入盛有浓硫酸的烧杯中并搅拌
B.酒精灯洒出的酒精万一在桌上着火,应立即用湿抹布扑盖
C.碱溶液沾到皮肤上,应尽快用抹布擦拭干净,再涂上稀盐酸
D.实验室产生的废液可以直接倒入下水道中用水冲走
5.下列叙述正确的是
A.蒸发结束后,用手直接拿走蒸发皿
B.分液漏斗使用前需要检查是否漏液
C.蒸馏时,应从冷凝管的上口通冷却水
D.用四氯化碳萃取碘水中的碘时,可用无水酒精代替四氯化碳
6.下列说法中正确的是
A.H2O的摩尔质量为18g·mol-1 B.1molO2质量为32g·mol-1
C.CO2的相对分子质量为44g D.1mo1OH-的质量为17
7.下列分离和提纯的实验中,所选用的方法或仪器错误的是
选项 A B C D
实验目的 制取蒸馏水 分离水和植物油 分离食盐水与泥沙 从浓食盐水中得到氯化钠晶体
分离方法 蒸馏 分液 萃取 蒸发
选用仪器
8.下列操作中不正确的是
A.过滤时,玻璃棒与三层滤纸的一边接触
B.过滤时,漏斗下端紧贴烧杯内壁
C.制作过滤器时,滤纸边缘应低于漏斗口
D.过滤时,将液体沿玻璃棒注入过滤器,并使液面高于滤纸边缘
9.下列实验操作中正确的是
A.进行蒸发操作时,待混合物中的水分完全蒸干后,及时熄灭酒精灯
B.进行蒸馏操作时,应使温度计水银球伸入液面下
C.进行蒸馏操作时,应弃去达到被提纯液体沸点前蒸出的馏分
D.进行萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
10.在3mL溴水中,加入1mL四氯化碳,振荡、静置后,观察到试管里的分层现象是
A. B. C. D.
11.苯是一种密度小于水且与水不互溶的有机溶剂,某学习小组从海带中提取碘单质并进行纯化。下列实验装置和操作能达到目的的是
A.装置甲灼烧海带 B.装置乙用苯萃取碘水中的I2
C.装置丙从碘苯溶液中提取I2 D.装置丁精制单质碘
12.在同温同压下,同体积的H2和CH4,它们的原子数之比是
A.2∶5 B.1∶1 C.1∶5 D.1∶8
13.下列说法正确的是
A.1 mol物质的质量就是该物质的摩尔质量
B.12 g 12C中含有碳原子的准确数目为6.02 × 1023
C.常温常压下,1 mol任何物质的体积都约为22. 4L
D.同温同压下,任何气体的体积之比等于其物质的量之比
14.为了除去粗盐中Ca2+、Mg2+、 SO及泥沙,可将粗盐溶于水,然后进行下列五项操作:①过滤②加过量的NaOH溶液③加适量盐酸④加过量Na2CO3溶液⑤加过量BaCl2溶液。其中正确的操作顺序是
A.①④②⑤③ B.④①②⑤③ C.②⑤④①③ D.⑤②④③①
15.设阿伏加德罗常数的值为,下列说法正确的是
A.1mol NH4+中含电子数目为11NA
B.含原子数目为
C.100g 质量分数为98% 的H2SO4溶液中含有氧原子的数目为4NA
D.标准状况下,2.7g Al与足量盐酸充分反应,生成H2的体积为3.36L
16.用NA表示阿伏德罗常数的值,下列叙述正确的是
A.标准状况下,22.4L CCl4含有的分子数为1NA
B.常温常压下,1.06g Na2CO3溶于水,溶液中含Na+离子数为0.02NA
C.25℃,101kPa下,NA个CO2分子占有的体积为22.4L
D.1 mol MgCl2中,含有Cl 数为NA个
17.下列说法正确的是
A.摩尔是国际单位制中七个基本物理量之一
B.2H既可表示2个氢原子,又可表示2mol氢原子
C.当1mol气态物质的体积为22.4L时,该气体一定处于标准状况
D.同温同压下,相同体积的CO和CO2所含的氧原子数目之比为1:2
18.下列叙述中正确的是
A.由同种元素组成的物质一定是单质
B.非金属氧化物不一定是酸性氧化物
C.金属氧化物一定是碱性氧化物
D.CO、NO、CO2均属于不成盐氧化物
19.为了检验某溶液中是否含有硫酸根离子,下列操作最合理的是
A.先加硝酸钡溶液产生白色沉淀,再加盐酸,白色沉淀不溶解则原溶液中含有硫酸根
B.先加硝酸钡溶液产生白色沉淀,再加稀硝酸,白色沉淀不溶解则原溶液中含有硫酸根
C.先用盐酸酸化无明显现象,再加氯化钡溶液,若有白色沉淀则原溶液中含有硫酸根
D.先用硝酸酸化无明显现象,再加氯化钡溶液,若有白色沉淀则原溶液中含有硫酸根
20.由CO2、H2和CO组成的混合气体在同温同压下与氮气的密度相同,则该混合气体中CO2、H2、CO的体积比为
A.29∶8∶13 B.22∶1∶14 C.8∶13∶29 D.26∶16∶57
二、非选择题(每空1分,共40分)
21.(共7分)可用于分离或提纯物质的方法有:a.过滤;b.高温分解;c.蒸发结晶;d.蒸馏;e.萃取;f.分液;g.降温结晶;h.升华,下列各组混合物的分离或提纯应选用上述哪种方法最合适(填字母)
①分离水和汽油的混合物,用_______。
②从溴水里提取溴,用_______。
③除去CaO中的CaCO3,用_______。
④除去NaCl溶液中的泥沙,用_______。
⑤分离乙酸(沸点118℃)与乙醚(沸点34℃)的混合物,用_______。
⑥从含有少量氯化钠的硝酸钾饱和溶液中获取硝酸钾,用_______。
⑦分离氯化钠固体和碘单质的混合物,用_______。
22.(共14分)化学是一门以实验为基础的科学。下列是中学化学中一些常见的实验装置,按要求回答下列问题:
(1)写出仪器名称:A___________、B___________、D___________。
(2)装置①中的错误是___________。
(3)粗盐提纯所需装置为___________和___________。
(4)除去自来水中的Cl 制取蒸馏水可选择的装置为___________,加热前应先加入几粒沸石,目的是___________;如何检验蒸馏得到的水中是否还存在氯离子___________。
23.(共7分)某化学课外小组以海带为原料制取了少量碘水,现用四氯化碳从碘水中萃取碘并用分液漏斗分离两种溶液。其实验步骤为
A.把盛有溶液的分液漏斗放在铁架台的铁圈中;
B.把20 mL碘水和5 mL四氯化碳加入分液漏斗中,并盖好玻璃塞;
C.检验分液漏斗活塞和上口的玻璃塞是否漏液;
D.倒转漏斗振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
E.旋开活塞,用烧杯接收下层溶液;
F.从分液漏斗上口倒出上层溶液;
G.将分液漏斗上口的玻璃塞打开或使塞上的凹槽对准分液漏斗口上的小孔;
H.静置、分层。
就此实验完成下列填空:
(1)实验步骤的顺序为_______→_______→_______→A→H→_______→E→F。
(2)实验结束后,容量瓶内下层溶液的颜色是_______。
(3)上述G步骤操作的目的是___________________________。
(4)能选用四氯化碳从碘水中萃取碘的原因是① ② ③_______。
24.(共12分)根据所学知识填空(NA表示阿伏加德罗常数的值):
(1)0.2molCl2含有______molCl,在标准状况下体积为______L。
(2)1.204×1022个CO2分子,含有C的物质的量为 。
(3)1molOH-中含有_____mol电子,有________个质子。
(4)物质的量相等的SO2和SO3,其质量之比为_______。
(5)等质量的SO2和SO3,其物质的量之比为_______,原子个数之比为 。
(6)有标准状况下的四种气体:①6.72 L CH4,②3.01×1023个H2分子,③3.4 g H2S,④0.2 mol NH3,则分子数按从大到小的顺序为 (填序号,下同),体积按从大到小的顺序为:__________,密度按从大到小的顺序为:__________。
(7)设NA为阿伏加德罗常数的数值,如果ag某未知气体中含有的分子数为b,则该气体的摩尔质量为__________(用a、b、NA的式子表示)。
答案
1、选择题(20×3分=60分)
1-5 BCCBB 6--10 ACDCD 11---15 DADCD 16---20 BDBCD
1、非选择题(共40分)
21. (共7分,每空1分)(应该填小写字母,若填成大写字母,按照错误处理)
①f;②e(f、d)选出e就得分,多选f和d不扣分,若有错选则扣分;
③b;④a;⑤d;⑥g;⑦h
22.(共14分)
(1)A蒸馏烧瓶(2分) B直形冷凝管(2分) D分液漏斗(2分)
(2)冷却水流向错,应下进上出;(2分)
(3)③(1分);④(1分)
(4)①(1分);防止暴沸(1分)取少量待测液于试管中,滴加稀硝酸酸化的硝酸银溶液,若无白色沉淀生成,则不含氯离子。(2分)
23.(共7分)
(1)C B D G (2分)
(2)紫红色 (1分)
(3)使分液漏斗内外空气相通,以保证进行E操作时漏斗里的液体顺利流出 (1分)
(4)①四氯化碳与水和碘都不反应;(1分)②四氯化碳与水不互溶;(1分)
③碘在四氯化碳中的溶解度比在水中大得多(1分)
24. (共12分,每空1分)
(1)0.4; 8.96
(2)0.02mol
(3)10; 9NA或5.418×1024
(4)4:5
(5)5:4; 15:16
(6)②①④③; ②①④③; ④①③②
(6) g/mol
同课章节目录
