第五单元定量研究化学反应测试题--2021-2022学年九年级化学鲁教版上册(word版 含答案)
文档属性
| 名称 | 第五单元定量研究化学反应测试题--2021-2022学年九年级化学鲁教版上册(word版 含答案) |  | |
| 格式 | zip | ||
| 文件大小 | 114.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-01 16:22:57 | ||
图片预览

文档简介
第五单元《定量研究化学反应》测试题
一、单选题
1.2Mg+O22MgO读法正确的是
A.镁加氧气点燃生成氧化镁
B.2Mg和O2 等于2MgO
C.2个镁和1个氧气点燃生成2个氧化镁
D.镁和氧气点燃生成氧化镁
2.下图中的四位同学对H2+Cl22HCl的认识中,不正确的是
A.该反应的条件是点燃 B.该反应前后原子种类和个数没变
C.反应前后分子个数变了 D.表示氢气在氯气中燃烧生成氯化氢
3.由元素X、Y组成的两种物质经化合生成Z,化学方程式为:3X2+2YX=2Z,则Z的化学式是
A.X3Y2 B.XY
C.X4Y D.YX4
4.将4.90g氯酸钾与1.62g二氧化锰混合后,放入试管加热,充分反应后,试管中剩余固体物质的质量约是
A.1.62g B.2.98g C.4.60g D.6.52g
5.关于化学方程式4P+5O22P2O5,获得信息不正确的是
A.磷和氧气在点燃的条件下生成五氧化二磷
B.该反应属于化合反应
C.参加反应的磷和氧气质量总和等于生成的五氧化二磷质量
D.点燃条件下,每4克磷和5克氧气反应生成2克五氧化二磷
6.小超同学做高温煅烧碳酸钙实验后得到CaCO3和CaO的混合物15.6g,取该混合物,再经高温充分煅烧质量不再改变后,将剩余固体投入足量水中,固体全部生成Ca(OH)2质量为14.8g,则小超实验中分解的CaCO3和未分解的CaCO3的质量比为
A.1:3 B.1:2 C.1:1 D.2:1
7.某物质在空气中完全燃烧生成二氧化碳和水。则对该物质的相关判断正确的是
A.该物质只含碳、氢元素
B.该物质由碳、氢、氧元素组成
C.该物质一定含有碳、氢元素,可能含有氧元素
D.可能含有三种以上的元素
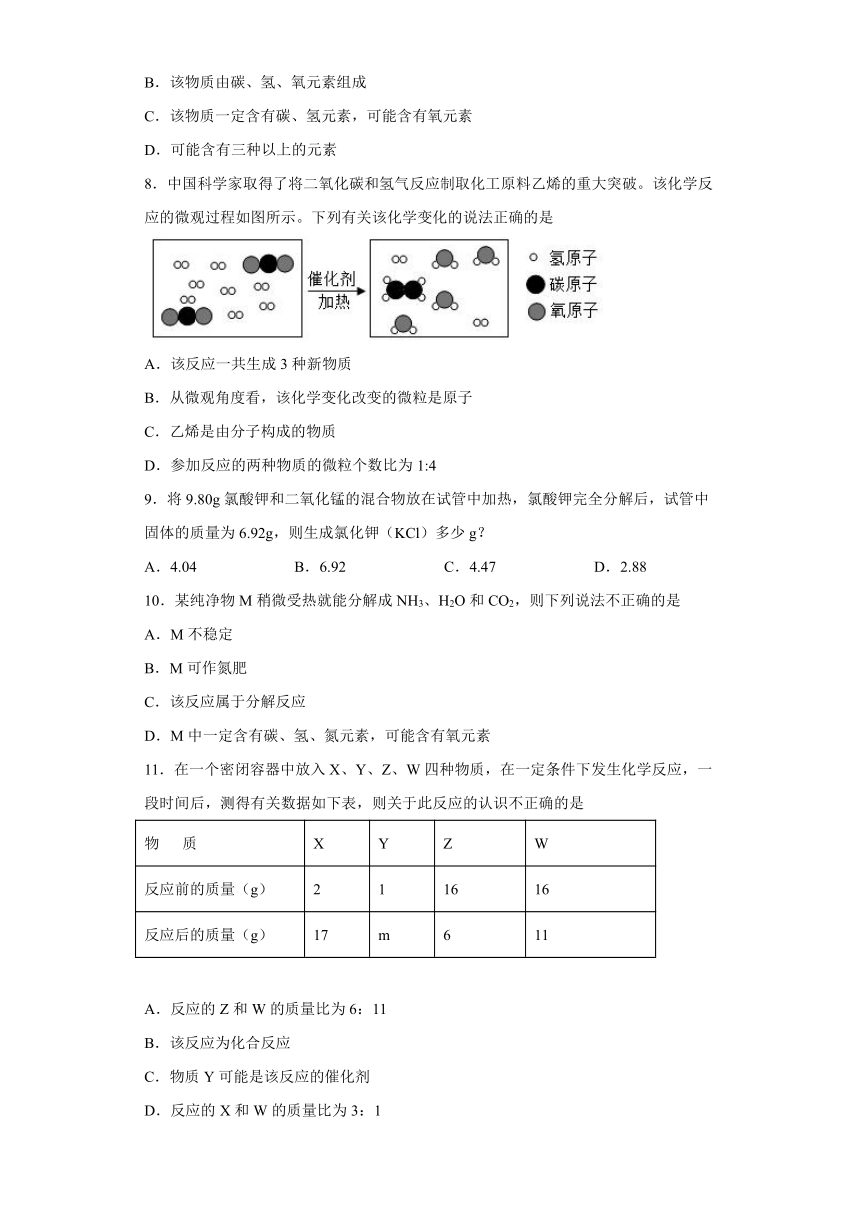
8.中国科学家取得了将二氧化碳和氢气反应制取化工原料乙烯的重大突破。该化学反应的微观过程如图所示。下列有关该化学变化的说法正确的是
A.该反应一共生成3种新物质
B.从微观角度看,该化学变化改变的微粒是原子
C.乙烯是由分子构成的物质
D.参加反应的两种物质的微粒个数比为1:4
9.将9.80g氯酸钾和二氧化锰的混合物放在试管中加热,氯酸钾完全分解后,试管中固体的质量为6.92g,则生成氯化钾(KCl)多少g?
A.4.04 B.6.92 C.4.47 D.2.88
10.某纯净物M稍微受热就能分解成NH3、H2O和CO2,则下列说法不正确的是
A.M不稳定
B.M可作氮肥
C.该反应属于分解反应
D.M中一定含有碳、氢、氮元素,可能含有氧元素
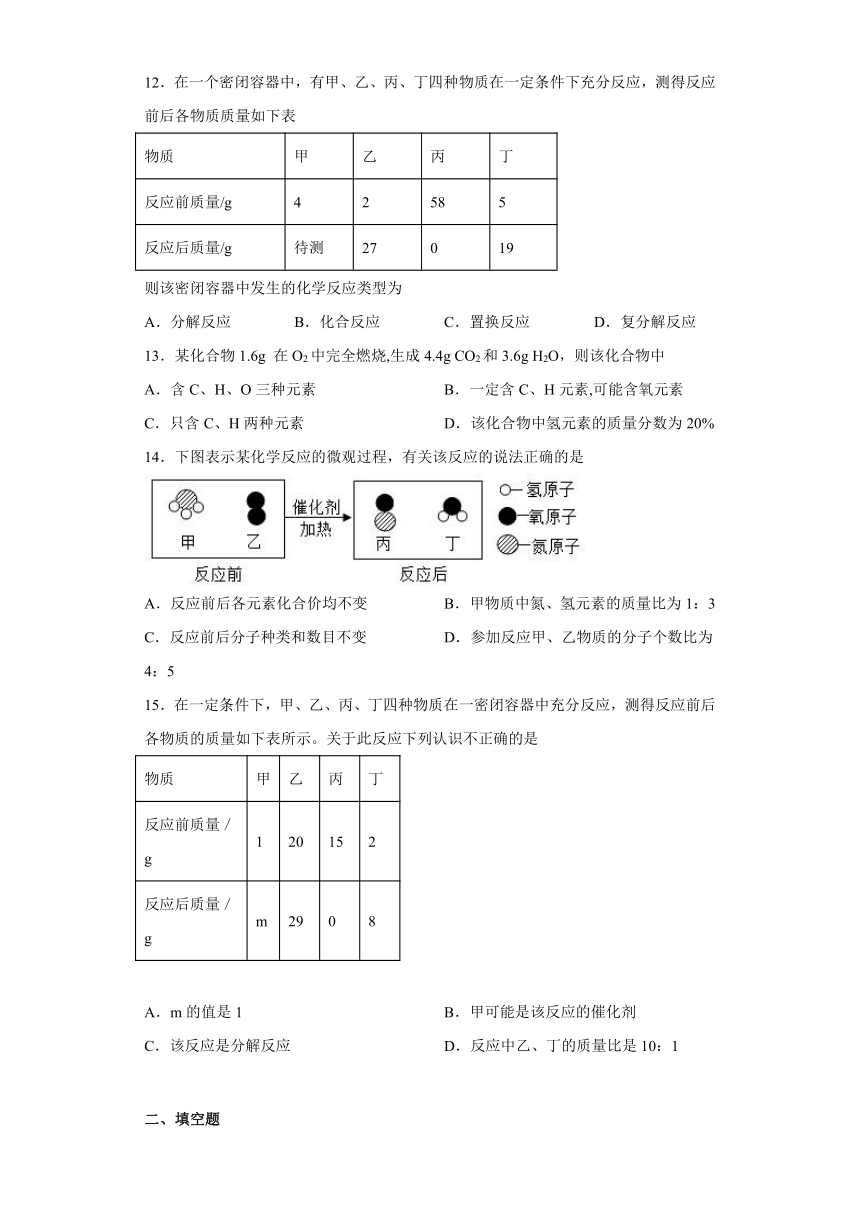
11.在一个密闭容器中放入X、Y、Z、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,则关于此反应的认识不正确的是
物 质 X Y Z W
反应前的质量(g) 2 1 16 16
反应后的质量(g) 17 m 6 11
A.反应的Z和W的质量比为6:11
B.该反应为化合反应
C.物质Y可能是该反应的催化剂
D.反应的X和W的质量比为3:1
12.在一个密闭容器中,有甲、乙、丙、丁四种物质在一定条件下充分反应,测得反应前后各物质质量如下表
物质 甲 乙 丙 丁
反应前质量/g 4 2 58 5
反应后质量/g 待测 27 0 19
则该密闭容器中发生的化学反应类型为
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
13.某化合物1.6g 在O2中完全燃烧,生成4.4g CO2和3.6g H2O,则该化合物中
A.含C、H、O三种元素 B.一定含C、H元素,可能含氧元素
C.只含C、H两种元素 D.该化合物中氢元素的质量分数为20%
14.下图表示某化学反应的微观过程,有关该反应的说法正确的是
A.反应前后各元素化合价均不变 B.甲物质中氮、氢元素的质量比为1:3
C.反应前后分子种类和数目不变 D.参加反应甲、乙物质的分子个数比为4:5
15.在一定条件下,甲、乙、丙、丁四种物质在一密闭容器中充分反应,测得反应前后 各物质的质量如下表所示。关于此反应下列认识不正确的是
物质 甲 乙 丙 丁
反应前质量/g 1 20 15 2
反应后质量/g m 29 0 8
A.m的值是1 B.甲可能是该反应的催化剂
C.该反应是分解反应 D.反应中乙、丁的质量比是10:1
二、填空题
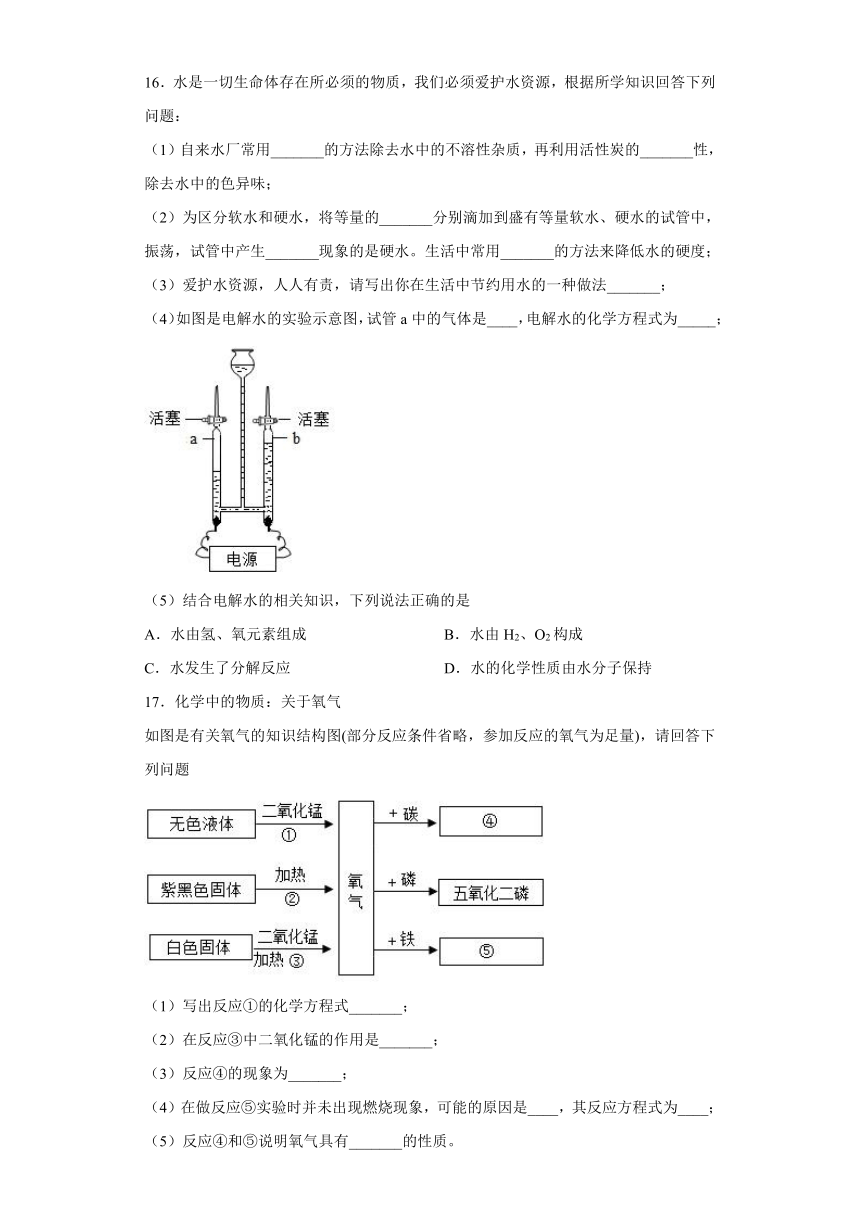
16.水是一切生命体存在所必须的物质,我们必须爱护水资源,根据所学知识回答下列问题:
(1)自来水厂常用_______的方法除去水中的不溶性杂质,再利用活性炭的_______性,除去水中的色异味;
(2)为区分软水和硬水,将等量的_______分别滴加到盛有等量软水、硬水的试管中,振荡,试管中产生_______现象的是硬水。生活中常用_______的方法来降低水的硬度;
(3)爱护水资源,人人有责,请写出你在生活中节约用水的一种做法_______;
(4)如图是电解水的实验示意图,试管a中的气体是____,电解水的化学方程式为_____;
(5)结合电解水的相关知识,下列说法正确的是
A.水由氢、氧元素组成 B.水由H2、O2构成
C.水发生了分解反应 D.水的化学性质由水分子保持
17.化学中的物质:关于氧气
如图是有关氧气的知识结构图(部分反应条件省略,参加反应的氧气为足量),请回答下列问题
(1)写出反应①的化学方程式_______;
(2)在反应③中二氧化锰的作用是_______;
(3)反应④的现象为_______;
(4)在做反应⑤实验时并未出现燃烧现象,可能的原因是____,其反应方程式为____;
(5)反应④和⑤说明氧气具有_______的性质。
(6)已知:常温下,氮气沸点为-196°C,氧气沸点为-183°C.将燃着的木条置于盛满液态空气的烧杯口,观察到的现象是_______。
18.水是生命之源,电解水实验如图所示,与直流电源正极相连的玻璃管中生成的气体是___________,正极与负极气体的体积之比为___________反应的化学方程式为___________。
三、推断题
19.A~H都是初中化学中的常见物质,它们之间的转化关系如图所示。A是天然气的主要成分,E是一种常见的食品干燥剂。请回答:
(1)A的化学式为_______;H的化学式为_______
(2)反应③的基本反应类型是_____________;
(3)反应②的化学方程式为__________;反应④的化学方程式为_________________。
20.A、B、C、D、E是初中化学中常见的物质,均由碳、氢、氧中的一种或几种元素组成。其中C能供给呼吸;D是一种气体肥料;E由三种元素组成,可作燃料。这些物质之间的转化关系如图所示。
(1)B的化学式为_______________。B→C的基本反应类型是_____________。
(2)反应A→B的化学方程式是____________________。
(3)反应E→D的化学方程式是____________________。
四、实验题
21.同学们用如图所示试验验证质量守恒定律。请根据图回答下列问题。
(1)①在实验一中,在实验前称量,天平左盘中物质的质量是27.6克,则右盘中砝码的质量是25g,则游码的质量是______。
②白磷燃烧过程中锥形瓶中观察到的现象为______,实验过程中小气球的变化为______。
③燃烧后冷却到室温,再次将锥形瓶放到托盘天平上称量,发现托盘天平不能保持平衡,造成这种现象的原因可能是______。
(2)实验二中铁钉与硫酸铜反应的化学方程式是______。该实验______(填“遵守”或“不遵守”)质量守恒定律。
(3)实验三中化学反应前后天平______(填“平衡”或“不平衡”),原因是:用化学方程式解释______。
22.实验室制取氧气,提供了下列药品和常用装置,请按要求回答有关问题:
药品:①过氧化氢溶液②氯酸钾③二氧化锰
(1)装置中仪器a的名称为___________。
(2)若小明选择装置A和C来制取氧气。则他选择的药品应为___________(填序号)。反应的符号表达式为___________。若用装置C收集氧气,则验满的操作方法为___________,观察木条是否复燃。
(3)某气体X可用D装置收集,若改用F装置收集,则气体X应从___________口进(填“b”或“c”)。
(4)若用过氧化氢溶液制取氧气时应选择的发生装置是___________,有关的符号表达式为___________。若收集一瓶更纯净的氧气应选择的收集装置是___________。
(5)使用F图所示装置收集O2,若将装置翻转过来再装满水,O2由___________口进入。
(6)今年我县正在进行“煤改气”工程。“气”的主要成分甲烷是一种无色、无味,密度小于空气的气体,难溶于水。实验室常用加热无水醋酸钠和碱石灰的固体混合物来制取,请选择实验室制取甲烷时的发生装置是___________,收集装置是___________或___________(从A-E中选)。
五、计算题
23.8.4gFe在氧气中完全燃烧,生成______克四氧化三铁,消耗______克氧气。
24.草酸亚铁(化学式为FeC2O4)是生产锂电池的原材料,它受热易分解,会产生一氧化碳、二氧化碳和铁的氧化物( FexOy)这三种物质,现将28.8g草酸亚铁放置于试管中进行加热,加热到最后得到铁的氧化物质量为14.4g,求铁的氧化物的化学式是__________。
(提示:化学反应前后元素的种类和质量不变)(写出详细的计算过程)。
参考答案
1.D 2.C 3.D 4.C 5.D 6.C 7.C 8.C 9.C 10.D 11.A 12.A 13.C 14.D 15.D
16.(1) 过滤 吸附
(2) 肥皂水 泡沫较少浮渣较多 煮沸
(3)一水多用
(4) 氢气
(5)ACD
17.(1)
(2)催化
(3)放出大量热,发出白光,生成使澄清石灰水变浑浊的气体
(4) 未等到火柴梗快要燃尽时铁丝就伸入集气瓶中或铁丝生锈等
(5)助燃性或氧化性
(6)木条立刻熄灭
18.氧气 1:2
19.CH4 CaCO3 化合反应 CO2+2NaOH=Na2CO3+H2O Ca(OH)2 + Na2CO3 = CaCO3↓ + 2NaOH
20.H2O 分解反应 2H2O22H2O+O2↑ C2H5OH+3O22CO2+3H2O
21.
(1) 2.6g 放出热量,产生大量白烟 气球先胀大,后缩小 装置漏气
(2)
遵守
(3) 不平衡
22.
(1)试管
(2) ②③ KClO3KCl+O2 将带火星木条伸到集气瓶口处
(3)c
(4) B H2O2H2O+O2 E
(5)b
(6) A D E
23.11.6 3.2
24.由质量守恒定律可知,反应前后,铁元素质量不变,所以可以计算出原草酸亚铁中铁元素的质量为:;
加热后得到的铁的氧化物中:
由此可求所得铁的氧化物中,铁原子和氧原子的原子个数比=
所以,所得的铁的氧化物的化学式为:
一、单选题
1.2Mg+O22MgO读法正确的是
A.镁加氧气点燃生成氧化镁
B.2Mg和O2 等于2MgO
C.2个镁和1个氧气点燃生成2个氧化镁
D.镁和氧气点燃生成氧化镁
2.下图中的四位同学对H2+Cl22HCl的认识中,不正确的是
A.该反应的条件是点燃 B.该反应前后原子种类和个数没变
C.反应前后分子个数变了 D.表示氢气在氯气中燃烧生成氯化氢
3.由元素X、Y组成的两种物质经化合生成Z,化学方程式为:3X2+2YX=2Z,则Z的化学式是
A.X3Y2 B.XY
C.X4Y D.YX4
4.将4.90g氯酸钾与1.62g二氧化锰混合后,放入试管加热,充分反应后,试管中剩余固体物质的质量约是
A.1.62g B.2.98g C.4.60g D.6.52g
5.关于化学方程式4P+5O22P2O5,获得信息不正确的是
A.磷和氧气在点燃的条件下生成五氧化二磷
B.该反应属于化合反应
C.参加反应的磷和氧气质量总和等于生成的五氧化二磷质量
D.点燃条件下,每4克磷和5克氧气反应生成2克五氧化二磷
6.小超同学做高温煅烧碳酸钙实验后得到CaCO3和CaO的混合物15.6g,取该混合物,再经高温充分煅烧质量不再改变后,将剩余固体投入足量水中,固体全部生成Ca(OH)2质量为14.8g,则小超实验中分解的CaCO3和未分解的CaCO3的质量比为
A.1:3 B.1:2 C.1:1 D.2:1
7.某物质在空气中完全燃烧生成二氧化碳和水。则对该物质的相关判断正确的是
A.该物质只含碳、氢元素
B.该物质由碳、氢、氧元素组成
C.该物质一定含有碳、氢元素,可能含有氧元素
D.可能含有三种以上的元素
8.中国科学家取得了将二氧化碳和氢气反应制取化工原料乙烯的重大突破。该化学反应的微观过程如图所示。下列有关该化学变化的说法正确的是
A.该反应一共生成3种新物质
B.从微观角度看,该化学变化改变的微粒是原子
C.乙烯是由分子构成的物质
D.参加反应的两种物质的微粒个数比为1:4
9.将9.80g氯酸钾和二氧化锰的混合物放在试管中加热,氯酸钾完全分解后,试管中固体的质量为6.92g,则生成氯化钾(KCl)多少g?
A.4.04 B.6.92 C.4.47 D.2.88
10.某纯净物M稍微受热就能分解成NH3、H2O和CO2,则下列说法不正确的是
A.M不稳定
B.M可作氮肥
C.该反应属于分解反应
D.M中一定含有碳、氢、氮元素,可能含有氧元素
11.在一个密闭容器中放入X、Y、Z、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表,则关于此反应的认识不正确的是
物 质 X Y Z W
反应前的质量(g) 2 1 16 16
反应后的质量(g) 17 m 6 11
A.反应的Z和W的质量比为6:11
B.该反应为化合反应
C.物质Y可能是该反应的催化剂
D.反应的X和W的质量比为3:1
12.在一个密闭容器中,有甲、乙、丙、丁四种物质在一定条件下充分反应,测得反应前后各物质质量如下表
物质 甲 乙 丙 丁
反应前质量/g 4 2 58 5
反应后质量/g 待测 27 0 19
则该密闭容器中发生的化学反应类型为
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
13.某化合物1.6g 在O2中完全燃烧,生成4.4g CO2和3.6g H2O,则该化合物中
A.含C、H、O三种元素 B.一定含C、H元素,可能含氧元素
C.只含C、H两种元素 D.该化合物中氢元素的质量分数为20%
14.下图表示某化学反应的微观过程,有关该反应的说法正确的是
A.反应前后各元素化合价均不变 B.甲物质中氮、氢元素的质量比为1:3
C.反应前后分子种类和数目不变 D.参加反应甲、乙物质的分子个数比为4:5
15.在一定条件下,甲、乙、丙、丁四种物质在一密闭容器中充分反应,测得反应前后 各物质的质量如下表所示。关于此反应下列认识不正确的是
物质 甲 乙 丙 丁
反应前质量/g 1 20 15 2
反应后质量/g m 29 0 8
A.m的值是1 B.甲可能是该反应的催化剂
C.该反应是分解反应 D.反应中乙、丁的质量比是10:1
二、填空题
16.水是一切生命体存在所必须的物质,我们必须爱护水资源,根据所学知识回答下列问题:
(1)自来水厂常用_______的方法除去水中的不溶性杂质,再利用活性炭的_______性,除去水中的色异味;
(2)为区分软水和硬水,将等量的_______分别滴加到盛有等量软水、硬水的试管中,振荡,试管中产生_______现象的是硬水。生活中常用_______的方法来降低水的硬度;
(3)爱护水资源,人人有责,请写出你在生活中节约用水的一种做法_______;
(4)如图是电解水的实验示意图,试管a中的气体是____,电解水的化学方程式为_____;
(5)结合电解水的相关知识,下列说法正确的是
A.水由氢、氧元素组成 B.水由H2、O2构成
C.水发生了分解反应 D.水的化学性质由水分子保持
17.化学中的物质:关于氧气
如图是有关氧气的知识结构图(部分反应条件省略,参加反应的氧气为足量),请回答下列问题
(1)写出反应①的化学方程式_______;
(2)在反应③中二氧化锰的作用是_______;
(3)反应④的现象为_______;
(4)在做反应⑤实验时并未出现燃烧现象,可能的原因是____,其反应方程式为____;
(5)反应④和⑤说明氧气具有_______的性质。
(6)已知:常温下,氮气沸点为-196°C,氧气沸点为-183°C.将燃着的木条置于盛满液态空气的烧杯口,观察到的现象是_______。
18.水是生命之源,电解水实验如图所示,与直流电源正极相连的玻璃管中生成的气体是___________,正极与负极气体的体积之比为___________反应的化学方程式为___________。
三、推断题
19.A~H都是初中化学中的常见物质,它们之间的转化关系如图所示。A是天然气的主要成分,E是一种常见的食品干燥剂。请回答:
(1)A的化学式为_______;H的化学式为_______
(2)反应③的基本反应类型是_____________;
(3)反应②的化学方程式为__________;反应④的化学方程式为_________________。
20.A、B、C、D、E是初中化学中常见的物质,均由碳、氢、氧中的一种或几种元素组成。其中C能供给呼吸;D是一种气体肥料;E由三种元素组成,可作燃料。这些物质之间的转化关系如图所示。
(1)B的化学式为_______________。B→C的基本反应类型是_____________。
(2)反应A→B的化学方程式是____________________。
(3)反应E→D的化学方程式是____________________。
四、实验题
21.同学们用如图所示试验验证质量守恒定律。请根据图回答下列问题。
(1)①在实验一中,在实验前称量,天平左盘中物质的质量是27.6克,则右盘中砝码的质量是25g,则游码的质量是______。
②白磷燃烧过程中锥形瓶中观察到的现象为______,实验过程中小气球的变化为______。
③燃烧后冷却到室温,再次将锥形瓶放到托盘天平上称量,发现托盘天平不能保持平衡,造成这种现象的原因可能是______。
(2)实验二中铁钉与硫酸铜反应的化学方程式是______。该实验______(填“遵守”或“不遵守”)质量守恒定律。
(3)实验三中化学反应前后天平______(填“平衡”或“不平衡”),原因是:用化学方程式解释______。
22.实验室制取氧气,提供了下列药品和常用装置,请按要求回答有关问题:
药品:①过氧化氢溶液②氯酸钾③二氧化锰
(1)装置中仪器a的名称为___________。
(2)若小明选择装置A和C来制取氧气。则他选择的药品应为___________(填序号)。反应的符号表达式为___________。若用装置C收集氧气,则验满的操作方法为___________,观察木条是否复燃。
(3)某气体X可用D装置收集,若改用F装置收集,则气体X应从___________口进(填“b”或“c”)。
(4)若用过氧化氢溶液制取氧气时应选择的发生装置是___________,有关的符号表达式为___________。若收集一瓶更纯净的氧气应选择的收集装置是___________。
(5)使用F图所示装置收集O2,若将装置翻转过来再装满水,O2由___________口进入。
(6)今年我县正在进行“煤改气”工程。“气”的主要成分甲烷是一种无色、无味,密度小于空气的气体,难溶于水。实验室常用加热无水醋酸钠和碱石灰的固体混合物来制取,请选择实验室制取甲烷时的发生装置是___________,收集装置是___________或___________(从A-E中选)。
五、计算题
23.8.4gFe在氧气中完全燃烧,生成______克四氧化三铁,消耗______克氧气。
24.草酸亚铁(化学式为FeC2O4)是生产锂电池的原材料,它受热易分解,会产生一氧化碳、二氧化碳和铁的氧化物( FexOy)这三种物质,现将28.8g草酸亚铁放置于试管中进行加热,加热到最后得到铁的氧化物质量为14.4g,求铁的氧化物的化学式是__________。
(提示:化学反应前后元素的种类和质量不变)(写出详细的计算过程)。
参考答案
1.D 2.C 3.D 4.C 5.D 6.C 7.C 8.C 9.C 10.D 11.A 12.A 13.C 14.D 15.D
16.(1) 过滤 吸附
(2) 肥皂水 泡沫较少浮渣较多 煮沸
(3)一水多用
(4) 氢气
(5)ACD
17.(1)
(2)催化
(3)放出大量热,发出白光,生成使澄清石灰水变浑浊的气体
(4) 未等到火柴梗快要燃尽时铁丝就伸入集气瓶中或铁丝生锈等
(5)助燃性或氧化性
(6)木条立刻熄灭
18.氧气 1:2
19.CH4 CaCO3 化合反应 CO2+2NaOH=Na2CO3+H2O Ca(OH)2 + Na2CO3 = CaCO3↓ + 2NaOH
20.H2O 分解反应 2H2O22H2O+O2↑ C2H5OH+3O22CO2+3H2O
21.
(1) 2.6g 放出热量,产生大量白烟 气球先胀大,后缩小 装置漏气
(2)
遵守
(3) 不平衡
22.
(1)试管
(2) ②③ KClO3KCl+O2 将带火星木条伸到集气瓶口处
(3)c
(4) B H2O2H2O+O2 E
(5)b
(6) A D E
23.11.6 3.2
24.由质量守恒定律可知,反应前后,铁元素质量不变,所以可以计算出原草酸亚铁中铁元素的质量为:;
加热后得到的铁的氧化物中:
由此可求所得铁的氧化物中,铁原子和氧原子的原子个数比=
所以,所得的铁的氧化物的化学式为:
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
