第三单元 物质构成的奥秘单元测试卷—2021-2022学年九年级化学人教版上册(word 含解析)
文档属性
| 名称 | 第三单元 物质构成的奥秘单元测试卷—2021-2022学年九年级化学人教版上册(word 含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 74.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-02 00:00:00 | ||
图片预览



文档简介
第三单元《物质构成的奥秘》单元测试卷
一、单选题(共15小题)
1.凉开水不宜养鱼,其主要原因是凉开水中几乎不含有( )
A. 水分子
B. 氧原子
C. 氧元素
D. 氧分子
2.干冰升华后体积变大的原因是( )
A. 分子体积变大
B. 分子间隔变大
C. 分子数量增多
D. 分子碰撞频率减小
3.紫薯中含有被誉为“抗癌大王”的硒元素。已知硒原子的核电荷数为34,中子数为44,则硒原子的核外电子数为( )
A. 10
B. 44
C. 34
D. 78
4.碳元素和氧元素最本质的区别是( )
A. 质子数不同
B. 中子数不同
C. 相对原子质量不同
D. 中子数和核外电子数之和不同
5.下列物质中,由离子构成的是( )
A. 氯化钠
B. 金
C. 氢气
D. 金刚石
6.元素在自然界里分布并不均匀,如智利富藏铜矿,澳大利亚多铁矿,山东的黄金储量居我国首位,但从整个的地壳含量的多少分析,最丰富的金属元素是( )
A. Fe
B. Al
C. O
D. Si
7.如图是元素周期表中锂元素的图例说明,图中没有直接给出的信息是( )
A. 原子序数
B. 元素符号
C. 最外层电子数
D. 相对原子质量
8.下列结构示意图表示元素周期表中第二周期元素的原子是( )
A. ①②③
B. ①②
C. ②④
D. ①②④
9.生活中的下列现象,可用分子的知识加以解释,其中正确的是( )
A. 蔗糖溶解是因为分子很小
B. 墙内开花墙外香是因为分子在不断运动
C. 热胀冷缩是因为分子大小随温度而改变
D. 气体易被压缩是因为气体分子间隔很小
10.美国为首的北约在科索沃战场上投下了至少10吨贫铀炸弹,使不少人患上“巴尔干综合征”。贫铀弹的主要成分是低放射性的铀,铀原子的相对原子质量为238,核电荷数为92,中子数应为( )
A. 146
B. 92
C. 136
D. 238
11.下列各种微粒结构示意图中,与表示的意义一致的是( )
A. 都属于阳离子:
B. 都属于阴离子:
C. 属于同一种元素:
D. 属于同一种原子:
12.日常生活中见到的“加碘食盐”“高钙牛奶”中“碘、钙”应理解为( )
A. 分子
B. 原子
C. 离子
D. 元素
13.原子序数为94的钚(Pu)是一种核原料,该元素一种原子的质子数和中子数之和为239,下列关于该原子的说法不正确的是( )
A. 中子数为145
B. 核外电子数为94
C. 质子数为94
D. 核电荷数为239
14.有关原子的相对质量的说法正确的是( )
A. 相对原子质量的单位是g
B. 相对原子质量就是原子的质量
C. 相对原子质量是以一种碳12原子质量的1/12作为标准,其他原子的质量跟它比较所得的比
D. 通常情况下,相对原子质量是以“千克” 为单位
15.下列现象中,能充分说明“分子在不停地运动”的是( )
A. 春天,冰雪开始融化
B. 气体热胀冷缩
C. 真金不怕火烧
D. 墙内开花墙外香
二、填空题(共3小题)
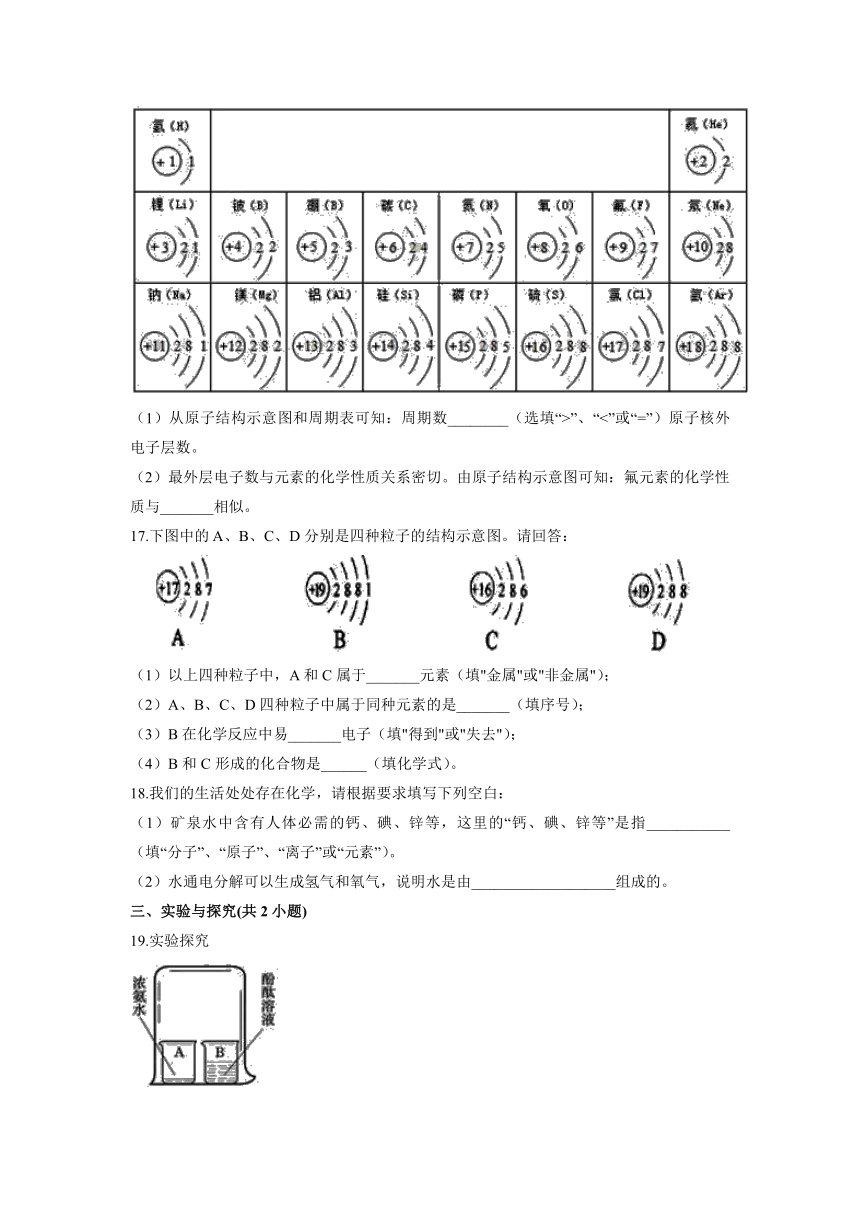
16.下图是元素周期表的一部分,请根据元素周期表回答下列问题。
(1)从原子结构示意图和周期表可知:周期数________(选填“>”、“<”或“=”)原子核外电子层数。
(2)最外层电子数与元素的化学性质关系密切。由原子结构示意图可知:氟元素的化学性质与_______相似。
17.下图中的 A、B、C、D 分别是四种粒子的结构示意图。请回答:
(1)以上四种粒子中,A 和 C 属于_______元素(填"金属"或"非金属");
(2)A、B、C、D 四种粒子中属于同种元素的是_______(填序号);
(3)B 在化学反应中易_______电子(填"得到"或"失去");
(4)B 和 C 形成的化合物是______(填化学式)。
18.我们的生活处处存在化学,请根据要求填写下列空白:
(1)矿泉水中含有人体必需的钙、碘、锌等,这里的“钙、碘、锌等”是指___________(填“分子”、“原子”、“离子”或“元素”)。
(2)水通电分解可以生成氢气和氧气,说明水是由___________________组成的。
三、实验与探究(共2小题)
19.实验探究
(1)实验方法:如图所示:在A烧杯中盛有浓氨水,在盛有20mL水的B烧杯中加入5~6滴酚酞溶液,从B烧杯中取少量溶液置于试管中,向其中滴加浓氨水,用一个大烧杯罩住AB两个小烧杯。
(2)实验现象:①过一会儿,观察到的现象:试管中的现象_________________________,
②AB烧杯中的现象__________________________________。
(3)你的猜想:_________________________________________________。
(4)讨论交流:与小组同学交流你的看法:往装有酚酞溶液的试管中加浓氨水这样操作的
目的_________________________________________________。
20.实验探究:某化学兴趣小组同学为了研究影响分子运动速率的因素,如下图所示,玻璃管左、右两端分别放有脱脂棉,注射器中分别装有浓盐酸和浓氨水。浓氨水挥发出来的氨气(NH3)和浓盐酸挥发出来的氯化氢气体(HCl)能发生反应生成白色的氯化铵固体。两个注射器同时向脱脂棉靠近里边的部位注入等体积的液体,过一会,先在A处产生大量白烟,然后白烟逐渐充满整个试管。
根据现象回答问题:
(1)A处形成白烟是因为分子在___________________________;
(2)有同学认为先在A处产生白烟是因为氯化氢分子比氨气分子运动速度__________,已知一个氯化氢分子的质量要大于一个氨气分子的质量,所以可以说分子的运动速度与其质量成__________比。(填正或反)
答案解析
1.【答案】D
【解析】鱼儿呼吸需要氧气,而氧气是由氧分子构成的;凉开水是由水分子构成的;水分子是由氢原子和氧原子构成的;凉开水是由氢元素和氧元素组成的。水烧开后,其中溶解的氧气会大量逸出,凉开水不宜养鱼,其主要原因是凉开水中几乎不含有氧气或者氧分子。故答案应选D。
2.【答案】B
【解析】干冰是固体的二氧化碳,升华后变为气体的二氧化碳,二氧化碳分子之间的间隔变大,所以干冰升华后体积变大,故选B。
3.【答案】C
【解析】在原子中,核电荷数=质子数=核外电子数,故答案选C。
4.【答案】A
【解析】元素为具有相同质子数即核电荷数的一类原子的总称,也就是说质子数决定元素种类,故碳元素和氧元素最本质的区别是质子数不同。故答案应选A。
5.【答案】A
【解析】构成物质的微粒有三种:分子、原子、离子,由分子直接构成的物质:非金属气体单质、酸和多数氧化物;由原子直接构成的物质:金属、稀有气体、金刚石、石墨等;由离子直接构成的物质:碱、盐,如氯化钠。故答案应选A。
6.【答案】B
【解析】地壳中含量最多的元素是铝元素,故选B。
7.【答案】C
【解析】根据元素周期表中的一格中获取的信息,该元素原子序数为3,元素符号为Li,相对原子质量为6.941,不能直接给出最外层电子数信息。所以应选C项。
8.【答案】C
【解析】周期数由电子层数决定,第二周期的元素的原子有两个电子层,原子中质子数等于电子数。①中质子数不等于电子数,不属于原子,选项A、B、D错误; ②④符合题目要求。故答案选C。
9.【答案】B
【解析】A.蔗糖溶解是因为分子在不断运动,而不是分子很小,错误;B.墙内开花墙外香是因为分子在不断运动,正确;C.热胀冷缩是因为分子的间隔大小随温度而改变,而不是分子大小,错误;D.气体易被压缩是因为气体分子间隔大,故容易压缩,错误。故选B
10.【答案】A
【解析】在原子中,原子序数=质子数=核外电子数=核电荷数;质子数+中子数=相对原子质量,故选A.
11.【答案】C
【解析】构成物质的微粒中质子数=核外电子数的为原子;质子数>核外电子数为阳离子;质子数<核外电子数为阴离子;质子数相同的微粒为同种元素的原子;A选项都属于阳离子是错误的,前者为原子。后者为阳离子;B选项都属于阴离子是错误的,前者为阴离子,后者为原子;C选项是同种元素的微粒是正确的,分别为镁离子和镁原子;D选项是同种元素的原子是错误的叙述,二者的质子数不同,属于不同种元素。故答案选C
12.【答案】D
【解析】日常生活中见到的“加碘食盐”“高钙牛奶”中“碘、钙”应理解为元素,故选D
13.【答案】D
【解析】在原子,中原子序数=质子数=核外电子数=核电荷数;质子数+中子数=相对原子质量,故选D
14.【答案】C
【解析】化学上规定,相对原子质量是以一种碳12原子质量的1/12作为标准,其他原子的质量跟它比较所得的比,无质量单位。所以答案选C。
15.【答案】D
【解析】春天,冰雪开始融化,是物质状态的改变,是由于水分子之间的间隔发生了改变;气体热胀冷缩是由于构成气体的分子之间的间隔发生改变的结果;真金不怕火烧说明了金的化学性质不活泼,很难和氧气发生化学反应;墙内开花墙外香是由于分子在不停运动的结果。所以答案选D。
16.【答案】(1)=(2)氯
【解析】从原子结构示意图和周期表可知:周期数等于原子核外电子层数,最外层电子数与元素的化学性质关系密切。由原子结构示意图可知:氟元素与氯元素的最外电子数相等,因此它们的化学性质相似。
17.【答案】(1)非金属 (2)BD (3)失去 (4)K2S
【解析】以上四种粒子中 A 和 C 都是原子结构示意图,最外层电子数多于4个,属于非金属元素;
元素的种类是由质子数决定的,则A、B、C、D 四种粒子中属于同种元素的是BD; B表示的是原子结构示意图,最外层有1个电子,在化学反应中易失去电子;根据B 和 C原子的最外层电子数,形成的化合物是K2S。
18.【答案】(1)元素 (2)氢元素和氧元素
【解析】(1)矿泉水中含有人体必需的钙、碘、锌等,这里的“钙、碘、锌等”是指元素。
(2)水通电分解可以生成氢气和氧气,说明水是由氢元素和氧元素组成的。
19.【答案】(2)①液体变为红色 ;②A无明显变化,B烧杯中酚酞变红;
(3)分子在不断地运动;
(4)说明浓氨水能使酚酞变红
【解析】浓氨水显碱性能够使无色酚酞变红色,A烧杯中浓氨水中的氨气分子是不断运动着的,氨气分子运动到B烧杯中,能够使B烧杯中的无色酚酞变红,所以可以观察到B烧杯中酚酞变红,这一现象从而也证明了分子是不断运动的。往装有酚酞溶液的试管中加浓氨水这样操作的目的正是说明浓氨水能使酚酞变红。
20.【答案】(1)不停地运动(2)慢 反
【解析】由于浓盐酸中的氯化氢分子和浓氨水中的氨气分子都在不停地运动,所以会在A处形成白烟。形成的白烟在A处,离浓盐酸较近,离浓氨水较远,这是因为氯化氢分子运动速度比氨气分子运动速度慢。已知一个氯化氢分子的质量要大于一个氨气分子的质量,所以可以说分子的运动速度与其质量成反比。
一、单选题(共15小题)
1.凉开水不宜养鱼,其主要原因是凉开水中几乎不含有( )
A. 水分子
B. 氧原子
C. 氧元素
D. 氧分子
2.干冰升华后体积变大的原因是( )
A. 分子体积变大
B. 分子间隔变大
C. 分子数量增多
D. 分子碰撞频率减小
3.紫薯中含有被誉为“抗癌大王”的硒元素。已知硒原子的核电荷数为34,中子数为44,则硒原子的核外电子数为( )
A. 10
B. 44
C. 34
D. 78
4.碳元素和氧元素最本质的区别是( )
A. 质子数不同
B. 中子数不同
C. 相对原子质量不同
D. 中子数和核外电子数之和不同
5.下列物质中,由离子构成的是( )
A. 氯化钠
B. 金
C. 氢气
D. 金刚石
6.元素在自然界里分布并不均匀,如智利富藏铜矿,澳大利亚多铁矿,山东的黄金储量居我国首位,但从整个的地壳含量的多少分析,最丰富的金属元素是( )
A. Fe
B. Al
C. O
D. Si
7.如图是元素周期表中锂元素的图例说明,图中没有直接给出的信息是( )
A. 原子序数
B. 元素符号
C. 最外层电子数
D. 相对原子质量
8.下列结构示意图表示元素周期表中第二周期元素的原子是( )
A. ①②③
B. ①②
C. ②④
D. ①②④
9.生活中的下列现象,可用分子的知识加以解释,其中正确的是( )
A. 蔗糖溶解是因为分子很小
B. 墙内开花墙外香是因为分子在不断运动
C. 热胀冷缩是因为分子大小随温度而改变
D. 气体易被压缩是因为气体分子间隔很小
10.美国为首的北约在科索沃战场上投下了至少10吨贫铀炸弹,使不少人患上“巴尔干综合征”。贫铀弹的主要成分是低放射性的铀,铀原子的相对原子质量为238,核电荷数为92,中子数应为( )
A. 146
B. 92
C. 136
D. 238
11.下列各种微粒结构示意图中,与表示的意义一致的是( )
A. 都属于阳离子:
B. 都属于阴离子:
C. 属于同一种元素:
D. 属于同一种原子:
12.日常生活中见到的“加碘食盐”“高钙牛奶”中“碘、钙”应理解为( )
A. 分子
B. 原子
C. 离子
D. 元素
13.原子序数为94的钚(Pu)是一种核原料,该元素一种原子的质子数和中子数之和为239,下列关于该原子的说法不正确的是( )
A. 中子数为145
B. 核外电子数为94
C. 质子数为94
D. 核电荷数为239
14.有关原子的相对质量的说法正确的是( )
A. 相对原子质量的单位是g
B. 相对原子质量就是原子的质量
C. 相对原子质量是以一种碳12原子质量的1/12作为标准,其他原子的质量跟它比较所得的比
D. 通常情况下,相对原子质量是以“千克” 为单位
15.下列现象中,能充分说明“分子在不停地运动”的是( )
A. 春天,冰雪开始融化
B. 气体热胀冷缩
C. 真金不怕火烧
D. 墙内开花墙外香
二、填空题(共3小题)
16.下图是元素周期表的一部分,请根据元素周期表回答下列问题。
(1)从原子结构示意图和周期表可知:周期数________(选填“>”、“<”或“=”)原子核外电子层数。
(2)最外层电子数与元素的化学性质关系密切。由原子结构示意图可知:氟元素的化学性质与_______相似。
17.下图中的 A、B、C、D 分别是四种粒子的结构示意图。请回答:
(1)以上四种粒子中,A 和 C 属于_______元素(填"金属"或"非金属");
(2)A、B、C、D 四种粒子中属于同种元素的是_______(填序号);
(3)B 在化学反应中易_______电子(填"得到"或"失去");
(4)B 和 C 形成的化合物是______(填化学式)。
18.我们的生活处处存在化学,请根据要求填写下列空白:
(1)矿泉水中含有人体必需的钙、碘、锌等,这里的“钙、碘、锌等”是指___________(填“分子”、“原子”、“离子”或“元素”)。
(2)水通电分解可以生成氢气和氧气,说明水是由___________________组成的。
三、实验与探究(共2小题)
19.实验探究
(1)实验方法:如图所示:在A烧杯中盛有浓氨水,在盛有20mL水的B烧杯中加入5~6滴酚酞溶液,从B烧杯中取少量溶液置于试管中,向其中滴加浓氨水,用一个大烧杯罩住AB两个小烧杯。
(2)实验现象:①过一会儿,观察到的现象:试管中的现象_________________________,
②AB烧杯中的现象__________________________________。
(3)你的猜想:_________________________________________________。
(4)讨论交流:与小组同学交流你的看法:往装有酚酞溶液的试管中加浓氨水这样操作的
目的_________________________________________________。
20.实验探究:某化学兴趣小组同学为了研究影响分子运动速率的因素,如下图所示,玻璃管左、右两端分别放有脱脂棉,注射器中分别装有浓盐酸和浓氨水。浓氨水挥发出来的氨气(NH3)和浓盐酸挥发出来的氯化氢气体(HCl)能发生反应生成白色的氯化铵固体。两个注射器同时向脱脂棉靠近里边的部位注入等体积的液体,过一会,先在A处产生大量白烟,然后白烟逐渐充满整个试管。
根据现象回答问题:
(1)A处形成白烟是因为分子在___________________________;
(2)有同学认为先在A处产生白烟是因为氯化氢分子比氨气分子运动速度__________,已知一个氯化氢分子的质量要大于一个氨气分子的质量,所以可以说分子的运动速度与其质量成__________比。(填正或反)
答案解析
1.【答案】D
【解析】鱼儿呼吸需要氧气,而氧气是由氧分子构成的;凉开水是由水分子构成的;水分子是由氢原子和氧原子构成的;凉开水是由氢元素和氧元素组成的。水烧开后,其中溶解的氧气会大量逸出,凉开水不宜养鱼,其主要原因是凉开水中几乎不含有氧气或者氧分子。故答案应选D。
2.【答案】B
【解析】干冰是固体的二氧化碳,升华后变为气体的二氧化碳,二氧化碳分子之间的间隔变大,所以干冰升华后体积变大,故选B。
3.【答案】C
【解析】在原子中,核电荷数=质子数=核外电子数,故答案选C。
4.【答案】A
【解析】元素为具有相同质子数即核电荷数的一类原子的总称,也就是说质子数决定元素种类,故碳元素和氧元素最本质的区别是质子数不同。故答案应选A。
5.【答案】A
【解析】构成物质的微粒有三种:分子、原子、离子,由分子直接构成的物质:非金属气体单质、酸和多数氧化物;由原子直接构成的物质:金属、稀有气体、金刚石、石墨等;由离子直接构成的物质:碱、盐,如氯化钠。故答案应选A。
6.【答案】B
【解析】地壳中含量最多的元素是铝元素,故选B。
7.【答案】C
【解析】根据元素周期表中的一格中获取的信息,该元素原子序数为3,元素符号为Li,相对原子质量为6.941,不能直接给出最外层电子数信息。所以应选C项。
8.【答案】C
【解析】周期数由电子层数决定,第二周期的元素的原子有两个电子层,原子中质子数等于电子数。①中质子数不等于电子数,不属于原子,选项A、B、D错误; ②④符合题目要求。故答案选C。
9.【答案】B
【解析】A.蔗糖溶解是因为分子在不断运动,而不是分子很小,错误;B.墙内开花墙外香是因为分子在不断运动,正确;C.热胀冷缩是因为分子的间隔大小随温度而改变,而不是分子大小,错误;D.气体易被压缩是因为气体分子间隔大,故容易压缩,错误。故选B
10.【答案】A
【解析】在原子中,原子序数=质子数=核外电子数=核电荷数;质子数+中子数=相对原子质量,故选A.
11.【答案】C
【解析】构成物质的微粒中质子数=核外电子数的为原子;质子数>核外电子数为阳离子;质子数<核外电子数为阴离子;质子数相同的微粒为同种元素的原子;A选项都属于阳离子是错误的,前者为原子。后者为阳离子;B选项都属于阴离子是错误的,前者为阴离子,后者为原子;C选项是同种元素的微粒是正确的,分别为镁离子和镁原子;D选项是同种元素的原子是错误的叙述,二者的质子数不同,属于不同种元素。故答案选C
12.【答案】D
【解析】日常生活中见到的“加碘食盐”“高钙牛奶”中“碘、钙”应理解为元素,故选D
13.【答案】D
【解析】在原子,中原子序数=质子数=核外电子数=核电荷数;质子数+中子数=相对原子质量,故选D
14.【答案】C
【解析】化学上规定,相对原子质量是以一种碳12原子质量的1/12作为标准,其他原子的质量跟它比较所得的比,无质量单位。所以答案选C。
15.【答案】D
【解析】春天,冰雪开始融化,是物质状态的改变,是由于水分子之间的间隔发生了改变;气体热胀冷缩是由于构成气体的分子之间的间隔发生改变的结果;真金不怕火烧说明了金的化学性质不活泼,很难和氧气发生化学反应;墙内开花墙外香是由于分子在不停运动的结果。所以答案选D。
16.【答案】(1)=(2)氯
【解析】从原子结构示意图和周期表可知:周期数等于原子核外电子层数,最外层电子数与元素的化学性质关系密切。由原子结构示意图可知:氟元素与氯元素的最外电子数相等,因此它们的化学性质相似。
17.【答案】(1)非金属 (2)BD (3)失去 (4)K2S
【解析】以上四种粒子中 A 和 C 都是原子结构示意图,最外层电子数多于4个,属于非金属元素;
元素的种类是由质子数决定的,则A、B、C、D 四种粒子中属于同种元素的是BD; B表示的是原子结构示意图,最外层有1个电子,在化学反应中易失去电子;根据B 和 C原子的最外层电子数,形成的化合物是K2S。
18.【答案】(1)元素 (2)氢元素和氧元素
【解析】(1)矿泉水中含有人体必需的钙、碘、锌等,这里的“钙、碘、锌等”是指元素。
(2)水通电分解可以生成氢气和氧气,说明水是由氢元素和氧元素组成的。
19.【答案】(2)①液体变为红色 ;②A无明显变化,B烧杯中酚酞变红;
(3)分子在不断地运动;
(4)说明浓氨水能使酚酞变红
【解析】浓氨水显碱性能够使无色酚酞变红色,A烧杯中浓氨水中的氨气分子是不断运动着的,氨气分子运动到B烧杯中,能够使B烧杯中的无色酚酞变红,所以可以观察到B烧杯中酚酞变红,这一现象从而也证明了分子是不断运动的。往装有酚酞溶液的试管中加浓氨水这样操作的目的正是说明浓氨水能使酚酞变红。
20.【答案】(1)不停地运动(2)慢 反
【解析】由于浓盐酸中的氯化氢分子和浓氨水中的氨气分子都在不停地运动,所以会在A处形成白烟。形成的白烟在A处,离浓盐酸较近,离浓氨水较远,这是因为氯化氢分子运动速度比氨气分子运动速度慢。已知一个氯化氢分子的质量要大于一个氨气分子的质量,所以可以说分子的运动速度与其质量成反比。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
