第五单元 课题1质量守恒定律学案—2021-2022学年九年级化学人教版上册
文档属性
| 名称 | 第五单元 课题1质量守恒定律学案—2021-2022学年九年级化学人教版上册 |
|
|
| 格式 | docx | ||
| 文件大小 | 416.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-02 00:00:00 | ||
图片预览

文档简介
第五单元 化学方程式
课题1 质量守恒定律
【本周必背】
知识点1. 质量守恒定律的内容
参加化学反应的________________等于反应后_________________叫做质量守恒定律。
注意:
质量守恒只强调“质量”守恒,不包含体积等守恒。
质量守恒定律是指 的各物质的质量总和等于生成的各物质质量总和,各物质应包含液态,固态,气态所有物质。
(3)给定物质的质量 都参与反应。
知识点2. 验证质量守恒定律
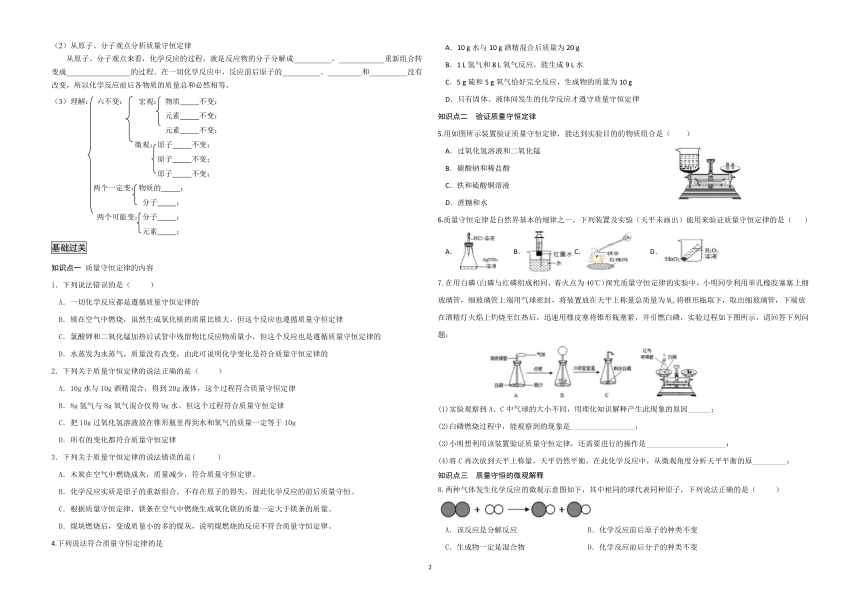
(1)红磷燃烧实验
原理: 。
现象: 气球 ,天平平衡。
结论:红磷燃烧前后,物质的总质量不变。
实验小结:
①实验成功的关键:装置的____________要良好。
②玻璃管下端与红磷接触的目的:点燃红磷。
③气球的作用:如不安装气球,则橡皮塞会被膨胀的气体冲起或导致锥形瓶炸裂。
④锥形瓶底部不铺上细沙的后果:锥形瓶__________。
(2)铁钉跟硫酸铜溶液反应实验
原理:
实验现象:铁钉表面附着一层__________物质,溶液由蓝色逐渐变成浅绿色。将烧杯放回托盘后,天平保持平衡。
结论:参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。
盐酸与碳酸钠粉末反应实验
原理: 。
现象: 粉末 ,有 生成,天平向 偏
原因: 生成的二氧化碳逸出
注意:有 生成时,验证质量守恒定律时必须在 体系中进行。
镁条燃烧实验
原理: 。
现象: 镁条燃烧,发出耀眼的 ,生成 固体,放出热量,天平向 偏
原因: 天平向 偏因为
知识点3. 质量守恒定律的原因
(1)水分解成氢气和氧气的示意图
m(参加反应的水)= m(氢气)+ m(氧气)
反应前后 没有改变, 没有增减, 也没有变化。
(2)从原子、分子观点分析质量守恒定律
从原子、分子观点来看,化学反应的过程,就是反应物的分子分解成__________,____________重新组合转变成_________________的过程。在一切化学反应中,反应前后原子的__________、_________和__________没有改变,所以化学反应前后各物质的质量总和必然相等。
(3)理解: 六不变: 宏观: 物质 不变;
元素 不变;
元素 不变;
微观:原子 不变;
原子 不变;
原子 不变;
两个一定变:物质的 ;
分子 ;
两个可能变:分子 ;
元素 ;
基础过关
知识点一 质量守恒定律的内容
1.下列说法错误的是( )
A.一切化学反应都是遵循质量守恒定律的
B.镁在空气中燃烧,虽然生成氧化镁的质量比镁大,但这个反应也遵循质量守恒定律
C.氯酸钾和二氧化锰加热后试管中残留物比反应物质量小,但这个反应也是遵循质量守恒定律的
D.水蒸发为水蒸气,质量没有改变,由此可说明化学变化是符合质量守恒定律的
2.下列关于质量守恒定律的说法正确的是( )
A.10g水与10g酒精混合,得到20g液体,这个过程符合质量守恒定律
B.8g氢气与8g氧气混合仅得9g水,但这个过程符合质量守恒定律
C.把10g过氧化氢溶液放在锥形瓶里得到水和氧气的质量一定等于10g
D.所有的变化都符合质量守恒定律
3.下列关于质量守恒定律的说法错误的是( )
A.木炭在空气中燃烧成灰,质量减少,符合质量守恒定律。
B.化学反应实质是原子的重新组合,不存在原子的得失,因此化学反应的前后质量守恒。
C.根据质量守恒定律,镁条在空气中燃烧生成氧化镁的质量一定大于镁条的质量。
D.煤块燃烧后,变成质量小的多的煤灰,说明煤燃烧的反应不符合质量守恒定律。
4.下列说法符合质量守恒定律的是
A.10 g水与10 g酒精混合后质量为20 g
B.1 L氢气和8 L氧气反应,能生成9 L水
C.5 g硫和5 g氧气恰好完全反应,生成物的质量为10 g
D.只有固体、液体间发生的化学反应才遵守质量守恒定律
知识点二 验证质量守恒定律
5.用如图所示装置验证质量守恒定律,能达到实验目的的物质组合是( )
A.过氧化氢溶液和二氧化锰
B.碳酸钠和稀盐酸
C.铁和硫酸铜溶液
D.蔗糖和水
6.质量守恒定律是自然界基本的规律之一。下列装置及实验(天平未画出)能用来验证质量守恒定律的是( )
A. B. C. D.
7.在用白磷(白磷与红磷组成相同,着火点为40℃)探究质量守恒定律的实验中,小明同学利用单孔橡胶塞塞上细玻璃管,细玻璃管上端用气球密封,将装置放在天平上称量总质量为M1,将锥形瓶取下,取出细玻璃管,下端放在酒精灯火焰上灼烧至红热后,迅速用橡皮塞将锥形瓶塞紧,并引燃白磷,实验过程如下图所示,请回答下列问题:
(1)实验观察到A、C中气球的大小不同,用理化知识解释产生此现象的原因______;
(2)白磷燃烧过程中,能观察到的现象是_________________;
(3)小明想利用该装置验证质量守恒定律,还需要进行的操作是_____________________;
(4)将C再次放到天平上称量,天平仍然平衡,在此化学反应中,从微观角度分析天平平衡的原_________;
知识点三 质量守恒的微观解释
8.两种气体发生化学反应的微观示意图如下,其中相同的球代表同种原子,下列说法正确的是( )
A.该反应是分解反应 B.化学反应前后原子的种类不变
C.生成物一定是混合物 D.化学反应前后分子的种类不变
9.如图是工业上将煤转化为清洁能源的微观示意图:
(其中“”表示碳原子,“”表示氧原子,“”表示氢原子)有关说法不正确的是( )
A.图中“” “” 都属于氧化物 B.该反应类型为置换反应
C.反应前后原子的种类和数目保持不变 D.由一个氧原子和一个氢分子构成
10.用 代表两种不同的单质分子,它们在一定条件下能发生化学反应,反应前后的模拟模型如下图所示,下列说法正确的是( )
A.参加反应的“ ”和“ ”分子的个数比是 2︰1
B.该反应是化合反应
C.该反应有2种生成物
D.每个生成物分子由3个原子构成
知识点四 质量守恒的应用
11.某物质和二氧化碳反应后只生成碳酸钠和氧气,则该物质中( )
A.只含氧元素 B.一定含钠元素和氧元素
C.只含钠元素 D.一定含钠元素,可能含氧元素
12.将“神舟七号”飞船送入太空的是“长征二号”F运载火箭,火箭工作中发生的反应为:C2H8N2+2R=3N2+4H2O+2CO2;其中R的化学式是( )
A.N2O4 B.NO2 C.N2O D.NH3
13. 在一个密闭容器中放入M、N、Q、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如表,则下列关于该反应的认识不正确的是( )
物质 M N Q P
反应前质量(g) 18 1 2 32
反应后质量(g) X 26 2 12
A.该变化的基本反应类型是分解反应 B.反应后物质M的质量为13g
C.发生改变的N、P的质量比为5:4 D.物质Q可能是该反应的催化剂
14.在化学反应A+2B = 2C+D中,6gA和8gB 恰好完全反应,生成9gD。若反应生成15gC,则参加反应的A的质量为( )
A.18g B.24g C.12g D.16g
达标巩固
1.下列变化,遵循质量守恒定律的是
A.铁丝在氧气中燃烧质量变大 B.2 g H2完全燃烧生成36 g H2O
C.铁锭压制成铁板 D.水的质量和受热变成水蒸气的质量相等
2.下列叙述完全符合质量守恒定律的是( )
A.水结成冰前后,质量保持不变
B.50mL水和50 mL乙醇混合后总体积小于100mL
C.在100g过氧化氢溶液中,含有30g过氧化氢和70g水
D.1.2g碳与3.2g氧气恰好完全反应可生成4.4g二氧化碳
3.下图是制取乙醇的反应微观示意图。下列说法正确的是( )
A.反应前后共有四种分子 B.反应物中只有一种物质是氧化物
C.反应前后催化剂的性质不变 D.参加反应的和分子个数比是3:2
4.从下图某化学反应的微观示意图中,获得的信息错误的是( )
A.参加反应的一种物质的化学式为C2H4 B.该反应的生成物为混合物
C.参加反应的两种物质的分子个数比为1:1 D.中碳、氢、氧原子个数比为2:6:1
5.金属铝的冶炼要用到冰晶石,制备冰晶石的化学方程式为(冰晶石用A表示):12HF+3Na2CO3+2Al(OH)32A+3CO2+9H2O,则A的化学式为
A.NaAlF6 B.Na2AlF4 C.Na3AlF6 D.Na3Al2F3
6.某纯净物 X 在空气中完全燃烧,反应的化学方程式为:X+2O2 = CO2+2H2O,下列关于 X 的说法正确的是( )
A.X 由碳、氢、氧三种元素组成
B.X 一定含碳、氢两种元素,可能含氧元素
C.X 中碳、氢元素的质量比为 1:4
D.X 的相对分子质量为 16
7.在反应A+3B=2C+3D中,已知A和B的相对分子质量之比为7:8,当2.8gA与一定量B恰好完全反应后,生成3.6gD,则C的质量为( )
A.6.8g B.9.6g C.8.8g D.4.4g
8.在化学反应A+B2=AB2中,A与B2反应的质量关系如图所示,将5gA与8gB2充分反应,则生成AB2的质量是( )
A.10g B.13g C.16g D.18g
9.某有机物在9.6g氧气中恰好完全燃烧,生成8.8gCO2和5.4gH2O,下列说法正确的是( )
A.该有机物只含碳、氢两种元素
B.该有机物中一定含有碳、氢元素,可能含有氧元素
C.该有机物中一定含有碳、氢、氧三种元素
D.无法确定
10.在一个密闭容器内有甲、乙、丙、丁四种物质,经过反应一段时间后,测得反应前后各物质的质量如下表所示,以下说法正确的是( )
物质 甲 乙 丙 丁
反应前质量/g 34 2 5 5
反应后质量/g 0 x 5 21
A.该反应可表示为:乙+丁=甲
B.x的值为18
C.该反应是分解反应
D.丙一定是催化剂
11.甲、乙、丙、丁种种物质在反应前后的质量关系如图所示,下列有关说法错误的是( )
A.参加反应的甲和乙质量比为2:7
B.丙可能是该反应的催化剂
C.丁一定是化合物
D.x的值是7
12.在“质量守恒定律”的课堂教学中,老师引导同学们进行“化学反应中,反应物与生成物的质量关系”的实验探究。
A,B,C,D四个实验分别巾甲、乙、丙、丁四个组的同学来完成,他们都进行了规范的操作,准确的称量和细致的观察。
(1)A实验中气球的作用是_____,该反应的化学方程式为 _;
(2)丙组同学认为C实验说明了质量守恒。该反应的化学方程式为_____;乙、丁两组同学得到的错误结论是“实验B,D均说明质量不守恒”。老师引导同学们分析了B,D两个实验反应后天平不平衡的原因。你认为B实验天平不平衡的原因是: __。D实验天平不平衡的原因是 。
(实验总结)凡是有气体参加或生成的反应,用来证明质量守恒定律时,都应该在_____中进行。
课题1 质量守恒定律
【本周必背】
知识点1. 质量守恒定律的内容
参加化学反应的________________等于反应后_________________叫做质量守恒定律。
注意:
质量守恒只强调“质量”守恒,不包含体积等守恒。
质量守恒定律是指 的各物质的质量总和等于生成的各物质质量总和,各物质应包含液态,固态,气态所有物质。
(3)给定物质的质量 都参与反应。
知识点2. 验证质量守恒定律
(1)红磷燃烧实验
原理: 。
现象: 气球 ,天平平衡。
结论:红磷燃烧前后,物质的总质量不变。
实验小结:
①实验成功的关键:装置的____________要良好。
②玻璃管下端与红磷接触的目的:点燃红磷。
③气球的作用:如不安装气球,则橡皮塞会被膨胀的气体冲起或导致锥形瓶炸裂。
④锥形瓶底部不铺上细沙的后果:锥形瓶__________。
(2)铁钉跟硫酸铜溶液反应实验
原理:
实验现象:铁钉表面附着一层__________物质,溶液由蓝色逐渐变成浅绿色。将烧杯放回托盘后,天平保持平衡。
结论:参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和。
盐酸与碳酸钠粉末反应实验
原理: 。
现象: 粉末 ,有 生成,天平向 偏
原因: 生成的二氧化碳逸出
注意:有 生成时,验证质量守恒定律时必须在 体系中进行。
镁条燃烧实验
原理: 。
现象: 镁条燃烧,发出耀眼的 ,生成 固体,放出热量,天平向 偏
原因: 天平向 偏因为
知识点3. 质量守恒定律的原因
(1)水分解成氢气和氧气的示意图
m(参加反应的水)= m(氢气)+ m(氧气)
反应前后 没有改变, 没有增减, 也没有变化。
(2)从原子、分子观点分析质量守恒定律
从原子、分子观点来看,化学反应的过程,就是反应物的分子分解成__________,____________重新组合转变成_________________的过程。在一切化学反应中,反应前后原子的__________、_________和__________没有改变,所以化学反应前后各物质的质量总和必然相等。
(3)理解: 六不变: 宏观: 物质 不变;
元素 不变;
元素 不变;
微观:原子 不变;
原子 不变;
原子 不变;
两个一定变:物质的 ;
分子 ;
两个可能变:分子 ;
元素 ;
基础过关
知识点一 质量守恒定律的内容
1.下列说法错误的是( )
A.一切化学反应都是遵循质量守恒定律的
B.镁在空气中燃烧,虽然生成氧化镁的质量比镁大,但这个反应也遵循质量守恒定律
C.氯酸钾和二氧化锰加热后试管中残留物比反应物质量小,但这个反应也是遵循质量守恒定律的
D.水蒸发为水蒸气,质量没有改变,由此可说明化学变化是符合质量守恒定律的
2.下列关于质量守恒定律的说法正确的是( )
A.10g水与10g酒精混合,得到20g液体,这个过程符合质量守恒定律
B.8g氢气与8g氧气混合仅得9g水,但这个过程符合质量守恒定律
C.把10g过氧化氢溶液放在锥形瓶里得到水和氧气的质量一定等于10g
D.所有的变化都符合质量守恒定律
3.下列关于质量守恒定律的说法错误的是( )
A.木炭在空气中燃烧成灰,质量减少,符合质量守恒定律。
B.化学反应实质是原子的重新组合,不存在原子的得失,因此化学反应的前后质量守恒。
C.根据质量守恒定律,镁条在空气中燃烧生成氧化镁的质量一定大于镁条的质量。
D.煤块燃烧后,变成质量小的多的煤灰,说明煤燃烧的反应不符合质量守恒定律。
4.下列说法符合质量守恒定律的是
A.10 g水与10 g酒精混合后质量为20 g
B.1 L氢气和8 L氧气反应,能生成9 L水
C.5 g硫和5 g氧气恰好完全反应,生成物的质量为10 g
D.只有固体、液体间发生的化学反应才遵守质量守恒定律
知识点二 验证质量守恒定律
5.用如图所示装置验证质量守恒定律,能达到实验目的的物质组合是( )
A.过氧化氢溶液和二氧化锰
B.碳酸钠和稀盐酸
C.铁和硫酸铜溶液
D.蔗糖和水
6.质量守恒定律是自然界基本的规律之一。下列装置及实验(天平未画出)能用来验证质量守恒定律的是( )
A. B. C. D.
7.在用白磷(白磷与红磷组成相同,着火点为40℃)探究质量守恒定律的实验中,小明同学利用单孔橡胶塞塞上细玻璃管,细玻璃管上端用气球密封,将装置放在天平上称量总质量为M1,将锥形瓶取下,取出细玻璃管,下端放在酒精灯火焰上灼烧至红热后,迅速用橡皮塞将锥形瓶塞紧,并引燃白磷,实验过程如下图所示,请回答下列问题:
(1)实验观察到A、C中气球的大小不同,用理化知识解释产生此现象的原因______;
(2)白磷燃烧过程中,能观察到的现象是_________________;
(3)小明想利用该装置验证质量守恒定律,还需要进行的操作是_____________________;
(4)将C再次放到天平上称量,天平仍然平衡,在此化学反应中,从微观角度分析天平平衡的原_________;
知识点三 质量守恒的微观解释
8.两种气体发生化学反应的微观示意图如下,其中相同的球代表同种原子,下列说法正确的是( )
A.该反应是分解反应 B.化学反应前后原子的种类不变
C.生成物一定是混合物 D.化学反应前后分子的种类不变
9.如图是工业上将煤转化为清洁能源的微观示意图:
(其中“”表示碳原子,“”表示氧原子,“”表示氢原子)有关说法不正确的是( )
A.图中“” “” 都属于氧化物 B.该反应类型为置换反应
C.反应前后原子的种类和数目保持不变 D.由一个氧原子和一个氢分子构成
10.用 代表两种不同的单质分子,它们在一定条件下能发生化学反应,反应前后的模拟模型如下图所示,下列说法正确的是( )
A.参加反应的“ ”和“ ”分子的个数比是 2︰1
B.该反应是化合反应
C.该反应有2种生成物
D.每个生成物分子由3个原子构成
知识点四 质量守恒的应用
11.某物质和二氧化碳反应后只生成碳酸钠和氧气,则该物质中( )
A.只含氧元素 B.一定含钠元素和氧元素
C.只含钠元素 D.一定含钠元素,可能含氧元素
12.将“神舟七号”飞船送入太空的是“长征二号”F运载火箭,火箭工作中发生的反应为:C2H8N2+2R=3N2+4H2O+2CO2;其中R的化学式是( )
A.N2O4 B.NO2 C.N2O D.NH3
13. 在一个密闭容器中放入M、N、Q、P四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如表,则下列关于该反应的认识不正确的是( )
物质 M N Q P
反应前质量(g) 18 1 2 32
反应后质量(g) X 26 2 12
A.该变化的基本反应类型是分解反应 B.反应后物质M的质量为13g
C.发生改变的N、P的质量比为5:4 D.物质Q可能是该反应的催化剂
14.在化学反应A+2B = 2C+D中,6gA和8gB 恰好完全反应,生成9gD。若反应生成15gC,则参加反应的A的质量为( )
A.18g B.24g C.12g D.16g
达标巩固
1.下列变化,遵循质量守恒定律的是
A.铁丝在氧气中燃烧质量变大 B.2 g H2完全燃烧生成36 g H2O
C.铁锭压制成铁板 D.水的质量和受热变成水蒸气的质量相等
2.下列叙述完全符合质量守恒定律的是( )
A.水结成冰前后,质量保持不变
B.50mL水和50 mL乙醇混合后总体积小于100mL
C.在100g过氧化氢溶液中,含有30g过氧化氢和70g水
D.1.2g碳与3.2g氧气恰好完全反应可生成4.4g二氧化碳
3.下图是制取乙醇的反应微观示意图。下列说法正确的是( )
A.反应前后共有四种分子 B.反应物中只有一种物质是氧化物
C.反应前后催化剂的性质不变 D.参加反应的和分子个数比是3:2
4.从下图某化学反应的微观示意图中,获得的信息错误的是( )
A.参加反应的一种物质的化学式为C2H4 B.该反应的生成物为混合物
C.参加反应的两种物质的分子个数比为1:1 D.中碳、氢、氧原子个数比为2:6:1
5.金属铝的冶炼要用到冰晶石,制备冰晶石的化学方程式为(冰晶石用A表示):12HF+3Na2CO3+2Al(OH)32A+3CO2+9H2O,则A的化学式为
A.NaAlF6 B.Na2AlF4 C.Na3AlF6 D.Na3Al2F3
6.某纯净物 X 在空气中完全燃烧,反应的化学方程式为:X+2O2 = CO2+2H2O,下列关于 X 的说法正确的是( )
A.X 由碳、氢、氧三种元素组成
B.X 一定含碳、氢两种元素,可能含氧元素
C.X 中碳、氢元素的质量比为 1:4
D.X 的相对分子质量为 16
7.在反应A+3B=2C+3D中,已知A和B的相对分子质量之比为7:8,当2.8gA与一定量B恰好完全反应后,生成3.6gD,则C的质量为( )
A.6.8g B.9.6g C.8.8g D.4.4g
8.在化学反应A+B2=AB2中,A与B2反应的质量关系如图所示,将5gA与8gB2充分反应,则生成AB2的质量是( )
A.10g B.13g C.16g D.18g
9.某有机物在9.6g氧气中恰好完全燃烧,生成8.8gCO2和5.4gH2O,下列说法正确的是( )
A.该有机物只含碳、氢两种元素
B.该有机物中一定含有碳、氢元素,可能含有氧元素
C.该有机物中一定含有碳、氢、氧三种元素
D.无法确定
10.在一个密闭容器内有甲、乙、丙、丁四种物质,经过反应一段时间后,测得反应前后各物质的质量如下表所示,以下说法正确的是( )
物质 甲 乙 丙 丁
反应前质量/g 34 2 5 5
反应后质量/g 0 x 5 21
A.该反应可表示为:乙+丁=甲
B.x的值为18
C.该反应是分解反应
D.丙一定是催化剂
11.甲、乙、丙、丁种种物质在反应前后的质量关系如图所示,下列有关说法错误的是( )
A.参加反应的甲和乙质量比为2:7
B.丙可能是该反应的催化剂
C.丁一定是化合物
D.x的值是7
12.在“质量守恒定律”的课堂教学中,老师引导同学们进行“化学反应中,反应物与生成物的质量关系”的实验探究。
A,B,C,D四个实验分别巾甲、乙、丙、丁四个组的同学来完成,他们都进行了规范的操作,准确的称量和细致的观察。
(1)A实验中气球的作用是_____,该反应的化学方程式为 _;
(2)丙组同学认为C实验说明了质量守恒。该反应的化学方程式为_____;乙、丁两组同学得到的错误结论是“实验B,D均说明质量不守恒”。老师引导同学们分析了B,D两个实验反应后天平不平衡的原因。你认为B实验天平不平衡的原因是: __。D实验天平不平衡的原因是 。
(实验总结)凡是有气体参加或生成的反应,用来证明质量守恒定律时,都应该在_____中进行。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
