第三单元 物质构成的奥秘 单元检测— 2021-2022学年九年级化学人教版上册(含部分解析)
文档属性
| 名称 | 第三单元 物质构成的奥秘 单元检测— 2021-2022学年九年级化学人教版上册(含部分解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 215.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-02 00:00:00 | ||
图片预览


文档简介
第三单元 物质构成的奥秘 单元检测
一、单项选择题(18小题)
1.物质的三态变化主要是由于 ( )
A.微粒质量发生变化
B.变成了新微粒
C.微粒大小发生变化
D.微粒间的间隔发生变化
2.核电荷数多于核外电子数的粒子一定是 ( )
A.分子 B.原子
C.阴离子 D.阳离子
3.极光是一种绚丽多彩的发光现象,其发生是由于太阳带电粒子流进入地球磁场。下列这些微粒中,不会引起极光的是 ( )
A.α粒子(氦的原子核) B.电子
C.质子 D.中子
4.氚也是一种氢原子,氚原子含有1个质子和2个中子,如图能正确表示氚原子结构的是 ( )
5.地壳中含量最多的元素是 ( )
A.氮 B.氧 C.碳 D.氢
6.与铝元素的化学性质关系最密切的是 ( )
A.铝原子的核外电子数
B.铝原子的最外层电子数
C.铝元素的相对原子质量
D.铝元素的核电荷数
7.下列符号所表示的元素中全部是金属元素的是( )
A.O、C、H、Cl B.Al、Fe、Zn、Hg
C.H、P、Si、K D.S、Mg、N、Ar
8.下列关于分子和原子的说法中错误的是 ( )
A.分子和原子都能直接构成物质
B.相同的原子可以构成不同的分子
C.在化学变化中,原子是最小的粒子
D.分子是保持物质性质的最小粒子
9.用分子的知识解释下列现象,其中合理的是 ( )
A.水结成冰,是因为水分子停止了运动
B.变瘪的乒乓球放在热水中鼓起,是由于分子的体积变大
C.加入糖的水变甜,是由于分子永不停息地做无规则运动
D.1 L大豆与1 L小米混合后体积小于2 L,是因为分子之间有间隔
10.X2+的核外有28个电子,其相对原子质量为65,则X原子的中子数为 ( )
A.35 B.37 C.36 D.34
11.在化学变化中,下列说法正确的是 ( )
①原子不能被创造,也不能被消灭
②原子核不能被创造,但能被消灭
③分子既可以被创造,也可以被消灭
④电子不能被创造,但能被消灭
A.②④ B.①④ C.①③ D.②③
12.用分子、原子的观点解释下列现象,其中不合理的是( )
A.花香四溢——分子在不停地运动
B.水烧开后把壶盖顶开——分子体积变大
C.1滴水中大约有1.67×1021个水分子——分子很小
D.变瘪的乒乓球放入热水中复原——分子之间有间隔
13. 地壳中的元素分布如图所示,其中区域②代表的元素是 ( )
A.氧 B.硅
C.铝 D.铁
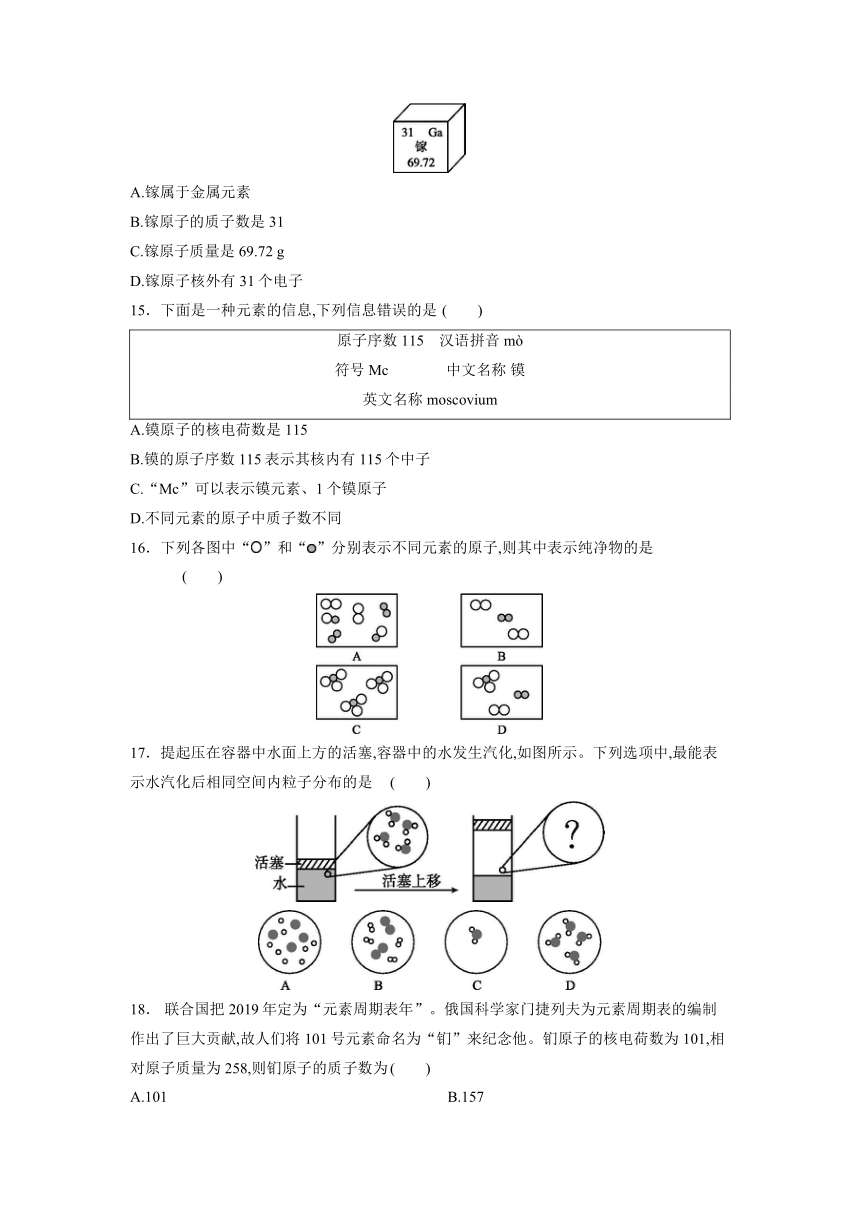
14. 我国的5G通信芯片主要由氮化镓材料制成,图是镓元素在元素周期表中的相关信息。下列说法错误的是 ( )
A.镓属于金属元素
B.镓原子的质子数是31
C.镓原子质量是69.72 g
D.镓原子核外有31个电子
15.下面是一种元素的信息,下列信息错误的是 ( )
原子序数 115 汉语拼音 mò
符号 Mc 中文名称 镆
英文名称 moscovium
A.镆原子的核电荷数是115
B.镆的原子序数115表示其核内有115个中子
C.“Mc”可以表示镆元素、1个镆原子
D.不同元素的原子中质子数不同
16.下列各图中“”和“”分别表示不同元素的原子,则其中表示纯净物的是 ( )
17.提起压在容器中水面上方的活塞,容器中的水发生汽化,如图所示。下列选项中,最能表示水汽化后相同空间内粒子分布的是 ( )
18. 联合国把2019年定为“元素周期表年”。俄国科学家门捷列夫为元素周期表的编制作出了巨大贡献,故人们将101号元素命名为“钔”来纪念他。钔原子的核电荷数为101,相对原子质量为258,则钔原子的质子数为 ( )
A.101 B.157
C.258 D.359
二、非选择题(6小题)
19.若将铝、铁、氯、硅、氢、氧、锌、硫、磷、铜、氮、碳、银、钙等元素分成A和B两组,且A组中必须包括氧元素,应该如何分 试把分组结果用它们的元素符号表示出来。
A组: ;
B组: 。
20.钒被誉为“合金中的维生素”。钒元素的部分信息如图所示。请回答下列问题。
(1)钒原子的质子数为 ,x= 。
(2)钒属于 (填“金属”或“非金属”)元素;钒的相对原子质量为 。
21.请用分子的相关知识解释生产或生活中的现象。
(1)酒香不怕巷子深: 。
(2)加压时,6000 L氧气装入容积为40 L的钢瓶中: 。
22. 图中的①是钾元素在元素周期表中的相关信息。A、B、C、D、E是五种粒子的结构示意图。请据图回答下列问题。
(1)钾元素原子核内质子数为 。
(2)图A中x= 。
(3)图A、B、C、D、E所示五种粒子共表示 种元素。
(4)图C所示粒子的化学性质与图A、B、D、E中 (填字母)所示粒子的化学性质相似。
23.我们可以借助模型来使抽象的问题形象化。如图为某反应的微观示意图,不同的“球”代表不同的原子,请你根据图示回答下列问题。
图
(1)该反应属于 (填“化合”或“分解”)反应。
(2)从图中你还可以获得的信息有 (填一条)。
24.同学们为探究物质微观现象,做了如图所示几个实验,请回答问题。
(1)图甲中可观察到的实验现象是 ;从分子角度分析,可以得出的结论是 。
(2)图乙、丙中无色透明塑料瓶的材质、大小、形状完全相同,瓶内用细线固定有用滤纸折叠成的大小和形状相同的小纸花,小纸花上都均匀喷有酚酞溶液,按照图丁的操作方式分别用注射器向图乙、丙的塑料瓶中同时注入5滴浓氨水,然后将针孔处密封,再将两个塑料瓶分别同时放入等体积的冷水和40℃的热水中。
①观察到的现象是 ;
②还可以得出的结论是 。
(3)图戊所示实验中空气和水都能被压缩,从分子的角度说明物质可被压缩的原因是 ,其中 更易被压缩,原因是 。
参考答案
一、单项选择题(18小题)
1.D
【解析】:物质的三态变化,主要是由于温度发生改变,微粒间的间隔发生了变化。
2.D
【解析】:分子和原子中,核电荷数=核外电子数;阴离子中,核电荷数=质子数<核外电子数;阳离子中,核电荷数=质子数>核外电子数。
3.D
【解析】:中子不带电,不会引起极光现象。
4.A
【解析】:根据在原子中核内质子数=核外电子数,其核内有1个质子和2个中子,氚原子核外有1个电子,故A正确。
5.B
6.B
7.B
8.D
【解析】: 相同的原子可以构成不同的分子,如氧原子可以构成氧分子,也可以构成臭氧分子;由分子构成的物质,分子是保持其化学性质的最小粒子。
9.C
【解析】: 分子在永不停息地做无规则运动,不会停止,水结成冰,温度降低,分子运动速率变慢,但不会停止;分子受热之后运动速率变快,分子之间的间隔变大,但是分子的体积不会变大;大豆和小米混合后体积变小,是由于物质之间有间隔,而不是由于分子之间有间隔。
10.A
【解析】:因为X2+的核外有28个电子,所以该原子有30个电子,则核内质子数是30,所以中子数是65-30=35。
11.C
【解析】:在化学变化中,原子不能被创造,也不能被消灭;分子既可以被创造,也可以被消灭。
12.B
【解析】:A.闻到花香,是因为花香中含有的分子是在不断运动的,向四周扩散,使人们闻到花香,选项正确;B.水烧开后把壶盖顶开,是因为温度升高,水分子间的间隔变大,选项错误;C.一滴水中有1.67×1021个水分子,说明分子的体积很小,选项正确;D.变瘪的乒乓球放入热水中能鼓起来,是由于受热后分子的间隔变大,使乒乓球内气体体积变大造成的,选项正确。
13.B
14.C
15.B
【解析】: 原子序数=质子数=核外电子数=核电荷数,原子序数与中子数不一定相等。
16.C
【解析】: 图C中只有一种分子,是纯净物。
17.C
【解析】: 容器中的水发生汽化时,发生的是物理变化,水分子本身没有发生改变,水分子之间的间隔变大。
18.A
【解析】: 在原子中,核内质子数=核电荷数,钔原子的核电荷数为101,则钔原子的质子数为101。
二、非选择题(6小题)
19.Cl、Si、H、O、S、P、N、C Al、Fe、Zn、Cu、Ag、Ca
(合理即可)
【解析】: 可按金属元素和非金属元素分类。
20.(1)23 2 (2)金属 50.94
21.(1)分子在不断地运动
(2)分子间存在着间隔
22.(1)19 (2)8 (3)四 (4)E
【解析】: (1)由图可知,钾元素的原子序数为19,对于原子,核电荷数=核内质子数=核外电子数=原子序数,所以钾元素原子核内质子数为19。(2)由结构示意图可知,图A为氖原子结构示意图,质子数为10,核外电子数也为10,所以x=8。(3)质子数相同,元素种类相同,所以A、B、C、D、E五种粒子共表示四种元素。(4)C粒子的最外层电子数为2,E粒子的最外层电子数为2,所以二者的化学性质相似。
23.(1)分解
(2)该反应前后原子的种类未改变(其他合理答案均可)
【解析】: (1)从此反应的微观示意图可知该反应的反应物是一种,生成物是两种,属于分解反应。(2)还可以获取的信息有:在化学反应中分子可以再分,原子不能再分;分子由原子构成;该反应前后原子的种类未改变等。
24.(1)酚酞溶液变红 分子在不断运动
(2)①小纸花自下而上依次变红,且图丙中的小纸花比图乙中的小纸花更快变红 ②温度越高,分子运动速率越快
(3)分子间有间隔 空气 空气中各分子间的间隔比水分子间的大
一、单项选择题(18小题)
1.物质的三态变化主要是由于 ( )
A.微粒质量发生变化
B.变成了新微粒
C.微粒大小发生变化
D.微粒间的间隔发生变化
2.核电荷数多于核外电子数的粒子一定是 ( )
A.分子 B.原子
C.阴离子 D.阳离子
3.极光是一种绚丽多彩的发光现象,其发生是由于太阳带电粒子流进入地球磁场。下列这些微粒中,不会引起极光的是 ( )
A.α粒子(氦的原子核) B.电子
C.质子 D.中子
4.氚也是一种氢原子,氚原子含有1个质子和2个中子,如图能正确表示氚原子结构的是 ( )
5.地壳中含量最多的元素是 ( )
A.氮 B.氧 C.碳 D.氢
6.与铝元素的化学性质关系最密切的是 ( )
A.铝原子的核外电子数
B.铝原子的最外层电子数
C.铝元素的相对原子质量
D.铝元素的核电荷数
7.下列符号所表示的元素中全部是金属元素的是( )
A.O、C、H、Cl B.Al、Fe、Zn、Hg
C.H、P、Si、K D.S、Mg、N、Ar
8.下列关于分子和原子的说法中错误的是 ( )
A.分子和原子都能直接构成物质
B.相同的原子可以构成不同的分子
C.在化学变化中,原子是最小的粒子
D.分子是保持物质性质的最小粒子
9.用分子的知识解释下列现象,其中合理的是 ( )
A.水结成冰,是因为水分子停止了运动
B.变瘪的乒乓球放在热水中鼓起,是由于分子的体积变大
C.加入糖的水变甜,是由于分子永不停息地做无规则运动
D.1 L大豆与1 L小米混合后体积小于2 L,是因为分子之间有间隔
10.X2+的核外有28个电子,其相对原子质量为65,则X原子的中子数为 ( )
A.35 B.37 C.36 D.34
11.在化学变化中,下列说法正确的是 ( )
①原子不能被创造,也不能被消灭
②原子核不能被创造,但能被消灭
③分子既可以被创造,也可以被消灭
④电子不能被创造,但能被消灭
A.②④ B.①④ C.①③ D.②③
12.用分子、原子的观点解释下列现象,其中不合理的是( )
A.花香四溢——分子在不停地运动
B.水烧开后把壶盖顶开——分子体积变大
C.1滴水中大约有1.67×1021个水分子——分子很小
D.变瘪的乒乓球放入热水中复原——分子之间有间隔
13. 地壳中的元素分布如图所示,其中区域②代表的元素是 ( )
A.氧 B.硅
C.铝 D.铁
14. 我国的5G通信芯片主要由氮化镓材料制成,图是镓元素在元素周期表中的相关信息。下列说法错误的是 ( )
A.镓属于金属元素
B.镓原子的质子数是31
C.镓原子质量是69.72 g
D.镓原子核外有31个电子
15.下面是一种元素的信息,下列信息错误的是 ( )
原子序数 115 汉语拼音 mò
符号 Mc 中文名称 镆
英文名称 moscovium
A.镆原子的核电荷数是115
B.镆的原子序数115表示其核内有115个中子
C.“Mc”可以表示镆元素、1个镆原子
D.不同元素的原子中质子数不同
16.下列各图中“”和“”分别表示不同元素的原子,则其中表示纯净物的是 ( )
17.提起压在容器中水面上方的活塞,容器中的水发生汽化,如图所示。下列选项中,最能表示水汽化后相同空间内粒子分布的是 ( )
18. 联合国把2019年定为“元素周期表年”。俄国科学家门捷列夫为元素周期表的编制作出了巨大贡献,故人们将101号元素命名为“钔”来纪念他。钔原子的核电荷数为101,相对原子质量为258,则钔原子的质子数为 ( )
A.101 B.157
C.258 D.359
二、非选择题(6小题)
19.若将铝、铁、氯、硅、氢、氧、锌、硫、磷、铜、氮、碳、银、钙等元素分成A和B两组,且A组中必须包括氧元素,应该如何分 试把分组结果用它们的元素符号表示出来。
A组: ;
B组: 。
20.钒被誉为“合金中的维生素”。钒元素的部分信息如图所示。请回答下列问题。
(1)钒原子的质子数为 ,x= 。
(2)钒属于 (填“金属”或“非金属”)元素;钒的相对原子质量为 。
21.请用分子的相关知识解释生产或生活中的现象。
(1)酒香不怕巷子深: 。
(2)加压时,6000 L氧气装入容积为40 L的钢瓶中: 。
22. 图中的①是钾元素在元素周期表中的相关信息。A、B、C、D、E是五种粒子的结构示意图。请据图回答下列问题。
(1)钾元素原子核内质子数为 。
(2)图A中x= 。
(3)图A、B、C、D、E所示五种粒子共表示 种元素。
(4)图C所示粒子的化学性质与图A、B、D、E中 (填字母)所示粒子的化学性质相似。
23.我们可以借助模型来使抽象的问题形象化。如图为某反应的微观示意图,不同的“球”代表不同的原子,请你根据图示回答下列问题。
图
(1)该反应属于 (填“化合”或“分解”)反应。
(2)从图中你还可以获得的信息有 (填一条)。
24.同学们为探究物质微观现象,做了如图所示几个实验,请回答问题。
(1)图甲中可观察到的实验现象是 ;从分子角度分析,可以得出的结论是 。
(2)图乙、丙中无色透明塑料瓶的材质、大小、形状完全相同,瓶内用细线固定有用滤纸折叠成的大小和形状相同的小纸花,小纸花上都均匀喷有酚酞溶液,按照图丁的操作方式分别用注射器向图乙、丙的塑料瓶中同时注入5滴浓氨水,然后将针孔处密封,再将两个塑料瓶分别同时放入等体积的冷水和40℃的热水中。
①观察到的现象是 ;
②还可以得出的结论是 。
(3)图戊所示实验中空气和水都能被压缩,从分子的角度说明物质可被压缩的原因是 ,其中 更易被压缩,原因是 。
参考答案
一、单项选择题(18小题)
1.D
【解析】:物质的三态变化,主要是由于温度发生改变,微粒间的间隔发生了变化。
2.D
【解析】:分子和原子中,核电荷数=核外电子数;阴离子中,核电荷数=质子数<核外电子数;阳离子中,核电荷数=质子数>核外电子数。
3.D
【解析】:中子不带电,不会引起极光现象。
4.A
【解析】:根据在原子中核内质子数=核外电子数,其核内有1个质子和2个中子,氚原子核外有1个电子,故A正确。
5.B
6.B
7.B
8.D
【解析】: 相同的原子可以构成不同的分子,如氧原子可以构成氧分子,也可以构成臭氧分子;由分子构成的物质,分子是保持其化学性质的最小粒子。
9.C
【解析】: 分子在永不停息地做无规则运动,不会停止,水结成冰,温度降低,分子运动速率变慢,但不会停止;分子受热之后运动速率变快,分子之间的间隔变大,但是分子的体积不会变大;大豆和小米混合后体积变小,是由于物质之间有间隔,而不是由于分子之间有间隔。
10.A
【解析】:因为X2+的核外有28个电子,所以该原子有30个电子,则核内质子数是30,所以中子数是65-30=35。
11.C
【解析】:在化学变化中,原子不能被创造,也不能被消灭;分子既可以被创造,也可以被消灭。
12.B
【解析】:A.闻到花香,是因为花香中含有的分子是在不断运动的,向四周扩散,使人们闻到花香,选项正确;B.水烧开后把壶盖顶开,是因为温度升高,水分子间的间隔变大,选项错误;C.一滴水中有1.67×1021个水分子,说明分子的体积很小,选项正确;D.变瘪的乒乓球放入热水中能鼓起来,是由于受热后分子的间隔变大,使乒乓球内气体体积变大造成的,选项正确。
13.B
14.C
15.B
【解析】: 原子序数=质子数=核外电子数=核电荷数,原子序数与中子数不一定相等。
16.C
【解析】: 图C中只有一种分子,是纯净物。
17.C
【解析】: 容器中的水发生汽化时,发生的是物理变化,水分子本身没有发生改变,水分子之间的间隔变大。
18.A
【解析】: 在原子中,核内质子数=核电荷数,钔原子的核电荷数为101,则钔原子的质子数为101。
二、非选择题(6小题)
19.Cl、Si、H、O、S、P、N、C Al、Fe、Zn、Cu、Ag、Ca
(合理即可)
【解析】: 可按金属元素和非金属元素分类。
20.(1)23 2 (2)金属 50.94
21.(1)分子在不断地运动
(2)分子间存在着间隔
22.(1)19 (2)8 (3)四 (4)E
【解析】: (1)由图可知,钾元素的原子序数为19,对于原子,核电荷数=核内质子数=核外电子数=原子序数,所以钾元素原子核内质子数为19。(2)由结构示意图可知,图A为氖原子结构示意图,质子数为10,核外电子数也为10,所以x=8。(3)质子数相同,元素种类相同,所以A、B、C、D、E五种粒子共表示四种元素。(4)C粒子的最外层电子数为2,E粒子的最外层电子数为2,所以二者的化学性质相似。
23.(1)分解
(2)该反应前后原子的种类未改变(其他合理答案均可)
【解析】: (1)从此反应的微观示意图可知该反应的反应物是一种,生成物是两种,属于分解反应。(2)还可以获取的信息有:在化学反应中分子可以再分,原子不能再分;分子由原子构成;该反应前后原子的种类未改变等。
24.(1)酚酞溶液变红 分子在不断运动
(2)①小纸花自下而上依次变红,且图丙中的小纸花比图乙中的小纸花更快变红 ②温度越高,分子运动速率越快
(3)分子间有间隔 空气 空气中各分子间的间隔比水分子间的大
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
