第三单元物质构成的奥秘单元测试卷 —2021—2022学年九年级化学人教版上册(word版 含解析)
文档属性
| 名称 | 第三单元物质构成的奥秘单元测试卷 —2021—2022学年九年级化学人教版上册(word版 含解析) |
|
|
| 格式 | docx | ||
| 文件大小 | 96.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-04 00:00:00 | ||
图片预览




文档简介
物质构成的奥秘单元测试
一、单选题(每题2分,共20小题)
1.下列实验现象或事实用分子的相关知识加以解释,其中不正确的是
A.热胀冷缩——分子的大小随温度的改变而改变
B.酒香不怕巷子深——分子不断运动
C.氧化汞在一定条件下变成汞和氧气——在化学变化中分子可以再分
D.的氧气可以装到的钢瓶中——分子之间有间隙
2.下列操作或现象与分子对应的特性不一致的选项是
选项 操作或现象 分子的特性
A 给篮球打气 分子间有间隙
B 100mL酒精和100mL水混合总体积小于200mL 分子是有质量的
C 在花园可闻到花香的气味 分子在不断运动
D 加热氧化汞可以得到金属汞和氧气 分子可以再分
A.A B.B C.C D.D
3.对照实验是一种重要的科学方法。根据下图所示实验,下列说法不正确的是
A.甲实验可证明氨分子能使酚酞变红
B.乙实验可证明温度不同分子的运动速率不同
C.甲、乙两个实验均能证明分子之间有间隔
D.甲、乙两个实验均能证明分子在不断运动
4.用分子的性质解释下列生活中的现象,其中不正确的是
A.墙内开花墙外可嗅到花香,说明分子在不停的运动
B.湿衣服在阳光下比在阴凉处易于晾干,说明分子运动速率随温度升高而加快
C.将100mL水与100mL酒精混合,体积小于200mL,说明分子间有间隔
D.水由液态变成气态,说明水分子体积变大
5.从分子的角度分析,下列解释不正确的是
A.水结冰体积变大﹣﹣分子大小发生改变
B.氧气加压后贮存在钢瓶中﹣﹣分子间有间隔
C.氧化汞加热生成汞和氧气﹣﹣分子在化学变化中可分
D.湿衣服在太阳下干得快﹣﹣分子运动速率与温度有关
6.下列物质由分子直接构成的是
A.蒸馏水 B.氦 C.氯化钠 D.铁
7.下列物质由离子构成的是
A.氯化钠 B.金刚石 C.氮气 D.铜
8.原子失去最外层电子或最外层得到电子之后一定不会引起改变的是
①元素种类 ②化学性质 ③相对原子质量 ④粒子的电性 ⑤原子核 ⑥电子层数 ⑦最外层电子数 ⑧核外电子总数
A.①③⑤ B.②③④⑥ C.②⑤ D.①⑤
9.下列叙述不正确的是
A.水是由氢分子和氧原子构成
B.“墙内开花墙外香”,说明分子在不断地运动
C.将50毫升水和50毫升酒精混合后体积小于100毫升,说明分子间有间隔
D.分子和原子都是构成物质的粒子
10.如图是甲、乙两种粒子的结构示意图,下列有说法正确的是
A.甲粒子是阳离子
B.乙粒子是原子
C.两种粒子的核电荷数相同
D.甲粒子的化学性质比乙粒子稳定
11.下列是几种微粒的结构示意图,有关说法错误的是
A.微粒①易得到电子 B.微粒②和④核外电子排布相同,所以质子数相同
C.微粒③易失去一个电子 D.微粒④带两个单位正电荷
12.下列符号表示2个氢离子的是
A.2H B.2H+ C.H2 D.2H2
13.某同学对所学部分化学知识归纳如下,完全正确的一组是
A.实验现象 B.微观解释
①铜片在空气中加热,铜片表面变黑,生成氧化铜 ②燃着的木条伸入呼出的气体中燃烧更旺 ①变瘪了的兵乓球放在热水中鼓起——分子的体积变大 ②1L酒精与1L水混合后总体积小于2L——分子间有间隙
C.由分子构成的物质 D.空气污染物
①氧气 ②水 ①二氧化碳 ②二氧化氮
A.A B.B C.C D.D
14.下列对某些基本概念的理解正确的是
A.有氧气参加的反应是氧化反应,所以氧化反应一定有氧气参加
B.混合物中至少含有两种物质,则混合物中至少含有两种元素
C.离子是带电荷的粒子,带电荷的粒子不一定是离子
D.质子数决定元素种类,因此质子数相同的一类粒子一定属于同种元素
15.在我们的日常生活中出现了“加碘食盐”、“增铁酱油、“高钙牛奶”、“富硒茶叶”、“含氟牙膏”等商品。这里的碘、铁、钙、硒、氟应理解为
A.元素 B.单质 C.分子 D.氧化物
16.如图为地壳中元素含量(质量分数)示意图。其中“b”代表的是
A.氧元素 B.铝元素 C.硅元素 D.氢元素
17.电子数相同、质子数不同的两种粒子,它们可能是
A.两种不同的元素的离子 B.两种不同元素的原子
C.两种不同的分子 D.同种元素的原子和离子
18.在我们的日常生活中出现了“加碘食盐”、“高钙牛奶”等商品。这里的“碘”、“钙”为
A.元素 B.离子 C.分子 D.原子
19.下列有关分子、原子、离子和元素的说法正确的是
A.原子不能直接构成物质 B.分子是化学变化中最小的微粒
C.元素只论个数,不论种类,决定元素化学性质的是原子的电子数 D.原子得到或失去电子变成离子
20.下列推理你认为正确的是
A.如果两种粒子属于同一种元素,则这两种粒子的原子核中质子数一定相同
B.如果两种粒子含有的质子数相同;则这两种粒子一定属于同一种元素
C.如果物质中只含有一种元素,则这种物质一定是纯净物
D.如果化学变化中构成物质的分子改变,则组成物质的元素也一定变
二、填空题(每空2分,共6小题)
21.用微粒的观点回答下列问题:
(1)保持水的化学性质的微粒是___________;
(2)过氧化氢分解生成水和氧气的过程中,不变的微粒是_________;
(3)用湿抹布擦过的桌面,一段时间后变干的原因是__________;
(4)一定质量的水蒸气冷凝成水时,其体积变小的原因是__________。
22.根据工业制取氨气反应的微观示意图,回答下列问题。
(1)反应中A、C的分子个数比___________。
(2)该反应的基本反应类型是___________。
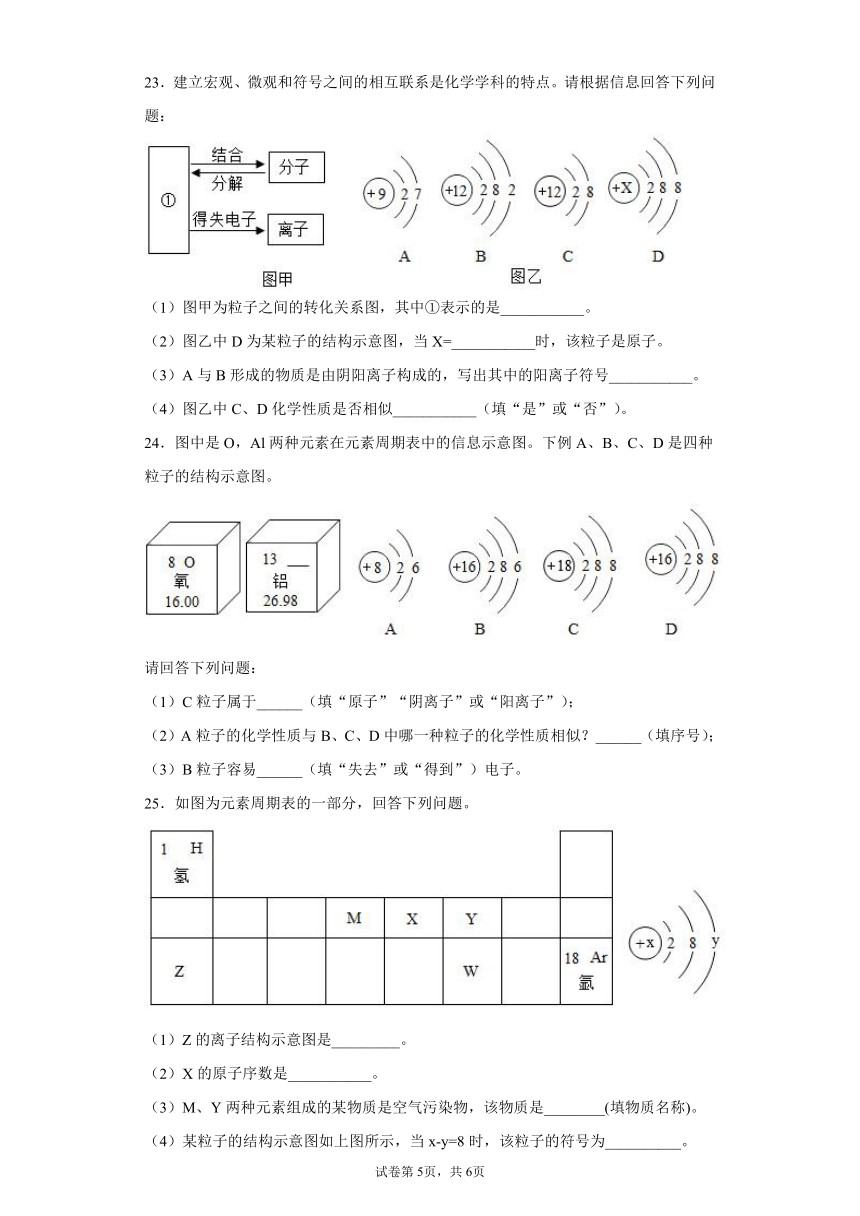
23.建立宏观、微观和符号之间的相互联系是化学学科的特点。请根据信息回答下列问题:
(1)图甲为粒子之间的转化关系图,其中①表示的是___________。
(2)图乙中D为某粒子的结构示意图,当X=___________时,该粒子是原子。
(3)A与B形成的物质是由阴阳离子构成的,写出其中的阳离子符号___________。
(4)图乙中C、D化学性质是否相似___________(填“是”或“否”)。
24.图中是O,Al两种元素在元素周期表中的信息示意图。下例A、B、C、D是四种粒子的结构示意图。
请回答下列问题:
(1)C粒子属于______(填“原子”“阴离子”或“阳离子”);
(2)A粒子的化学性质与B、C、D中哪一种粒子的化学性质相似?______(填序号);
(3)B粒子容易______(填“失去”或“得到”)电子。
25.如图为元素周期表的一部分,回答下列问题。
(1)Z的离子结构示意图是_________。
(2)X的原子序数是___________。
(3)M、Y两种元素组成的某物质是空气污染物,该物质是________(填物质名称)。
(4)某粒子的结构示意图如上图所示,当x-y=8时,该粒子的符号为__________。
(5)下列粒子结构示意图中,属于同种元素的是______(填字母编号,下同),化学性质相似的原子有________。
26.元素周期表是学习化学的重要工具,下表是元素周期表中1-18号元素的原子核外电子排布。
(1)13号元素的符号是_______,位于元素周期表中第______周期,它属于________元素(选填“金属”或“非金属”);
(2)写出表中关于10号元素的一条信息__________。
(3)列举8号元素对应单质的一种用途________。
(4)同周期元素,从左到右,各元素原子随原子序数的增加,最外层电子数依次_________。
试卷第1页,共3页
试卷第1页,共3页
参考答案
1.A
【详解】
A、热胀冷缩,说明分子大小随温度改变而改变,此说法错误,符合题意;
B、酒香不怕巷子深,说明分子在不断地运动,此说法正确,不符合题意;
C、氧化汞在一定条件下变成汞和氧气---在化学变化中分子可以再分,所以解释正确,不符合题意;
D、气体能被压缩,说明分子之间有间隔,且间隔大小可以改变,此说法正确,不符合题意。
故选A。
【点睛】
2.B
【详解】
A:给篮球打气,其中气体越来越多,压强增大,分子间间隔变小。故A说法正确。
B:100mL酒精和100mL水混合总体积小于200mL是由于分子之间有间隔,分子相互占据了间隔。故B错误。
C:在花园可闻到花香的气味,说明分子在不断运动,香味分子进入鼻孔。故C正确。
D:加热氧化汞可以得到金属汞和氧气,原因是氧化汞分子,分成汞原子和氧原子,氧原子构成氧分子,汞原子聚集成汞,说明了分子可以再分。故D正确。
综上所述:选择B。
3.A
【详解】
A:浓氨水具有挥发性,挥发出的氨气遇到酚酞溶液变红。故A烧杯中溶液由无色变红,所以甲实验可证明氨分子是不断运动的。当溶解在水中能生成氨水,氨水使酚酞溶液变红,而不是氨分子使酚酞溶液变红。故A错误。
B:品红放在冷水和热水中,品红在热水中比冷水中扩散快,所以,乙实验可证明温度不同分子的运动速率不同。B正确。
C:实验甲中从浓氨水中挥发的氨分子不断运动,使A烧杯中溶液变红,说明大烧杯里空气中的分子存在间隔。实验乙中,品红扩散实验说明分子间有间隔,分子不断运动。故C正确。
D: 根据前面分析可知甲、乙两个实验均能证明分子在不断运动。故D正确。
综上所述:选择A。
4.D
【详解】
A、墙内开花墙外可嗅到花香,是因为花香中含有的分子是在不断运动的,向四周扩散,使人们闻到花香,选项正确,不符合题意;
B、分子运动速率随温度升高而加快,湿衣服在阳光下比在阴凉处易于晾干,是因为阳光下温度高,选项正确,不符合题意;
C、将100mL水与100mL酒精混合,体积小于200mL,是因为分子之间有间隔,一部分水分子和酒精分子会互相占据分子之间的间隔,选项正确,不符合题意。
D、水由液态变成气态,是因为水分子间的间隔变大,水分子的大小不变,选项错误,符合题意。
故选D。
5.A
【详解】
A.水结冰体积变大——分子间隔发生改变,分子本身没有改变,说法错误;
B.氧气加压后贮存在钢瓶中——分子间有间隔,加压后分子间隔变小,物质体积变小,说法正确;
C.氧化汞加热生成汞和氧气——分子在化学变化中可分,氧化汞分子分解为氧原子和汞原子,氧原子结合成氧分子,汞原子聚集金属汞,说法正确;
D.湿衣服在太阳下干得快——分子运动速率与温度有关,温度越高分子运动越快,说法正确。
故选A。
6.A
【详解】
A、蒸馏水是由水分子构成的,故A正确;
B、氦是由氦原子构成的,故B不正确;
C、氯化钠是由钠离子和氯离子构成的,故C不正确;
D、铁是金属单质,是由铁原子直接构成的,故D不正确。故选A。
7.A
【详解】
A、氯化钠由钠离子和氯离子构成,符合题意;
B、金刚石由碳原子构成,不符合题意;
C、氮气由氮分子构成,不符合题意;
D、铜由铜原子构成,不符合题意。
故选A。
8.A
【详解】
原子在变成离子的过程中,发生改变的是原子的最外层电子数,核内质子数不变,所以元素种类不变;由于原子得失电子,原子的电子总数一定发生了改变,原子也带上了电荷,化学性质变得稳定了;原子的质量主要集中在原子核上,由质子数和中子数决定,故得失电子对相对原子质量无影响;至于电子层数,如原子是得到电子,电子层数不发生改变,如是失电子,则最外层电子失去,次外层变成了最外层,少了一个电子层,电子层数可能改变,也可能不改变。
所以,原子失去最外层电子或最外层得到电子之后一定不会引起改变的是元素种类;相对原子质量;原子核 。
故选择A。
9.A
【详解】
A、水是由水分子构成的,故A不正确;
B、“墙内开花墙外香”,说明分子在不停地运动,花香分子运动到空气中,被人们嗅到,故B正确;
C、50mL酒精和50mL水混合体积小于100mL,说明分子之间有间隔,酒精分子和水分子进入彼此的间隔中去了,故C正确;
D、物质可以由分子构成,也可以由原子或离子构成,分子和原子都是构成物质的粒子,故D正确。
故选A。
10.C
【详解】
A、甲粒子的质子数是8,核外电子数是8,属于原子,故A说法不正确;
B、乙粒子的质子数是8,核外电子数是10,属于阴离子,故B说法不正确;
C、由于甲、乙的核内的质子数相同,属于同种元素,故C说法正确;
D、由上述分析可知,甲粒子的最外层电子数是6,在反应中易得到两个电子,乙粒子是带两个单位的负电荷阴离子,是稳定结构,故D说法不正确。
故选C。
11.B
【详解】
A、微粒①最外层7个电子,大于4个,容易得到电子,故A正确;
B、元素种类由质子数决定,微粒②和④质子数分别为9和12,不相等,不属于同种元素,故B错误;
C、微粒③最外层1个电子,容易失去1个电子,故C正确;
D、微粒④质子数12,电子数10,一个质子带一个单位的正电荷,一个电子带一个单位的负电荷,故微粒④带两个单位正电荷,故D正确。
故选B。
12.B
【详解】
A、由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,2H表示的是两个氢原子,故选项错误。
B、离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略;表示多个该离子,在其符号前加上相应的数字;2H+表示两个氢离子,故选项正确。
C、H2可表示氢分子、氢气、氢气是由氢元素组成的,不能表示氢离子,故选项错误。
D、2H2可表示2个氢分子,故选项错误。
故选B。
13.C
【详解】
A、①生成氧化铜是实验结论,不是现象;错误;
②呼出的气体中氧气含量较低,燃着的木条伸入呼出的气体中,燃着的木条会熄灭,错误;
B、①变瘪了的乒乓球放在热水中鼓起,是因为温度升高,分子的间隔变大,错误;
②1L酒精与1L水混合后总体积小于2L说明分子间有间隙,正确;
C、①氧气由氧气分子构成,正确;
②水由水分子构成,正确;
D、①二氧化碳是空气成分之一,不是空气污染物,错误;
②二氧化氮是空气污染物之一,正确。
故选C。
14.C
【详解】
A、物质和氧发生的化学反应,叫做氧化反应,这里的氧包括氧气和氧元素,物质和氧气发生的化学反应都是氧化反应,有的氧化反应是物质和氧元素发生的化学反应,故选项推理错误;
B、混合物中至少含有两种物质,但混合物中不一定至少含有两种元素,也可能只含有一种元素,如金刚石和石墨的混合物中只含有一种元素,故选项推理错误;
C、离子是带电荷的微粒,但带电荷的微粒不一定是离子,也可能是质子、电子等,故选项推理正确;
D、质子数相同的粒子不一定属于同种元素,例如水分子和氖原子质子数都是10,故选项推理错误。
故选:C。
15.A
【详解】
元素组成物质,这里的碘、铁、钙、硒、氟指的是物质的组成,指的是组成物质的元素,故选A。
16.C
【详解】
地壳含量较多的元素(前四种)按含量从高到低的排序为:氧、硅、铝、铁,由图可知,b含量第二多的元素,即b代表的是硅元素,故选C。
17.A
【详解】
元素是具有相同质子数的一类原子的总称,质子数不同则是不同种元素。原子中质子数=核外电子数。离子由原子得失电子得到。电子数相同则这两种微粒可能是两种不同的元素的离子或一种元素的离子与另一种元素的原子。
如两种微粒中有分子,因分子中质子数=核外电子数,所以最多有1种分子,另外一种为离子。
故选A。
18.A
【详解】
物质是由元素组成。在我们的日常生活中出现了“加碘食盐”、“高钙牛奶”等商品。这里的“碘”、“钙”为元素。
故选:A。
19.D
【详解】
A、分子、原子、离子都是构成物质的微粒,所以分子、原子、离子都可以直接构成物质,选项说法不正确;
B、原子是化学变化中的最小微粒,而分子是保持物质的化学性质的最小微粒,选项说法不正确;
C、元素只论种类,不论个数;原子的最外层电子数决定了元素的化学性质,不是原子的电子数,选项说法不正确;
D、原子得失电子后形成了离子,原子得到电子形成阴离子,原子失去电子形成阳离子,选项说法正确。
故选D。
20.A
【详解】
A、同一元素的质子数相同;如果两种粒子属于同一种元素,则这两种粒子的原子核中质子数一定相同,正确;
B、含有的质子数相同的两种粒子不一定属于同一种元素,例如氖原子和水分子质子数相同,不是同一元素,错误;
C、物质中只含有一种元素,这种物质不一定是纯净物,例如氧气和臭氧组成的混合物,错误;
D、化学变化中构成物质的分子改变,组成物质的元素一定不变,例如氧气转化为臭氧,错误。
故选A。
21.
(1)水分子H2O
(2)氢原子、氧原子
(3)分子不断运动
(4)温度降低,分子间隔变小
【解析】
(1)
分子是保持物质化学性质的最小粒子,保持水的化学性质的微粒是水分子;
(2)
原子是化学变化中最小的粒子,过氧化氢分解生成水和氧气的过程中,不变的微粒是氢原子、氧原子;
(3)
用湿抹布擦过的桌面,一段时间后变干的原因是分子不断运动的,水分子运动到空气中去了;
(4)
分子之间有间隔,一定质量的水蒸气冷凝成水时,其体积变小的原因是温度降低,分子间隔变小。
22.
(1)1:2
(2)化合反应
【分析】
(1)
从图中可知,A、C的分子个数比是1:2。
(2)
从图中可知,反应物有2种,生成物有1种,符合多变一的特点,属于化合反应。
23.
(1)原子
(2)18
(3)Mg2+
(4)否
【分析】
(1)
原子构成分子,分子分裂成为原子,原子得失电子变为离子,故①表示原子。
(2)
在原子中质子数等于核外电子数,该粒子是原子,核外有18个电子,故其核内有18个质子,所以X=18,故填18。
(3)
A是氟元素,B是镁元素,能够形成阳离子的是镁,故其离子符号为:Mg2+。
(4)
C是镁离子,D是氩原子,故其化学性质不相似,故选否。
24.
(1)原子
(2)B
(3)得到
【分析】
(1)
C粒子的核外电子数等于核内的质子数,微粒不带电,故属于原子。
(2)
最外层电子数决定原子的化学性质,A粒子与B粒子的最外层电子数都是6,故两种粒子的化学性质相似。
(3)
B粒子的最外层电子数是6,大于4个,易得到电子变成稳定结构。
25.
(1)
(2)7
(3)一氧化碳
(4)S2-
(5) BC AD
【分析】
(1)
根据元素周期表可知,Z是钠元素,其核电荷数为11,原子核电子排布是2、8、1,在形成离子时,失去1个电子形成稳定结构。离子结构示意图为: ;
(2)
根据元素周期表可知,X的原子序数是7;
(3)
根据元素周期表可知,M、Y两种元素分别为C、O,组成的某物质是空气污染物,该物质是CO,CO有毒性;
(4)
当x-y=8时,该粒子是带2个单位负电荷的硫离子,硫离子的符号为S2-;
(5)
同种元素质子数相同,BC的质子数都是8,所以BC属于同种元素;最外层电子数是8的是一种稳定结构,第一层也是最外层时,达到2个电子也是一种稳定结构。AD最外层电子数都达到了稳定结构,化学性质不活泼,所以AD化学性质相似。
【点睛】
26.
(1) Al 三 金属
(2)化学性质稳定(合理即可)
(3)供给呼吸(合理即可)
(4)增加
【分析】
(1)
根据元素周期表可知,13号元素的符号是Al,位于元素周期表中第三周期,它最外层电子数为3,少于4个电子,属于金属元素;
(2)
根据元素周期表可知,10号元素原子的最外层电子数为8,是一种稳定结构,所以它的化学性质稳定;
(3)
8号元素是氧气,氧元素组成的单质可以是氧气,氧气能供给呼吸;
(4)
根据元素周期表可知,同周期元素,从左到右,各元素原子随原子序数的增加,最外层电子数依次增加。
【点睛】
答案第1页,共2页
答案第1页,共2页
一、单选题(每题2分,共20小题)
1.下列实验现象或事实用分子的相关知识加以解释,其中不正确的是
A.热胀冷缩——分子的大小随温度的改变而改变
B.酒香不怕巷子深——分子不断运动
C.氧化汞在一定条件下变成汞和氧气——在化学变化中分子可以再分
D.的氧气可以装到的钢瓶中——分子之间有间隙
2.下列操作或现象与分子对应的特性不一致的选项是
选项 操作或现象 分子的特性
A 给篮球打气 分子间有间隙
B 100mL酒精和100mL水混合总体积小于200mL 分子是有质量的
C 在花园可闻到花香的气味 分子在不断运动
D 加热氧化汞可以得到金属汞和氧气 分子可以再分
A.A B.B C.C D.D
3.对照实验是一种重要的科学方法。根据下图所示实验,下列说法不正确的是
A.甲实验可证明氨分子能使酚酞变红
B.乙实验可证明温度不同分子的运动速率不同
C.甲、乙两个实验均能证明分子之间有间隔
D.甲、乙两个实验均能证明分子在不断运动
4.用分子的性质解释下列生活中的现象,其中不正确的是
A.墙内开花墙外可嗅到花香,说明分子在不停的运动
B.湿衣服在阳光下比在阴凉处易于晾干,说明分子运动速率随温度升高而加快
C.将100mL水与100mL酒精混合,体积小于200mL,说明分子间有间隔
D.水由液态变成气态,说明水分子体积变大
5.从分子的角度分析,下列解释不正确的是
A.水结冰体积变大﹣﹣分子大小发生改变
B.氧气加压后贮存在钢瓶中﹣﹣分子间有间隔
C.氧化汞加热生成汞和氧气﹣﹣分子在化学变化中可分
D.湿衣服在太阳下干得快﹣﹣分子运动速率与温度有关
6.下列物质由分子直接构成的是
A.蒸馏水 B.氦 C.氯化钠 D.铁
7.下列物质由离子构成的是
A.氯化钠 B.金刚石 C.氮气 D.铜
8.原子失去最外层电子或最外层得到电子之后一定不会引起改变的是
①元素种类 ②化学性质 ③相对原子质量 ④粒子的电性 ⑤原子核 ⑥电子层数 ⑦最外层电子数 ⑧核外电子总数
A.①③⑤ B.②③④⑥ C.②⑤ D.①⑤
9.下列叙述不正确的是
A.水是由氢分子和氧原子构成
B.“墙内开花墙外香”,说明分子在不断地运动
C.将50毫升水和50毫升酒精混合后体积小于100毫升,说明分子间有间隔
D.分子和原子都是构成物质的粒子
10.如图是甲、乙两种粒子的结构示意图,下列有说法正确的是
A.甲粒子是阳离子
B.乙粒子是原子
C.两种粒子的核电荷数相同
D.甲粒子的化学性质比乙粒子稳定
11.下列是几种微粒的结构示意图,有关说法错误的是
A.微粒①易得到电子 B.微粒②和④核外电子排布相同,所以质子数相同
C.微粒③易失去一个电子 D.微粒④带两个单位正电荷
12.下列符号表示2个氢离子的是
A.2H B.2H+ C.H2 D.2H2
13.某同学对所学部分化学知识归纳如下,完全正确的一组是
A.实验现象 B.微观解释
①铜片在空气中加热,铜片表面变黑,生成氧化铜 ②燃着的木条伸入呼出的气体中燃烧更旺 ①变瘪了的兵乓球放在热水中鼓起——分子的体积变大 ②1L酒精与1L水混合后总体积小于2L——分子间有间隙
C.由分子构成的物质 D.空气污染物
①氧气 ②水 ①二氧化碳 ②二氧化氮
A.A B.B C.C D.D
14.下列对某些基本概念的理解正确的是
A.有氧气参加的反应是氧化反应,所以氧化反应一定有氧气参加
B.混合物中至少含有两种物质,则混合物中至少含有两种元素
C.离子是带电荷的粒子,带电荷的粒子不一定是离子
D.质子数决定元素种类,因此质子数相同的一类粒子一定属于同种元素
15.在我们的日常生活中出现了“加碘食盐”、“增铁酱油、“高钙牛奶”、“富硒茶叶”、“含氟牙膏”等商品。这里的碘、铁、钙、硒、氟应理解为
A.元素 B.单质 C.分子 D.氧化物
16.如图为地壳中元素含量(质量分数)示意图。其中“b”代表的是
A.氧元素 B.铝元素 C.硅元素 D.氢元素
17.电子数相同、质子数不同的两种粒子,它们可能是
A.两种不同的元素的离子 B.两种不同元素的原子
C.两种不同的分子 D.同种元素的原子和离子
18.在我们的日常生活中出现了“加碘食盐”、“高钙牛奶”等商品。这里的“碘”、“钙”为
A.元素 B.离子 C.分子 D.原子
19.下列有关分子、原子、离子和元素的说法正确的是
A.原子不能直接构成物质 B.分子是化学变化中最小的微粒
C.元素只论个数,不论种类,决定元素化学性质的是原子的电子数 D.原子得到或失去电子变成离子
20.下列推理你认为正确的是
A.如果两种粒子属于同一种元素,则这两种粒子的原子核中质子数一定相同
B.如果两种粒子含有的质子数相同;则这两种粒子一定属于同一种元素
C.如果物质中只含有一种元素,则这种物质一定是纯净物
D.如果化学变化中构成物质的分子改变,则组成物质的元素也一定变
二、填空题(每空2分,共6小题)
21.用微粒的观点回答下列问题:
(1)保持水的化学性质的微粒是___________;
(2)过氧化氢分解生成水和氧气的过程中,不变的微粒是_________;
(3)用湿抹布擦过的桌面,一段时间后变干的原因是__________;
(4)一定质量的水蒸气冷凝成水时,其体积变小的原因是__________。
22.根据工业制取氨气反应的微观示意图,回答下列问题。
(1)反应中A、C的分子个数比___________。
(2)该反应的基本反应类型是___________。
23.建立宏观、微观和符号之间的相互联系是化学学科的特点。请根据信息回答下列问题:
(1)图甲为粒子之间的转化关系图,其中①表示的是___________。
(2)图乙中D为某粒子的结构示意图,当X=___________时,该粒子是原子。
(3)A与B形成的物质是由阴阳离子构成的,写出其中的阳离子符号___________。
(4)图乙中C、D化学性质是否相似___________(填“是”或“否”)。
24.图中是O,Al两种元素在元素周期表中的信息示意图。下例A、B、C、D是四种粒子的结构示意图。
请回答下列问题:
(1)C粒子属于______(填“原子”“阴离子”或“阳离子”);
(2)A粒子的化学性质与B、C、D中哪一种粒子的化学性质相似?______(填序号);
(3)B粒子容易______(填“失去”或“得到”)电子。
25.如图为元素周期表的一部分,回答下列问题。
(1)Z的离子结构示意图是_________。
(2)X的原子序数是___________。
(3)M、Y两种元素组成的某物质是空气污染物,该物质是________(填物质名称)。
(4)某粒子的结构示意图如上图所示,当x-y=8时,该粒子的符号为__________。
(5)下列粒子结构示意图中,属于同种元素的是______(填字母编号,下同),化学性质相似的原子有________。
26.元素周期表是学习化学的重要工具,下表是元素周期表中1-18号元素的原子核外电子排布。
(1)13号元素的符号是_______,位于元素周期表中第______周期,它属于________元素(选填“金属”或“非金属”);
(2)写出表中关于10号元素的一条信息__________。
(3)列举8号元素对应单质的一种用途________。
(4)同周期元素,从左到右,各元素原子随原子序数的增加,最外层电子数依次_________。
试卷第1页,共3页
试卷第1页,共3页
参考答案
1.A
【详解】
A、热胀冷缩,说明分子大小随温度改变而改变,此说法错误,符合题意;
B、酒香不怕巷子深,说明分子在不断地运动,此说法正确,不符合题意;
C、氧化汞在一定条件下变成汞和氧气---在化学变化中分子可以再分,所以解释正确,不符合题意;
D、气体能被压缩,说明分子之间有间隔,且间隔大小可以改变,此说法正确,不符合题意。
故选A。
【点睛】
2.B
【详解】
A:给篮球打气,其中气体越来越多,压强增大,分子间间隔变小。故A说法正确。
B:100mL酒精和100mL水混合总体积小于200mL是由于分子之间有间隔,分子相互占据了间隔。故B错误。
C:在花园可闻到花香的气味,说明分子在不断运动,香味分子进入鼻孔。故C正确。
D:加热氧化汞可以得到金属汞和氧气,原因是氧化汞分子,分成汞原子和氧原子,氧原子构成氧分子,汞原子聚集成汞,说明了分子可以再分。故D正确。
综上所述:选择B。
3.A
【详解】
A:浓氨水具有挥发性,挥发出的氨气遇到酚酞溶液变红。故A烧杯中溶液由无色变红,所以甲实验可证明氨分子是不断运动的。当溶解在水中能生成氨水,氨水使酚酞溶液变红,而不是氨分子使酚酞溶液变红。故A错误。
B:品红放在冷水和热水中,品红在热水中比冷水中扩散快,所以,乙实验可证明温度不同分子的运动速率不同。B正确。
C:实验甲中从浓氨水中挥发的氨分子不断运动,使A烧杯中溶液变红,说明大烧杯里空气中的分子存在间隔。实验乙中,品红扩散实验说明分子间有间隔,分子不断运动。故C正确。
D: 根据前面分析可知甲、乙两个实验均能证明分子在不断运动。故D正确。
综上所述:选择A。
4.D
【详解】
A、墙内开花墙外可嗅到花香,是因为花香中含有的分子是在不断运动的,向四周扩散,使人们闻到花香,选项正确,不符合题意;
B、分子运动速率随温度升高而加快,湿衣服在阳光下比在阴凉处易于晾干,是因为阳光下温度高,选项正确,不符合题意;
C、将100mL水与100mL酒精混合,体积小于200mL,是因为分子之间有间隔,一部分水分子和酒精分子会互相占据分子之间的间隔,选项正确,不符合题意。
D、水由液态变成气态,是因为水分子间的间隔变大,水分子的大小不变,选项错误,符合题意。
故选D。
5.A
【详解】
A.水结冰体积变大——分子间隔发生改变,分子本身没有改变,说法错误;
B.氧气加压后贮存在钢瓶中——分子间有间隔,加压后分子间隔变小,物质体积变小,说法正确;
C.氧化汞加热生成汞和氧气——分子在化学变化中可分,氧化汞分子分解为氧原子和汞原子,氧原子结合成氧分子,汞原子聚集金属汞,说法正确;
D.湿衣服在太阳下干得快——分子运动速率与温度有关,温度越高分子运动越快,说法正确。
故选A。
6.A
【详解】
A、蒸馏水是由水分子构成的,故A正确;
B、氦是由氦原子构成的,故B不正确;
C、氯化钠是由钠离子和氯离子构成的,故C不正确;
D、铁是金属单质,是由铁原子直接构成的,故D不正确。故选A。
7.A
【详解】
A、氯化钠由钠离子和氯离子构成,符合题意;
B、金刚石由碳原子构成,不符合题意;
C、氮气由氮分子构成,不符合题意;
D、铜由铜原子构成,不符合题意。
故选A。
8.A
【详解】
原子在变成离子的过程中,发生改变的是原子的最外层电子数,核内质子数不变,所以元素种类不变;由于原子得失电子,原子的电子总数一定发生了改变,原子也带上了电荷,化学性质变得稳定了;原子的质量主要集中在原子核上,由质子数和中子数决定,故得失电子对相对原子质量无影响;至于电子层数,如原子是得到电子,电子层数不发生改变,如是失电子,则最外层电子失去,次外层变成了最外层,少了一个电子层,电子层数可能改变,也可能不改变。
所以,原子失去最外层电子或最外层得到电子之后一定不会引起改变的是元素种类;相对原子质量;原子核 。
故选择A。
9.A
【详解】
A、水是由水分子构成的,故A不正确;
B、“墙内开花墙外香”,说明分子在不停地运动,花香分子运动到空气中,被人们嗅到,故B正确;
C、50mL酒精和50mL水混合体积小于100mL,说明分子之间有间隔,酒精分子和水分子进入彼此的间隔中去了,故C正确;
D、物质可以由分子构成,也可以由原子或离子构成,分子和原子都是构成物质的粒子,故D正确。
故选A。
10.C
【详解】
A、甲粒子的质子数是8,核外电子数是8,属于原子,故A说法不正确;
B、乙粒子的质子数是8,核外电子数是10,属于阴离子,故B说法不正确;
C、由于甲、乙的核内的质子数相同,属于同种元素,故C说法正确;
D、由上述分析可知,甲粒子的最外层电子数是6,在反应中易得到两个电子,乙粒子是带两个单位的负电荷阴离子,是稳定结构,故D说法不正确。
故选C。
11.B
【详解】
A、微粒①最外层7个电子,大于4个,容易得到电子,故A正确;
B、元素种类由质子数决定,微粒②和④质子数分别为9和12,不相等,不属于同种元素,故B错误;
C、微粒③最外层1个电子,容易失去1个电子,故C正确;
D、微粒④质子数12,电子数10,一个质子带一个单位的正电荷,一个电子带一个单位的负电荷,故微粒④带两个单位正电荷,故D正确。
故选B。
12.B
【详解】
A、由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,2H表示的是两个氢原子,故选项错误。
B、离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略;表示多个该离子,在其符号前加上相应的数字;2H+表示两个氢离子,故选项正确。
C、H2可表示氢分子、氢气、氢气是由氢元素组成的,不能表示氢离子,故选项错误。
D、2H2可表示2个氢分子,故选项错误。
故选B。
13.C
【详解】
A、①生成氧化铜是实验结论,不是现象;错误;
②呼出的气体中氧气含量较低,燃着的木条伸入呼出的气体中,燃着的木条会熄灭,错误;
B、①变瘪了的乒乓球放在热水中鼓起,是因为温度升高,分子的间隔变大,错误;
②1L酒精与1L水混合后总体积小于2L说明分子间有间隙,正确;
C、①氧气由氧气分子构成,正确;
②水由水分子构成,正确;
D、①二氧化碳是空气成分之一,不是空气污染物,错误;
②二氧化氮是空气污染物之一,正确。
故选C。
14.C
【详解】
A、物质和氧发生的化学反应,叫做氧化反应,这里的氧包括氧气和氧元素,物质和氧气发生的化学反应都是氧化反应,有的氧化反应是物质和氧元素发生的化学反应,故选项推理错误;
B、混合物中至少含有两种物质,但混合物中不一定至少含有两种元素,也可能只含有一种元素,如金刚石和石墨的混合物中只含有一种元素,故选项推理错误;
C、离子是带电荷的微粒,但带电荷的微粒不一定是离子,也可能是质子、电子等,故选项推理正确;
D、质子数相同的粒子不一定属于同种元素,例如水分子和氖原子质子数都是10,故选项推理错误。
故选:C。
15.A
【详解】
元素组成物质,这里的碘、铁、钙、硒、氟指的是物质的组成,指的是组成物质的元素,故选A。
16.C
【详解】
地壳含量较多的元素(前四种)按含量从高到低的排序为:氧、硅、铝、铁,由图可知,b含量第二多的元素,即b代表的是硅元素,故选C。
17.A
【详解】
元素是具有相同质子数的一类原子的总称,质子数不同则是不同种元素。原子中质子数=核外电子数。离子由原子得失电子得到。电子数相同则这两种微粒可能是两种不同的元素的离子或一种元素的离子与另一种元素的原子。
如两种微粒中有分子,因分子中质子数=核外电子数,所以最多有1种分子,另外一种为离子。
故选A。
18.A
【详解】
物质是由元素组成。在我们的日常生活中出现了“加碘食盐”、“高钙牛奶”等商品。这里的“碘”、“钙”为元素。
故选:A。
19.D
【详解】
A、分子、原子、离子都是构成物质的微粒,所以分子、原子、离子都可以直接构成物质,选项说法不正确;
B、原子是化学变化中的最小微粒,而分子是保持物质的化学性质的最小微粒,选项说法不正确;
C、元素只论种类,不论个数;原子的最外层电子数决定了元素的化学性质,不是原子的电子数,选项说法不正确;
D、原子得失电子后形成了离子,原子得到电子形成阴离子,原子失去电子形成阳离子,选项说法正确。
故选D。
20.A
【详解】
A、同一元素的质子数相同;如果两种粒子属于同一种元素,则这两种粒子的原子核中质子数一定相同,正确;
B、含有的质子数相同的两种粒子不一定属于同一种元素,例如氖原子和水分子质子数相同,不是同一元素,错误;
C、物质中只含有一种元素,这种物质不一定是纯净物,例如氧气和臭氧组成的混合物,错误;
D、化学变化中构成物质的分子改变,组成物质的元素一定不变,例如氧气转化为臭氧,错误。
故选A。
21.
(1)水分子H2O
(2)氢原子、氧原子
(3)分子不断运动
(4)温度降低,分子间隔变小
【解析】
(1)
分子是保持物质化学性质的最小粒子,保持水的化学性质的微粒是水分子;
(2)
原子是化学变化中最小的粒子,过氧化氢分解生成水和氧气的过程中,不变的微粒是氢原子、氧原子;
(3)
用湿抹布擦过的桌面,一段时间后变干的原因是分子不断运动的,水分子运动到空气中去了;
(4)
分子之间有间隔,一定质量的水蒸气冷凝成水时,其体积变小的原因是温度降低,分子间隔变小。
22.
(1)1:2
(2)化合反应
【分析】
(1)
从图中可知,A、C的分子个数比是1:2。
(2)
从图中可知,反应物有2种,生成物有1种,符合多变一的特点,属于化合反应。
23.
(1)原子
(2)18
(3)Mg2+
(4)否
【分析】
(1)
原子构成分子,分子分裂成为原子,原子得失电子变为离子,故①表示原子。
(2)
在原子中质子数等于核外电子数,该粒子是原子,核外有18个电子,故其核内有18个质子,所以X=18,故填18。
(3)
A是氟元素,B是镁元素,能够形成阳离子的是镁,故其离子符号为:Mg2+。
(4)
C是镁离子,D是氩原子,故其化学性质不相似,故选否。
24.
(1)原子
(2)B
(3)得到
【分析】
(1)
C粒子的核外电子数等于核内的质子数,微粒不带电,故属于原子。
(2)
最外层电子数决定原子的化学性质,A粒子与B粒子的最外层电子数都是6,故两种粒子的化学性质相似。
(3)
B粒子的最外层电子数是6,大于4个,易得到电子变成稳定结构。
25.
(1)
(2)7
(3)一氧化碳
(4)S2-
(5) BC AD
【分析】
(1)
根据元素周期表可知,Z是钠元素,其核电荷数为11,原子核电子排布是2、8、1,在形成离子时,失去1个电子形成稳定结构。离子结构示意图为: ;
(2)
根据元素周期表可知,X的原子序数是7;
(3)
根据元素周期表可知,M、Y两种元素分别为C、O,组成的某物质是空气污染物,该物质是CO,CO有毒性;
(4)
当x-y=8时,该粒子是带2个单位负电荷的硫离子,硫离子的符号为S2-;
(5)
同种元素质子数相同,BC的质子数都是8,所以BC属于同种元素;最外层电子数是8的是一种稳定结构,第一层也是最外层时,达到2个电子也是一种稳定结构。AD最外层电子数都达到了稳定结构,化学性质不活泼,所以AD化学性质相似。
【点睛】
26.
(1) Al 三 金属
(2)化学性质稳定(合理即可)
(3)供给呼吸(合理即可)
(4)增加
【分析】
(1)
根据元素周期表可知,13号元素的符号是Al,位于元素周期表中第三周期,它最外层电子数为3,少于4个电子,属于金属元素;
(2)
根据元素周期表可知,10号元素原子的最外层电子数为8,是一种稳定结构,所以它的化学性质稳定;
(3)
8号元素是氧气,氧元素组成的单质可以是氧气,氧气能供给呼吸;
(4)
根据元素周期表可知,同周期元素,从左到右,各元素原子随原子序数的增加,最外层电子数依次增加。
【点睛】
答案第1页,共2页
答案第1页,共2页
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
