2021-2022学年九年级化学人教版上册5.2如何正确书写化学方程式 课件(19张PPT)
文档属性
| 名称 | 2021-2022学年九年级化学人教版上册5.2如何正确书写化学方程式 课件(19张PPT) |  | |
| 格式 | zip | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-04 12:47:15 | ||
图片预览


文档简介
(共19张PPT)
课题2 如何正确书写化学方程式
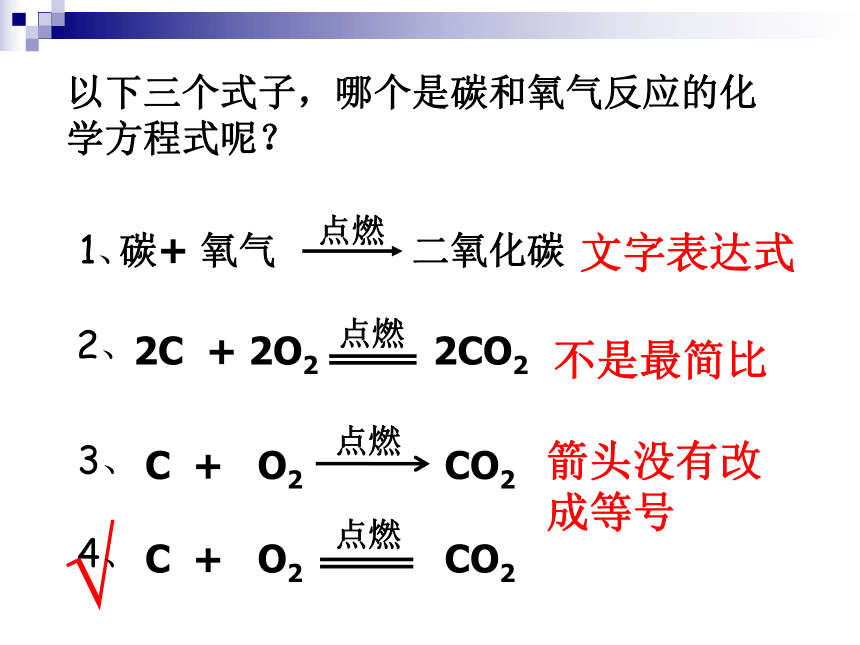
以下三个式子,哪个是碳和氧气反应的化学方程式呢?
碳+ 氧气 二氧化碳
点燃
1、
C + O2 CO2
点燃
3、
2C + 2O2 2CO2
点燃
2、
√
不是最简比
C + O2 CO2
点燃
4、
箭头没有改
成等号
文字表达式
一、化学方程式的书写原则
2、 遵守质量守恒定律,等号两边各
原子的种类和数目必须相等。
1、 必须以客观事实为基础,决不能
凭空臆想、臆造事实上不存在的
物质和化学反应。
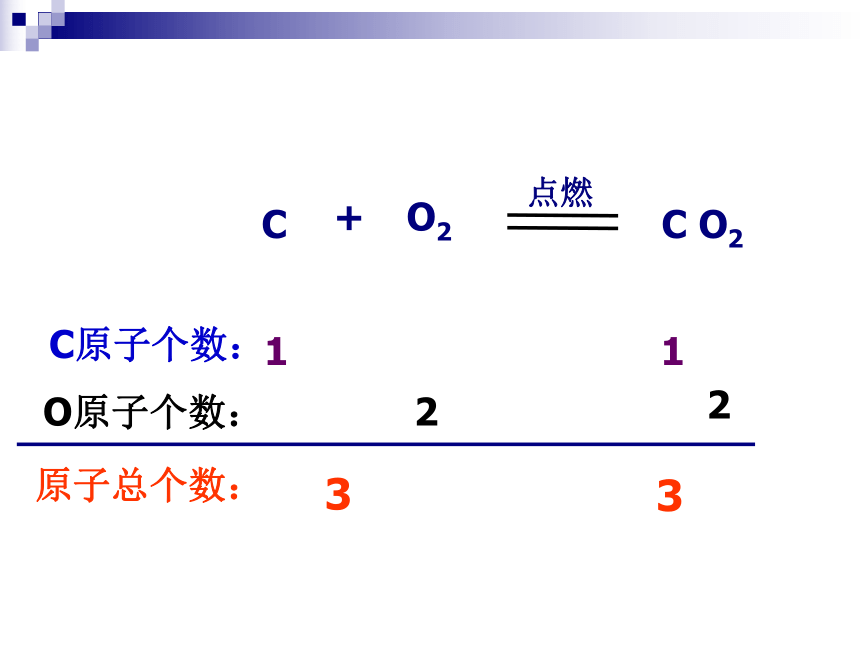
C
O2
+
点燃
C O2
C原子个数:
1
1
O原子个数:
2
2
3
3
原子总个数:
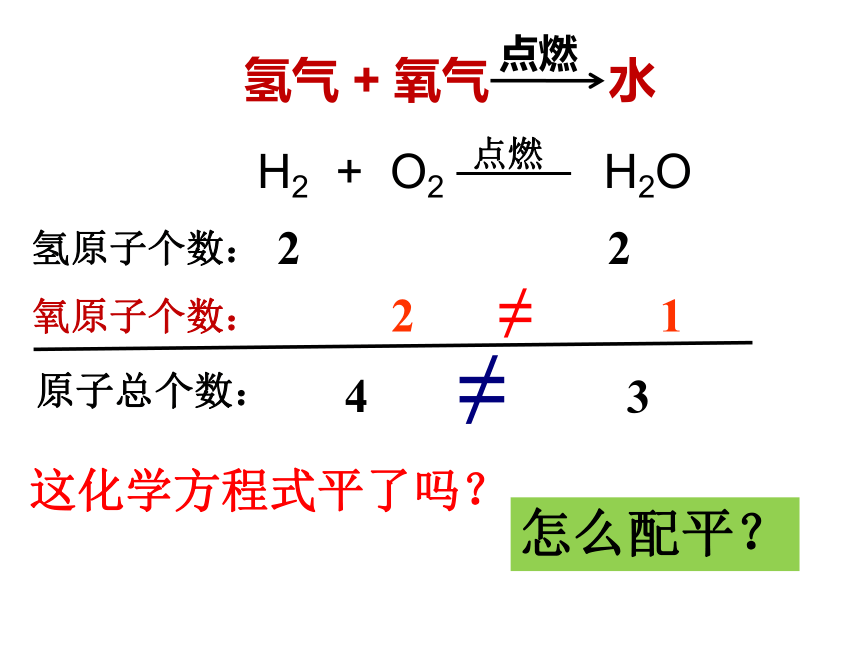
氢气 + 氧气 水
H2 + O2 H2O
氢原子个数:
2
2
氧原子个数:
2
1
原子总个数:
4
3
点燃
点燃
≠
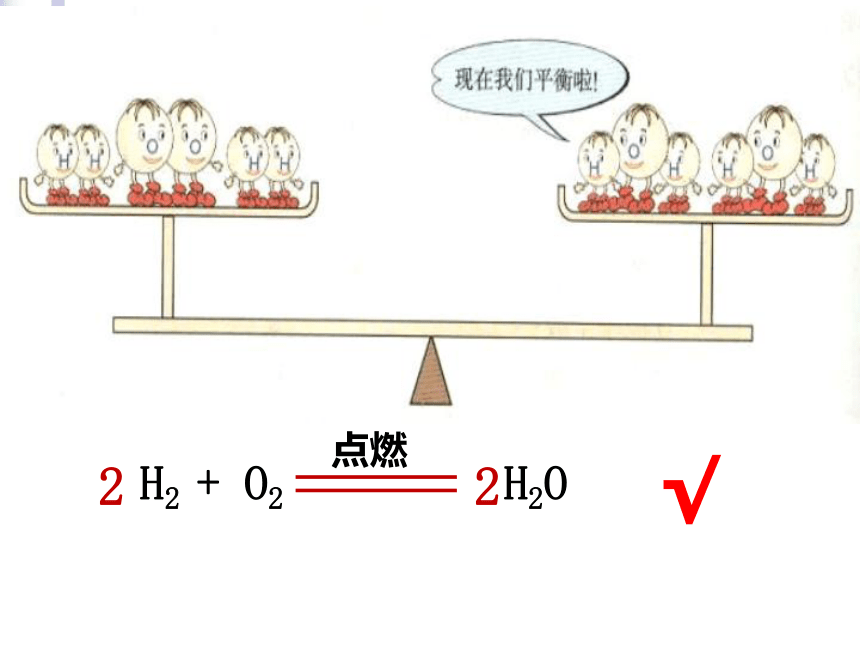
这化学方程式平了吗?
怎么配平?
≠
H2 + O2 H2O
×
你认为写成什么样才是对的呢?
点燃
甲同学:
H2 + O2 H2O
2
2
√
点燃
二、化学方程式的书写5个步骤
写、配、注、改、查
P
O2
+
P2O5
左边写反应物化学式,
右边写生成物化学式,
式子两边用一条短线连接。
1、写
最小公倍数为:2×5=10
2、配:
O
2
P
+
P O
2
5
4
根据质量守恒定律,在式子两边的化学式前配上适当的化学计量数,使式子两边每一种元素原子的数目相等
10÷5=2
10÷2=5
方法一:最小公倍数法
通常找只出现过一次,且原子个数最多的。
2
5
3、注:
O
2
P
+
P O
2
5
4
5
2
4、改:
注明反应的条件,生成物状态 ( 气态用“↑”、沉淀用“↓” )
把短线改成等号
点燃
5、查:
检查化学式是否正确;原子种类、原子个数、是否相等;反应条件、生成物状态是否注明等
对第3点:“注”的解析
1、加热常用“△”表示
2、条件多个时,可在等号上下方标注
3、加热 ≠高温 ≠点燃
4、 两边都有气体不需标“↑”,
左边没有,右边有气体的才标 “↑”
5、 溶液中,两边都有固体不需标“↓”,
左边没有,右边有固体的才标 “↓”
切记:所有的箭头都是标在右边的
巧记:无中生有标上下,两边都有不用标
练习:
1、 H2O H2 + O2
通电
2、 Al + O2 Al2O3
2
3
4
2
2
↑
3、 KClO3 KCl + O2
MnO2
△
2
2
3
↑
↑
Fe2O3 + CO Fe + CO2
(在溶液中,反应物中没有固体,而生成物中有固体(沉淀)时,则注“↓ ” )
方法二:观察法(有原子团的优先)
CuSO4+ NaOH Na2SO4 + Cu(OH) 2
2
例如:铁在氧气中燃烧生成四氧化三铁
Fe + O2 Fe3O4
点燃
2
3
3
3
2
高温
KMnO4 K2MnO4+MnO2+O2
2
H2O2 H2O + O2
S + O2 SO2
点燃
等号两边都有气体时不标 “ ↑ ”,左边没
有气体,右边有气体的 ,则在右边标“↑ ”
MnO2
2
2
试一试:
方法三:奇数变偶数
Al + O2 Al2O3
通常找原子个数最多的,在左右两边出现“奇数”和“偶数”的元素。
2
3
2
4
8
11
FeS2 + O2 Fe2O3 + SO2
高温
4
2
3
2
↑
KClO3 KCl+ O2
MnO2
△
方法四:设一法
找出关键的化学式(如有机物),定其化学式前的化学计量数为1,然后根据关键化学式去配平其他化学式前的化学计量数.若学计量数为分数,则将各计量数同时乘以同一整数,化分数为整数。
1
1
3
_
2
5
_
4
去分母,两边各项同时乘于4
4NH3 + 5O2 4NO+ 6H2O
高温
Pt
NH3 + O2 NO+ H2O
Pt
高温
小结
1、书写化学方程式时要切记两条原则:
(1)以客观事实为基础,不能凭空臆造事
实上不 存在的物质和化学反应
(2)遵守质量守恒定律
2、书写化学方程式时,在式子左、右两边的化学式前面要配上适当的化学计量数,使得每一种元素的原子总数相等,这个过程就是化学方程式的配平。
化学方程式
1、定义:用化学式表示化学反应的式子。
2、意义:
(1)表示反应物,生成物和反应条件
(2)表示各物质之间的质 量比,
3、书写原则
一是必须以客观事实为基础
二是要遵守质量守恒定律,等号
两边原子种类、原子数目必须相等
4、书写步骤:
写:左反右生一横线
配:配平
注:注明反应条件、生成物的状态( 、)
改:短线改等号
(3)表示各物质之间的粒子个数比,
查:
再见,请预习课题3
课题2 如何正确书写化学方程式
以下三个式子,哪个是碳和氧气反应的化学方程式呢?
碳+ 氧气 二氧化碳
点燃
1、
C + O2 CO2
点燃
3、
2C + 2O2 2CO2
点燃
2、
√
不是最简比
C + O2 CO2
点燃
4、
箭头没有改
成等号
文字表达式
一、化学方程式的书写原则
2、 遵守质量守恒定律,等号两边各
原子的种类和数目必须相等。
1、 必须以客观事实为基础,决不能
凭空臆想、臆造事实上不存在的
物质和化学反应。
C
O2
+
点燃
C O2
C原子个数:
1
1
O原子个数:
2
2
3
3
原子总个数:
氢气 + 氧气 水
H2 + O2 H2O
氢原子个数:
2
2
氧原子个数:
2
1
原子总个数:
4
3
点燃
点燃
≠
这化学方程式平了吗?
怎么配平?
≠
H2 + O2 H2O
×
你认为写成什么样才是对的呢?
点燃
甲同学:
H2 + O2 H2O
2
2
√
点燃
二、化学方程式的书写5个步骤
写、配、注、改、查
P
O2
+
P2O5
左边写反应物化学式,
右边写生成物化学式,
式子两边用一条短线连接。
1、写
最小公倍数为:2×5=10
2、配:
O
2
P
+
P O
2
5
4
根据质量守恒定律,在式子两边的化学式前配上适当的化学计量数,使式子两边每一种元素原子的数目相等
10÷5=2
10÷2=5
方法一:最小公倍数法
通常找只出现过一次,且原子个数最多的。
2
5
3、注:
O
2
P
+
P O
2
5
4
5
2
4、改:
注明反应的条件,生成物状态 ( 气态用“↑”、沉淀用“↓” )
把短线改成等号
点燃
5、查:
检查化学式是否正确;原子种类、原子个数、是否相等;反应条件、生成物状态是否注明等
对第3点:“注”的解析
1、加热常用“△”表示
2、条件多个时,可在等号上下方标注
3、加热 ≠高温 ≠点燃
4、 两边都有气体不需标“↑”,
左边没有,右边有气体的才标 “↑”
5、 溶液中,两边都有固体不需标“↓”,
左边没有,右边有固体的才标 “↓”
切记:所有的箭头都是标在右边的
巧记:无中生有标上下,两边都有不用标
练习:
1、 H2O H2 + O2
通电
2、 Al + O2 Al2O3
2
3
4
2
2
↑
3、 KClO3 KCl + O2
MnO2
△
2
2
3
↑
↑
Fe2O3 + CO Fe + CO2
(在溶液中,反应物中没有固体,而生成物中有固体(沉淀)时,则注“↓ ” )
方法二:观察法(有原子团的优先)
CuSO4+ NaOH Na2SO4 + Cu(OH) 2
2
例如:铁在氧气中燃烧生成四氧化三铁
Fe + O2 Fe3O4
点燃
2
3
3
3
2
高温
KMnO4 K2MnO4+MnO2+O2
2
H2O2 H2O + O2
S + O2 SO2
点燃
等号两边都有气体时不标 “ ↑ ”,左边没
有气体,右边有气体的 ,则在右边标“↑ ”
MnO2
2
2
试一试:
方法三:奇数变偶数
Al + O2 Al2O3
通常找原子个数最多的,在左右两边出现“奇数”和“偶数”的元素。
2
3
2
4
8
11
FeS2 + O2 Fe2O3 + SO2
高温
4
2
3
2
↑
KClO3 KCl+ O2
MnO2
△
方法四:设一法
找出关键的化学式(如有机物),定其化学式前的化学计量数为1,然后根据关键化学式去配平其他化学式前的化学计量数.若学计量数为分数,则将各计量数同时乘以同一整数,化分数为整数。
1
1
3
_
2
5
_
4
去分母,两边各项同时乘于4
4NH3 + 5O2 4NO+ 6H2O
高温
Pt
NH3 + O2 NO+ H2O
Pt
高温
小结
1、书写化学方程式时要切记两条原则:
(1)以客观事实为基础,不能凭空臆造事
实上不 存在的物质和化学反应
(2)遵守质量守恒定律
2、书写化学方程式时,在式子左、右两边的化学式前面要配上适当的化学计量数,使得每一种元素的原子总数相等,这个过程就是化学方程式的配平。
化学方程式
1、定义:用化学式表示化学反应的式子。
2、意义:
(1)表示反应物,生成物和反应条件
(2)表示各物质之间的质 量比,
3、书写原则
一是必须以客观事实为基础
二是要遵守质量守恒定律,等号
两边原子种类、原子数目必须相等
4、书写步骤:
写:左反右生一横线
配:配平
注:注明反应条件、生成物的状态( 、)
改:短线改等号
(3)表示各物质之间的粒子个数比,
查:
再见,请预习课题3
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
