5.1初步认识化学元素同步练习--2021-2022学年九年级化学京改版(2013)上册(word版 含答案)
文档属性
| 名称 | 5.1初步认识化学元素同步练习--2021-2022学年九年级化学京改版(2013)上册(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 100.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-04 21:11:57 | ||
图片预览



文档简介
初步认识化学元素
一、单选题
1.决定元素种类的是( )
A.质子数 B.最外层电子数 C.核外电子数 D.中子数
2.“加铁酱油”“高锌奶粉”“富硒茶叶”中,“铁、锌、硒”指的是( )
A.单质 B.分子 C.元素 D.原子
3.患贫血病的人可以多吃韭菜,因为韭菜是一种含铁量很高的蔬菜,每100克韭菜中含铁8.9毫克。这里的铁指的是( )
A.铁元素 B.铁单质 C.氧化铁 D.铁的化合物
4.对2H表述正确的是的( )
A.氢元素 B.氢原子 C.氢气 D.两个氢原子
5.红宝石的主要成分是Al2O3、Al2O3由铝和氧两种元素组成,这两种元素的本质区别是( )
A.电子数不同 B.质子数不同 C.最外层电子数不同 D.相对原子质量不同
6.银的元素符号是( )
A.Ag B.Hg C.Mg D.He
7.下列符号既能表示一种元素,又能表示一种原子,还能表示某种物质的是( )
A.N B.2H C.Ca2+ D.Ne
8.“高钙牛奶”中的“钙”应理解为( )
A.单质 B.原子 C.离子 D.元素
9.如图是元素周期表中某元素的相关信息,从图中不能直接获得的信息是( )
A.该元素属于非金属元素
B.该元素的原子序数为7
C.该元素的相对原子质量是14.01
D.氮原子的中子数为7
10.2021年5月22日,“祝融号"火星车安全驶离着陆平台,到达火星表面,开始巡视探测。锂离子蓄电池在“祝融号”供配电系统中起着十分重要的作用。在元素周期表中锂元素的某些信息如图所示,下列有关锂的说法不正确的是 ( )
A.原子序数为 3 B.元素符号为 Li C.属于金属元素 D.相对原子质量为 6.94kg
11.下列符号既能表示一种元素,又能表示一个原子,还能表示一种物质的是:( )
A.H2 B.He C.O D.2Fe
12.一种元素与另一种元素的本质区别是( )
A.质子数不同 B.中子数不同
C.相对原子质量不同 D.电子数不同
二、填空题
13.图甲是铝元素在元素周期表中的相关信息,图乙是几种微粒的结构示意图,仔细分析答题:
(1)图甲中,铝元素的信息有处错误,请加以改正_________;
(2)铝元素的相对原子质量是_________ ;
(3)图乙中,属于稳定结构的原子是__________ (填序号);
14.用分子、原子、元素观点解释下列问题。
(1)博物馆把贵重的书画保存在充满N2的圆桶中,是利用常温下N2___________。
(2)从微观角度解释,变瘪的乒乓球放在热水中又鼓起来的原因是___________。
(3)氧原子和磷原子是两种不同的原子___________。
15.见如图,完成填空。
(1)地壳中含量最多的金属元素是(写元素符号)_________。
(2)铁元素与铝元素两种元素本质区别是_________不同。
(3)氧元素位于第________周期,同一周期元素________相同。
16.填表:
元素名称 铝 ________ ________ ________ 镁 银 汞
元素符号 ________ Cl Na Si ________ ________ ________
17.元素周期表是学习化学的重要工具,下表是元素周期表中1-18号元素的原子核外电子排布。
(1)13号元素的符号是_______,位于元素周期表中第______周期,它属于________元素(选填“金属”或“非金属”);
(2)写出表中关于10号元素的一条信息__________。
(3)列举8号元素对应单质的一种用途________。
(4)同周期元素,从左到右,各元素原子随原子序数的增加,最外层电子数依次_________。
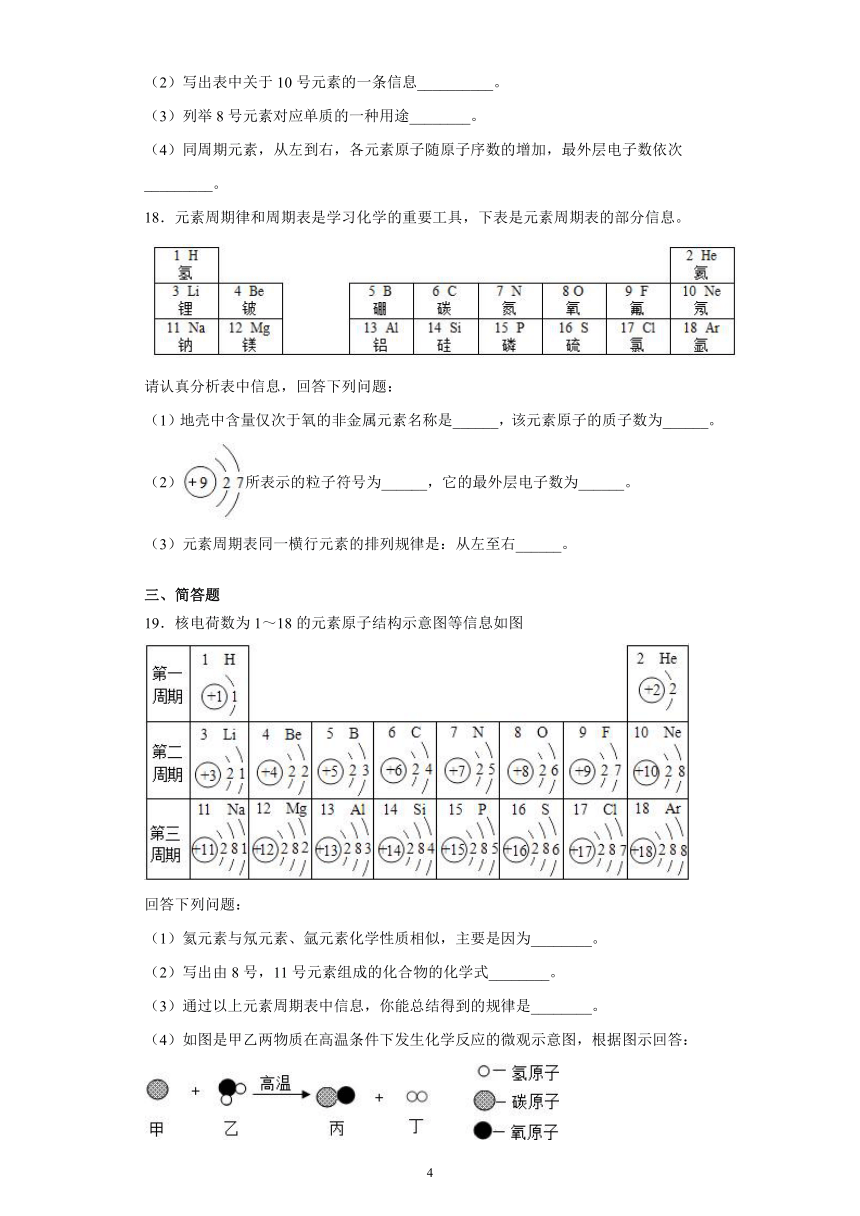
18.元素周期律和周期表是学习化学的重要工具,下表是元素周期表的部分信息。
请认真分析表中信息,回答下列问题:
(1)地壳中含量仅次于氧的非金属元素名称是______,该元素原子的质子数为______。
(2)所表示的粒子符号为______,它的最外层电子数为______。
(3)元素周期表同一横行元素的排列规律是:从左至右______。
三、简答题
19.核电荷数为1~18的元素原子结构示意图等信息如图
回答下列问题:
(1)氦元素与氖元素、氩元素化学性质相似,主要是因为________。
(2)写出由8号,11号元素组成的化合物的化学式________。
(3)通过以上元素周期表中信息,你能总结得到的规律是________。
(4)如图是甲乙两物质在高温条件下发生化学反应的微观示意图,根据图示回答:
①属于化合物的是________(写化学式)。
②上述反应中,不发生改变的粒子是________(填“分子”或“原子”) 。
③写出上述反应的化学方程式_________反应类型为_____。
四、科学探究题
20.元素周期表是学习和研究化学的重要工具,它的内容十分丰富。下表是依据元素周期表画出的1~18号元素的原子结构示意图。我对它进行研究:
(1)原子序数为16的元素名称是______,在化学反应中,该元素的原子容易______电子,变成_______(填符号);原子序数为11的元素属于__________填“金属”或“非金属”)元素。
(2)根据图示信息,推测一个一氧化碳分子中所含的电子总数为_____________。
(3)我发现如下规律:①原子最外层电子数一般不超过8个;
②金属元素的原子最外层电子数一般少于4个,非金属元素的原子原子最外层电子数一般多于4个;
③__________________________;
④__________________________;
(4)下图表示碘元素的_________(填“原子”、“阳离子”或“阴离子”)结构示意图。由图 可知,碘元素应位于元素周期表中的第___________ 周期。
参考答案
1.A
2.C
3.A
4.D
5.B
6.A
7.D
8.D
9.D
10.D
11.B
12.A
13.
(1)Al
(2)26.98
(3)ABD
14.
(1)化学性质稳定(或不活泼)
(2)温度升高,分子间的间隔变大
(3)原子的核内质子数不同
15.
(1)Al
(2)质子数
(3) 二 电子层数
16.氯 钠 硅 Al Mg Ag Hg
17.
(1) Al 三 金属
(2)化学性质稳定(合理即可)
(3)供给呼吸(合理即可)
(4)增加
18.
(1) 硅 14
(2) F 7
(3)最外层电子数依次增加1
19.
(1)三种原子的最外层电子数都达到稳定结构
(2)Na2O
(3)横行规律:同一横行的元素,原子的电子层数相同,由左至右最外层电子数依次递增;纵行规律:同一纵行的元素,原子的最外层电子数相等,由上到下电子层数逐渐增多
(4) H2O、CO 原子 C+H2OCO+H2 置换反应
20.硫 得到 S2- 金属 14 同一周期,原子的电子层数相同,最外层电子数逐渐增加 同一族,原子的最外层电子数相同 原子 5
一、单选题
1.决定元素种类的是( )
A.质子数 B.最外层电子数 C.核外电子数 D.中子数
2.“加铁酱油”“高锌奶粉”“富硒茶叶”中,“铁、锌、硒”指的是( )
A.单质 B.分子 C.元素 D.原子
3.患贫血病的人可以多吃韭菜,因为韭菜是一种含铁量很高的蔬菜,每100克韭菜中含铁8.9毫克。这里的铁指的是( )
A.铁元素 B.铁单质 C.氧化铁 D.铁的化合物
4.对2H表述正确的是的( )
A.氢元素 B.氢原子 C.氢气 D.两个氢原子
5.红宝石的主要成分是Al2O3、Al2O3由铝和氧两种元素组成,这两种元素的本质区别是( )
A.电子数不同 B.质子数不同 C.最外层电子数不同 D.相对原子质量不同
6.银的元素符号是( )
A.Ag B.Hg C.Mg D.He
7.下列符号既能表示一种元素,又能表示一种原子,还能表示某种物质的是( )
A.N B.2H C.Ca2+ D.Ne
8.“高钙牛奶”中的“钙”应理解为( )
A.单质 B.原子 C.离子 D.元素
9.如图是元素周期表中某元素的相关信息,从图中不能直接获得的信息是( )
A.该元素属于非金属元素
B.该元素的原子序数为7
C.该元素的相对原子质量是14.01
D.氮原子的中子数为7
10.2021年5月22日,“祝融号"火星车安全驶离着陆平台,到达火星表面,开始巡视探测。锂离子蓄电池在“祝融号”供配电系统中起着十分重要的作用。在元素周期表中锂元素的某些信息如图所示,下列有关锂的说法不正确的是 ( )
A.原子序数为 3 B.元素符号为 Li C.属于金属元素 D.相对原子质量为 6.94kg
11.下列符号既能表示一种元素,又能表示一个原子,还能表示一种物质的是:( )
A.H2 B.He C.O D.2Fe
12.一种元素与另一种元素的本质区别是( )
A.质子数不同 B.中子数不同
C.相对原子质量不同 D.电子数不同
二、填空题
13.图甲是铝元素在元素周期表中的相关信息,图乙是几种微粒的结构示意图,仔细分析答题:
(1)图甲中,铝元素的信息有处错误,请加以改正_________;
(2)铝元素的相对原子质量是_________ ;
(3)图乙中,属于稳定结构的原子是__________ (填序号);
14.用分子、原子、元素观点解释下列问题。
(1)博物馆把贵重的书画保存在充满N2的圆桶中,是利用常温下N2___________。
(2)从微观角度解释,变瘪的乒乓球放在热水中又鼓起来的原因是___________。
(3)氧原子和磷原子是两种不同的原子___________。
15.见如图,完成填空。
(1)地壳中含量最多的金属元素是(写元素符号)_________。
(2)铁元素与铝元素两种元素本质区别是_________不同。
(3)氧元素位于第________周期,同一周期元素________相同。
16.填表:
元素名称 铝 ________ ________ ________ 镁 银 汞
元素符号 ________ Cl Na Si ________ ________ ________
17.元素周期表是学习化学的重要工具,下表是元素周期表中1-18号元素的原子核外电子排布。
(1)13号元素的符号是_______,位于元素周期表中第______周期,它属于________元素(选填“金属”或“非金属”);
(2)写出表中关于10号元素的一条信息__________。
(3)列举8号元素对应单质的一种用途________。
(4)同周期元素,从左到右,各元素原子随原子序数的增加,最外层电子数依次_________。
18.元素周期律和周期表是学习化学的重要工具,下表是元素周期表的部分信息。
请认真分析表中信息,回答下列问题:
(1)地壳中含量仅次于氧的非金属元素名称是______,该元素原子的质子数为______。
(2)所表示的粒子符号为______,它的最外层电子数为______。
(3)元素周期表同一横行元素的排列规律是:从左至右______。
三、简答题
19.核电荷数为1~18的元素原子结构示意图等信息如图
回答下列问题:
(1)氦元素与氖元素、氩元素化学性质相似,主要是因为________。
(2)写出由8号,11号元素组成的化合物的化学式________。
(3)通过以上元素周期表中信息,你能总结得到的规律是________。
(4)如图是甲乙两物质在高温条件下发生化学反应的微观示意图,根据图示回答:
①属于化合物的是________(写化学式)。
②上述反应中,不发生改变的粒子是________(填“分子”或“原子”) 。
③写出上述反应的化学方程式_________反应类型为_____。
四、科学探究题
20.元素周期表是学习和研究化学的重要工具,它的内容十分丰富。下表是依据元素周期表画出的1~18号元素的原子结构示意图。我对它进行研究:
(1)原子序数为16的元素名称是______,在化学反应中,该元素的原子容易______电子,变成_______(填符号);原子序数为11的元素属于__________填“金属”或“非金属”)元素。
(2)根据图示信息,推测一个一氧化碳分子中所含的电子总数为_____________。
(3)我发现如下规律:①原子最外层电子数一般不超过8个;
②金属元素的原子最外层电子数一般少于4个,非金属元素的原子原子最外层电子数一般多于4个;
③__________________________;
④__________________________;
(4)下图表示碘元素的_________(填“原子”、“阳离子”或“阴离子”)结构示意图。由图 可知,碘元素应位于元素周期表中的第___________ 周期。
参考答案
1.A
2.C
3.A
4.D
5.B
6.A
7.D
8.D
9.D
10.D
11.B
12.A
13.
(1)Al
(2)26.98
(3)ABD
14.
(1)化学性质稳定(或不活泼)
(2)温度升高,分子间的间隔变大
(3)原子的核内质子数不同
15.
(1)Al
(2)质子数
(3) 二 电子层数
16.氯 钠 硅 Al Mg Ag Hg
17.
(1) Al 三 金属
(2)化学性质稳定(合理即可)
(3)供给呼吸(合理即可)
(4)增加
18.
(1) 硅 14
(2) F 7
(3)最外层电子数依次增加1
19.
(1)三种原子的最外层电子数都达到稳定结构
(2)Na2O
(3)横行规律:同一横行的元素,原子的电子层数相同,由左至右最外层电子数依次递增;纵行规律:同一纵行的元素,原子的最外层电子数相等,由上到下电子层数逐渐增多
(4) H2O、CO 原子 C+H2OCO+H2 置换反应
20.硫 得到 S2- 金属 14 同一周期,原子的电子层数相同,最外层电子数逐渐增加 同一族,原子的最外层电子数相同 原子 5
同课章节目录
- 第1章 走进化学
- 第一节 化学让世界更美好
- 第二节 实验是化学的基础
- 第2章 空气之谜
- 第一节 空气
- 第二节 氧气的制法
- 第三节 氧气的性质
- 第3章 构成物质的微粒
- 第一节 原子
- 第二节 原子核外电子的排布 离子
- 第三节 分子
- 第4章 最常见的液体——水
- 第一节 水的净化
- 第二节 水的变化
- 第三节 水资源的开发、利用和保护
- 第5章 化学元素与物质组成的表示
- 第一节 初步认识化学元素
- 第二节 物质组成的表示——化学式
- 第三节 化合价
- 第6章 燃烧的学问
- 第一节 探索燃烧与灭火
- 第二节 化学反应中的能量变化
- 第三节 化石燃料
- 第7章 化学反应的定量研究
- 第一节 质量守恒定律
- 第二节 化学方程式
- 第三节 依据化学方程式的简单计算
- 第8章 碳的世界
- 第一节 碳的单质
- 第二节 二氧化碳的性质和用途
- 第三节 二氧化碳的实验室制法
