5.1质量守恒定律课后习题 --2021-2022学年九年级化学人教版上册(word版含答案)
文档属性
| 名称 | 5.1质量守恒定律课后习题 --2021-2022学年九年级化学人教版上册(word版含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 171.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-04 00:00:00 | ||
图片预览


文档简介
课题一 质量守恒定律
一、单选题
1.下列说法错误的是( )
A.原子核一般由质子、中子构成
B.花香四溢主要是因为分子之间有间隔
C.保持水化学性质的最小微粒是水分子
D.化学反应前后原子的种类不会改变
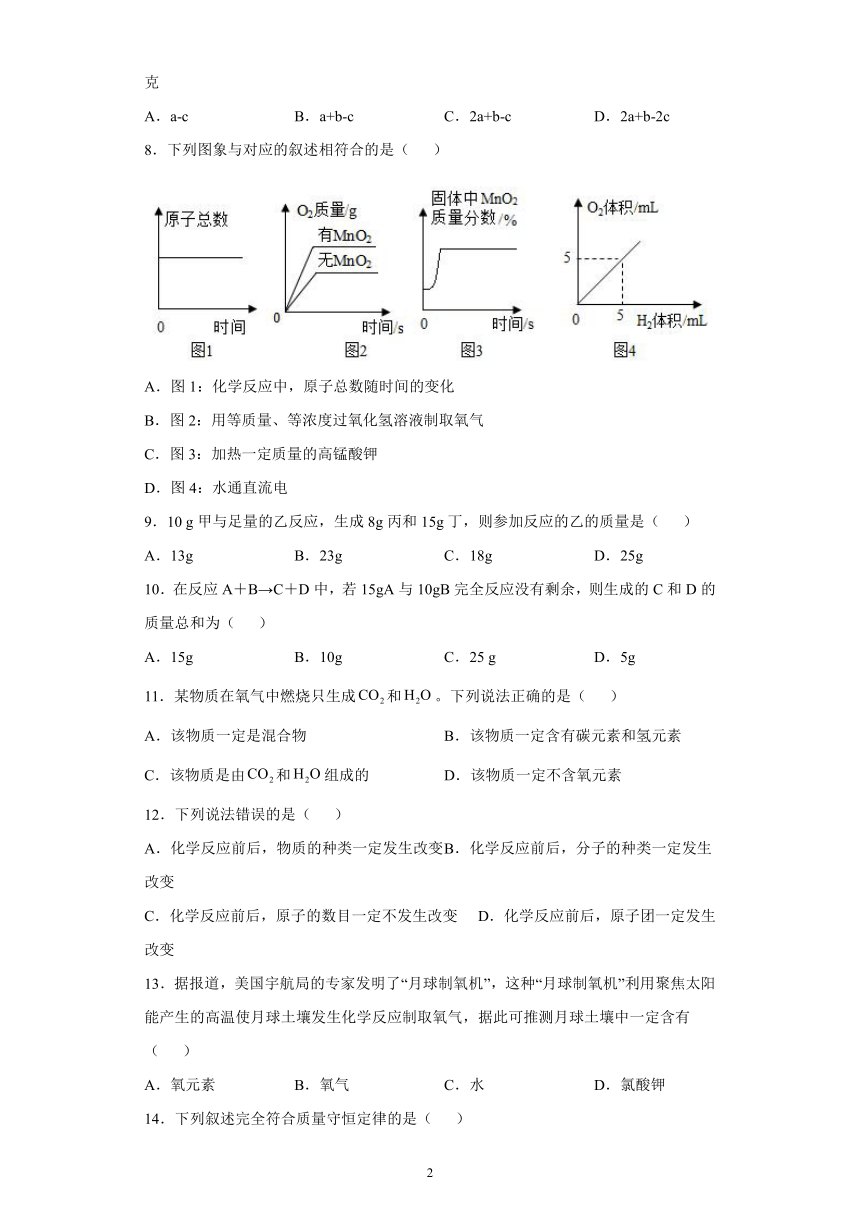
2.图甲、乙是电解水的实验及电解时水分子分解的示意图。有关叙述正确的是( )
A.反应前水分子的能量和等于反应后生成的氢分子和氧分子能量之和
B.此实验证明水是由氢气和氧气组成
C.水电解的过程中,氢原子和氧原子数不变
D.电解水的变化只是分子间的间隔发生了变化
3.氯酸钾m克和二氧化锰n克共热后完全分解得到氧气a克,则剩余固体中所含氯化钾的质量为( )
A.(m-n)克 B.(m+n-a)克
C.(m-a)克 D.(m-n-a)克
4.现将足量的A和10gB混合加热,A与B发生化学反应,10gB完全反应后生成4gC和8gBD,则参加反应的A与B的质量比是( )
A.1:1 B.1:5 C.5:1 D.2:1
5.在化学反应前后,一定不发生改变的是( )
A.分子的种类 B.原子的种类 C.分子的质量 D.物质的种类
6.3.6g某物质在足量的氧气中燃烧,生成二氧化碳4.4g,水3.6g则某物质的组成是( )
A.一定有C、H元素,可能有氧元素 B.只含C、H元素
C.一定含有C、H、O三种元素 D.无法确定
7.a克氯酸钾和b克二氧化锰混合加热至完全分解,生成c克固体,则生成氧气( )克
A.a-c B.a+b-c C.2a+b-c D.2a+b-2c
8.下列图象与对应的叙述相符合的是( )
A.图1:化学反应中,原子总数随时间的变化
B.图2:用等质量、等浓度过氧化氢溶液制取氧气
C.图3:加热一定质量的高锰酸钾
D.图4:水通直流电
9.10 g甲与足量的乙反应,生成8g丙和15g丁,则参加反应的乙的质量是( )
A.13g B.23g C.18g D.25g
10.在反应A+B→C+D中,若15gA与10gB完全反应没有剩余,则生成的C和D的质量总和为( )
A.15g B.10g C.25 g D.5g
11.某物质在氧气中燃烧只生成和。下列说法正确的是( )
A.该物质一定是混合物 B.该物质一定含有碳元素和氢元素
C.该物质是由和组成的 D.该物质一定不含氧元素
12.下列说法错误的是( )
A.化学反应前后,物质的种类一定发生改变 B.化学反应前后,分子的种类一定发生改变
C.化学反应前后,原子的数目一定不发生改变 D.化学反应前后,原子团一定发生改变
13.据报道,美国宇航局的专家发明了“月球制氧机”,这种“月球制氧机”利用聚焦太阳能产生的高温使月球土壤发生化学反应制取氧气,据此可推测月球土壤中一定含有( )
A.氧元素 B.氧气 C.水 D.氯酸钾
14.下列叙述完全符合质量守恒定律的是( )
A.水结成冰前后,质量保持不变
B.50mL水和50 mL乙醇混合后总体积小于100 mL
C.在100g30%过氧化氢溶液中,含有30g过氧化氢和70g水
D.1.2g碳与3.2g氧气恰好完全反应可生成4.4g二氧化碳
15.取两份等质量的xCuCO3· yCu(OH)2固体,在一份中加入过量盐酸,生成6.6gCO2;加热另一份使其完全分解,得到20.0gCuO。则下列关系正确的是( )
A.y∶x=1∶1 B.y∶x=1∶3 C.y∶x=3∶2 D.y∶x=2∶3
二、填空题
16.下图是初中化学教材中的一些实验,按要求回答下列问题:
(1)为确保实验一测量结果的准确,需要注意的事项有________(写一条即可)
(2)通过水电解生成氢气和氧气的事实,得出的实验结论是__________。
(3)实验三中反应后天平不平衡,该反应是否遵守质量守恒定律____(填“是”或“否”)
17.化学用语是学习化学的基本工具,请用化学符号填空:
(1)3个亚铁离子_____________。
(2)2个氮分子_____________。
(3)3个硫酸根离子_____________。
(4)氧化铁中铁元素的化合价_____________。
(5)地壳中含量最高的金属元素与非金属元素形成的化合物是_____________。
(6)分析过氧化氢(H2O2)和过氧化钠(Na2O2)中氧元素的化合价,写出过氧化钙的化学式为-_____________。
(7)气体X在氧气中燃烧生成氮气和水,X分子中一定含有的原子是________(填符号)
18.某有机物4.6g在氧气中完全燃烧后,只生成了8.8g二氧化碳和5.4g水,由此推测此有机物由__________元素组成,此有机物的化学式是___________________。
三、实验题
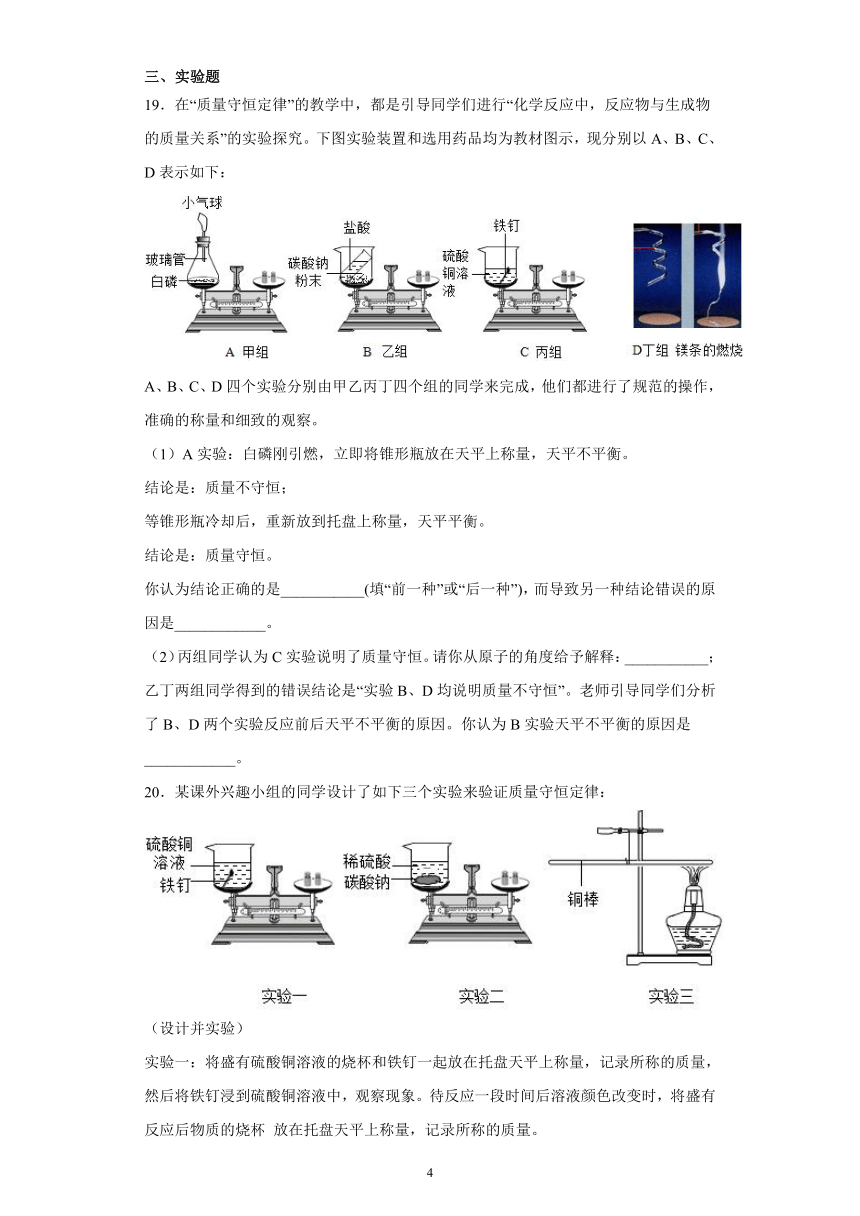
19.在“质量守恒定律”的教学中,都是引导同学们进行“化学反应中,反应物与生成物的质量关系”的实验探究。下图实验装置和选用药品均为教材图示,现分别以A、B、C、D表示如下:
A、B、C、D四个实验分别由甲乙丙丁四个组的同学来完成,他们都进行了规范的操作,准确的称量和细致的观察。
(1)A实验:白磷刚引燃,立即将锥形瓶放在天平上称量,天平不平衡。
结论是:质量不守恒;
等锥形瓶冷却后,重新放到托盘上称量,天平平衡。
结论是:质量守恒。
你认为结论正确的是___________(填“前一种”或“后一种”),而导致另一种结论错误的原因是____________。
(2)丙组同学认为C实验说明了质量守恒。请你从原子的角度给予解释:___________;乙丁两组同学得到的错误结论是“实验B、D均说明质量不守恒”。老师引导同学们分析了B、D两个实验反应前后天平不平衡的原因。你认为B实验天平不平衡的原因是____________。
20.某课外兴趣小组的同学设计了如下三个实验来验证质量守恒定律:
(设计并实验)
实验一:将盛有硫酸铜溶液的烧杯和铁钉一起放在托盘天平上称量,记录所称的质量,然后将铁钉浸到硫酸铜溶液中,观察现象。待反应一段时间后溶液颜色改变时,将盛有反应后物质的烧杯 放在托盘天平上称量,记录所称的质量。
实验二:将盛有稀硫酸的烧杯和碳酸钠一起放在托盘天平上称量,然后将碳酸钠加到稀硫酸中,观察现象 (已知碳酸钠和稀硫酸反应后,会生成大量二氧化碳 )。待反应一段时间后不再放出气泡时,将盛有反应后物质的烧杯放在托盘天平上称量,记录所称的质量。
实验三:用细线系住铜棒中点使之平衡,然后在铜棒一端用酒精灯加热。加热一段时间后,观察 到铜棒的平衡情况是________。
(分析与讨论)
①实验一中,铁和硫酸铜反应,生成硫酸亚铁和一种红色物质,请写出符号表达式______。
②在这三个实验中,你认为:实验_______直接正确反映了反应物与生成物之间的质量关系,由此得出的结论是:在化学反应中生成物的总质量与反应物的总质量相等。
③另外两个实验得出的结论是:在化学反应中生成物的总质量与反应物的总质量不相等,你认为导致这结论错误的原因是______。(只写其中一个实验的原因即可)
(实验反思)
小组成员讨论后达成了以下共识:设计实验验证质量守恒定律时,对于有空气中的气体(成分)参与或有气体生成的化学反应,一般应使反应在______(“开放”或“密闭”)装置中进行。
(拓展与应用)
同学根据质量守恒定律研究物质 W的组成。一定条件下, 在密闭容器内发生反应,反应前后 各物质的质量(单位:g)如图所示:
图中x=______g, 物质W由_____ 种元素组成,其中碳、氢原子个数比为_____(填最简比)。
21.小明用盐酸与碳酸钙粉末反应验证质量守恒定律,实验装置如图。
(1)根据实验目的,小李必须测量的数据是______。
A.锥形瓶质量
B.气球质量
C.反应前整个反应装置(包括里边的物质)质量
D.反应后整个反应装置(包括里边的物质)质量
(2)将反应装置放在天平左盘,使天平平衡后,丙将碳酸钙粉末倒入锥形瓶中、反应结束后,气球鼓起(若不考虑气球膨胀浮力影响),观察到的现象______,从而验证了质量守恒定律,若锥形瓶上方未套气球,则不能验证质量守恒定律,原因是______。
(3)根据化学反应遵循质量守恒定律的本质原因是______。
参考答案
1.B
2.C
3.C
4.B
5.B
6.C
7.A
8.A
9.A
10.C
11.B
12.D
13.A
14.D
15.D
16.
(1)红磷的量要充足,或装置气密性良好,或装置冷却至室温后再打开止水夹
(2)水由氢元素与氧元素组成
(3)是
17.
(1)3Fe2+
(2)2N2
(3)
(4)
(5)Al2O3
(6)CaO2
(7)N、H
18.C H O三种 C2H6O等
19.
(1) 后一种 白磷引燃时燃烧放出大量的热,使装置内气体受热膨胀将气球胀大,装置受到浮力
(2) 化学反应是反应物的原子重新组合,原子的种类、数目、质量不变,生成物的质量也不会改变 反应时产生的二氧化碳气体扩散到空气中,剩余物的质量减少
20.铜棒向有酒精灯加热的一端向下倾斜 一 实验二镁条和稀硫酸反应产生的氢气免逸散到空气中或者实验三有空气中的氧气参加反应 密闭 52 3三 1:3
21.
(1)CD
(2) 天平平衡 有二氧化碳气体逸出
(3)化学反应前后原子种类没有改变、原子数目没有增减、原子质量也没有改变
一、单选题
1.下列说法错误的是( )
A.原子核一般由质子、中子构成
B.花香四溢主要是因为分子之间有间隔
C.保持水化学性质的最小微粒是水分子
D.化学反应前后原子的种类不会改变
2.图甲、乙是电解水的实验及电解时水分子分解的示意图。有关叙述正确的是( )
A.反应前水分子的能量和等于反应后生成的氢分子和氧分子能量之和
B.此实验证明水是由氢气和氧气组成
C.水电解的过程中,氢原子和氧原子数不变
D.电解水的变化只是分子间的间隔发生了变化
3.氯酸钾m克和二氧化锰n克共热后完全分解得到氧气a克,则剩余固体中所含氯化钾的质量为( )
A.(m-n)克 B.(m+n-a)克
C.(m-a)克 D.(m-n-a)克
4.现将足量的A和10gB混合加热,A与B发生化学反应,10gB完全反应后生成4gC和8gBD,则参加反应的A与B的质量比是( )
A.1:1 B.1:5 C.5:1 D.2:1
5.在化学反应前后,一定不发生改变的是( )
A.分子的种类 B.原子的种类 C.分子的质量 D.物质的种类
6.3.6g某物质在足量的氧气中燃烧,生成二氧化碳4.4g,水3.6g则某物质的组成是( )
A.一定有C、H元素,可能有氧元素 B.只含C、H元素
C.一定含有C、H、O三种元素 D.无法确定
7.a克氯酸钾和b克二氧化锰混合加热至完全分解,生成c克固体,则生成氧气( )克
A.a-c B.a+b-c C.2a+b-c D.2a+b-2c
8.下列图象与对应的叙述相符合的是( )
A.图1:化学反应中,原子总数随时间的变化
B.图2:用等质量、等浓度过氧化氢溶液制取氧气
C.图3:加热一定质量的高锰酸钾
D.图4:水通直流电
9.10 g甲与足量的乙反应,生成8g丙和15g丁,则参加反应的乙的质量是( )
A.13g B.23g C.18g D.25g
10.在反应A+B→C+D中,若15gA与10gB完全反应没有剩余,则生成的C和D的质量总和为( )
A.15g B.10g C.25 g D.5g
11.某物质在氧气中燃烧只生成和。下列说法正确的是( )
A.该物质一定是混合物 B.该物质一定含有碳元素和氢元素
C.该物质是由和组成的 D.该物质一定不含氧元素
12.下列说法错误的是( )
A.化学反应前后,物质的种类一定发生改变 B.化学反应前后,分子的种类一定发生改变
C.化学反应前后,原子的数目一定不发生改变 D.化学反应前后,原子团一定发生改变
13.据报道,美国宇航局的专家发明了“月球制氧机”,这种“月球制氧机”利用聚焦太阳能产生的高温使月球土壤发生化学反应制取氧气,据此可推测月球土壤中一定含有( )
A.氧元素 B.氧气 C.水 D.氯酸钾
14.下列叙述完全符合质量守恒定律的是( )
A.水结成冰前后,质量保持不变
B.50mL水和50 mL乙醇混合后总体积小于100 mL
C.在100g30%过氧化氢溶液中,含有30g过氧化氢和70g水
D.1.2g碳与3.2g氧气恰好完全反应可生成4.4g二氧化碳
15.取两份等质量的xCuCO3· yCu(OH)2固体,在一份中加入过量盐酸,生成6.6gCO2;加热另一份使其完全分解,得到20.0gCuO。则下列关系正确的是( )
A.y∶x=1∶1 B.y∶x=1∶3 C.y∶x=3∶2 D.y∶x=2∶3
二、填空题
16.下图是初中化学教材中的一些实验,按要求回答下列问题:
(1)为确保实验一测量结果的准确,需要注意的事项有________(写一条即可)
(2)通过水电解生成氢气和氧气的事实,得出的实验结论是__________。
(3)实验三中反应后天平不平衡,该反应是否遵守质量守恒定律____(填“是”或“否”)
17.化学用语是学习化学的基本工具,请用化学符号填空:
(1)3个亚铁离子_____________。
(2)2个氮分子_____________。
(3)3个硫酸根离子_____________。
(4)氧化铁中铁元素的化合价_____________。
(5)地壳中含量最高的金属元素与非金属元素形成的化合物是_____________。
(6)分析过氧化氢(H2O2)和过氧化钠(Na2O2)中氧元素的化合价,写出过氧化钙的化学式为-_____________。
(7)气体X在氧气中燃烧生成氮气和水,X分子中一定含有的原子是________(填符号)
18.某有机物4.6g在氧气中完全燃烧后,只生成了8.8g二氧化碳和5.4g水,由此推测此有机物由__________元素组成,此有机物的化学式是___________________。
三、实验题
19.在“质量守恒定律”的教学中,都是引导同学们进行“化学反应中,反应物与生成物的质量关系”的实验探究。下图实验装置和选用药品均为教材图示,现分别以A、B、C、D表示如下:
A、B、C、D四个实验分别由甲乙丙丁四个组的同学来完成,他们都进行了规范的操作,准确的称量和细致的观察。
(1)A实验:白磷刚引燃,立即将锥形瓶放在天平上称量,天平不平衡。
结论是:质量不守恒;
等锥形瓶冷却后,重新放到托盘上称量,天平平衡。
结论是:质量守恒。
你认为结论正确的是___________(填“前一种”或“后一种”),而导致另一种结论错误的原因是____________。
(2)丙组同学认为C实验说明了质量守恒。请你从原子的角度给予解释:___________;乙丁两组同学得到的错误结论是“实验B、D均说明质量不守恒”。老师引导同学们分析了B、D两个实验反应前后天平不平衡的原因。你认为B实验天平不平衡的原因是____________。
20.某课外兴趣小组的同学设计了如下三个实验来验证质量守恒定律:
(设计并实验)
实验一:将盛有硫酸铜溶液的烧杯和铁钉一起放在托盘天平上称量,记录所称的质量,然后将铁钉浸到硫酸铜溶液中,观察现象。待反应一段时间后溶液颜色改变时,将盛有反应后物质的烧杯 放在托盘天平上称量,记录所称的质量。
实验二:将盛有稀硫酸的烧杯和碳酸钠一起放在托盘天平上称量,然后将碳酸钠加到稀硫酸中,观察现象 (已知碳酸钠和稀硫酸反应后,会生成大量二氧化碳 )。待反应一段时间后不再放出气泡时,将盛有反应后物质的烧杯放在托盘天平上称量,记录所称的质量。
实验三:用细线系住铜棒中点使之平衡,然后在铜棒一端用酒精灯加热。加热一段时间后,观察 到铜棒的平衡情况是________。
(分析与讨论)
①实验一中,铁和硫酸铜反应,生成硫酸亚铁和一种红色物质,请写出符号表达式______。
②在这三个实验中,你认为:实验_______直接正确反映了反应物与生成物之间的质量关系,由此得出的结论是:在化学反应中生成物的总质量与反应物的总质量相等。
③另外两个实验得出的结论是:在化学反应中生成物的总质量与反应物的总质量不相等,你认为导致这结论错误的原因是______。(只写其中一个实验的原因即可)
(实验反思)
小组成员讨论后达成了以下共识:设计实验验证质量守恒定律时,对于有空气中的气体(成分)参与或有气体生成的化学反应,一般应使反应在______(“开放”或“密闭”)装置中进行。
(拓展与应用)
同学根据质量守恒定律研究物质 W的组成。一定条件下, 在密闭容器内发生反应,反应前后 各物质的质量(单位:g)如图所示:
图中x=______g, 物质W由_____ 种元素组成,其中碳、氢原子个数比为_____(填最简比)。
21.小明用盐酸与碳酸钙粉末反应验证质量守恒定律,实验装置如图。
(1)根据实验目的,小李必须测量的数据是______。
A.锥形瓶质量
B.气球质量
C.反应前整个反应装置(包括里边的物质)质量
D.反应后整个反应装置(包括里边的物质)质量
(2)将反应装置放在天平左盘,使天平平衡后,丙将碳酸钙粉末倒入锥形瓶中、反应结束后,气球鼓起(若不考虑气球膨胀浮力影响),观察到的现象______,从而验证了质量守恒定律,若锥形瓶上方未套气球,则不能验证质量守恒定律,原因是______。
(3)根据化学反应遵循质量守恒定律的本质原因是______。
参考答案
1.B
2.C
3.C
4.B
5.B
6.C
7.A
8.A
9.A
10.C
11.B
12.D
13.A
14.D
15.D
16.
(1)红磷的量要充足,或装置气密性良好,或装置冷却至室温后再打开止水夹
(2)水由氢元素与氧元素组成
(3)是
17.
(1)3Fe2+
(2)2N2
(3)
(4)
(5)Al2O3
(6)CaO2
(7)N、H
18.C H O三种 C2H6O等
19.
(1) 后一种 白磷引燃时燃烧放出大量的热,使装置内气体受热膨胀将气球胀大,装置受到浮力
(2) 化学反应是反应物的原子重新组合,原子的种类、数目、质量不变,生成物的质量也不会改变 反应时产生的二氧化碳气体扩散到空气中,剩余物的质量减少
20.铜棒向有酒精灯加热的一端向下倾斜 一 实验二镁条和稀硫酸反应产生的氢气免逸散到空气中或者实验三有空气中的氧气参加反应 密闭 52 3三 1:3
21.
(1)CD
(2) 天平平衡 有二氧化碳气体逸出
(3)化学反应前后原子种类没有改变、原子数目没有增减、原子质量也没有改变
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
