11-12版高中化学课时讲练通配套课件:1化学家眼中的物质世界(苏教版必修1)
文档属性
| 名称 | 11-12版高中化学课时讲练通配套课件:1化学家眼中的物质世界(苏教版必修1) |
|
|
| 格式 | zip | ||
| 文件大小 | 2.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2012-09-12 00:00:00 | ||
图片预览




文档简介
(共28张PPT)
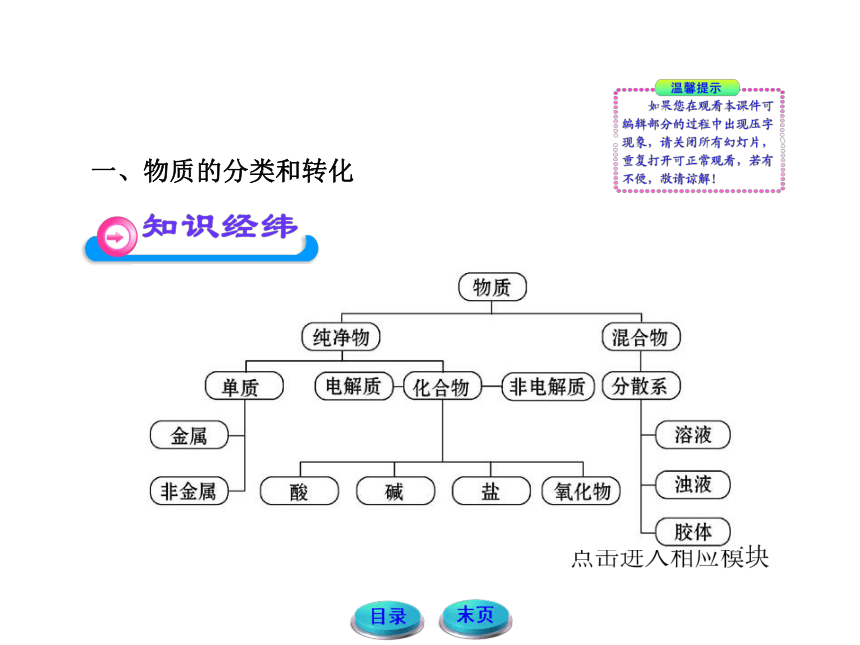
一、物质的分类和转化
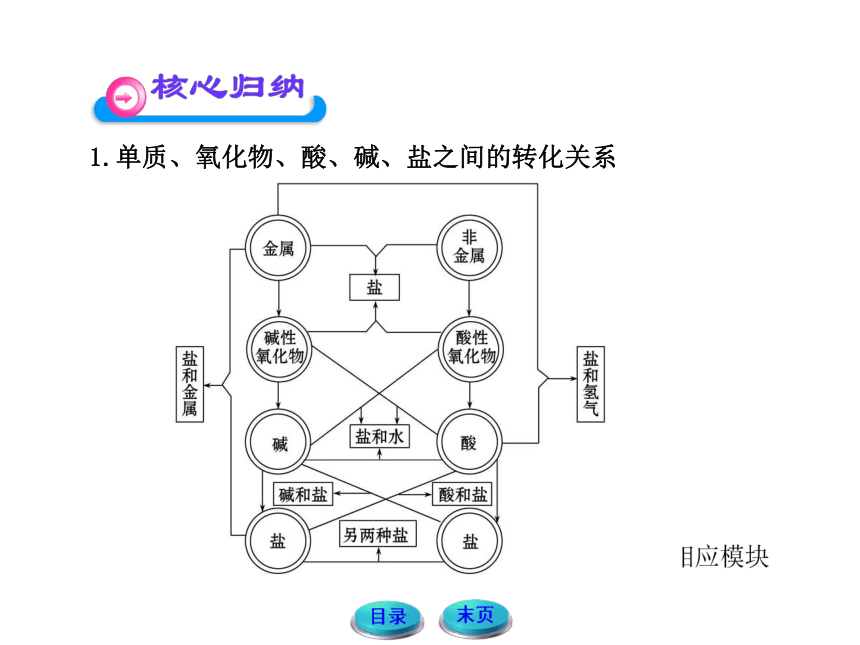
1.单质、氧化物、酸、碱、盐之间的转化关系
2.重要规律
(1)酸性氧化物的一般性质:
①酸性氧化物+水====对应的酸;
②酸性氧化物+碱====盐+水;
③酸性氧化物+碱性氧化物====盐。
(2)碱性氧化物的一般性质:
①碱性氧化物+水====对应的碱;
②碱性氧化物+酸====盐+水;
③碱性氧化物+酸性氧化物====盐。
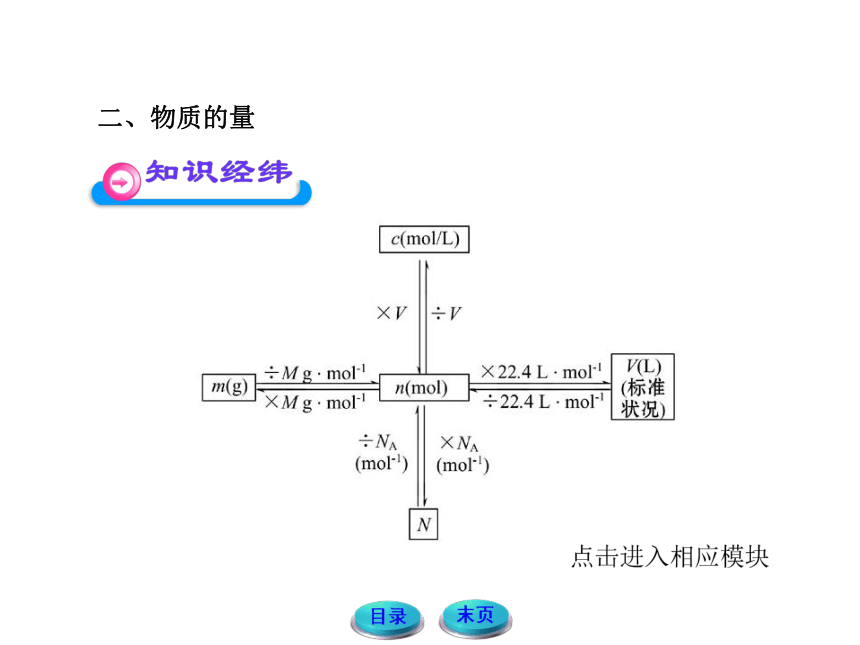
二、物质的量
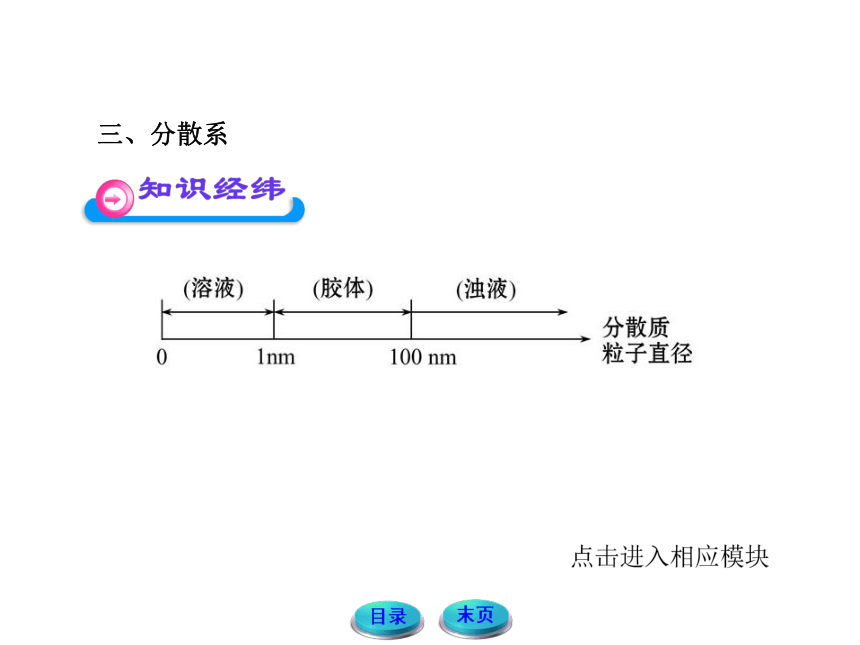
三、分散系
三种分散系的比较
四、物质的分离、提纯和物质检验
1.分离和提纯
2.常见物质的检验
五、溶液的配制
六、原子结构
1.原子的组成微粒及微粒间的关系
(1) 质量关系:质量数(A)=质子数(Z)+中子数(N)
(2) 电性关系
原子:核电荷数=质子数=核外电子数
阴离子:质子数=核外电子数-电荷数
阳离子:质子数=核外电子数+电荷数
Q)世纪金稻
N
山东世纪金榜书业有限公司
世纪金榜
山东世纪金榜书业有限公司
目录)首页,(末页
章首
点击返回目录
温馨提示
●●
如果您在观看本课件可8
编辑部分的过程中出现压
现象,请关闭所有幻灯片
重复打开可正常观看,若有
不便,敬请谅解
课兰教学同课P
东世纪金榜书业有限公司
第三单元
第一单元
第二单元
专题质量评估
专题精要·归纳
)专题精要·归纳
识经纬,
核心归纳
专题1化学家眼的物质世界
(物质
纯净物)
混合物
单质)(电解质)(化合物)(非电解质)(分散系
金属
(溶液
非金属)(酸)(碱)(盐)(氧化物)(浊液
(胶体
金属
非
金属
碱性
酸性
盐和金属
氧化物
氧化物
盐和氢
碱
盐和水
酸
碱和盐
酸和盐
盐
另两种盐
盐
c(mol/L)
V÷V
Mg·mol
×224L·mol4(L
m(g)
n(mo
M
÷22.4L·m
o/)(标准
状况
÷NA×N
(mol-')
mo
1.有关计算公式
即
2.阿伏加德罗定律及其推论
(1)内容:同温、同压、同体积、同分子数
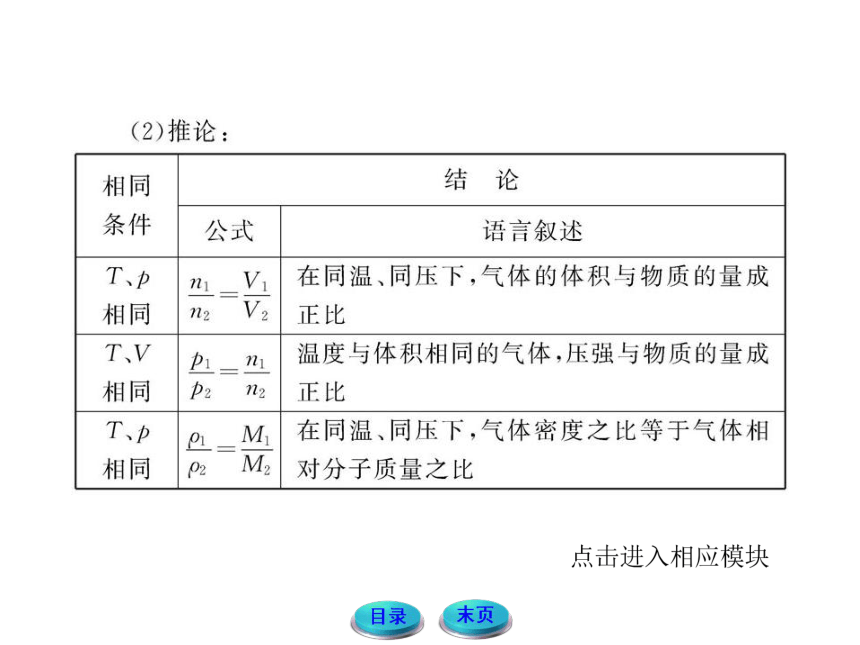
(2)推论
相同
结论
条件公式
语言叙述
T、pn1V1在同温、同压下,气体的体积与物质的量成
相同n2V2|正比
TV|p=m温度与体积相同的气体,压强与物质的量成
相同P2n2正比
T、|p_M1在同温、同压下,气体密度之比等于气体相
相同2M2对分子质量之比
(溶液)
(胶体)
(浊液)
分散质
Inm
100nm
粒子直径
一、物质的分类和转化
1.单质、氧化物、酸、碱、盐之间的转化关系
2.重要规律
(1)酸性氧化物的一般性质:
①酸性氧化物+水====对应的酸;
②酸性氧化物+碱====盐+水;
③酸性氧化物+碱性氧化物====盐。
(2)碱性氧化物的一般性质:
①碱性氧化物+水====对应的碱;
②碱性氧化物+酸====盐+水;
③碱性氧化物+酸性氧化物====盐。
二、物质的量
三、分散系
三种分散系的比较
四、物质的分离、提纯和物质检验
1.分离和提纯
2.常见物质的检验
五、溶液的配制
六、原子结构
1.原子的组成微粒及微粒间的关系
(1) 质量关系:质量数(A)=质子数(Z)+中子数(N)
(2) 电性关系
原子:核电荷数=质子数=核外电子数
阴离子:质子数=核外电子数-电荷数
阳离子:质子数=核外电子数+电荷数
Q)世纪金稻
N
山东世纪金榜书业有限公司
世纪金榜
山东世纪金榜书业有限公司
目录)首页,(末页
章首
点击返回目录
温馨提示
●●
如果您在观看本课件可8
编辑部分的过程中出现压
现象,请关闭所有幻灯片
重复打开可正常观看,若有
不便,敬请谅解
课兰教学同课P
东世纪金榜书业有限公司
第三单元
第一单元
第二单元
专题质量评估
专题精要·归纳
)专题精要·归纳
识经纬,
核心归纳
专题1化学家眼的物质世界
(物质
纯净物)
混合物
单质)(电解质)(化合物)(非电解质)(分散系
金属
(溶液
非金属)(酸)(碱)(盐)(氧化物)(浊液
(胶体
金属
非
金属
碱性
酸性
盐和金属
氧化物
氧化物
盐和氢
碱
盐和水
酸
碱和盐
酸和盐
盐
另两种盐
盐
c(mol/L)
V÷V
Mg·mol
×224L·mol4(L
m(g)
n(mo
M
÷22.4L·m
o/)(标准
状况
÷NA×N
(mol-')
mo
1.有关计算公式
即
2.阿伏加德罗定律及其推论
(1)内容:同温、同压、同体积、同分子数
(2)推论
相同
结论
条件公式
语言叙述
T、pn1V1在同温、同压下,气体的体积与物质的量成
相同n2V2|正比
TV|p=m温度与体积相同的气体,压强与物质的量成
相同P2n2正比
T、|p_M1在同温、同压下,气体密度之比等于气体相
相同2M2对分子质量之比
(溶液)
(胶体)
(浊液)
分散质
Inm
100nm
粒子直径
