11-12版高中化学课时讲练通配套课件:专题质量评估(一)(苏教版必修1)
文档属性
| 名称 | 11-12版高中化学课时讲练通配套课件:专题质量评估(一)(苏教版必修1) |

|
|
| 格式 | zip | ||
| 文件大小 | 317.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2012-09-12 00:00:00 | ||
图片预览











文档简介
(共43张PPT)
(一)
专题1 化学家眼中的物质世界
(90分钟 100分)
一、选择题(本题包括15小题,每小题3分,共45分)
1.“低碳生活,节能减排”越来越被人们认可。下列气体会造成空气污染且属于酸性氧化物的是( )
A.CO2 B.SO2 C.CO D.Na2O
【解析】选B。SO2、CO为污染性气体,CO不是酸性氧化物,Na2O是固体,是碱性氧化物。
2.下列关于化学反应类型的叙述正确的是( )
A.凡是生成盐和水的反应都是中和反应
B.复分解反应一定没有单质参加
C.生成一种单质和一种化合物的反应一定是置换反应
D.分解反应的生成物一定有单质
【解析】选B。A错误,生成盐和水的反应不一定是中和反应,如酸性氧化物与碱反应;C错误,生成一种单质和一种化合物的反应也可以是分解反应,如氯酸钾分解;D错误,分解反应的生成物可能没有单质,如碳酸钙高温分解。
3.(2011·如皋高一检测)下列是某同学对KHSO4的物质类型进行的分析,其中不正确的是( )
A.根据元素组成知它是化合物
B.因它含有钾元素,故KHSO4是钾盐
C.KHSO4可以称为硫酸盐
D.因为它含有与酸相同的元素氢,故KHSO4也可称为酸
【解析】选D。酸是指电离产生的阳离子全部为H+的化合物,KHSO4的电离方程式为KHSO4====K++H++SO42-,故KHSO4不可称为酸。
4.下列实验操作均要用玻璃棒,其中玻璃棒的作用相同的是( )
①过滤 ②蒸发 ③溶解 ④向容量瓶转移溶液
A.①和② B.①和③ C.③和④ D.①和④
【解析】选D。过滤和向容量瓶转移溶液操作时玻璃棒的作用都是引流,D项正确;蒸发和溶解操作时玻璃棒的作用都是搅拌。
5.下列反应属于氧化还原反应的是( )
A.CaCO3+2HCl====CaCl2+H2O+CO2↑
B.2NaHCO3 Na2CO3+H2O+CO2↑
C.Cl2+2NaOH====NaCl+NaClO+H2O
D.NaBr+AgNO3====AgBr↓+NaNO3
【解析】选C。有元素化合价发生变化的反应属于氧化还原反应,C项中氯元素的化合价有两个变化:0→-1、0→+1。
△
====
6.(双选)下列关于胶体和溶液的叙述正确的是( )
A.胶体带电荷,而溶液呈电中性
B.胶体加入电解质可产生沉淀,而溶液不能
C.胶体和溶液都是稳定的分散系
D.胶体能够发生丁达尔效应,而溶液不能
【解析】选C、D。胶体中的胶粒因吸附作用带电荷,胶体呈电中性;溶液中加入适当的电解质溶液也可产生沉淀;胶体是一种介稳性的分散系,而溶液是一种非常稳定的分散系,可以利用丁达尔效应鉴别胶体和溶液。
7.(2011·宿州高一检测)物质的量相同的甲烷(CH4)和氨气(NH3),可能相同的物理量是( )
A.质量 B.体积 C.摩尔质量 D.原子数
【解析】选B。物质的量相同的甲烷(CH4)和氨气(NH3),二者摩尔质量不同,质量不同,A、C错;在相同的温度和压强下,二者的气体摩尔体积相同,体积相同,B正确;二者的分子数相同,但一个分子中所含有的原子数不同,故物质的量相同的甲烷(CH4)和氨气(NH3)的原子总数不同,D错。
8.(2011·邯郸高一检测)在NaCl、MgCl2和MgSO4三种盐制成的混合溶液中,若Na+为0.1 mol· L-1,Mg2+为0.25 mol·L-1,Cl-为0.2 mol· L-1,则SO42-为( )
A.0.2 mol· L-1 B.0.5 mol· L-1
C.0.15 mol · L-1 D.0.25 mol· L-1
【解析】选A。根据溶液中阴阳离子所带电荷数相等可得答案为A。
9.下列表述错误的一项是( )
A.分离醋酸和水的混合物可以用蒸馏法
B.用结晶的方法分离氯化钠和硝酸钾
C.鉴别NaCl和KCl可以用金属的焰色反应来完成
D.可以选用稀盐酸酸化的Ba(NO3)2溶液除去NaCl溶液中混有的少量Na2SO4
【解析】选D。除杂过程中最根本的原则是不能引入新的杂质,除去NaCl中的Na2SO4,用Ba(NO3)2会引入NaNO3杂质,故D项错误。
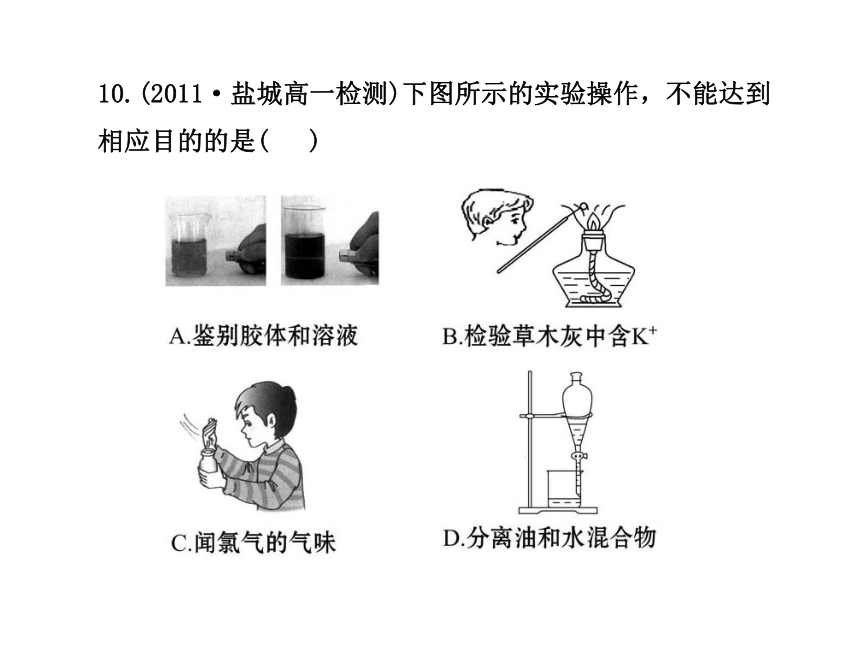
10.(2011·盐城高一检测)下图所示的实验操作,不能达到相应目的的是( )
【解析】选B。利用丁达尔效应可鉴别胶体和溶液,A正确;利用焰色反应鉴别K+时必须透过蓝色钴玻璃,B错;闻气体气味时应用手在集气瓶口轻轻扇动,使极少量气体飘入鼻孔,C正确;分离油和水的混合物应使用分液法,D正确。
11.(2011·合肥高一检测)下列叙述中正确的是( )
A.在标准状况下,1 mol任何物质的体积均约为22.4 L
B.等物质的量浓度的盐酸和硫酸中, H+浓度相同
C.1 mol H2和1 mol He中,所含的分子数相同、原子数相同、质量也相同
D.体积为6 L的O2,其质量可能为8 g
【解析】选D。在标准状况下,1 mol任何气体的体积均约为22.4 L,液体和固体不是,A错;由于HCl====H++Cl-,H2SO4 ==== 2H++ SO42-,等物质的量浓度的盐酸和硫酸,硫酸中的H+浓度是盐酸中的2倍,B错;由于H2和He分子中的原子数不同,摩尔质量不同,故1 mol H2和1 mol He中,所含的分子数相同、原子数不同、质量不同,C错;在一定的温度和压强下,体积为6 L的O2,其物质的量可能为
0.5 mol,其质量可能为8 g,D正确。
12.与铂同族的金属钯(Pd)有多种同位素。下列关于10346Pd、10446Pd的说法正确的是( )
A.质子数相同,互称为同位素
B.中子数相同,化学性质不同
C.核外电子数相同,是同一种核素
D.最外层电子数不同,化学性质不同
【解析】选A。10346Pd和10446Pd是质子数相同,中子数不同的同种元素形成的不同核素,互为同位素。
13.配制100 mL 1 mol·L-1氢氧化钠溶液,下列操作错误的是( )
A.在托盘天平上放两张大小、质量一样的纸,然后将氢氧化钠放在纸上进行称量
B.把称得的氢氧化钠放入盛有适量蒸馏水的烧杯中,溶解、冷却,再把溶液转移到容量瓶中
C.用蒸馏水洗涤烧杯、玻璃棒2~3次,洗涤液也转移到容量瓶中
D.沿着玻璃棒往容量瓶中加入蒸馏水,到离刻度线1~2 cm 时改用胶头滴管滴加,直到溶液凹液面最低处恰好与刻度线相切
【解析】选A。氢氧化钠等极易潮解的药品应该放在小烧杯中称量,不能放在纸片上称量。
14.下列示意图中,白球代表氢原子,黑球代表氦原子,方框代表容器,容器中间有一个可以上下滑动的隔板(其质量忽略不计)。其中能表示等质量的氢气与氦气的是( )
【解析】选A。等质量的He与H2的物质的量之比为1∶2,则H2的体积是He的2倍,H2的分子个数是He的2倍,且氢气为双原子分子,而He为单原子分子。
15.检验某未知溶液中是否含有SO42- ,正确的方法是( )
A.加盐酸酸化的氯化钡溶液
B.先加氯化钡溶液,再加稀盐酸
C.加氯化钡溶液或硝酸钡溶液
D.先加足量盐酸酸化,再加氯化钡溶液
【解析】选D。检验SO42-,Ag+、CO32-、SO32-等可能会造成干扰。A中和B中若有白色沉淀生成,可能为BaSO4也可能为AgCl,不能证明含SO42-。C中若生成白色沉淀可能为BaSO4,也可能为BaSO3或AgCl,也不能证明含SO42-。先加足量盐酸酸化可以将Ag+、CO32-、SO32-等离子的干扰排除,产生的白色沉淀是BaSO4,可以证明含SO42-。
二、非选择题(本题包括6小题,共55分)
16.(6分)在标准状况下,A气体的密度为0.09 g/L,B气体的密度为1.43 g/L,A的相对分子质量为_____,B的相对分子质量为_____。由此可知,相同条件下气体的密度之比等于_____。
【解析】MA=0.09 g/L×22.4 L/mol=2 g/mol,MB=1.43 g/L
×22.4 L/mol=32 g/mol,由上述计算可知相同条件下气体的密度之比等于其摩尔质量之比。
答案:2 32 气体的摩尔质量之比
17.(9分)为除去Na2SO4溶液中含有的杂质Na2CO3,甲、乙、丙三位同学分别选用一种试剂(适量)进行实验。请你对他们所选用的试剂进行评价:
【解析】本题是一道有关混合物分离和提纯的实验原理的评价试题。可以从以下几方面进行判断:①引入的试剂一般只与杂质反应,且不引入新的杂质;②步骤及操作简单;③污染最小或不污染环境等。
答案:
甲:不可行,除去Na2CO3的同时又引入了新杂质NaCl
乙:可行,除去Na2CO3的同时增加了Na2SO4,而且没引入新杂质
丙:不可行,除去Na2CO3的同时也除去了Na2SO4,并引入了新杂质NaOH
18.(12分)(1)0.3 mol NH3分子中所含氢原子数与_____个H2O分子中所含氢原子数相等。
(2)含0.4 mol Al3+的Al2(SO4)3中所含的SO42-的物质的量是_____。
(3)已知16 g A和20 g B恰好完全反应生成0.04 mol C和31.76 g D,则C的摩尔质量为_____。
(4)2.3 g Na中含电子的物质的量为_____mol,在跟足量水反应后失去电子的物质的量为_____mol。
(5)如果a g某气体中含有的分子数为b,则c g该气体在标准状况下的体积是(设NA为阿伏加德罗常数)_____。
【解析】(1)0.3 mol NH3分子含氢原子0.9 mol,与0.45 mol H2O分子所含氢原子数相同,H2O分子个数为0.45×6.02
×1023=2.709×1023。
(2)含0.4 mol Al3+的Al2(SO4)3的物质的量为0.2 mol,含SO42- 0.6 mol。
(3)0.04 mol C的质量为16 g+20 g-31.76 g=4.24 g,故C的摩尔质量为
(4)2.3 g Na的物质的量为0.1 mol,含1.1 mol e-,与足量水反应失去0.1 mol e-。
(5)a g气体所占的体积为 ×22.4 L,该气体摩尔质量为
g/mol,则c g该气体所占的体积为
答案:(1)2.709×1023 (2)0.6 mol
(3)106 g/mol (4)1.1 0.1 (5)
19.(8分)(2011·金华高一检测)西汉刘安著《淮南万毕术》中记载“曾青得铁则化为铜”。“曾青”可能是硫酸铜一类的物质,将孔雀石[化学式为Cu2(OH)2CO3]溶于硫酸中得此溶液,把铁粉投入此溶液中即可得铜。
(1)下列关于“曾青”和孔雀石的水溶性分析,判断正确的是_____。
A.前者可溶,后者难溶
B.前者难溶,后者可溶
C.两者均可溶
D.两者均难溶
(2)以孔雀石为原料的冶炼过程中,用现代化学的观念审视,可能涉及的化学反应有_____。
①Cu2 (OH)2 CO3 2CuO+CO2↑+H2O
②2CuO+C 2Cu+CO2↑
③CuO+CO Cu+CO2
④CO2+C 2CO
A.①② B.①③
C.①②③ D.①②③④
高温
====
高温
====
高温
====
△
====
(3)在(2)的四个反应中,不属于四种基本反应类型的有 (填序号,下同) _____,不属于氧化还原反应的有_____。
(4)资料中,假设溶解孔雀石的酸是稀硫酸,写出用“曾青得铁则化为铜”的方法冶炼铜的化学方程式___________
_____________________________________________。
【解析】(1)CuSO4易溶于水,孔雀石能以矿石的形式存在于自然界,应该是难溶于水。
(2)高温下冶炼铜,碳是足量的,则上述四个反应均可发生。
(3)①反应中没有元素的化合价变化,不属于氧化还原反应;③反应不属于四种基本反应类型的任何一种,但属于氧化还原反应。
答案:(1)A (2)D (3)③ ①
(4)Cu2(OH)2CO3+2H2SO4====2CuSO4+CO2↑+3H2O,
Fe+CuSO4====FeSO4+Cu
20.(9分)观察下列A、B、C、D、E五种粒子(原子或离子)的结构示意图,回答有关问题。
(1)与离子相对应的元素的符号是_____,与原子相对应的离子的结构示意图是_____。
(2)电子层结构相同的是 (填写代号,下同) _____,性质最稳定的是_____,最容易失去电子的是_____,最容易得到电子的是_____。
(3)可直接相互结合形成化合物的化学式是_____,可经过得失电子后再相互结合形成化合物的化学式是________。
(4)在核电荷数1~10的元素内,列举两个与B电子层结构相同的离子,写出离子的符号_____________________。
【解析】(1)在A~E这五种粒子中,A是Cl,B是O2-,C是Ne,D是Na,E是Mg2+。Ne的特殊稳定性决定了它不能形成离子。
(2)电子层结构相同,即电子层数和各个电子层上的电子数目都相同,但与原子核无关。O2-、Ne和Mg2+都具有稳定的电子层结构,但最稳定的是Ne。
(3)阳离子与阴离子可直接相互结合形成化合物;活泼金属元素的原子与活泼非金属元素的原子经过得失电子后可相互结合形成化合物;在化合物中,Na显+1价、Mg显+2价、Cl显-1价、O显-2价。
(4)在核电荷数1~10的元素内,N原子的核外共有7个电子,其中最外层上有5个,N原子得到3个电子后形成的N3-与B的电子层结构相同;F原子的核外共有9个电子,其中最外层上有7个,F原子得到1个电子后形成的F-与B的电子层结构相同。
答案:(1)O、Mg
(2)B、C、E C D A
(3)MgO NaCl (4)N3-、F-
21.(11分)(2011·泰安高一检测)实验室需配制0.10 mol·L-1 NaCl溶液250 mL。
(一)容量瓶上需要标有_____。
①温度 ②浓度 ③容量 ④压强 ⑤刻度线
⑥酸(碱)式
(二)按下列操作步骤填上适当的文字,以使整个操作完整。
第一步:选择仪器。完成本实验所必需的仪器有:
天平(精确到0.1 g)、药匙____、____、____、____以及等质量的两片纸。
第二步:计算。配制该溶液需取NaCl晶体____ g。
第三步:称量。
①天平调平之后,应将天平的游码调至某个位置,请在下图中用一根竖线标出游码左边缘所处的位置:
②称量过程中NaCl晶体应放于天平的_____(填“左盘”或“右盘”)。
③称量完毕,将药品倒入_____中。
第四步:_______。该步实验中还需进行的操作是:
_____________________________________________。
第五步:转移、洗涤。
第六步:_____________________________________。
第七步:_____________________________________。
第八步:将配好的溶液静置一段时间后,倒入指定的试剂瓶,并贴好标签,注明配制的时间、名称及浓度。
(三)定容摇匀后,某同学发现液面略低于刻度线,又用蒸馏水添加至刻度线。该操作是否会对所配制的溶液浓度造成影响?为什么?_________________________________
_______________________________________________。
【解析】(一)考查容量瓶的相关知识。
(二)n(NaCl)=0.25 L×0.10 mol·L-1=0.025 mol
m(NaCl)=0.025 mol×58.5 g·mol-1≈1.5 g。
(三)定容摇匀后部分溶液遗留在容量瓶壁上,致使液面低于刻度线,此时不应再加入蒸馏水,否则溶液体积增大,溶液浓度变低。
答案:(一)①③⑤
(二)第一步:烧杯 玻璃棒 250 mL容量瓶 胶头滴管
第二步:1.5
第三步:①
②左盘 ③烧杯
第四步:溶解 用玻璃棒搅拌
第六步:定容
第七步:摇匀
(三)使所配制溶液浓度偏低。若再加水,会使溶液体积偏大,故溶液浓度偏低
【规律方法】一定物质的量浓度溶液的配制实验通常考查形式
(1)计算。计算出所需固体的质量或所需溶液的体积。
(2)步骤。对零乱的实验步骤或错误的操作步骤作出分析,给出正确的步骤或改正错误实验步骤。
(3)仪器。最常见的考查形式为给出一部分仪器,先删去无用或不需要的仪器,再补上缺少的仪器,通常易缺仪器有3个:容量瓶、玻璃棒、胶头滴管。
(4)误差分析。准确把握c= 的含义,据此分析给出的操作对n、V的影响,从而做出判断。
(一)
专题1 化学家眼中的物质世界
(90分钟 100分)
一、选择题(本题包括15小题,每小题3分,共45分)
1.“低碳生活,节能减排”越来越被人们认可。下列气体会造成空气污染且属于酸性氧化物的是( )
A.CO2 B.SO2 C.CO D.Na2O
【解析】选B。SO2、CO为污染性气体,CO不是酸性氧化物,Na2O是固体,是碱性氧化物。
2.下列关于化学反应类型的叙述正确的是( )
A.凡是生成盐和水的反应都是中和反应
B.复分解反应一定没有单质参加
C.生成一种单质和一种化合物的反应一定是置换反应
D.分解反应的生成物一定有单质
【解析】选B。A错误,生成盐和水的反应不一定是中和反应,如酸性氧化物与碱反应;C错误,生成一种单质和一种化合物的反应也可以是分解反应,如氯酸钾分解;D错误,分解反应的生成物可能没有单质,如碳酸钙高温分解。
3.(2011·如皋高一检测)下列是某同学对KHSO4的物质类型进行的分析,其中不正确的是( )
A.根据元素组成知它是化合物
B.因它含有钾元素,故KHSO4是钾盐
C.KHSO4可以称为硫酸盐
D.因为它含有与酸相同的元素氢,故KHSO4也可称为酸
【解析】选D。酸是指电离产生的阳离子全部为H+的化合物,KHSO4的电离方程式为KHSO4====K++H++SO42-,故KHSO4不可称为酸。
4.下列实验操作均要用玻璃棒,其中玻璃棒的作用相同的是( )
①过滤 ②蒸发 ③溶解 ④向容量瓶转移溶液
A.①和② B.①和③ C.③和④ D.①和④
【解析】选D。过滤和向容量瓶转移溶液操作时玻璃棒的作用都是引流,D项正确;蒸发和溶解操作时玻璃棒的作用都是搅拌。
5.下列反应属于氧化还原反应的是( )
A.CaCO3+2HCl====CaCl2+H2O+CO2↑
B.2NaHCO3 Na2CO3+H2O+CO2↑
C.Cl2+2NaOH====NaCl+NaClO+H2O
D.NaBr+AgNO3====AgBr↓+NaNO3
【解析】选C。有元素化合价发生变化的反应属于氧化还原反应,C项中氯元素的化合价有两个变化:0→-1、0→+1。
△
====
6.(双选)下列关于胶体和溶液的叙述正确的是( )
A.胶体带电荷,而溶液呈电中性
B.胶体加入电解质可产生沉淀,而溶液不能
C.胶体和溶液都是稳定的分散系
D.胶体能够发生丁达尔效应,而溶液不能
【解析】选C、D。胶体中的胶粒因吸附作用带电荷,胶体呈电中性;溶液中加入适当的电解质溶液也可产生沉淀;胶体是一种介稳性的分散系,而溶液是一种非常稳定的分散系,可以利用丁达尔效应鉴别胶体和溶液。
7.(2011·宿州高一检测)物质的量相同的甲烷(CH4)和氨气(NH3),可能相同的物理量是( )
A.质量 B.体积 C.摩尔质量 D.原子数
【解析】选B。物质的量相同的甲烷(CH4)和氨气(NH3),二者摩尔质量不同,质量不同,A、C错;在相同的温度和压强下,二者的气体摩尔体积相同,体积相同,B正确;二者的分子数相同,但一个分子中所含有的原子数不同,故物质的量相同的甲烷(CH4)和氨气(NH3)的原子总数不同,D错。
8.(2011·邯郸高一检测)在NaCl、MgCl2和MgSO4三种盐制成的混合溶液中,若Na+为0.1 mol· L-1,Mg2+为0.25 mol·L-1,Cl-为0.2 mol· L-1,则SO42-为( )
A.0.2 mol· L-1 B.0.5 mol· L-1
C.0.15 mol · L-1 D.0.25 mol· L-1
【解析】选A。根据溶液中阴阳离子所带电荷数相等可得答案为A。
9.下列表述错误的一项是( )
A.分离醋酸和水的混合物可以用蒸馏法
B.用结晶的方法分离氯化钠和硝酸钾
C.鉴别NaCl和KCl可以用金属的焰色反应来完成
D.可以选用稀盐酸酸化的Ba(NO3)2溶液除去NaCl溶液中混有的少量Na2SO4
【解析】选D。除杂过程中最根本的原则是不能引入新的杂质,除去NaCl中的Na2SO4,用Ba(NO3)2会引入NaNO3杂质,故D项错误。
10.(2011·盐城高一检测)下图所示的实验操作,不能达到相应目的的是( )
【解析】选B。利用丁达尔效应可鉴别胶体和溶液,A正确;利用焰色反应鉴别K+时必须透过蓝色钴玻璃,B错;闻气体气味时应用手在集气瓶口轻轻扇动,使极少量气体飘入鼻孔,C正确;分离油和水的混合物应使用分液法,D正确。
11.(2011·合肥高一检测)下列叙述中正确的是( )
A.在标准状况下,1 mol任何物质的体积均约为22.4 L
B.等物质的量浓度的盐酸和硫酸中, H+浓度相同
C.1 mol H2和1 mol He中,所含的分子数相同、原子数相同、质量也相同
D.体积为6 L的O2,其质量可能为8 g
【解析】选D。在标准状况下,1 mol任何气体的体积均约为22.4 L,液体和固体不是,A错;由于HCl====H++Cl-,H2SO4 ==== 2H++ SO42-,等物质的量浓度的盐酸和硫酸,硫酸中的H+浓度是盐酸中的2倍,B错;由于H2和He分子中的原子数不同,摩尔质量不同,故1 mol H2和1 mol He中,所含的分子数相同、原子数不同、质量不同,C错;在一定的温度和压强下,体积为6 L的O2,其物质的量可能为
0.5 mol,其质量可能为8 g,D正确。
12.与铂同族的金属钯(Pd)有多种同位素。下列关于10346Pd、10446Pd的说法正确的是( )
A.质子数相同,互称为同位素
B.中子数相同,化学性质不同
C.核外电子数相同,是同一种核素
D.最外层电子数不同,化学性质不同
【解析】选A。10346Pd和10446Pd是质子数相同,中子数不同的同种元素形成的不同核素,互为同位素。
13.配制100 mL 1 mol·L-1氢氧化钠溶液,下列操作错误的是( )
A.在托盘天平上放两张大小、质量一样的纸,然后将氢氧化钠放在纸上进行称量
B.把称得的氢氧化钠放入盛有适量蒸馏水的烧杯中,溶解、冷却,再把溶液转移到容量瓶中
C.用蒸馏水洗涤烧杯、玻璃棒2~3次,洗涤液也转移到容量瓶中
D.沿着玻璃棒往容量瓶中加入蒸馏水,到离刻度线1~2 cm 时改用胶头滴管滴加,直到溶液凹液面最低处恰好与刻度线相切
【解析】选A。氢氧化钠等极易潮解的药品应该放在小烧杯中称量,不能放在纸片上称量。
14.下列示意图中,白球代表氢原子,黑球代表氦原子,方框代表容器,容器中间有一个可以上下滑动的隔板(其质量忽略不计)。其中能表示等质量的氢气与氦气的是( )
【解析】选A。等质量的He与H2的物质的量之比为1∶2,则H2的体积是He的2倍,H2的分子个数是He的2倍,且氢气为双原子分子,而He为单原子分子。
15.检验某未知溶液中是否含有SO42- ,正确的方法是( )
A.加盐酸酸化的氯化钡溶液
B.先加氯化钡溶液,再加稀盐酸
C.加氯化钡溶液或硝酸钡溶液
D.先加足量盐酸酸化,再加氯化钡溶液
【解析】选D。检验SO42-,Ag+、CO32-、SO32-等可能会造成干扰。A中和B中若有白色沉淀生成,可能为BaSO4也可能为AgCl,不能证明含SO42-。C中若生成白色沉淀可能为BaSO4,也可能为BaSO3或AgCl,也不能证明含SO42-。先加足量盐酸酸化可以将Ag+、CO32-、SO32-等离子的干扰排除,产生的白色沉淀是BaSO4,可以证明含SO42-。
二、非选择题(本题包括6小题,共55分)
16.(6分)在标准状况下,A气体的密度为0.09 g/L,B气体的密度为1.43 g/L,A的相对分子质量为_____,B的相对分子质量为_____。由此可知,相同条件下气体的密度之比等于_____。
【解析】MA=0.09 g/L×22.4 L/mol=2 g/mol,MB=1.43 g/L
×22.4 L/mol=32 g/mol,由上述计算可知相同条件下气体的密度之比等于其摩尔质量之比。
答案:2 32 气体的摩尔质量之比
17.(9分)为除去Na2SO4溶液中含有的杂质Na2CO3,甲、乙、丙三位同学分别选用一种试剂(适量)进行实验。请你对他们所选用的试剂进行评价:
【解析】本题是一道有关混合物分离和提纯的实验原理的评价试题。可以从以下几方面进行判断:①引入的试剂一般只与杂质反应,且不引入新的杂质;②步骤及操作简单;③污染最小或不污染环境等。
答案:
甲:不可行,除去Na2CO3的同时又引入了新杂质NaCl
乙:可行,除去Na2CO3的同时增加了Na2SO4,而且没引入新杂质
丙:不可行,除去Na2CO3的同时也除去了Na2SO4,并引入了新杂质NaOH
18.(12分)(1)0.3 mol NH3分子中所含氢原子数与_____个H2O分子中所含氢原子数相等。
(2)含0.4 mol Al3+的Al2(SO4)3中所含的SO42-的物质的量是_____。
(3)已知16 g A和20 g B恰好完全反应生成0.04 mol C和31.76 g D,则C的摩尔质量为_____。
(4)2.3 g Na中含电子的物质的量为_____mol,在跟足量水反应后失去电子的物质的量为_____mol。
(5)如果a g某气体中含有的分子数为b,则c g该气体在标准状况下的体积是(设NA为阿伏加德罗常数)_____。
【解析】(1)0.3 mol NH3分子含氢原子0.9 mol,与0.45 mol H2O分子所含氢原子数相同,H2O分子个数为0.45×6.02
×1023=2.709×1023。
(2)含0.4 mol Al3+的Al2(SO4)3的物质的量为0.2 mol,含SO42- 0.6 mol。
(3)0.04 mol C的质量为16 g+20 g-31.76 g=4.24 g,故C的摩尔质量为
(4)2.3 g Na的物质的量为0.1 mol,含1.1 mol e-,与足量水反应失去0.1 mol e-。
(5)a g气体所占的体积为 ×22.4 L,该气体摩尔质量为
g/mol,则c g该气体所占的体积为
答案:(1)2.709×1023 (2)0.6 mol
(3)106 g/mol (4)1.1 0.1 (5)
19.(8分)(2011·金华高一检测)西汉刘安著《淮南万毕术》中记载“曾青得铁则化为铜”。“曾青”可能是硫酸铜一类的物质,将孔雀石[化学式为Cu2(OH)2CO3]溶于硫酸中得此溶液,把铁粉投入此溶液中即可得铜。
(1)下列关于“曾青”和孔雀石的水溶性分析,判断正确的是_____。
A.前者可溶,后者难溶
B.前者难溶,后者可溶
C.两者均可溶
D.两者均难溶
(2)以孔雀石为原料的冶炼过程中,用现代化学的观念审视,可能涉及的化学反应有_____。
①Cu2 (OH)2 CO3 2CuO+CO2↑+H2O
②2CuO+C 2Cu+CO2↑
③CuO+CO Cu+CO2
④CO2+C 2CO
A.①② B.①③
C.①②③ D.①②③④
高温
====
高温
====
高温
====
△
====
(3)在(2)的四个反应中,不属于四种基本反应类型的有 (填序号,下同) _____,不属于氧化还原反应的有_____。
(4)资料中,假设溶解孔雀石的酸是稀硫酸,写出用“曾青得铁则化为铜”的方法冶炼铜的化学方程式___________
_____________________________________________。
【解析】(1)CuSO4易溶于水,孔雀石能以矿石的形式存在于自然界,应该是难溶于水。
(2)高温下冶炼铜,碳是足量的,则上述四个反应均可发生。
(3)①反应中没有元素的化合价变化,不属于氧化还原反应;③反应不属于四种基本反应类型的任何一种,但属于氧化还原反应。
答案:(1)A (2)D (3)③ ①
(4)Cu2(OH)2CO3+2H2SO4====2CuSO4+CO2↑+3H2O,
Fe+CuSO4====FeSO4+Cu
20.(9分)观察下列A、B、C、D、E五种粒子(原子或离子)的结构示意图,回答有关问题。
(1)与离子相对应的元素的符号是_____,与原子相对应的离子的结构示意图是_____。
(2)电子层结构相同的是 (填写代号,下同) _____,性质最稳定的是_____,最容易失去电子的是_____,最容易得到电子的是_____。
(3)可直接相互结合形成化合物的化学式是_____,可经过得失电子后再相互结合形成化合物的化学式是________。
(4)在核电荷数1~10的元素内,列举两个与B电子层结构相同的离子,写出离子的符号_____________________。
【解析】(1)在A~E这五种粒子中,A是Cl,B是O2-,C是Ne,D是Na,E是Mg2+。Ne的特殊稳定性决定了它不能形成离子。
(2)电子层结构相同,即电子层数和各个电子层上的电子数目都相同,但与原子核无关。O2-、Ne和Mg2+都具有稳定的电子层结构,但最稳定的是Ne。
(3)阳离子与阴离子可直接相互结合形成化合物;活泼金属元素的原子与活泼非金属元素的原子经过得失电子后可相互结合形成化合物;在化合物中,Na显+1价、Mg显+2价、Cl显-1价、O显-2价。
(4)在核电荷数1~10的元素内,N原子的核外共有7个电子,其中最外层上有5个,N原子得到3个电子后形成的N3-与B的电子层结构相同;F原子的核外共有9个电子,其中最外层上有7个,F原子得到1个电子后形成的F-与B的电子层结构相同。
答案:(1)O、Mg
(2)B、C、E C D A
(3)MgO NaCl (4)N3-、F-
21.(11分)(2011·泰安高一检测)实验室需配制0.10 mol·L-1 NaCl溶液250 mL。
(一)容量瓶上需要标有_____。
①温度 ②浓度 ③容量 ④压强 ⑤刻度线
⑥酸(碱)式
(二)按下列操作步骤填上适当的文字,以使整个操作完整。
第一步:选择仪器。完成本实验所必需的仪器有:
天平(精确到0.1 g)、药匙____、____、____、____以及等质量的两片纸。
第二步:计算。配制该溶液需取NaCl晶体____ g。
第三步:称量。
①天平调平之后,应将天平的游码调至某个位置,请在下图中用一根竖线标出游码左边缘所处的位置:
②称量过程中NaCl晶体应放于天平的_____(填“左盘”或“右盘”)。
③称量完毕,将药品倒入_____中。
第四步:_______。该步实验中还需进行的操作是:
_____________________________________________。
第五步:转移、洗涤。
第六步:_____________________________________。
第七步:_____________________________________。
第八步:将配好的溶液静置一段时间后,倒入指定的试剂瓶,并贴好标签,注明配制的时间、名称及浓度。
(三)定容摇匀后,某同学发现液面略低于刻度线,又用蒸馏水添加至刻度线。该操作是否会对所配制的溶液浓度造成影响?为什么?_________________________________
_______________________________________________。
【解析】(一)考查容量瓶的相关知识。
(二)n(NaCl)=0.25 L×0.10 mol·L-1=0.025 mol
m(NaCl)=0.025 mol×58.5 g·mol-1≈1.5 g。
(三)定容摇匀后部分溶液遗留在容量瓶壁上,致使液面低于刻度线,此时不应再加入蒸馏水,否则溶液体积增大,溶液浓度变低。
答案:(一)①③⑤
(二)第一步:烧杯 玻璃棒 250 mL容量瓶 胶头滴管
第二步:1.5
第三步:①
②左盘 ③烧杯
第四步:溶解 用玻璃棒搅拌
第六步:定容
第七步:摇匀
(三)使所配制溶液浓度偏低。若再加水,会使溶液体积偏大,故溶液浓度偏低
【规律方法】一定物质的量浓度溶液的配制实验通常考查形式
(1)计算。计算出所需固体的质量或所需溶液的体积。
(2)步骤。对零乱的实验步骤或错误的操作步骤作出分析,给出正确的步骤或改正错误实验步骤。
(3)仪器。最常见的考查形式为给出一部分仪器,先删去无用或不需要的仪器,再补上缺少的仪器,通常易缺仪器有3个:容量瓶、玻璃棒、胶头滴管。
(4)误差分析。准确把握c= 的含义,据此分析给出的操作对n、V的影响,从而做出判断。
