鲁教版(五四制)化学九年级全一册 2.4 酸碱中和反应 课件(共19张PPT)
文档属性
| 名称 | 鲁教版(五四制)化学九年级全一册 2.4 酸碱中和反应 课件(共19张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-06 00:00:00 | ||
图片预览





文档简介
(共19张PPT)
第四节 酸碱中和反应
酸碱的中和反应
教学目标
1.实验探究“酸和碱能否发生化学反应”
2.寻找酸和碱反应的规律,正确书写相关化学方程式
3.认识中和反应的实质。学会利用中和反应来改变溶液的酸碱性
实验探究
盐酸(HCl)和氢氧化钠(NaOH)溶液能否发生化学反应?
猜想与假设
可能反应?
HCl + NaOH =
可能不反应?
设计实验
用胶头滴管向盛有约2ml,溶质质量分数为0.4%的氢氧化钠溶液的试管中滴加0.4%的盐酸,观察现象.
无明显现象
收集证据:
1,用PH试纸分别测定水.氢氧化钠溶液和稀盐酸的PH。
2,分别量取2ml水和2ml的氢氧化钠溶液于试管中,然后分别滴入2ml稀盐酸,充分震荡后,测定所得溶液的PH。
水 氢氧化钠溶液 稀盐酸
加酸前的PH
加酸后的PH
解释与结论:
你认为氢氧化钠溶液中加入稀盐酸后,溶液的PH变化原因是什么?能否说明酸和碱之间了化学反应?
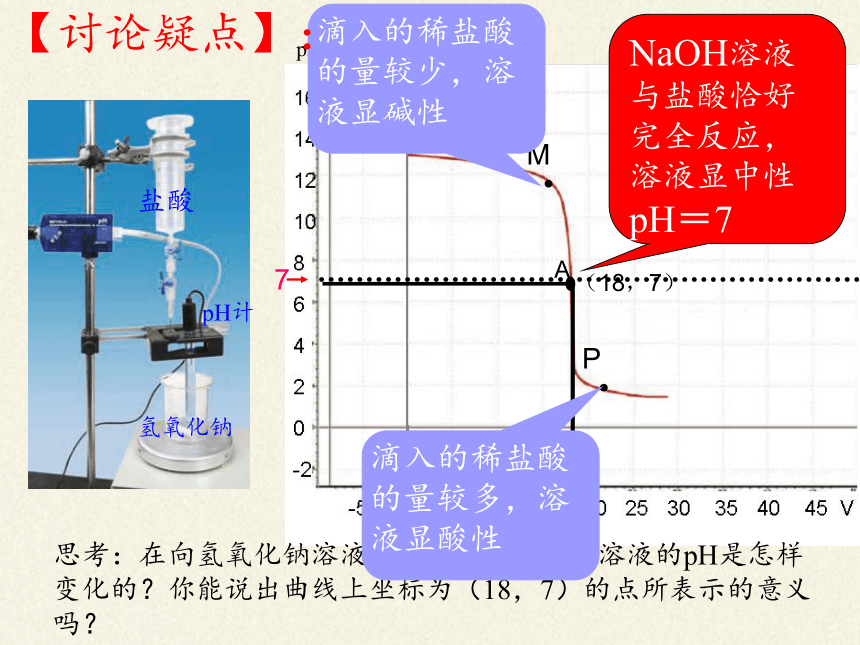
思考:在向氢氧化钠溶液中滴加稀盐酸时,溶液的pH是怎样变化的?你能说出曲线上坐标为(18,7)的点所表示的意义吗?
pH
(18,7)
A
M
P
NaOH溶液与盐酸恰好完全反应,溶液显中性pH=7
氢氧化钠
盐酸
pH计
7
滴入的稀盐酸的量较少,溶液显碱性
【讨论疑点】:
滴入的稀盐酸的量较多,溶液显酸性
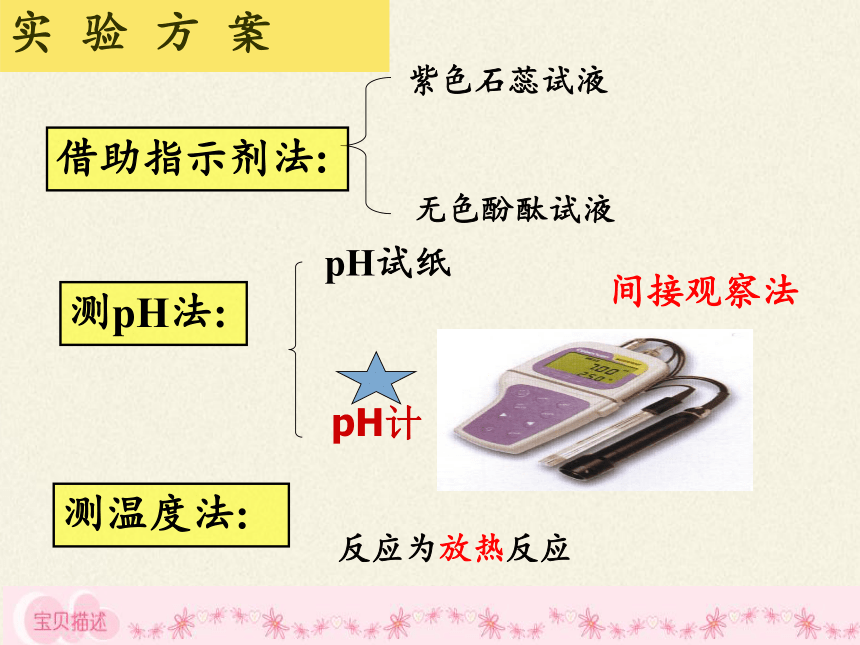
测pH法:
借助指示剂法;测PH法
测温度法:
pH试纸
pH计
紫色石蕊试液
无色酚酞试液
实 验 方 案
间接观察法
借助指示剂法:
反应为放热反应
合作探究:氢氧化钠和盐酸会发生什么?
NaOH溶液
滴入( )溶液
溶液为( )色
再滴入( )溶液
溶液为( )色
无色酚酞
红
盐酸
无
NaOH溶液
滴入(紫色石蕊) 溶液
溶液为( )色
再滴入( HCl )溶液
溶液为( )色
合作探究:
对比:以上两种方案,哪一种更好些?
并分析原因?
蓝
无
上述实验中:盐酸和氢氧化钠溶液混合后,溶液的PH发生了明显的变化,显然不是由于溶液混合后相互____________造成的,而是溶液中的______和_____结合成了_____,导致溶液原有的酸碱性相互“中和”的结果。
NaOH+HCI=NaCI+H2O
中和反应的实质:H+ + OH- =H2O
反应实质
Na+ 和Cl- 不变而H+和OH_消失
思考:
氢氧化钠和盐酸的反应有
什么特点?
NaOH + HCl = NaCl + H2O
碱
酸
水
盐
中和反应:
归纳总结:
酸和碱作用生成盐和水的反应。
酸 + 碱 → 盐 + 水
写出下列反应的化学方程式,有何共同特点?
1、胃酸(HCl)过多,口服碱性药物(例:Mg(OH)2)
2、向酸性土壤(H2SO4)中撒熟石灰(Ca(OH)2)
3、向酸性废水(HCl)中加熟石灰(Ca(OH)2)
胃酸(HCl)过多,口服碱性药物(例:Al(OH)3)
寻找规律
中和反应的应用
你认为判断一个反应是不是中和反应的关键是什么?
讨论
反应物必须是酸与碱,
生成物必须是盐和水
注意:有盐和水生成的反应一定是中和反应吗?
1.在滴有石蕊的稀盐酸中,加入足量NaOH溶液,加酸前后溶液颜色依次为 ( )
A.红色、紫色 、蓝色 B.紫色、红色、蓝色
C.红色、蓝色、紫色 D.蓝色、紫色、红色
2.在实验室里,欲使碱性溶液变成中性,下列试剂中最好选用哪一种组合 ( )
① NaOH溶液②稀盐酸 ③石灰水 ④酚酞试液
A. ①或③ B. 只有②
C. 只有① D. ②和④
A
D
达标检测
3、下列各组物质间的反应,由于现象不明显
需要借助酸碱指示剂才能判断出反应发生的
是( )
A、 镁和稀盐酸
B 、烧碱溶液和稀硫酸
C、氧化铁和稀硫酸
D、澄清石灰水中通入二氧化碳
归纳总结:
1.中和反应:___________________
2.实质:如图体现了稀盐酸和氢氧化钠溶液反应的实质:
3.现象:做酸碱中和实验时,取一支试管,倒入10 mL氢氧化钠稀溶液,再滴入1—2滴酚酞试液,溶液呈红色。然后用___________逐渐滴入稀盐酸,同时不停地___________,直至溶液恰好变成___________色为止。
4.图形分析.
. 小松同学在进行酸碱中和反应的实验时,向烧杯中的氢氧化钠溶液中滴加稀盐酸一会儿后,发现忘记了滴加指示剂。为了确定盐酸与氢氧化钠是否恰好完全反应,小松同学从烧杯中取少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到酚酞试液不变色。于是他得出“两种物质已恰好完全中和”的结论。
(1)写出该反应的化学方程式: 。
(2)你认为他得出的结论是否正确 ,
理由是 。
(3)为了验证小松同学的结论,你可以选择的试剂是( ) A、紫色石蕊试液 B、稀硫酸
C、铁粉 D、铜片 E、碳酸钠
稀盐酸
氢氧化钠
不正确
如果盐酸滴加过量,滴入酚酞试液也不变色
A
C
E
NaOH+HCl=NaCl+H2O
拓展训练
谢 谢
第四节 酸碱中和反应
酸碱的中和反应
教学目标
1.实验探究“酸和碱能否发生化学反应”
2.寻找酸和碱反应的规律,正确书写相关化学方程式
3.认识中和反应的实质。学会利用中和反应来改变溶液的酸碱性
实验探究
盐酸(HCl)和氢氧化钠(NaOH)溶液能否发生化学反应?
猜想与假设
可能反应?
HCl + NaOH =
可能不反应?
设计实验
用胶头滴管向盛有约2ml,溶质质量分数为0.4%的氢氧化钠溶液的试管中滴加0.4%的盐酸,观察现象.
无明显现象
收集证据:
1,用PH试纸分别测定水.氢氧化钠溶液和稀盐酸的PH。
2,分别量取2ml水和2ml的氢氧化钠溶液于试管中,然后分别滴入2ml稀盐酸,充分震荡后,测定所得溶液的PH。
水 氢氧化钠溶液 稀盐酸
加酸前的PH
加酸后的PH
解释与结论:
你认为氢氧化钠溶液中加入稀盐酸后,溶液的PH变化原因是什么?能否说明酸和碱之间了化学反应?
思考:在向氢氧化钠溶液中滴加稀盐酸时,溶液的pH是怎样变化的?你能说出曲线上坐标为(18,7)的点所表示的意义吗?
pH
(18,7)
A
M
P
NaOH溶液与盐酸恰好完全反应,溶液显中性pH=7
氢氧化钠
盐酸
pH计
7
滴入的稀盐酸的量较少,溶液显碱性
【讨论疑点】:
滴入的稀盐酸的量较多,溶液显酸性
测pH法:
借助指示剂法;测PH法
测温度法:
pH试纸
pH计
紫色石蕊试液
无色酚酞试液
实 验 方 案
间接观察法
借助指示剂法:
反应为放热反应
合作探究:氢氧化钠和盐酸会发生什么?
NaOH溶液
滴入( )溶液
溶液为( )色
再滴入( )溶液
溶液为( )色
无色酚酞
红
盐酸
无
NaOH溶液
滴入(紫色石蕊) 溶液
溶液为( )色
再滴入( HCl )溶液
溶液为( )色
合作探究:
对比:以上两种方案,哪一种更好些?
并分析原因?
蓝
无
上述实验中:盐酸和氢氧化钠溶液混合后,溶液的PH发生了明显的变化,显然不是由于溶液混合后相互____________造成的,而是溶液中的______和_____结合成了_____,导致溶液原有的酸碱性相互“中和”的结果。
NaOH+HCI=NaCI+H2O
中和反应的实质:H+ + OH- =H2O
反应实质
Na+ 和Cl- 不变而H+和OH_消失
思考:
氢氧化钠和盐酸的反应有
什么特点?
NaOH + HCl = NaCl + H2O
碱
酸
水
盐
中和反应:
归纳总结:
酸和碱作用生成盐和水的反应。
酸 + 碱 → 盐 + 水
写出下列反应的化学方程式,有何共同特点?
1、胃酸(HCl)过多,口服碱性药物(例:Mg(OH)2)
2、向酸性土壤(H2SO4)中撒熟石灰(Ca(OH)2)
3、向酸性废水(HCl)中加熟石灰(Ca(OH)2)
胃酸(HCl)过多,口服碱性药物(例:Al(OH)3)
寻找规律
中和反应的应用
你认为判断一个反应是不是中和反应的关键是什么?
讨论
反应物必须是酸与碱,
生成物必须是盐和水
注意:有盐和水生成的反应一定是中和反应吗?
1.在滴有石蕊的稀盐酸中,加入足量NaOH溶液,加酸前后溶液颜色依次为 ( )
A.红色、紫色 、蓝色 B.紫色、红色、蓝色
C.红色、蓝色、紫色 D.蓝色、紫色、红色
2.在实验室里,欲使碱性溶液变成中性,下列试剂中最好选用哪一种组合 ( )
① NaOH溶液②稀盐酸 ③石灰水 ④酚酞试液
A. ①或③ B. 只有②
C. 只有① D. ②和④
A
D
达标检测
3、下列各组物质间的反应,由于现象不明显
需要借助酸碱指示剂才能判断出反应发生的
是( )
A、 镁和稀盐酸
B 、烧碱溶液和稀硫酸
C、氧化铁和稀硫酸
D、澄清石灰水中通入二氧化碳
归纳总结:
1.中和反应:___________________
2.实质:如图体现了稀盐酸和氢氧化钠溶液反应的实质:
3.现象:做酸碱中和实验时,取一支试管,倒入10 mL氢氧化钠稀溶液,再滴入1—2滴酚酞试液,溶液呈红色。然后用___________逐渐滴入稀盐酸,同时不停地___________,直至溶液恰好变成___________色为止。
4.图形分析.
. 小松同学在进行酸碱中和反应的实验时,向烧杯中的氢氧化钠溶液中滴加稀盐酸一会儿后,发现忘记了滴加指示剂。为了确定盐酸与氢氧化钠是否恰好完全反应,小松同学从烧杯中取少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到酚酞试液不变色。于是他得出“两种物质已恰好完全中和”的结论。
(1)写出该反应的化学方程式: 。
(2)你认为他得出的结论是否正确 ,
理由是 。
(3)为了验证小松同学的结论,你可以选择的试剂是( ) A、紫色石蕊试液 B、稀硫酸
C、铁粉 D、铜片 E、碳酸钠
稀盐酸
氢氧化钠
不正确
如果盐酸滴加过量,滴入酚酞试液也不变色
A
C
E
NaOH+HCl=NaCl+H2O
拓展训练
谢 谢
同课章节目录
- 第一单元 溶液
- 1 溶液的形成
- 2 溶液组成的定量表示
- 3物质的溶解性
- 到实验室去:配制一定溶质质量分数的溶液
- 第二单元 常见的酸和碱
- 1 酸及其性质
- 2 碱及其性质
- 3 溶液的酸碱性
- 4 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 到图书馆去:分子变成离子
- 第三单元 海水中的化学
- 1 海洋化学资源
- 2 海水“晒盐”
- 3 海水“制碱”
- 到实验室去:粗盐中难溶性杂质的去除
- 第四单元 金属
- 1 常见的金属材料
- 2 金属的化学性质
- 3 钢铁的锈蚀与防护
- 到实验室去:探究金属的性质
- 第五单元 化学与健康
- 1 食物中的有机物
- 2 化学元素与人体健康
- 3 远离有毒物质
- 第六单元 化学与社会发展
- 1 化学与能源开发
- 2 化学与材料研制
- 3 化学与农业生产
- 4 化学与环境保护
