2021-2022学年人教版(2019)化学选择性必修第一册课件 第一章 第一节 第一课时 反应热 焓变(52张ppt)
文档属性
| 名称 | 2021-2022学年人教版(2019)化学选择性必修第一册课件 第一章 第一节 第一课时 反应热 焓变(52张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 3.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-07 00:00:00 | ||
图片预览











文档简介
(共52张PPT)
第一章 化学反应的热效应
第一节 反应热
第一课时 反应热 焓变
分点突破1
反应热及其测定
分点突破2
反应热与焓变
分点突破3
化学反应中能量变化的原因
关键能力培养
分析与推理能力
[分级训练·课课过关]
200
00
150
250
100
50
40
50m|
m
50
00
20
8—
50
30
tO
AAT
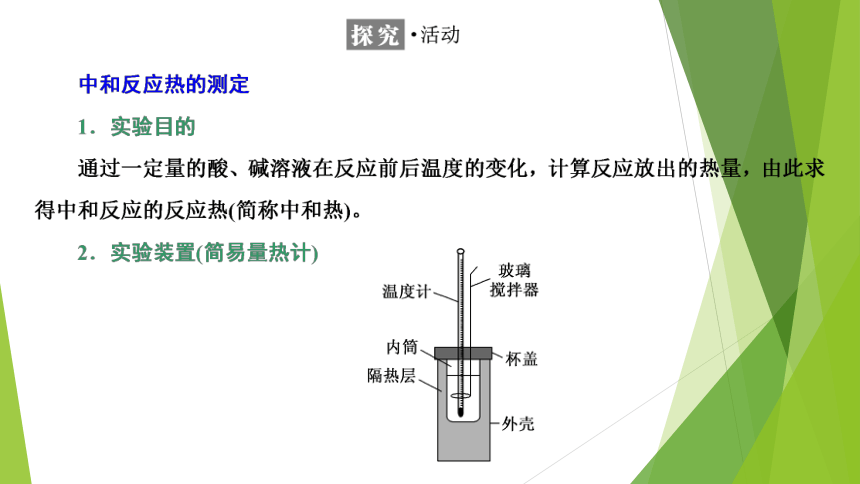
探究·活动
玻璃
温度计‖搅拌器
内筒
杯盖
隔热层
外壳
归纳·总结
绝热装置的准备减少热量损失
量取反应物
测反应前温度
用NaOH稀溶液,稀盐酸
混合反应物
测反应后温度
测反应后混合液的最高温度
重复实验
减少实验误差
练习·应用
必备·知识
焓
反应物的
总焓
生成物的
总焓
联想·质疑
C
键
断裂
⑩⑩
436 kJ. mol-I
能量
键
断裂
243kJ·mol1
能量
键形成一
431kJ·mol
431 kJ.mol
能量←
能量
物质变心「反应物
生成物
化学反应
旧化学键断裂
新化学键形成
化吸收能量
放出能量
差值
热效应
能↑反应物
能
生成物
量
量
吸收
放出↑△H的符号热量
热量;为“-”或
△H的符号
为“+”或
△H<0
△H>0
生成物
反应物
反应过程
反应过程
放热反应
吸热反应
能↑2H(g)+O(g)
不一不
H2(g)+2O2(g)
不
h,o(g)
反应过程
反应物
△H1年成物
反应历程
迁移·应用
个能量/(kJ·mol)
2H2O2
2H2O()+O2(g
反应过程
温
HCH3产物①
H-C—C-CH3
CH3
Cl正
C=c +HCl
HGH3产物②
H
CH3
H-C—C-CH3
H Cl
反应过程
课堂·巩固练
第一章 化学反应的热效应
第一节 反应热
第一课时 反应热 焓变
分点突破1
反应热及其测定
分点突破2
反应热与焓变
分点突破3
化学反应中能量变化的原因
关键能力培养
分析与推理能力
[分级训练·课课过关]
200
00
150
250
100
50
40
50m|
m
50
00
20
8—
50
30
tO
AAT
探究·活动
玻璃
温度计‖搅拌器
内筒
杯盖
隔热层
外壳
归纳·总结
绝热装置的准备减少热量损失
量取反应物
测反应前温度
用NaOH稀溶液,稀盐酸
混合反应物
测反应后温度
测反应后混合液的最高温度
重复实验
减少实验误差
练习·应用
必备·知识
焓
反应物的
总焓
生成物的
总焓
联想·质疑
C
键
断裂
⑩⑩
436 kJ. mol-I
能量
键
断裂
243kJ·mol1
能量
键形成一
431kJ·mol
431 kJ.mol
能量←
能量
物质变心「反应物
生成物
化学反应
旧化学键断裂
新化学键形成
化吸收能量
放出能量
差值
热效应
能↑反应物
能
生成物
量
量
吸收
放出↑△H的符号热量
热量;为“-”或
△H的符号
为“+”或
△H<0
△H>0
生成物
反应物
反应过程
反应过程
放热反应
吸热反应
能↑2H(g)+O(g)
不一不
H2(g)+2O2(g)
不
h,o(g)
反应过程
反应物
△H1年成物
反应历程
迁移·应用
个能量/(kJ·mol)
2H2O2
2H2O()+O2(g
反应过程
温
HCH3产物①
H-C—C-CH3
CH3
Cl正
C=c +HCl
HGH3产物②
H
CH3
H-C—C-CH3
H Cl
反应过程
课堂·巩固练
