5.1质量守恒定律同步习题—2021—2022学年九年级化学人教版上册(有答案)
文档属性
| 名称 | 5.1质量守恒定律同步习题—2021—2022学年九年级化学人教版上册(有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 125.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-08 00:00:00 | ||
图片预览




文档简介
5.1质量守恒定理
一、单选题
1.10 g甲与足量的乙反应,生成8g丙和15g丁,则参加反应的乙的质量是
A.13g B.23g C.18g D.25g
2.化学反应的实质是
A.分子的间隔发生改变 B.分子的运动速度改变
C.原子的种类发生改变 D.分子破裂,原子重新组合
3.化学方程式2H2 + O22H2O的错误读法是
A.氢气和氧气在点燃条件下生成水 B.氢气加氧气等于水
C.2个氢分子和1个氧分子生成2个水分子 D.4份质量的氢气和32份质量的氧气生成36份质量的水
4.如图为某反应的微观示意图。关于该反应说法错误的是
A.甲的化学式为CH2O B.该反应涉及3种氧化物
C.反应前后原子种类不变 D.保持乙的化学性质的是氧分子
5.下列说法错误的是
A.原子核一般由质子、中子构成
B.花香四溢主要是因为分子之间有间隔
C.保持水化学性质的最小微粒是水分子
D.化学反应前后原子的种类不会改变
6.用足量的氢气还原8gCuO,反应后生成铜的质量为
A.8g B.大于8g C.小于8g D.小于等于8g
7.用“”和“”代表两种不同的单质分子,它们在一定条件下能发生化学反应,反应前后的微观示意图如图所示,下列说法不正确的是
A.该反应是化合反应
B.该反应有1种生成物
C.每个生成物分子由4个原子构成
D.参加反应的“”和“”分子的个数比是2:1
8.下列事实符合质量守恒定律的是
A.汽油挥发后质量变小 B.水变成冰后体积变大
C.木材燃烧后质量变小 D.酒精和水混合后质量不变
9.小明在练习制作“糖葫芦”时,在给蔗糖加热时产生了炭黑和水(整个过程密闭),这一事实说明了
A.蔗糖是由炭黑和水组成的纯净物
B.蔗糖是炭黑和水组成的混合物
C.蔗糖分子是由碳元素和水分子组成的
D.蔗糖是由碳、氢、氧元素组成的
10.元素观是化学的重要观念之一,下列有关元素的说法中正确的是
A.元素是具有相同核电荷数的一种原子的总称
B.元素周期表中,元素的原子序数与该元素原子核电荷数在数值上相同
C.同种元素的原子核内质子数与中子数一定相等
D.物质发生化学变化时,原子种类改变,元素种类也改变
11.下列说法符合质量守恒定律的是
A.4g硫和2g氧气充分反应生成6g二氧化硫
B.3g碳和8g氧气充分反应生成11g二氧化碳
C.100g高锰酸钾完全分解所得固体的质量为100g
D.将6000L氧气通过加压装入40L的钢瓶中,质量没变
12.下列四个图像分别与选项中的操作相对应,其中合理的是
A.一定质量的高锰酸钾制取氧气
B.一定质量的氯酸钾和二氧化锰制取氧气
C.一定质量的汞在氧气中密闭加热
D.一定质量的过氧化氢溶液和二氧化锰制取氧气
13.某有机物在空气中完全燃烧,共得到二氧化碳和水,则该化合物的组成元素是
A.该物质由碳、氢、氧三种元素组成
B.该物质只含有碳、氢两种元素
C.一定含有碳、氢元素,可能含有氧元素
D.该物质的分子中碳原子和氢原子的个数比为1:3
14.如图为某化学反应的微观模拟图,“”和“”分别表示两种不同的原子,下列说法不正确的是
A.该反应的基本反应类型为置换反应 B.反应前后原子的种类和数目保持不变
C.甲物质是化合物 D.参加反应的甲、乙两种反应物的分子个数比为2:1
二、填空题
15.蜡烛燃烧后生成水和二氧化碳,由此可以推测出蜡烛肯定含有哪些元素?______,依据是______。
16.在宏观、微观建立联系,是学习化学特有的思维方式。电解水的微观示意图如图所示:
依据图所给信息,回答下列问题:
(1)从微观角度分析,该反应前后___________不变(写一点)。该反应的基本反应类型是___________。
(2)H2O和H2O2的组成元素相同,但化学性质不同,其原因是___________。
三、推断题
17.图中A~E是初中化学常见的物质,已知A和E都有可燃性,C是能使澄清石灰水变浑浊的气体,D是实验室常见的一种液体。请分析回答:
(1)写出物质的化学式:C_____;D_____;E_____;
(2)根据图示可推出:A中一定含有_____元素和_____元素,可能含有_____元素。
18.已知A~F都是初中常见的物质,A、C为无色液体,且组成元素相同,D为氧气,它们之间的转化关系如图所示。
(1)物质B在反应①中的作用是_____,请写出反应①的文字表达式_____。
(2)检验气体D的方法是_____。
(3)若E为铁丝,反应②的实验现象为_____。
(4)若F为二氧化碳,则E中必然含有的元素是_____(填元素名称)。
四、实验题
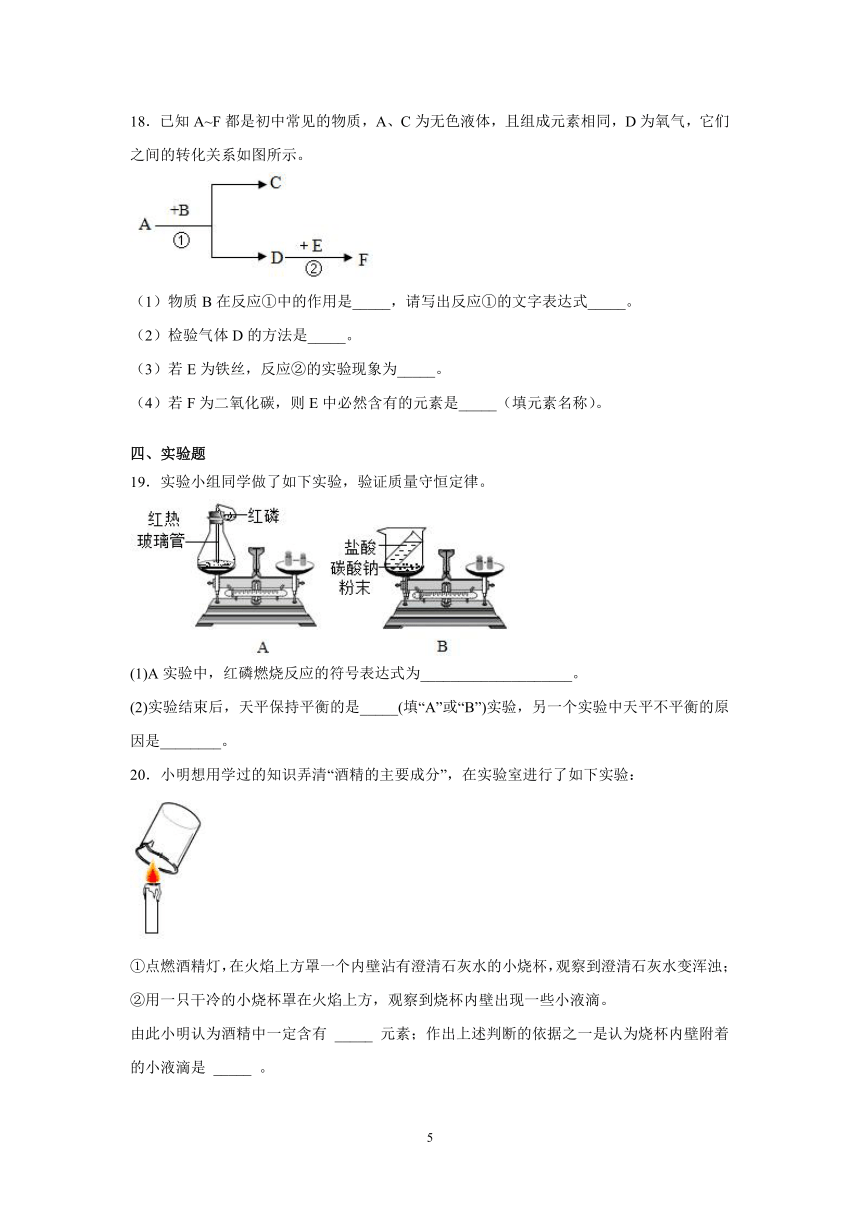
19.实验小组同学做了如下实验,验证质量守恒定律。
(1)A实验中,红磷燃烧反应的符号表达式为____________________。
(2)实验结束后,天平保持平衡的是_____(填“A”或“B”)实验,另一个实验中天平不平衡的原因是________。
20.小明想用学过的知识弄清“酒精的主要成分”,在实验室进行了如下实验:
①点燃酒精灯,在火焰上方罩一个内壁沾有澄清石灰水的小烧杯,观察到澄清石灰水变浑浊;
②用一只干冷的小烧杯罩在火焰上方,观察到烧杯内壁出现一些小液滴。
由此小明认为酒精中一定含有 _____ 元素;作出上述判断的依据之一是认为烧杯内壁附着的小液滴是 _____ 。
五、计算题
21.在一定条件下,将A、B、C、D四种物质放在密闭容器内反应一段时间,测得化学反应前后各物质的质量如下表:
物质 A B C D
反应前质量/g 5 112 16 4
反应后质量/g x 0 32 100
根据上表数据计算:
(1)该反应的反应物是_____,生成物是_____(字母连续写,不要加符号或空格);
(2)表中“x”值为_____g;
(3)该反应属于_____反应(填“化合”或“分解”);
(4)B、C两种物质变化的质量比为_____(化为最简整数比)。
22.根据要求完成下列计算:
①三氧化二铁中铁元素的质量分数;
②含Fe2O380%的赤铁矿100吨.可炼得纯铁t。(假设冶炼过程中铁无损失)
参考答案
1.A
【详解】
10g甲与足量的乙反应,生成8g丙和15g丁,由质量守恒定律,参加反应的甲和乙的质量之和等于生成丙和丁的质量之和,则参加反应的乙的质量为8g+15g-10g=13g。
故选:A。
2.D
【详解】
A、分子的间隔发生改变不会发生化学变化,故A错误;
B、分子的运动速率改变不会发生化学变化,故B错误;
C、化学变化中原子的种类不发生改变,故C错误;
D、由分子构成的物质发生化学变化的实质是分子发生了破裂,原子发生重新组合生成了新的分子,故D正确。
故选D。
3.B
【详解】
A、化学方程式读法:氢气和氧气在点燃的条件下生成水,故选项正确;
B、“+”不能读作“加”、“═”不能读作“等于”,故选项错误;
C、微观上应读作:两个氢分子和一个氧分子在点燃条件下生成两个水分子,故选项正确;
D、从物质质量的变化来读,每4份质量的氢气和32份质量的氧气在点燃条件下恰好生成36份质量的水,故选项正确。
故选B。
4.B
【分析】
由反应的微粒模型图可知此反应的化学方程式为CH2O+O2CO2+H2O
【详解】
A.由微粒模型可知甲的化学式为CH2O,故正确;
B.氧化物是由两种元素组成且其中一种是氧元素的化合物,所以此反应中只有二氧化碳和水两种氧化物,故错误;
C.任何一个化学反应都遵守质量守恒定律,所以反应前后的原子种类一定不变,故正确;
D.乙表示氧气,氧气是由氧分子构成的,所以保持氧气化学性质的粒子是氧分子,故正确。故选B。
5.B
【详解】
A、原子一般是由质子和中子构成的,说法正确;
B、花香四溢主要是因为分子在不断运动,说法错误;
C、分子是保持物质化学性质的最小微粒,水是由水分子构成,所以保持水化学性质的最小微粒是水分子,说法正确;
D、由质量守恒定律可知,化学反应前后原子的种类不会改变,说法正确。
故选:B。
6.C
【详解】
根据质量守恒定律可知:化学反应前后铜元素的质量不会变化,所以生成铜的质量等于氧化铜中铜元素质量相同,故铜的质量一定小于8g。
故选:C。
7.D
【分析】
由反应前后的微观示意图结合质量守恒定律可知,各物质反应的微粒个数关系是:
。
【详解】
A、由上图可知,该反应由两种物质生成了一种物质,符合多变一的特点,属于化合反应,故说法正确;
B、由上图可知,该反应生成了一种物质,故说法正确;
C、由上图可知,该反应有1种生成物,每个生成物分子由4个原子构成,故说法正确;
D、由上图可知,参加反应的和分子的个数比是6:2=3:1,故说法不正确。
故选:D。
8.C
【详解】
A、汽油挥发后质量变小,是因为汽油的状态发生了改变,无新物质生成,属于物理变化,不符合质量守恒定律, 不符合题意;
B、水变成冰后体积变大,是因为分子之间的间隔变大,无新物质生成,属于物理变化,不符合质量守恒定律,不符合题意;
C、木材燃烧后质量变小,是因为生成了二氧化碳等气体,有新物质生成,属于化学变化,符合质量守恒定律,符合题意;
D、酒精和水混合后质量不变,无新物质生成,属于物理变化,不符合质量守恒定律,不符合题意。
故选C。
9.D
【详解】
A、加热蔗糖的产物是炭黑和水,但蔗糖不是由炭黑和水组成的,该选项说法不正确;
B、蔗糖属于纯净物,而炭黑和水组成的物质属于混合物,该选项说法不正确;
C、蔗糖分子是由碳原子、氢原子和氧原子构成的,不能说蔗糖分子由碳元素和水分子组成的,该选项说法不正确;
D、化学反应前后元素种类不变,加热蔗糖产生炭黑和水,说明蔗糖是由碳元素、氢元素和氧元素组成的,该选项说法正确。
故选:D。
10.B
【详解】
A、化学元素就是具有相同的核电荷数(核内质子数)的一类原子的总称,不是指某种原子,故A错误;
B、化学元素周期表中,是按照原子序数依次增多的顺序排列起来的,在数值上,原子序数等于原子核电荷数,故B正确;
C、同种元素的原子核内质子数与中子数不一定相同,故C错误;
D、物质发生化学变化时,原子种类没有改变,元素种类也没有改变,只有分子种类发生了改变,故D错误;
故选择B
【点睛】
11.B
【详解】
A、根据硫燃烧的化学方程式可知, 参加反应的硫与氧气的质量比为1:1,故4g硫和2g氧气充分反应时,硫过量,生成二氧化硫的质量应为4g,此选项不正确;
B、根据碳燃烧的化学方程式可知,参加反应的碳与氧气的质量比为3:8,故3g碳和8g氧气充分反应生成11g二氧化碳,符合质量守恒定律,此选项正确;
C、根据高锰酸钾分解的化学方程式可知分解后会生成一定质量的氧气,所得固体为锰酸钾和二氧化锰的质量,故反应后所得固体的总质量一定小于100g,此选项不正确;
D、将氧气压入钢瓶过程中没有生成新物质,属于物理变化,质量守恒定律是指在化学反应前后物质的总质量不变,故此过程不符合质量守恒定律,此选项不正确。
故选B。
12.C
【详解】
A、高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气,剩余物中含有锰酸钾、二氧化锰,反应后固体质量不会是0,故选项图像不正确;
B、二氧化锰是该反应的催化剂,反应前后二氧化锰的质量保持不变,故选项图像不正确;
C、根据质量守恒定律,反应前后元素种类不变,故选项图像正确;
D、用一定量的过氧化氢溶液与二氧化锰混合制取氧气,当过氧化氢完全分解时,生成氧气的质量不再变化,故选项图像不正确。
故选C。
【点睛】
本题是一道图像坐标与化学知识相结合的综合题,解题的关键是结合所涉及的化学知识,正确分析各变化的过程,注意分析坐标轴表示的意义、曲线的起点、折点及变化趋势,进而确定正确的图像。
13.A
【详解】
8.8g 二氧化碳中含有碳元素质量=
3.6g 水中含有氢元素质量=
A、根据质量守恒定律,反应前后元素种类不变,该物质中C、H元素质量之和=2.4g+0.4g=2.8g,小于反应前的6g,因此该物质除了C、H元素外还含有O元素,O元素质量=6g-2.8g=3.2g,故A正确;
B、根据A的分析可知,B错误;
C、根据A的分析可知,C错误;
D、该物质的C、H质量比为2.4g:0.4g=24:4,C、H元素的相对分子质量分别为12和1,则该物质的分子中碳原子和氢原子的个数比为=1:2,故D错误;
故选A。
14.A
【详解】
A、该反应是单质和化合物反应生成新的化合物,属于化合反应,A说法错误;
B、所有化学反应都符合质量守恒定律,故反应前后原子的种类和数目不变,B说法正确;
C、甲物质是由两种元素组成,属于化合物,C说法正确;
D、由图可以看出,该反应是两个甲分子和一个乙分子反应,甲和乙反应的分子个数比为2:1,D说法正确;
故选A。
15.C、H 质量守恒定律
【详解】
略
16.原子数目或原子种类 分解反应 分子构成不同
【详解】
(1)从微观角度分析,该反应前后原子数目或原子种类不变;一种物质参与反应生成多种物质的反应叫做分解反应,该反应的基本反应类型是分解反应。
故填:原子数目或原子种类;分解反应。
(2)H2O和H2O2的组成元素相同,但化学性质不同,其原因是分子构成不同。
故填:分子构成不同。
17.CO2 H2O H2 碳或C 氢或H 氧或O
【分析】
根据A~E是初中化学常见的物质,A和E都有可燃性,C是能使澄清石灰水变浑浊的气体,所以C是二氧化碳,D是实验室常见的一种液体,D通电会生成E、B,所以D是水,A、B点燃会生成水和二氧化碳,所以B是氧气,E是氢气,A可能是甲烷等有机物,有机物和氧气点燃生成水和二氧化碳,然后将推出的物质进行验证即可。
【详解】
(1)A~E是初中化学常见的物质,A和E都有可燃性,C是能使澄清石灰水变浑浊的气体,所以C是二氧化碳,D是实验室常见的一种液体,D通电会生成E、B,所以D是水,A、B点燃会生成水和二氧化碳,所以B是氧气,E是氢气,A可能是甲烷等有机物,有机物和氧气点燃生成水和二氧化碳,经过验证,推导正确,所以C是CO2,D是H2O,E是H2;
(2)根据图示可推出A燃烧生成二氧化碳和水,据质量守恒定律可知反应前后元素的种类不变可知:A中一定含有碳元素和氢元素,可能含有氧元素。
18.催化作用(催化剂) 过氧化氢水+氧气 将带火星的木条伸入集气瓶,若木条复燃,证明是氧气 剧烈燃烧,火星四射,生成黑色固体,放出大量的热 碳
【分析】
通常状况下,A、C为无色液体且组成元素相同,D为氧气,过氧化氢在二氧化锰的催化作用下分解生成水和氧气,所以A是过氧化氢溶液,B是二氧化锰,C是水,氧气和E反应会生成F,所以E可以是铁、碳、硫等物质,经过验证,推断正确。
【详解】
(1)由分析可知,物质B是二氧化锰,在反应①中作催化剂,其作用是催化作用;
反应①是过氧化氢在二氧化锰的催化作用下分解生成水和氧气,反应的文字表达式为:过氧化氢水+氧气;
(2)D为氧气,具有助燃性,检验氧气的方法为:将带火星的木条伸入集气瓶,若木条复燃,证明是氧气;
(3)若E为铁丝,反应②是铁和氧气在点燃的条件下生成四氧化三铁,实验现象为:剧烈燃烧,火星四射,放出大量热,生成黑色固体;
(4)若F为二氧化碳,氧气只能提供氧元素,所以E中必然含有的元素是碳元素。
19.P+O2P2O5 A 反应不是在密闭体系中进行,有二氧化碳逸出
【详解】
(1)红磷(P)在氧气(O2)中燃烧生成五氧化二磷(P2O5),因此此反应的符号表达式为P+O2P2O5
(2)A和B两个实验中,都是有气体参加或者生成的反应。在有气体参与的化学反应想验证质量守恒定律,必须是在密闭的条件下验证。其中A为密闭条件,而B为开放条件。故反应后平衡的为A;又B是开放条件且反应后有气二氧化碳体生成,因此B不能平衡。
故答案为(1). P+O2P2O5;(2). A;(3). 反应不是在密闭体系中进行,有二氧化碳逸出
20.碳、氢 水
【详解】
根据点燃酒精灯,在火焰上方罩一个内壁沾有澄清石灰水的小烧杯,观察到澄清石灰水变浑浊,证明生成了二氧化碳,由质量守恒定律可知,酒精中含有碳元素;用一只干冷的小烧杯罩在火焰上方,观察到烧杯内壁出现一些小液滴,说明有水生成,由质量守恒定律可知,酒精中含有氢元素。酒精中一定含有碳、氢元素;作出上述判断的依据之一是认为烧杯内壁附着的小液滴是水。
21.B;CD;5;分解;7:1
【详解】
根据质量守恒定律可知,x=5g+112g+16g+4g-32g-100g=5g;
(1)反应前后,C、D的质量增大,是生成物;B质量减轻,是反应物;
(2)表中“x”值为5;
(3)该反应是B→C+D,故该反应是分解反应;
(4)B、C两种物质变化的质量比为112g:(32-16)g=7:1。
22.70%;56
【详解】
①三氧化二铁中铁元素的质量分数为: ;
②根据反应前后元素的种类、质量不变,氧化铁中铁元素的质量与得到纯铁的质量相同,含Fe2O380%的赤铁矿100吨,可炼得纯铁:100吨×80%×70%=56吨。
一、单选题
1.10 g甲与足量的乙反应,生成8g丙和15g丁,则参加反应的乙的质量是
A.13g B.23g C.18g D.25g
2.化学反应的实质是
A.分子的间隔发生改变 B.分子的运动速度改变
C.原子的种类发生改变 D.分子破裂,原子重新组合
3.化学方程式2H2 + O22H2O的错误读法是
A.氢气和氧气在点燃条件下生成水 B.氢气加氧气等于水
C.2个氢分子和1个氧分子生成2个水分子 D.4份质量的氢气和32份质量的氧气生成36份质量的水
4.如图为某反应的微观示意图。关于该反应说法错误的是
A.甲的化学式为CH2O B.该反应涉及3种氧化物
C.反应前后原子种类不变 D.保持乙的化学性质的是氧分子
5.下列说法错误的是
A.原子核一般由质子、中子构成
B.花香四溢主要是因为分子之间有间隔
C.保持水化学性质的最小微粒是水分子
D.化学反应前后原子的种类不会改变
6.用足量的氢气还原8gCuO,反应后生成铜的质量为
A.8g B.大于8g C.小于8g D.小于等于8g
7.用“”和“”代表两种不同的单质分子,它们在一定条件下能发生化学反应,反应前后的微观示意图如图所示,下列说法不正确的是
A.该反应是化合反应
B.该反应有1种生成物
C.每个生成物分子由4个原子构成
D.参加反应的“”和“”分子的个数比是2:1
8.下列事实符合质量守恒定律的是
A.汽油挥发后质量变小 B.水变成冰后体积变大
C.木材燃烧后质量变小 D.酒精和水混合后质量不变
9.小明在练习制作“糖葫芦”时,在给蔗糖加热时产生了炭黑和水(整个过程密闭),这一事实说明了
A.蔗糖是由炭黑和水组成的纯净物
B.蔗糖是炭黑和水组成的混合物
C.蔗糖分子是由碳元素和水分子组成的
D.蔗糖是由碳、氢、氧元素组成的
10.元素观是化学的重要观念之一,下列有关元素的说法中正确的是
A.元素是具有相同核电荷数的一种原子的总称
B.元素周期表中,元素的原子序数与该元素原子核电荷数在数值上相同
C.同种元素的原子核内质子数与中子数一定相等
D.物质发生化学变化时,原子种类改变,元素种类也改变
11.下列说法符合质量守恒定律的是
A.4g硫和2g氧气充分反应生成6g二氧化硫
B.3g碳和8g氧气充分反应生成11g二氧化碳
C.100g高锰酸钾完全分解所得固体的质量为100g
D.将6000L氧气通过加压装入40L的钢瓶中,质量没变
12.下列四个图像分别与选项中的操作相对应,其中合理的是
A.一定质量的高锰酸钾制取氧气
B.一定质量的氯酸钾和二氧化锰制取氧气
C.一定质量的汞在氧气中密闭加热
D.一定质量的过氧化氢溶液和二氧化锰制取氧气
13.某有机物在空气中完全燃烧,共得到二氧化碳和水,则该化合物的组成元素是
A.该物质由碳、氢、氧三种元素组成
B.该物质只含有碳、氢两种元素
C.一定含有碳、氢元素,可能含有氧元素
D.该物质的分子中碳原子和氢原子的个数比为1:3
14.如图为某化学反应的微观模拟图,“”和“”分别表示两种不同的原子,下列说法不正确的是
A.该反应的基本反应类型为置换反应 B.反应前后原子的种类和数目保持不变
C.甲物质是化合物 D.参加反应的甲、乙两种反应物的分子个数比为2:1
二、填空题
15.蜡烛燃烧后生成水和二氧化碳,由此可以推测出蜡烛肯定含有哪些元素?______,依据是______。
16.在宏观、微观建立联系,是学习化学特有的思维方式。电解水的微观示意图如图所示:
依据图所给信息,回答下列问题:
(1)从微观角度分析,该反应前后___________不变(写一点)。该反应的基本反应类型是___________。
(2)H2O和H2O2的组成元素相同,但化学性质不同,其原因是___________。
三、推断题
17.图中A~E是初中化学常见的物质,已知A和E都有可燃性,C是能使澄清石灰水变浑浊的气体,D是实验室常见的一种液体。请分析回答:
(1)写出物质的化学式:C_____;D_____;E_____;
(2)根据图示可推出:A中一定含有_____元素和_____元素,可能含有_____元素。
18.已知A~F都是初中常见的物质,A、C为无色液体,且组成元素相同,D为氧气,它们之间的转化关系如图所示。
(1)物质B在反应①中的作用是_____,请写出反应①的文字表达式_____。
(2)检验气体D的方法是_____。
(3)若E为铁丝,反应②的实验现象为_____。
(4)若F为二氧化碳,则E中必然含有的元素是_____(填元素名称)。
四、实验题
19.实验小组同学做了如下实验,验证质量守恒定律。
(1)A实验中,红磷燃烧反应的符号表达式为____________________。
(2)实验结束后,天平保持平衡的是_____(填“A”或“B”)实验,另一个实验中天平不平衡的原因是________。
20.小明想用学过的知识弄清“酒精的主要成分”,在实验室进行了如下实验:
①点燃酒精灯,在火焰上方罩一个内壁沾有澄清石灰水的小烧杯,观察到澄清石灰水变浑浊;
②用一只干冷的小烧杯罩在火焰上方,观察到烧杯内壁出现一些小液滴。
由此小明认为酒精中一定含有 _____ 元素;作出上述判断的依据之一是认为烧杯内壁附着的小液滴是 _____ 。
五、计算题
21.在一定条件下,将A、B、C、D四种物质放在密闭容器内反应一段时间,测得化学反应前后各物质的质量如下表:
物质 A B C D
反应前质量/g 5 112 16 4
反应后质量/g x 0 32 100
根据上表数据计算:
(1)该反应的反应物是_____,生成物是_____(字母连续写,不要加符号或空格);
(2)表中“x”值为_____g;
(3)该反应属于_____反应(填“化合”或“分解”);
(4)B、C两种物质变化的质量比为_____(化为最简整数比)。
22.根据要求完成下列计算:
①三氧化二铁中铁元素的质量分数;
②含Fe2O380%的赤铁矿100吨.可炼得纯铁t。(假设冶炼过程中铁无损失)
参考答案
1.A
【详解】
10g甲与足量的乙反应,生成8g丙和15g丁,由质量守恒定律,参加反应的甲和乙的质量之和等于生成丙和丁的质量之和,则参加反应的乙的质量为8g+15g-10g=13g。
故选:A。
2.D
【详解】
A、分子的间隔发生改变不会发生化学变化,故A错误;
B、分子的运动速率改变不会发生化学变化,故B错误;
C、化学变化中原子的种类不发生改变,故C错误;
D、由分子构成的物质发生化学变化的实质是分子发生了破裂,原子发生重新组合生成了新的分子,故D正确。
故选D。
3.B
【详解】
A、化学方程式读法:氢气和氧气在点燃的条件下生成水,故选项正确;
B、“+”不能读作“加”、“═”不能读作“等于”,故选项错误;
C、微观上应读作:两个氢分子和一个氧分子在点燃条件下生成两个水分子,故选项正确;
D、从物质质量的变化来读,每4份质量的氢气和32份质量的氧气在点燃条件下恰好生成36份质量的水,故选项正确。
故选B。
4.B
【分析】
由反应的微粒模型图可知此反应的化学方程式为CH2O+O2CO2+H2O
【详解】
A.由微粒模型可知甲的化学式为CH2O,故正确;
B.氧化物是由两种元素组成且其中一种是氧元素的化合物,所以此反应中只有二氧化碳和水两种氧化物,故错误;
C.任何一个化学反应都遵守质量守恒定律,所以反应前后的原子种类一定不变,故正确;
D.乙表示氧气,氧气是由氧分子构成的,所以保持氧气化学性质的粒子是氧分子,故正确。故选B。
5.B
【详解】
A、原子一般是由质子和中子构成的,说法正确;
B、花香四溢主要是因为分子在不断运动,说法错误;
C、分子是保持物质化学性质的最小微粒,水是由水分子构成,所以保持水化学性质的最小微粒是水分子,说法正确;
D、由质量守恒定律可知,化学反应前后原子的种类不会改变,说法正确。
故选:B。
6.C
【详解】
根据质量守恒定律可知:化学反应前后铜元素的质量不会变化,所以生成铜的质量等于氧化铜中铜元素质量相同,故铜的质量一定小于8g。
故选:C。
7.D
【分析】
由反应前后的微观示意图结合质量守恒定律可知,各物质反应的微粒个数关系是:
。
【详解】
A、由上图可知,该反应由两种物质生成了一种物质,符合多变一的特点,属于化合反应,故说法正确;
B、由上图可知,该反应生成了一种物质,故说法正确;
C、由上图可知,该反应有1种生成物,每个生成物分子由4个原子构成,故说法正确;
D、由上图可知,参加反应的和分子的个数比是6:2=3:1,故说法不正确。
故选:D。
8.C
【详解】
A、汽油挥发后质量变小,是因为汽油的状态发生了改变,无新物质生成,属于物理变化,不符合质量守恒定律, 不符合题意;
B、水变成冰后体积变大,是因为分子之间的间隔变大,无新物质生成,属于物理变化,不符合质量守恒定律,不符合题意;
C、木材燃烧后质量变小,是因为生成了二氧化碳等气体,有新物质生成,属于化学变化,符合质量守恒定律,符合题意;
D、酒精和水混合后质量不变,无新物质生成,属于物理变化,不符合质量守恒定律,不符合题意。
故选C。
9.D
【详解】
A、加热蔗糖的产物是炭黑和水,但蔗糖不是由炭黑和水组成的,该选项说法不正确;
B、蔗糖属于纯净物,而炭黑和水组成的物质属于混合物,该选项说法不正确;
C、蔗糖分子是由碳原子、氢原子和氧原子构成的,不能说蔗糖分子由碳元素和水分子组成的,该选项说法不正确;
D、化学反应前后元素种类不变,加热蔗糖产生炭黑和水,说明蔗糖是由碳元素、氢元素和氧元素组成的,该选项说法正确。
故选:D。
10.B
【详解】
A、化学元素就是具有相同的核电荷数(核内质子数)的一类原子的总称,不是指某种原子,故A错误;
B、化学元素周期表中,是按照原子序数依次增多的顺序排列起来的,在数值上,原子序数等于原子核电荷数,故B正确;
C、同种元素的原子核内质子数与中子数不一定相同,故C错误;
D、物质发生化学变化时,原子种类没有改变,元素种类也没有改变,只有分子种类发生了改变,故D错误;
故选择B
【点睛】
11.B
【详解】
A、根据硫燃烧的化学方程式可知, 参加反应的硫与氧气的质量比为1:1,故4g硫和2g氧气充分反应时,硫过量,生成二氧化硫的质量应为4g,此选项不正确;
B、根据碳燃烧的化学方程式可知,参加反应的碳与氧气的质量比为3:8,故3g碳和8g氧气充分反应生成11g二氧化碳,符合质量守恒定律,此选项正确;
C、根据高锰酸钾分解的化学方程式可知分解后会生成一定质量的氧气,所得固体为锰酸钾和二氧化锰的质量,故反应后所得固体的总质量一定小于100g,此选项不正确;
D、将氧气压入钢瓶过程中没有生成新物质,属于物理变化,质量守恒定律是指在化学反应前后物质的总质量不变,故此过程不符合质量守恒定律,此选项不正确。
故选B。
12.C
【详解】
A、高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气,剩余物中含有锰酸钾、二氧化锰,反应后固体质量不会是0,故选项图像不正确;
B、二氧化锰是该反应的催化剂,反应前后二氧化锰的质量保持不变,故选项图像不正确;
C、根据质量守恒定律,反应前后元素种类不变,故选项图像正确;
D、用一定量的过氧化氢溶液与二氧化锰混合制取氧气,当过氧化氢完全分解时,生成氧气的质量不再变化,故选项图像不正确。
故选C。
【点睛】
本题是一道图像坐标与化学知识相结合的综合题,解题的关键是结合所涉及的化学知识,正确分析各变化的过程,注意分析坐标轴表示的意义、曲线的起点、折点及变化趋势,进而确定正确的图像。
13.A
【详解】
8.8g 二氧化碳中含有碳元素质量=
3.6g 水中含有氢元素质量=
A、根据质量守恒定律,反应前后元素种类不变,该物质中C、H元素质量之和=2.4g+0.4g=2.8g,小于反应前的6g,因此该物质除了C、H元素外还含有O元素,O元素质量=6g-2.8g=3.2g,故A正确;
B、根据A的分析可知,B错误;
C、根据A的分析可知,C错误;
D、该物质的C、H质量比为2.4g:0.4g=24:4,C、H元素的相对分子质量分别为12和1,则该物质的分子中碳原子和氢原子的个数比为=1:2,故D错误;
故选A。
14.A
【详解】
A、该反应是单质和化合物反应生成新的化合物,属于化合反应,A说法错误;
B、所有化学反应都符合质量守恒定律,故反应前后原子的种类和数目不变,B说法正确;
C、甲物质是由两种元素组成,属于化合物,C说法正确;
D、由图可以看出,该反应是两个甲分子和一个乙分子反应,甲和乙反应的分子个数比为2:1,D说法正确;
故选A。
15.C、H 质量守恒定律
【详解】
略
16.原子数目或原子种类 分解反应 分子构成不同
【详解】
(1)从微观角度分析,该反应前后原子数目或原子种类不变;一种物质参与反应生成多种物质的反应叫做分解反应,该反应的基本反应类型是分解反应。
故填:原子数目或原子种类;分解反应。
(2)H2O和H2O2的组成元素相同,但化学性质不同,其原因是分子构成不同。
故填:分子构成不同。
17.CO2 H2O H2 碳或C 氢或H 氧或O
【分析】
根据A~E是初中化学常见的物质,A和E都有可燃性,C是能使澄清石灰水变浑浊的气体,所以C是二氧化碳,D是实验室常见的一种液体,D通电会生成E、B,所以D是水,A、B点燃会生成水和二氧化碳,所以B是氧气,E是氢气,A可能是甲烷等有机物,有机物和氧气点燃生成水和二氧化碳,然后将推出的物质进行验证即可。
【详解】
(1)A~E是初中化学常见的物质,A和E都有可燃性,C是能使澄清石灰水变浑浊的气体,所以C是二氧化碳,D是实验室常见的一种液体,D通电会生成E、B,所以D是水,A、B点燃会生成水和二氧化碳,所以B是氧气,E是氢气,A可能是甲烷等有机物,有机物和氧气点燃生成水和二氧化碳,经过验证,推导正确,所以C是CO2,D是H2O,E是H2;
(2)根据图示可推出A燃烧生成二氧化碳和水,据质量守恒定律可知反应前后元素的种类不变可知:A中一定含有碳元素和氢元素,可能含有氧元素。
18.催化作用(催化剂) 过氧化氢水+氧气 将带火星的木条伸入集气瓶,若木条复燃,证明是氧气 剧烈燃烧,火星四射,生成黑色固体,放出大量的热 碳
【分析】
通常状况下,A、C为无色液体且组成元素相同,D为氧气,过氧化氢在二氧化锰的催化作用下分解生成水和氧气,所以A是过氧化氢溶液,B是二氧化锰,C是水,氧气和E反应会生成F,所以E可以是铁、碳、硫等物质,经过验证,推断正确。
【详解】
(1)由分析可知,物质B是二氧化锰,在反应①中作催化剂,其作用是催化作用;
反应①是过氧化氢在二氧化锰的催化作用下分解生成水和氧气,反应的文字表达式为:过氧化氢水+氧气;
(2)D为氧气,具有助燃性,检验氧气的方法为:将带火星的木条伸入集气瓶,若木条复燃,证明是氧气;
(3)若E为铁丝,反应②是铁和氧气在点燃的条件下生成四氧化三铁,实验现象为:剧烈燃烧,火星四射,放出大量热,生成黑色固体;
(4)若F为二氧化碳,氧气只能提供氧元素,所以E中必然含有的元素是碳元素。
19.P+O2P2O5 A 反应不是在密闭体系中进行,有二氧化碳逸出
【详解】
(1)红磷(P)在氧气(O2)中燃烧生成五氧化二磷(P2O5),因此此反应的符号表达式为P+O2P2O5
(2)A和B两个实验中,都是有气体参加或者生成的反应。在有气体参与的化学反应想验证质量守恒定律,必须是在密闭的条件下验证。其中A为密闭条件,而B为开放条件。故反应后平衡的为A;又B是开放条件且反应后有气二氧化碳体生成,因此B不能平衡。
故答案为(1). P+O2P2O5;(2). A;(3). 反应不是在密闭体系中进行,有二氧化碳逸出
20.碳、氢 水
【详解】
根据点燃酒精灯,在火焰上方罩一个内壁沾有澄清石灰水的小烧杯,观察到澄清石灰水变浑浊,证明生成了二氧化碳,由质量守恒定律可知,酒精中含有碳元素;用一只干冷的小烧杯罩在火焰上方,观察到烧杯内壁出现一些小液滴,说明有水生成,由质量守恒定律可知,酒精中含有氢元素。酒精中一定含有碳、氢元素;作出上述判断的依据之一是认为烧杯内壁附着的小液滴是水。
21.B;CD;5;分解;7:1
【详解】
根据质量守恒定律可知,x=5g+112g+16g+4g-32g-100g=5g;
(1)反应前后,C、D的质量增大,是生成物;B质量减轻,是反应物;
(2)表中“x”值为5;
(3)该反应是B→C+D,故该反应是分解反应;
(4)B、C两种物质变化的质量比为112g:(32-16)g=7:1。
22.70%;56
【详解】
①三氧化二铁中铁元素的质量分数为: ;
②根据反应前后元素的种类、质量不变,氧化铁中铁元素的质量与得到纯铁的质量相同,含Fe2O380%的赤铁矿100吨,可炼得纯铁:100吨×80%×70%=56吨。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
