课题1 第1课时 空气是由什么组成的(课件)
文档属性
| 名称 | 课题1 第1课时 空气是由什么组成的(课件) |

|
|
| 格式 | ppt | ||
| 文件大小 | 618.5KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-09 00:00:00 | ||
图片预览





文档简介
(共18张PPT)
课题1 空气
第1课时 空气是由什么组成的
第二单元 我们周围的空气
观察与思考
有一种物质,“看不见,摸不着,不香不臭没味道,说它宝贵到处有,动物植物离不了” 。猜猜看,这是什么呢?
空气
学习目标
认知与了解
掌握测定空气中氧气的体积分数的实验方法
2.了解空气的主要成分,各成分占空气体积的体积分数
3.知道物质的组成;明确概念,能区分混合物和纯净物
拉瓦锡探究空气成分的实验
一
观察与思考
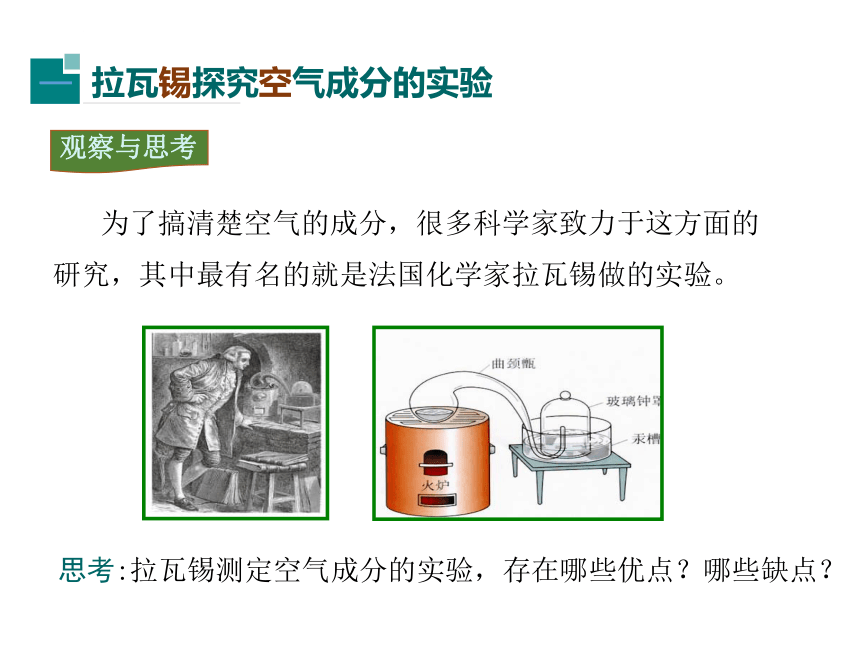
为了搞清楚空气的成分,很多科学家致力于这方面的研究,其中最有名的就是法国化学家拉瓦锡做的实验。
思考:拉瓦锡测定空气成分的实验,存在哪些优点?哪些缺点?
实验与探究
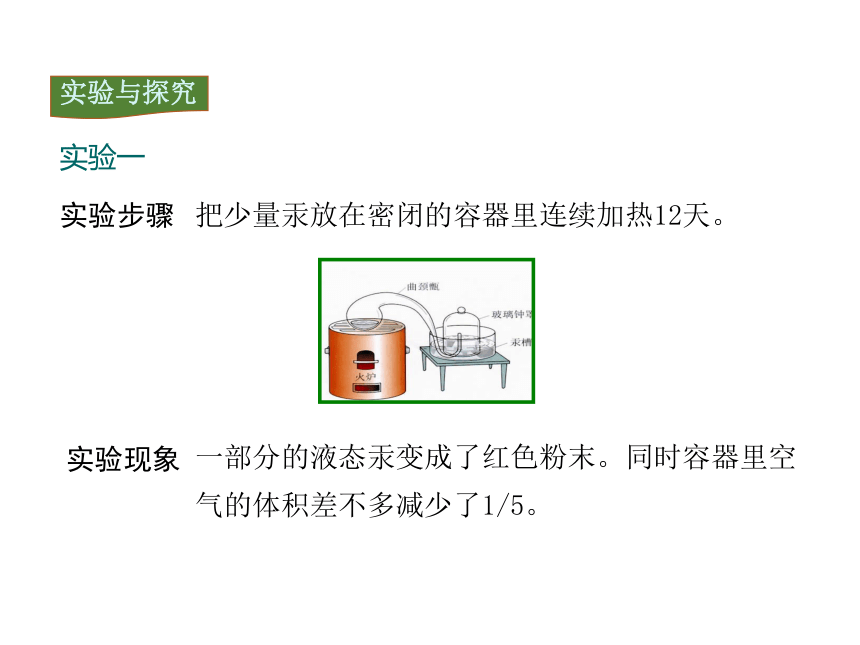
实验步骤
把少量汞放在密闭的容器里连续加热12天。
实验现象
一部分的液态汞变成了红色粉末。同时容器里空气的体积差不多减少了1/5。
实验一
实验与探究
实验步骤
把汞表面上所生成的红色粉末收集起来,放在另一个较小的容器里再加强热。
实验现象
红色粉末又生成了银白色物质和能使带火星木条复燃的气体。
实验二
实验结论
空气由氮气和氧气组成,其中氧气约占空气总体积1/5的结论。
交流与讨论
优点
科学家用严肃认真的科学态度进行反复的实验。
缺点
实验时间较长,操作装置比较复杂,且实验过程中对环境有污染。
拉瓦锡测定空气成分的实验
探究空气成分的实验
二
观察与思考
实验原理
利用红磷燃烧消耗密闭容器内空气中的氧气,使密闭容器内压强减小,在大气压的作用下,水进入容器,进入容器内水的体积即为减少的氧气的体积
实验装置
①仪器:集气瓶、橡胶塞、燃烧匙、导气管、
乳胶管、弹簧夹、烧杯、酒精灯及火柴
②药品:红磷、水
实验与探究
实验步骤
①连接装置并检查装置的气密性;
②在集气瓶内装入少量的水,再把剩余的容积分成五等份,
并用橡皮筋做上记号;
③用弹簧夹夹紧乳胶管,点燃燃烧匙内的红磷,立即伸入瓶
中,并把塞子塞紧;
④燃烧结束并冷却至室温后,打开弹簧夹。
实验与探究
实验现象
①红磷燃烧,发出黄色火焰,有大量白烟生成,放出热量;
②冷却后,打开弹簧夹,水沿导管进入集气瓶,进入集气瓶
内水的体积约占集气瓶内空气总体积的1/5。
实验分析
实验与探究
实验结论
空气中氧气约占空气总体积的1/5。
注意事项
①红磷要过量; ②装置必须密封;
③完全冷却后打开弹簧夹; ④插入燃烧匙的速度要快;
⑤弹簧夹要夹紧; ⑥集气瓶内加入少量水
⑦实验所用药品一般为红磷,不能用硫、木炭、铁丝等物质代替。
交流与讨论
1.上述实验结束后集气瓶内剩余的气体具有哪些性质?
2.利用燃烧法测定空气中氧气的含量的原理我们还可以设计
出其他的装置图吗?
归纳与小结
成分 氮气N2 氧气O2 稀有气体 二氧化碳CO2 其他气体和杂质
体积分数 78% 21% 0.94% 0.03% 0.03%
空气的成分(按体积分数计算)
纯净物和混合物
三
观察与思考
物质按种类如何划分?
由两种或两种以上的物质混合而成的物质叫作混合物。
只由一种物质组成的物质叫作纯净物。
它们之间有怎样的联系呢?
交流与讨论
纯净物 混合物
特性
表示方法
举例
联系
有固定的组成和性质,如熔点、沸点等
没有固定的组成和性质,各物质都保持各自的性质
可用化学符号表示,如氮气(N2)、二氧化碳(CO2)等
不能用固定的化学符号来表示
氧气(O2)、硫(S)、一氧化碳(CO)等
空气、稀有气体、海水、糖水等
混合物 纯净物
分离、提纯
混合
一、空气中氧气含量的测定
实验现象:红磷燃烧产生大量白烟、放出热量,水进入集气瓶的体积约占集气瓶容积的1/5
反应的文字表达式:红磷+氧气 五氧化二磷
实验结论:氧气约占空气体积的1/5
二、空气的成分及含量
按体积分数:氮气78%,氧气21%,稀有气体0.94%,二氧化碳0.03%,其他气体和杂质0.03%
三、纯净物和混合物
1.纯净物:只由一种物质组成
2.混合物:由多种物质组成
点燃
归纳与小结
1.夏天从冰箱里拿出一瓶饮料,放在空气中,饮料外壁会潮湿,说明空气中含有( )
A.氮气 B.氧气
C.水蒸气 D.二氧化碳
C
知识与拓展
巩固与提高
2.在一充满空气的瓶子中,要将其中的氧气除去,又不增加其他气体的成分。下列物质在瓶中燃烧可达到目的的是( )
A.木灰 B.硫磺 C.铁丝 D.红磷
D
知识与拓展
巩固与提高
课题1 空气
第1课时 空气是由什么组成的
第二单元 我们周围的空气
观察与思考
有一种物质,“看不见,摸不着,不香不臭没味道,说它宝贵到处有,动物植物离不了” 。猜猜看,这是什么呢?
空气
学习目标
认知与了解
掌握测定空气中氧气的体积分数的实验方法
2.了解空气的主要成分,各成分占空气体积的体积分数
3.知道物质的组成;明确概念,能区分混合物和纯净物
拉瓦锡探究空气成分的实验
一
观察与思考
为了搞清楚空气的成分,很多科学家致力于这方面的研究,其中最有名的就是法国化学家拉瓦锡做的实验。
思考:拉瓦锡测定空气成分的实验,存在哪些优点?哪些缺点?
实验与探究
实验步骤
把少量汞放在密闭的容器里连续加热12天。
实验现象
一部分的液态汞变成了红色粉末。同时容器里空气的体积差不多减少了1/5。
实验一
实验与探究
实验步骤
把汞表面上所生成的红色粉末收集起来,放在另一个较小的容器里再加强热。
实验现象
红色粉末又生成了银白色物质和能使带火星木条复燃的气体。
实验二
实验结论
空气由氮气和氧气组成,其中氧气约占空气总体积1/5的结论。
交流与讨论
优点
科学家用严肃认真的科学态度进行反复的实验。
缺点
实验时间较长,操作装置比较复杂,且实验过程中对环境有污染。
拉瓦锡测定空气成分的实验
探究空气成分的实验
二
观察与思考
实验原理
利用红磷燃烧消耗密闭容器内空气中的氧气,使密闭容器内压强减小,在大气压的作用下,水进入容器,进入容器内水的体积即为减少的氧气的体积
实验装置
①仪器:集气瓶、橡胶塞、燃烧匙、导气管、
乳胶管、弹簧夹、烧杯、酒精灯及火柴
②药品:红磷、水
实验与探究
实验步骤
①连接装置并检查装置的气密性;
②在集气瓶内装入少量的水,再把剩余的容积分成五等份,
并用橡皮筋做上记号;
③用弹簧夹夹紧乳胶管,点燃燃烧匙内的红磷,立即伸入瓶
中,并把塞子塞紧;
④燃烧结束并冷却至室温后,打开弹簧夹。
实验与探究
实验现象
①红磷燃烧,发出黄色火焰,有大量白烟生成,放出热量;
②冷却后,打开弹簧夹,水沿导管进入集气瓶,进入集气瓶
内水的体积约占集气瓶内空气总体积的1/5。
实验分析
实验与探究
实验结论
空气中氧气约占空气总体积的1/5。
注意事项
①红磷要过量; ②装置必须密封;
③完全冷却后打开弹簧夹; ④插入燃烧匙的速度要快;
⑤弹簧夹要夹紧; ⑥集气瓶内加入少量水
⑦实验所用药品一般为红磷,不能用硫、木炭、铁丝等物质代替。
交流与讨论
1.上述实验结束后集气瓶内剩余的气体具有哪些性质?
2.利用燃烧法测定空气中氧气的含量的原理我们还可以设计
出其他的装置图吗?
归纳与小结
成分 氮气N2 氧气O2 稀有气体 二氧化碳CO2 其他气体和杂质
体积分数 78% 21% 0.94% 0.03% 0.03%
空气的成分(按体积分数计算)
纯净物和混合物
三
观察与思考
物质按种类如何划分?
由两种或两种以上的物质混合而成的物质叫作混合物。
只由一种物质组成的物质叫作纯净物。
它们之间有怎样的联系呢?
交流与讨论
纯净物 混合物
特性
表示方法
举例
联系
有固定的组成和性质,如熔点、沸点等
没有固定的组成和性质,各物质都保持各自的性质
可用化学符号表示,如氮气(N2)、二氧化碳(CO2)等
不能用固定的化学符号来表示
氧气(O2)、硫(S)、一氧化碳(CO)等
空气、稀有气体、海水、糖水等
混合物 纯净物
分离、提纯
混合
一、空气中氧气含量的测定
实验现象:红磷燃烧产生大量白烟、放出热量,水进入集气瓶的体积约占集气瓶容积的1/5
反应的文字表达式:红磷+氧气 五氧化二磷
实验结论:氧气约占空气体积的1/5
二、空气的成分及含量
按体积分数:氮气78%,氧气21%,稀有气体0.94%,二氧化碳0.03%,其他气体和杂质0.03%
三、纯净物和混合物
1.纯净物:只由一种物质组成
2.混合物:由多种物质组成
点燃
归纳与小结
1.夏天从冰箱里拿出一瓶饮料,放在空气中,饮料外壁会潮湿,说明空气中含有( )
A.氮气 B.氧气
C.水蒸气 D.二氧化碳
C
知识与拓展
巩固与提高
2.在一充满空气的瓶子中,要将其中的氧气除去,又不增加其他气体的成分。下列物质在瓶中燃烧可达到目的的是( )
A.木灰 B.硫磺 C.铁丝 D.红磷
D
知识与拓展
巩固与提高
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
