山东省泰安市2021-2022学年九年级上学期期中考试化学试题(word版含答案)
文档属性
| 名称 | 山东省泰安市2021-2022学年九年级上学期期中考试化学试题(word版含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 265.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-10 00:00:00 | ||
图片预览


文档简介
第一学期期中学情抽测
初四化学样题
(时间:60分钟;满分100分)
相对原子质量:H1 O16 S32 Na23
一、选择题(本题包括12小题,每小题3分,共36分。每小题只有一个选项符合题意将符合题意的选项序号填入下表相应空格内。)
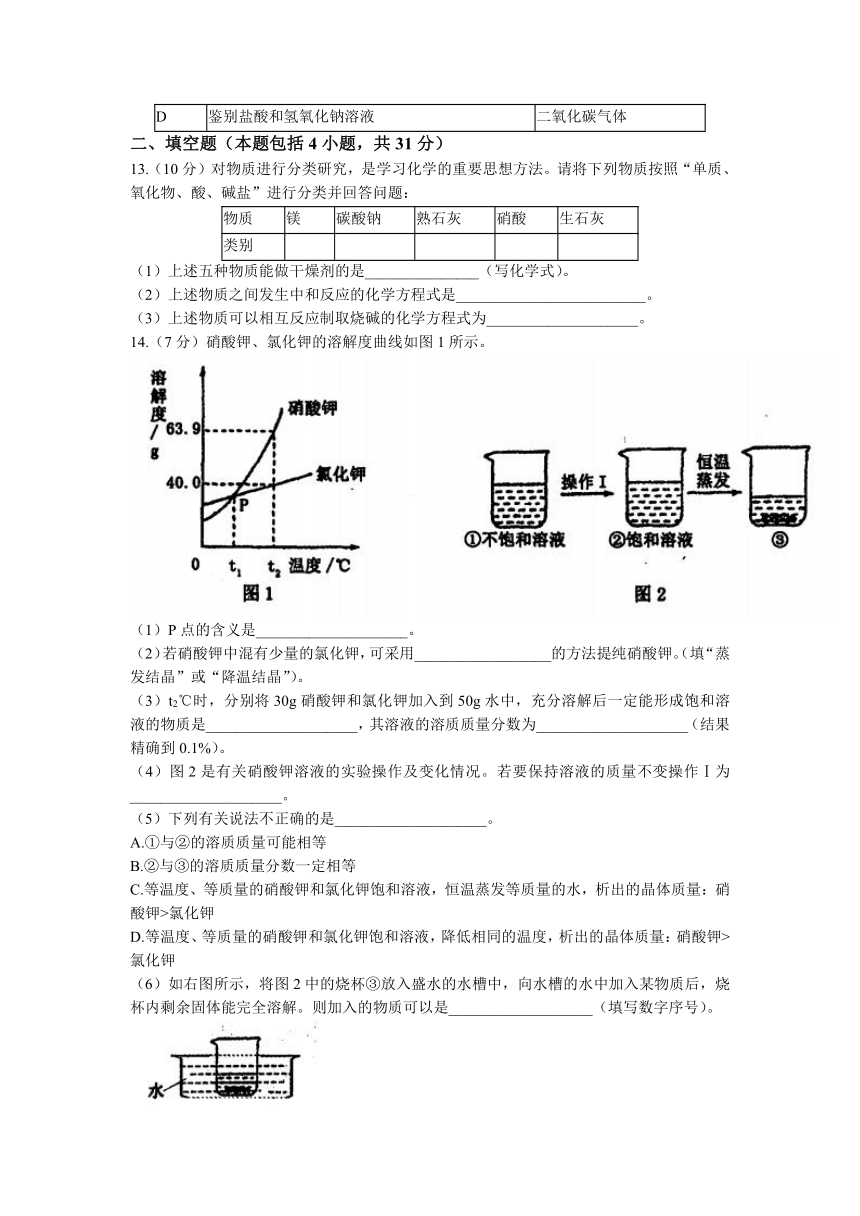
1.下列物质不属于溶液的是
A.啤酒 B.矿泉水 C.汽水 D.液氧
2.下图是物质X溶于水发生解离后的微观示意图,其中能说明X是一种盐的是
A. B. C. D.
3.下列实验操作正确的是
A.测定溶液pH B.配制溶液
C.称量固体 D.稀释浓硫酸
4.下列物质为了防止其变质而需要密封保存的是
A.浓盐酸 B.浓硫酸 C.烧碱 D.石灰石
5.不同品牌的洗手液pH一般不同,25℃时四种洗手液的pH如图所示。下列说法错误的是
A.洗手液a用蒸馏水稀释后pH减小 B.洗手液b的酸性比a弱
C.洗手液c能使石蕊试液变蓝 D.洗手液d和a混合后pH可能等于7
6.关于溶液下列说法错误的是
A.某种溶质的饱和溶液一定比它的不饱和溶液浓
B.均一、稳定的液体不一定是溶液
C.汽油去除油污是因为汽油能溶解油
D.氢氧化钠固体溶于水时温度升高是因为钠离子和氢氧根离子在水中的扩散过程吸收的热量小于水合过程放出的热量
7.下列物质的俗名与化学式及其用途对应完全正确的一组是
A B C D
熟石灰 火碱 食盐 生石灰
Ca(OH)2 Na2CO3 NaCl CaCO3
制备生石灰 制造玻璃 做调味品 做干燥剂
8.服用含氢氧化铝的药物可以治疗胃酸过多症其反应原理是 ,该反应属于
A.分解反应 B.化合反应 C.复分解反应 D.氧化反应
9.物质的性质决定其用途。稀盐酸常用于除铁锈,是利用了酸的一种化学通性,下列酸的用途中也利用了该通性的是
A.用锌粒和稀硫酸制取氢气 B.用氧化铜和稀硫酸制备硫酸铜
C.用稀盐酸除去氯化钠中的碳酸钠 D.用硼酸处理皮肤上沾有的碱
10.有一接近饱和的溶液,下列方法中一定能使其成为饱和溶液的是
①蒸发溶剂②增加溶质⑤降低温度④加热升温
A.①② B.①②③ C.②③ D.①②④
11.右图是a、b、c三种固体物质(不含结晶水)的溶解度曲线。下列叙述正确的是
A.t1℃时,a、c两种物质饱和溶液的溶质质量分数为20%
B.将接近饱和的c物质的溶液变成饱和溶液,可采用加溶质、降温等方法
C.将a、b、c三种物质的饱和溶液从t2℃降温至t1℃,所得溶液中溶质质量分数的大小关系为b>a=c
D.将150ga物质的饱和溶液从t3℃降温至t1℃,可析出30ga物质
12.为了达到实验目的,下列实验方案所选用的试剂正确的是
选项 实验目的 实验方案所用试剂
A 除去生石灰中混有的少量石灰石 足量的稀盐酸
B 除去二氧化碳中混有的水蒸气 足量的氢氧化钠固体
C 鉴别碳酸钙、氢氧化钠和硝酸铵三种固体 适量的水
D 鉴别盐酸和氢氧化钠溶液 二氧化碳气体
二、填空题(本题包括4小题,共31分)
13.(10分)对物质进行分类研究,是学习化学的重要思想方法。请将下列物质按照“单质、氧化物、酸、碱盐”进行分类并回答问题:
物质 镁 碳酸钠 熟石灰 硝酸 生石灰
类别
(1)上述五种物质能做干燥剂的是_______________(写化学式)。
(2)上述物质之间发生中和反应的化学方程式是_________________________。
(3)上述物质可以相互反应制取烧碱的化学方程式为____________________。
14.(7分)硝酸钾、氯化钾的溶解度曲线如图1所示。
(1)P点的含义是____________________。
(2)若硝酸钾中混有少量的氯化钾,可采用__________________的方法提纯硝酸钾。(填“蒸发结晶”或“降温结晶”)。
(3)t2℃时,分别将30g硝酸钾和氯化钾加入到50g水中,充分溶解后一定能形成饱和溶液的物质是____________________,其溶液的溶质质量分数为____________________(结果精确到0.1%)。
(4)图2是有关硝酸钾溶液的实验操作及变化情况。若要保持溶液的质量不变操作Ⅰ为____________________。
(5)下列有关说法不正确的是____________________。
A.①与②的溶质质量可能相等
B.②与③的溶质质量分数一定相等
C.等温度、等质量的硝酸钾和氯化钾饱和溶液,恒温蒸发等质量的水,析出的晶体质量:硝酸钾>氯化钾
D.等温度、等质量的硝酸钾和氯化钾饱和溶液,降低相同的温度,析出的晶体质量:硝酸钾>氯化钾
(6)如右图所示,将图2中的烧杯③放入盛水的水槽中,向水槽的水中加入某物质后,烧杯内剩余固体能完全溶解。则加入的物质可以是___________________(填写数字序号)。
①冰块②生石灰固体③硝酸铵固体④干冰⑤浓硫酸⑥氢氧化钠固体
15.(7分)学习了酸的化学性质后,小华同学以稀硫酸为主题绘制了“多彩酸世界”思维导图。
(1)若用Cu(OH)2实现②的现象,会得到______________色溶液,该反应的化学方程式为___________________。
(2)若想实现③得到浅绿色溶液可选用单质______________(写化学式)。
(3)得到黄色溶液的反应可用于工业除锈,写出该反应的化学方程式___________________。
(4)若想看到⑤的现象,可用__________________溶液(填化学式)与稀硫酸反应。
16.(7分)中和反应是一类重要的化学反应。某同学利用图1装置研究稀盐酸与氢氧化钠溶液反应的过程,并用pH和温度传感器测量反应过程中相关物理量的变化情况,得到图2和图3。
(1)烧杯中发生反应的化学方程式为___________________。
(2)仪器A中溶液的溶质是__________________(填化学式);
(3)图3中V的数值最接近__________________(填“6”、“12”或“16”);
(4)下列说法错误的是___________________(填序号)。
A.图2中b点所示溶液中的溶质是NaCl和NaOH
B.取图2中d点所示溶液加热蒸干所得固体为纯净物
C.图2中c→d所示溶液中NaCl的质量不断增加;
D.图3中e→f变化趋势可说明该反应是放热反应
(5)由图4可知,该反应的微观实质是___________________。
(6)若要证明反应已经进行到d点,除了观察pH和温度变化,还可以向反应后的溶液中加入下列物质中的___________________。(填序号)
A.紫色石蕊试液 B.无色酚酞试液 C.镁条 D.碳酸钠 E.硝酸银溶液
三、实验题(本题包括2小题共23分)
17.(9分)某实验小组利用如图所示仪器进行“配制一定溶质质量分数的氯化钠溶液”的实验:
(1)上图中仪器a的名称是________________;该实验的操作步骤是计算、______________、___________、_____________;按实验要求,图中还缺少的玻璃仪器是______________(填名称),它的作用是______________________________。
(2)小婧按如图的操作称取氯化钠,小民发现小婧的操作有错误。你认为小婧操作中的错误是__________________;她称取的氯化钠实际质量为___________________g。
(3)小民所取蒸馏水的体积如图所示,则该实验小组原计划配制的氯化钠溶液中溶质质量分数为(水的密度为1g/cm3)___________________。
18.(14分)学习了常见的酸和碱后,同学们对碱的化学性质进行整理归纳并进行如下实验活动。
【验证实验】
序号 实验一 实验二 实验三 实验四
实验内容
实验现象 溶液变___________色 产生蓝色沉淀 无明显现象 无明显现象
分析与结论 Ca(OH)2能与指示剂作用 反应的化学方程式为_____________ 无法确定是否发生反应 无法确定是否发生反应
请填写实验记录中空缺的内容①________________②____________________。
【发现问题】
通过实验,同学们发现实验三、实验四无明显现象无法确定是否发生了化学反应。于是继续进行探究。
【探究实验】
Ⅰ.取少量实验三中的剩余溶液,滴加______________试液,溶液仍为无色,证明稀盐酸和Ca(OH)2溶液发生了化学反应,判断依据是溶液中_____________完全反应了。
Ⅱ.取少量实验四中的剩余溶液,滴加足量的_____________溶液,观察到产生气体,证明CO2和NaOH溶液发生了化学反应。请写出产生气体的反应的化学方程式______________________。
【拓展延伸】
同学们针对实验四又进行了如图所示的对比实验:
Ⅲ.将充满CO2的两支相同的试管分别倒扣入盛有不同液体(液体温度相同)的两个烧杯中,根据试管内液面上升的高度不同,确定CO2和NaOH发生了化学反应。图中横线处对右侧烧杯中液体的说明应填写______________________;CO2和NaOH发生反应的化学方程式为_______________________。
【总结提升】
(1)通过上述实验验证了碱溶液的化学性质。
(2)没有明显现象的化学反应,可以依据A检验反应物消失(或减少)或B。证明新物质生成这两种思路,利用间接观察法证明反应发生。上述三个实验分别是依据哪种思路设计实验方案的:Ⅰ_______________;Ⅱ_______________;Ⅲ_______________(填“A”或“B”)。
四、计算题:(本题包括2小题共10分)
19.(4分)过氧化氢是一种有效的防疫新冠病毒的消毒剂。现有一瓶新售的过氧化氢溶液,标签如图所示,若要配制1500g溶质的质量分数为3%的医用过氧化氢溶液,需用这种过氧化氢溶液的质量是________________g,需要加水_________________g。
(直接填写答案,无需写出计算过程)
20.(6分)学习小组的同学通过下面实验测定一瓶失去标签的稀硫酸中溶质的质量分数。
请完成下列分析与计算:
(1)反应中用去稀硫酸的质量____________________g。
(2)计算稀硫酸中溶质的质量分数。(写出计算过程)
初四化学试题参考答案及评分标准
一、选择题(本题包括12小题,每题3分,共36分)
题号 1 2 3 4 5 6 7 8 9 10 11 12
答案 D B A C A A C C B A D C
二、填空题:(共31分,每空1分化学方程式2分)
13.
物质 镁 碳酸钠 熟石灰 硝酸 生石灰
类别 单质 盐 碱 酸 氧化物
(1)CaO
(2)
(3)
14.(1)t1℃时,硝酸钾和氯化钾的溶解度相同(2)降温结晶
(3)氯化钾;28.6%(4)降低温度(5)c(6)②⑤⑥
15(1)蓝; (2)Fe
(3) (4)BaCl2(或Ba( OH)2或 Ba( NO3)2)
16(1) (2)HCl(3)12 (4)C (5)
(6)ACD
三、实验题(共23分每空1分,化学方程式2分)
17.(1)烧杯;称量、溶解、装瓶存放;玻璃棒;搅拌,加速溶解。
(2)左码右物称量药品;12(3)18%
18.【验证实验】①红②
【探究实验】Ⅰ:酚酞;氢氧化钙(或填Ca(OH)2或OH-)
Ⅱ:HCl(或H2SO4等);
【拓展延伸】50mL水;
【总结提升】Ⅰ:A Ⅱ:B Ⅲ:A
四、计算题(共10分)
19(4分)150;1350
20.(6分)(1)20g
(2)解:设参加反应的H2SO4的溶质质量分数为x
答:稀硫酸中溶质的质量分数为24.5%。
初四化学样题
(时间:60分钟;满分100分)
相对原子质量:H1 O16 S32 Na23
一、选择题(本题包括12小题,每小题3分,共36分。每小题只有一个选项符合题意将符合题意的选项序号填入下表相应空格内。)
1.下列物质不属于溶液的是
A.啤酒 B.矿泉水 C.汽水 D.液氧
2.下图是物质X溶于水发生解离后的微观示意图,其中能说明X是一种盐的是
A. B. C. D.
3.下列实验操作正确的是
A.测定溶液pH B.配制溶液
C.称量固体 D.稀释浓硫酸
4.下列物质为了防止其变质而需要密封保存的是
A.浓盐酸 B.浓硫酸 C.烧碱 D.石灰石
5.不同品牌的洗手液pH一般不同,25℃时四种洗手液的pH如图所示。下列说法错误的是
A.洗手液a用蒸馏水稀释后pH减小 B.洗手液b的酸性比a弱
C.洗手液c能使石蕊试液变蓝 D.洗手液d和a混合后pH可能等于7
6.关于溶液下列说法错误的是
A.某种溶质的饱和溶液一定比它的不饱和溶液浓
B.均一、稳定的液体不一定是溶液
C.汽油去除油污是因为汽油能溶解油
D.氢氧化钠固体溶于水时温度升高是因为钠离子和氢氧根离子在水中的扩散过程吸收的热量小于水合过程放出的热量
7.下列物质的俗名与化学式及其用途对应完全正确的一组是
A B C D
熟石灰 火碱 食盐 生石灰
Ca(OH)2 Na2CO3 NaCl CaCO3
制备生石灰 制造玻璃 做调味品 做干燥剂
8.服用含氢氧化铝的药物可以治疗胃酸过多症其反应原理是 ,该反应属于
A.分解反应 B.化合反应 C.复分解反应 D.氧化反应
9.物质的性质决定其用途。稀盐酸常用于除铁锈,是利用了酸的一种化学通性,下列酸的用途中也利用了该通性的是
A.用锌粒和稀硫酸制取氢气 B.用氧化铜和稀硫酸制备硫酸铜
C.用稀盐酸除去氯化钠中的碳酸钠 D.用硼酸处理皮肤上沾有的碱
10.有一接近饱和的溶液,下列方法中一定能使其成为饱和溶液的是
①蒸发溶剂②增加溶质⑤降低温度④加热升温
A.①② B.①②③ C.②③ D.①②④
11.右图是a、b、c三种固体物质(不含结晶水)的溶解度曲线。下列叙述正确的是
A.t1℃时,a、c两种物质饱和溶液的溶质质量分数为20%
B.将接近饱和的c物质的溶液变成饱和溶液,可采用加溶质、降温等方法
C.将a、b、c三种物质的饱和溶液从t2℃降温至t1℃,所得溶液中溶质质量分数的大小关系为b>a=c
D.将150ga物质的饱和溶液从t3℃降温至t1℃,可析出30ga物质
12.为了达到实验目的,下列实验方案所选用的试剂正确的是
选项 实验目的 实验方案所用试剂
A 除去生石灰中混有的少量石灰石 足量的稀盐酸
B 除去二氧化碳中混有的水蒸气 足量的氢氧化钠固体
C 鉴别碳酸钙、氢氧化钠和硝酸铵三种固体 适量的水
D 鉴别盐酸和氢氧化钠溶液 二氧化碳气体
二、填空题(本题包括4小题,共31分)
13.(10分)对物质进行分类研究,是学习化学的重要思想方法。请将下列物质按照“单质、氧化物、酸、碱盐”进行分类并回答问题:
物质 镁 碳酸钠 熟石灰 硝酸 生石灰
类别
(1)上述五种物质能做干燥剂的是_______________(写化学式)。
(2)上述物质之间发生中和反应的化学方程式是_________________________。
(3)上述物质可以相互反应制取烧碱的化学方程式为____________________。
14.(7分)硝酸钾、氯化钾的溶解度曲线如图1所示。
(1)P点的含义是____________________。
(2)若硝酸钾中混有少量的氯化钾,可采用__________________的方法提纯硝酸钾。(填“蒸发结晶”或“降温结晶”)。
(3)t2℃时,分别将30g硝酸钾和氯化钾加入到50g水中,充分溶解后一定能形成饱和溶液的物质是____________________,其溶液的溶质质量分数为____________________(结果精确到0.1%)。
(4)图2是有关硝酸钾溶液的实验操作及变化情况。若要保持溶液的质量不变操作Ⅰ为____________________。
(5)下列有关说法不正确的是____________________。
A.①与②的溶质质量可能相等
B.②与③的溶质质量分数一定相等
C.等温度、等质量的硝酸钾和氯化钾饱和溶液,恒温蒸发等质量的水,析出的晶体质量:硝酸钾>氯化钾
D.等温度、等质量的硝酸钾和氯化钾饱和溶液,降低相同的温度,析出的晶体质量:硝酸钾>氯化钾
(6)如右图所示,将图2中的烧杯③放入盛水的水槽中,向水槽的水中加入某物质后,烧杯内剩余固体能完全溶解。则加入的物质可以是___________________(填写数字序号)。
①冰块②生石灰固体③硝酸铵固体④干冰⑤浓硫酸⑥氢氧化钠固体
15.(7分)学习了酸的化学性质后,小华同学以稀硫酸为主题绘制了“多彩酸世界”思维导图。
(1)若用Cu(OH)2实现②的现象,会得到______________色溶液,该反应的化学方程式为___________________。
(2)若想实现③得到浅绿色溶液可选用单质______________(写化学式)。
(3)得到黄色溶液的反应可用于工业除锈,写出该反应的化学方程式___________________。
(4)若想看到⑤的现象,可用__________________溶液(填化学式)与稀硫酸反应。
16.(7分)中和反应是一类重要的化学反应。某同学利用图1装置研究稀盐酸与氢氧化钠溶液反应的过程,并用pH和温度传感器测量反应过程中相关物理量的变化情况,得到图2和图3。
(1)烧杯中发生反应的化学方程式为___________________。
(2)仪器A中溶液的溶质是__________________(填化学式);
(3)图3中V的数值最接近__________________(填“6”、“12”或“16”);
(4)下列说法错误的是___________________(填序号)。
A.图2中b点所示溶液中的溶质是NaCl和NaOH
B.取图2中d点所示溶液加热蒸干所得固体为纯净物
C.图2中c→d所示溶液中NaCl的质量不断增加;
D.图3中e→f变化趋势可说明该反应是放热反应
(5)由图4可知,该反应的微观实质是___________________。
(6)若要证明反应已经进行到d点,除了观察pH和温度变化,还可以向反应后的溶液中加入下列物质中的___________________。(填序号)
A.紫色石蕊试液 B.无色酚酞试液 C.镁条 D.碳酸钠 E.硝酸银溶液
三、实验题(本题包括2小题共23分)
17.(9分)某实验小组利用如图所示仪器进行“配制一定溶质质量分数的氯化钠溶液”的实验:
(1)上图中仪器a的名称是________________;该实验的操作步骤是计算、______________、___________、_____________;按实验要求,图中还缺少的玻璃仪器是______________(填名称),它的作用是______________________________。
(2)小婧按如图的操作称取氯化钠,小民发现小婧的操作有错误。你认为小婧操作中的错误是__________________;她称取的氯化钠实际质量为___________________g。
(3)小民所取蒸馏水的体积如图所示,则该实验小组原计划配制的氯化钠溶液中溶质质量分数为(水的密度为1g/cm3)___________________。
18.(14分)学习了常见的酸和碱后,同学们对碱的化学性质进行整理归纳并进行如下实验活动。
【验证实验】
序号 实验一 实验二 实验三 实验四
实验内容
实验现象 溶液变___________色 产生蓝色沉淀 无明显现象 无明显现象
分析与结论 Ca(OH)2能与指示剂作用 反应的化学方程式为_____________ 无法确定是否发生反应 无法确定是否发生反应
请填写实验记录中空缺的内容①________________②____________________。
【发现问题】
通过实验,同学们发现实验三、实验四无明显现象无法确定是否发生了化学反应。于是继续进行探究。
【探究实验】
Ⅰ.取少量实验三中的剩余溶液,滴加______________试液,溶液仍为无色,证明稀盐酸和Ca(OH)2溶液发生了化学反应,判断依据是溶液中_____________完全反应了。
Ⅱ.取少量实验四中的剩余溶液,滴加足量的_____________溶液,观察到产生气体,证明CO2和NaOH溶液发生了化学反应。请写出产生气体的反应的化学方程式______________________。
【拓展延伸】
同学们针对实验四又进行了如图所示的对比实验:
Ⅲ.将充满CO2的两支相同的试管分别倒扣入盛有不同液体(液体温度相同)的两个烧杯中,根据试管内液面上升的高度不同,确定CO2和NaOH发生了化学反应。图中横线处对右侧烧杯中液体的说明应填写______________________;CO2和NaOH发生反应的化学方程式为_______________________。
【总结提升】
(1)通过上述实验验证了碱溶液的化学性质。
(2)没有明显现象的化学反应,可以依据A检验反应物消失(或减少)或B。证明新物质生成这两种思路,利用间接观察法证明反应发生。上述三个实验分别是依据哪种思路设计实验方案的:Ⅰ_______________;Ⅱ_______________;Ⅲ_______________(填“A”或“B”)。
四、计算题:(本题包括2小题共10分)
19.(4分)过氧化氢是一种有效的防疫新冠病毒的消毒剂。现有一瓶新售的过氧化氢溶液,标签如图所示,若要配制1500g溶质的质量分数为3%的医用过氧化氢溶液,需用这种过氧化氢溶液的质量是________________g,需要加水_________________g。
(直接填写答案,无需写出计算过程)
20.(6分)学习小组的同学通过下面实验测定一瓶失去标签的稀硫酸中溶质的质量分数。
请完成下列分析与计算:
(1)反应中用去稀硫酸的质量____________________g。
(2)计算稀硫酸中溶质的质量分数。(写出计算过程)
初四化学试题参考答案及评分标准
一、选择题(本题包括12小题,每题3分,共36分)
题号 1 2 3 4 5 6 7 8 9 10 11 12
答案 D B A C A A C C B A D C
二、填空题:(共31分,每空1分化学方程式2分)
13.
物质 镁 碳酸钠 熟石灰 硝酸 生石灰
类别 单质 盐 碱 酸 氧化物
(1)CaO
(2)
(3)
14.(1)t1℃时,硝酸钾和氯化钾的溶解度相同(2)降温结晶
(3)氯化钾;28.6%(4)降低温度(5)c(6)②⑤⑥
15(1)蓝; (2)Fe
(3) (4)BaCl2(或Ba( OH)2或 Ba( NO3)2)
16(1) (2)HCl(3)12 (4)C (5)
(6)ACD
三、实验题(共23分每空1分,化学方程式2分)
17.(1)烧杯;称量、溶解、装瓶存放;玻璃棒;搅拌,加速溶解。
(2)左码右物称量药品;12(3)18%
18.【验证实验】①红②
【探究实验】Ⅰ:酚酞;氢氧化钙(或填Ca(OH)2或OH-)
Ⅱ:HCl(或H2SO4等);
【拓展延伸】50mL水;
【总结提升】Ⅰ:A Ⅱ:B Ⅲ:A
四、计算题(共10分)
19(4分)150;1350
20.(6分)(1)20g
(2)解:设参加反应的H2SO4的溶质质量分数为x
答:稀硫酸中溶质的质量分数为24.5%。
同课章节目录
