第五单元 定量研究化学反应 测试题-2021-2022学年九年级化学鲁教版上册(有答案)
文档属性
| 名称 | 第五单元 定量研究化学反应 测试题-2021-2022学年九年级化学鲁教版上册(有答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 144.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-10 00:00:00 | ||
图片预览


文档简介
第五单元《定量研究化学反应》测试题
一、单选题
1.水蒸气通过红热的铁粉,发生的反应为3Fe+4H2O(气)X+4H2,则X为
A.FeO B.Fe2O3 C.Fe3O4 D.Fe(OH)2
2.根据化学方程式不能获得的信息是
A.反应中的反应物和生成物 B.化学反应速率的快慢程度
C.各反应物、生成物之间的质量比 D.反应发生所需要的条件
3.由元素X、Y组成的两种物质经化合生成Z,化学方程式为:3X2+2YX=2Z,则Z的化学式是
A.X3Y2 B.XY C.X4Y D.YX4
4.自然科学的发展使我们的生活变得丰富多彩。通过化学的学习,你觉得下列情况中不可能实现的是
A.通过化学反应使水直接变成汽油 B.用肥皂水区分硬水和软水
C.用人工的方法合成结晶牛胰岛素 D.通过分离液态空气法得到氧气
5.在反应A+B→C+D中,若15gA与10gB完全反应没有剩余,则生成的C和D的质量总和为
A.15g B.10g C.25 g D.5g
6.氯化钠是重要的化工原料,是氯碱工业的基础。电解饱和食盐水一定不能得到的物质是
A.H2 B.Cl2 C.Na2CO3 D.NaOH
7.下列叙述完全符合质量守恒定律的是
A.水结成冰前后,质量保持不变
B.50mL水和50 mL乙醇混合后总体积小于100 mL
C.在100g30%过氧化氢溶液中,含有30g过氧化氢和70g水
D.1.2g碳与3.2g氧气恰好完全反应可生成4.4g二氧化碳
8.甲烷是天然气的主要成分,其完全燃烧的化学方程式为CH4+2O2CO2+2H2O,根据该化学方程式无法获取的信息是
A.反应物和生成物 B.反应所需条件
C.反应物的颜色和状态 D.生成物的分子个数比
9.推理是学习化学常用的方法,下列推理正确的是
A.单质由同种元素组成,则只含有一种元素的物质一定是单质
B.化学变化中常伴随发光放热的现象所以有发光放热现象产生时一定发生了化学变化
C.同种元素的质子数相同,则质子数相同的粒子一定属于同种元素
D.蜡烛燃烧生成二氧化碳和水,所以蜡烛组成中一定有碳元素和氢元素
10.下列说法错误的是
A.化学反应前后,物质的种类一定发生改变
B.化学反应前后,分子的种类一定发生改变
C.化学反应前后,原子的数目一定不发生改变
D.化学反应前后,原子团一定发生改变
11.在一个密闭容器中有X、Y、Z、Q四种物质,一定条件下充分反应,测得反应前后各物质的质量如下表所示:已知X和Q两种物质的相对分子质量均为M,下列推理中正确的是
X Y Z Q
反应前的质量/g 8 10 1 21
反应后的质量/g 0 21 待测 9
A.反应后物质Z的质量为9g B.反应中物质Y与Q的质量比为1:1
C.反应生成Y的质量为11g D.该反成的化学方程式中,物质X与Q的化学计量数之比为3:2
12.向一密闭容器中加入甲、乙、丙、丁4种物质,在一定条件下发生化学反应,测得有关数据如图,下列说法不正确的是
A.a的数值是4 B.乙和丙的质量变化比为5:3
C.该反应是化合反应 D.丁可能是该反应的催化剂
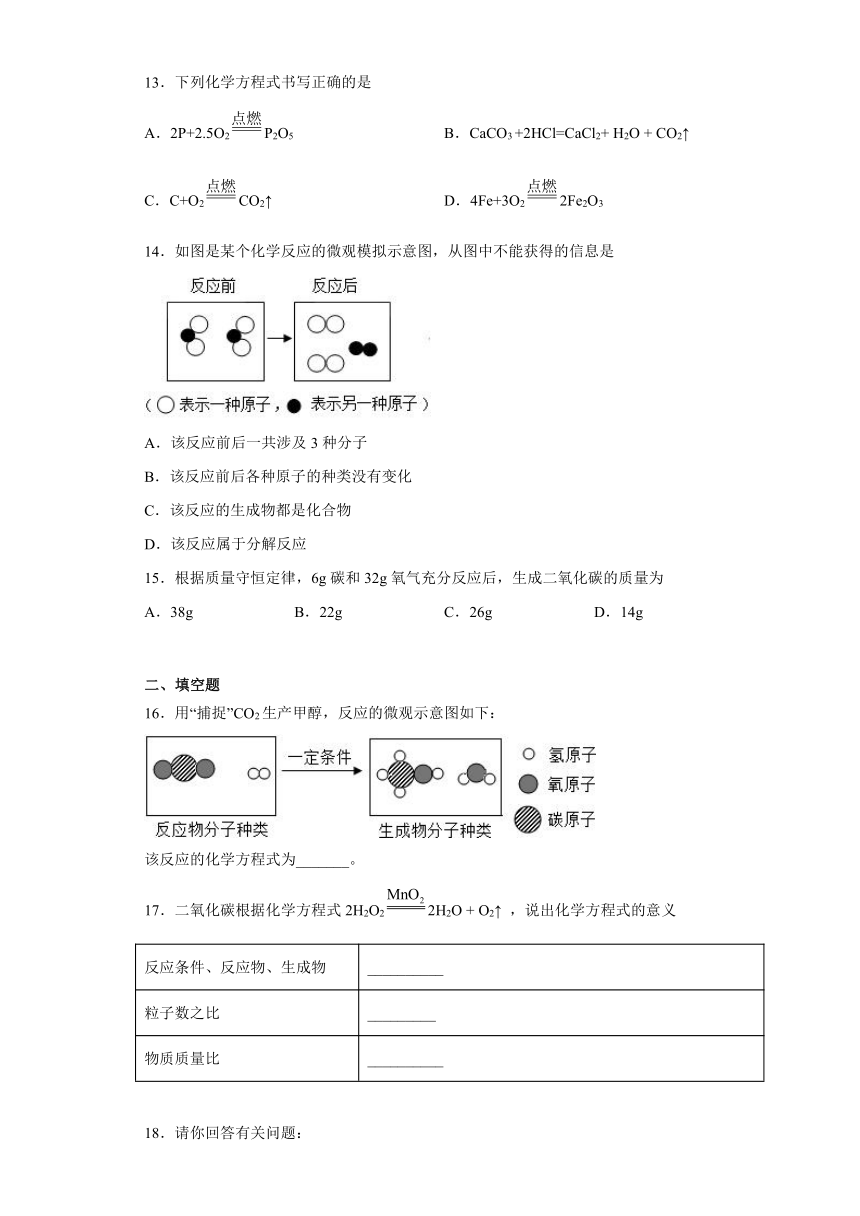
13.下列化学方程式书写正确的是
A.2P+2.5O2P2O5 B.CaCO3 +2HCl=CaCl2+ H2O + CO2↑
C.C+O2CO2↑ D.4Fe+3O22Fe2O3
14.如图是某个化学反应的微观模拟示意图,从图中不能获得的信息是
A.该反应前后一共涉及3种分子
B.该反应前后各种原子的种类没有变化
C.该反应的生成物都是化合物
D.该反应属于分解反应
15.根据质量守恒定律,6g碳和32g氧气充分反应后,生成二氧化碳的质量为
A.38g B.22g C.26g D.14g
二、填空题
16.用“捕捉”CO2生产甲醇,反应的微观示意图如下:
该反应的化学方程式为_______。
17.二氧化碳根据化学方程式2H2O22H2O + O2↑ ,说出化学方程式的意义
反应条件、反应物、生成物 __________
粒子数之比 _________
物质质量比 __________
18.请你回答有关问题:
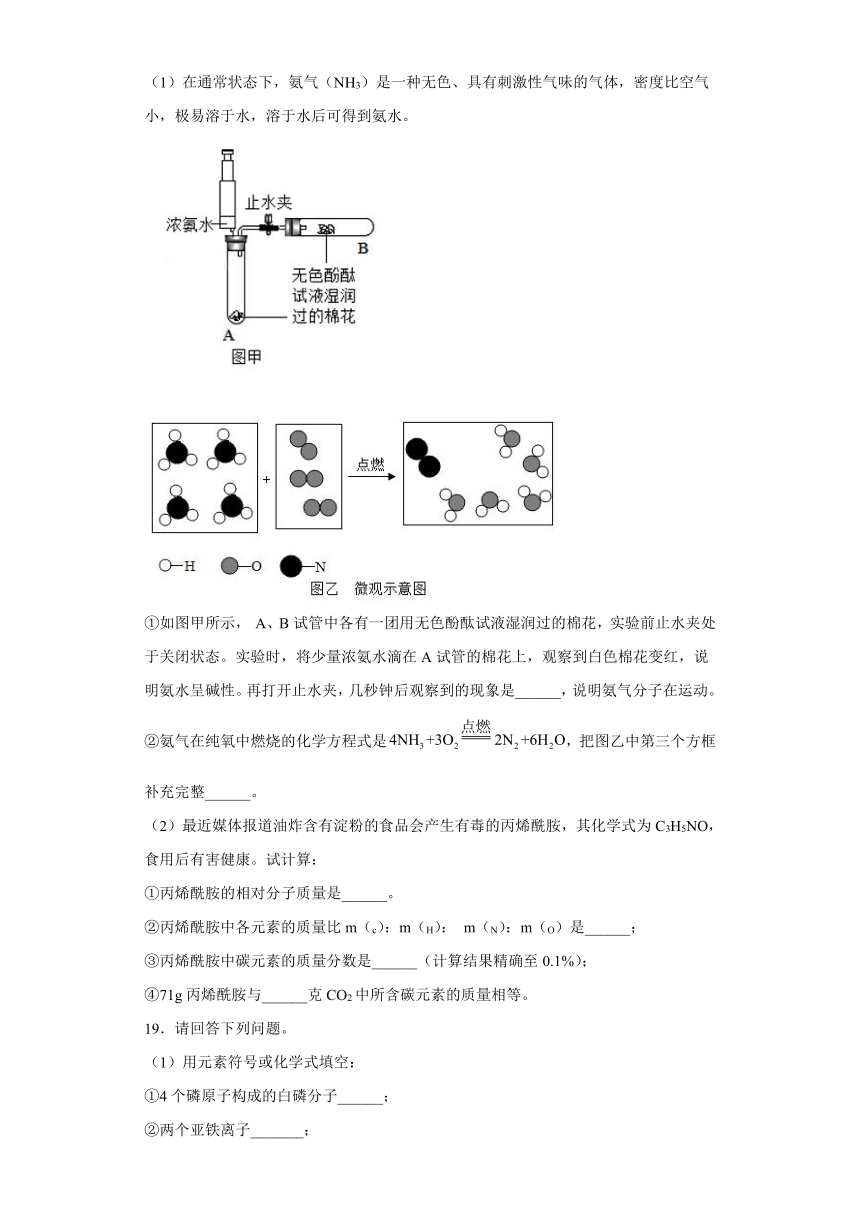
(1)在通常状态下,氨气(NH3)是一种无色、具有刺激性气味的气体,密度比空气小,极易溶于水,溶于水后可得到氨水。
①如图甲所示, A、B试管中各有一团用无色酚酞试液湿润过的棉花,实验前止水夹处于关闭状态。实验时,将少量浓氨水滴在A试管的棉花上,观察到白色棉花变红,说明氨水呈碱性。再打开止水夹,几秒钟后观察到的现象是______,说明氨气分子在运动。
②氨气在纯氧中燃烧的化学方程式是,把图乙中第三个方框补充完整______。
(2)最近媒体报道油炸含有淀粉的食品会产生有毒的丙烯酰胺,其化学式为C3H5NO,食用后有害健康。试计算:
①丙烯酰胺的相对分子质量是______。
②丙烯酰胺中各元素的质量比m(c):m(H): m(N):m(O)是______;
③丙烯酰胺中碳元素的质量分数是______(计算结果精确至0.1%);
④71g丙烯酰胺与______克CO2中所含碳元素的质量相等。
19.请回答下列问题。
(1)用元素符号或化学式填空:
①4个磷原子构成的白磷分子______;
②两个亚铁离子_______;
(2)下图中A、B、C、D是四种粒子的结构示意图。
请回答下列问题:
①图中A、B、C、D属于_______种元素的粒子;
②D中X=________;
(3)下图是某一变化过程的微观示意图,请回答下列问题:
请写出上述变化中发生化学反应的化学方式______,标出反应物中氧元素的化合价_______。
(4)上述化学反应中的反应物可以和Fe(OH)2发生化合反应,尝试书写该化合反应的化学方程式_______。
三、推断题
20.A~E是初中化学已学过的5种物质,它们有如图所示的转化关系,部分产物已略去,已知A、B是无色液体,E是一种白色粉末固体粉末
(1)保持物质D化学性质最小的粒子是___________(用化学式表示),写出E的化学式___________。
(2)写出反应①的化学方程式___________。
(3)写出物质C的一种用途___________。
(4)从铜锈(Cu2(OH)2CO3)的化学式中判斯,可以推测,铜锈是金属Cu能与空气中的O2、H2O和___________(用化学式表示)反应生成的。
21.A、B…H八种物质,其中D有助燃性,H是一种有刺激性气味的气体。且已知A是高锰酸钾,B的作用是催化。
(1)写出反应①的化学方程式_________。
(2)写出③反应的化学方程式_________。
四、实验题
22.物质发生化学变化前后总质量是增加、减少还是不变呢?甲、乙、丙三位同学按下面的步骤进行实验探究。
(提出假设)物质发生化学反应前后总质量不变。
(设计并进行实验)甲设计的实验装置和选用药品如图A,乙设计的实验装置和选用药品如图B,他们在反应前后都进行了规范操作,准确地称量和细致地观察。(提示信息:图A发生的反应为)
(1)丙进行了如图C的实验,在一根用细铜丝吊着的长玻璃棒两端,分别绕上粗铜丝,并使玻璃棒保持水平。然后用酒精灯给a端铜丝加热数分钟。停止加热后冷却,他观察到的现象是______,________。
(2)实验结论。甲认为,在化学反应中生成物的总质量与反应物的总质量相等;乙、丙认为,在化学反应中生成物的总质量与反应物的总质量不相等。你认为__________的结论正确,请从原子的角度分析,结论正确的理由是________________、________________、______________。
(3)导致其他实验结论错误的原因分别是_____________;___________。如果用_____________的反应验证质量守恒定律,则一定要设计反应在密闭容器中进行实验。
23.如图为实验室制取并收集气体的装置图,请回答下列问题:
(1)写出指定仪器的名称:①______;②______;
(2)实验室用氯酸钾与二氧化锰共热制取干燥的氧气,则选择的制取装置是______,反应的化学方程式为______。
(3)实验室在常温下用块状电石与水反应制取乙炔气体,如果要控制化学反应速率,你认为上图中最适合制取乙炔气体的发生装置是______(填装置序号);如果用E图所示装置收集乙炔,气体应从______(填“a”或“b”)端管口通入。
五、计算题
24.实验室用高锰酸钾制取氧气。先取 32.6g 高锰酸钾固体,加热一段时间后,剩余固体的质量为 29.4g, 请回答下列问题。
(1)生成氧气的质量为_____g;
(2)剩余固体成分有_____种物质;
(3)求剩余固体中二氧化锰的质量分数_____(写出计算过程,结果精确到 0.1%)。
25.酸奶作为世界公认的长寿食品之一,正愈来愈受到人们的喜爱,酸奶中的酸味来自乳酸(化学式为C3H6O3)。
(1)乳酸中C、H、O三种元素的质量比为_______。
(2)乳酸在人体内消化吸收后,最终完全氧化为CO2和H2O。试计算当4.5g乳酸完全氧化,生成H2O的质量为 _______g。(乳酸氧化反应方程式:C3H6O3+3O2═3CO2+3H2O)
(3)为了测定某品牌酸奶中乳酸的含量,某同学取100mL酸奶和100mL蒸馏水于烧杯中,慢慢滴入0.2%的NaOH溶液并不断搅拌,测得当加入NaOH体积10mL时恰好完全反应。请计算该酸奶中乳酸的含量为_______g/L。(已知乳酸和氢氧化钠的反应方程式表示为:C3H6O3+NaOH═C3H5O3Na+H2O,测定所用NaOH溶液的密度为1.0g/mL)
参考答案
1.C 2.B 3.D 4.A 5.C 6.C 7.D 8.C 9.D 10.D 11.C 12.B 13.B 14.C 15.B 16.
17.在二氧化锰的催化作用下过氧化氢分解成水和氧气 H2O2:H2O:O2 为2:2:1 H2O2:H2O:O2 为68:36:32
18.(1) B试管中白色棉花变红
(2) 71 36:5:14:16 50.7% 132
19.
(1) P4 2Fe2+
(2) 3 8
(3)
(4)
20.H2 KClO3 用于医疗急救 CO2
21.
22.
(1) a端上铜丝变黑 玻璃棒a端下沉
(2) 甲 原子种类不变 原子的数目不变 原子质量不变
(3) 乙中反应生成的气体从装置中逸出 丙中空气中的氧气参加了反应 有气体参加、生成
23.
(1) 试管
集气瓶
(2) C
(3) A b
24.
(1)3.2
(2)三(或3)
(3)29.6%
剩余固体中二氧化锰的质量分数为×100%≈29.6%。
答:剩余固体中二氧化锰的质量分数为29.6%。
25.
(1)6:1:8
(2)2.7
(3)0.45
一、单选题
1.水蒸气通过红热的铁粉,发生的反应为3Fe+4H2O(气)X+4H2,则X为
A.FeO B.Fe2O3 C.Fe3O4 D.Fe(OH)2
2.根据化学方程式不能获得的信息是
A.反应中的反应物和生成物 B.化学反应速率的快慢程度
C.各反应物、生成物之间的质量比 D.反应发生所需要的条件
3.由元素X、Y组成的两种物质经化合生成Z,化学方程式为:3X2+2YX=2Z,则Z的化学式是
A.X3Y2 B.XY C.X4Y D.YX4
4.自然科学的发展使我们的生活变得丰富多彩。通过化学的学习,你觉得下列情况中不可能实现的是
A.通过化学反应使水直接变成汽油 B.用肥皂水区分硬水和软水
C.用人工的方法合成结晶牛胰岛素 D.通过分离液态空气法得到氧气
5.在反应A+B→C+D中,若15gA与10gB完全反应没有剩余,则生成的C和D的质量总和为
A.15g B.10g C.25 g D.5g
6.氯化钠是重要的化工原料,是氯碱工业的基础。电解饱和食盐水一定不能得到的物质是
A.H2 B.Cl2 C.Na2CO3 D.NaOH
7.下列叙述完全符合质量守恒定律的是
A.水结成冰前后,质量保持不变
B.50mL水和50 mL乙醇混合后总体积小于100 mL
C.在100g30%过氧化氢溶液中,含有30g过氧化氢和70g水
D.1.2g碳与3.2g氧气恰好完全反应可生成4.4g二氧化碳
8.甲烷是天然气的主要成分,其完全燃烧的化学方程式为CH4+2O2CO2+2H2O,根据该化学方程式无法获取的信息是
A.反应物和生成物 B.反应所需条件
C.反应物的颜色和状态 D.生成物的分子个数比
9.推理是学习化学常用的方法,下列推理正确的是
A.单质由同种元素组成,则只含有一种元素的物质一定是单质
B.化学变化中常伴随发光放热的现象所以有发光放热现象产生时一定发生了化学变化
C.同种元素的质子数相同,则质子数相同的粒子一定属于同种元素
D.蜡烛燃烧生成二氧化碳和水,所以蜡烛组成中一定有碳元素和氢元素
10.下列说法错误的是
A.化学反应前后,物质的种类一定发生改变
B.化学反应前后,分子的种类一定发生改变
C.化学反应前后,原子的数目一定不发生改变
D.化学反应前后,原子团一定发生改变
11.在一个密闭容器中有X、Y、Z、Q四种物质,一定条件下充分反应,测得反应前后各物质的质量如下表所示:已知X和Q两种物质的相对分子质量均为M,下列推理中正确的是
X Y Z Q
反应前的质量/g 8 10 1 21
反应后的质量/g 0 21 待测 9
A.反应后物质Z的质量为9g B.反应中物质Y与Q的质量比为1:1
C.反应生成Y的质量为11g D.该反成的化学方程式中,物质X与Q的化学计量数之比为3:2
12.向一密闭容器中加入甲、乙、丙、丁4种物质,在一定条件下发生化学反应,测得有关数据如图,下列说法不正确的是
A.a的数值是4 B.乙和丙的质量变化比为5:3
C.该反应是化合反应 D.丁可能是该反应的催化剂
13.下列化学方程式书写正确的是
A.2P+2.5O2P2O5 B.CaCO3 +2HCl=CaCl2+ H2O + CO2↑
C.C+O2CO2↑ D.4Fe+3O22Fe2O3
14.如图是某个化学反应的微观模拟示意图,从图中不能获得的信息是
A.该反应前后一共涉及3种分子
B.该反应前后各种原子的种类没有变化
C.该反应的生成物都是化合物
D.该反应属于分解反应
15.根据质量守恒定律,6g碳和32g氧气充分反应后,生成二氧化碳的质量为
A.38g B.22g C.26g D.14g
二、填空题
16.用“捕捉”CO2生产甲醇,反应的微观示意图如下:
该反应的化学方程式为_______。
17.二氧化碳根据化学方程式2H2O22H2O + O2↑ ,说出化学方程式的意义
反应条件、反应物、生成物 __________
粒子数之比 _________
物质质量比 __________
18.请你回答有关问题:
(1)在通常状态下,氨气(NH3)是一种无色、具有刺激性气味的气体,密度比空气小,极易溶于水,溶于水后可得到氨水。
①如图甲所示, A、B试管中各有一团用无色酚酞试液湿润过的棉花,实验前止水夹处于关闭状态。实验时,将少量浓氨水滴在A试管的棉花上,观察到白色棉花变红,说明氨水呈碱性。再打开止水夹,几秒钟后观察到的现象是______,说明氨气分子在运动。
②氨气在纯氧中燃烧的化学方程式是,把图乙中第三个方框补充完整______。
(2)最近媒体报道油炸含有淀粉的食品会产生有毒的丙烯酰胺,其化学式为C3H5NO,食用后有害健康。试计算:
①丙烯酰胺的相对分子质量是______。
②丙烯酰胺中各元素的质量比m(c):m(H): m(N):m(O)是______;
③丙烯酰胺中碳元素的质量分数是______(计算结果精确至0.1%);
④71g丙烯酰胺与______克CO2中所含碳元素的质量相等。
19.请回答下列问题。
(1)用元素符号或化学式填空:
①4个磷原子构成的白磷分子______;
②两个亚铁离子_______;
(2)下图中A、B、C、D是四种粒子的结构示意图。
请回答下列问题:
①图中A、B、C、D属于_______种元素的粒子;
②D中X=________;
(3)下图是某一变化过程的微观示意图,请回答下列问题:
请写出上述变化中发生化学反应的化学方式______,标出反应物中氧元素的化合价_______。
(4)上述化学反应中的反应物可以和Fe(OH)2发生化合反应,尝试书写该化合反应的化学方程式_______。
三、推断题
20.A~E是初中化学已学过的5种物质,它们有如图所示的转化关系,部分产物已略去,已知A、B是无色液体,E是一种白色粉末固体粉末
(1)保持物质D化学性质最小的粒子是___________(用化学式表示),写出E的化学式___________。
(2)写出反应①的化学方程式___________。
(3)写出物质C的一种用途___________。
(4)从铜锈(Cu2(OH)2CO3)的化学式中判斯,可以推测,铜锈是金属Cu能与空气中的O2、H2O和___________(用化学式表示)反应生成的。
21.A、B…H八种物质,其中D有助燃性,H是一种有刺激性气味的气体。且已知A是高锰酸钾,B的作用是催化。
(1)写出反应①的化学方程式_________。
(2)写出③反应的化学方程式_________。
四、实验题
22.物质发生化学变化前后总质量是增加、减少还是不变呢?甲、乙、丙三位同学按下面的步骤进行实验探究。
(提出假设)物质发生化学反应前后总质量不变。
(设计并进行实验)甲设计的实验装置和选用药品如图A,乙设计的实验装置和选用药品如图B,他们在反应前后都进行了规范操作,准确地称量和细致地观察。(提示信息:图A发生的反应为)
(1)丙进行了如图C的实验,在一根用细铜丝吊着的长玻璃棒两端,分别绕上粗铜丝,并使玻璃棒保持水平。然后用酒精灯给a端铜丝加热数分钟。停止加热后冷却,他观察到的现象是______,________。
(2)实验结论。甲认为,在化学反应中生成物的总质量与反应物的总质量相等;乙、丙认为,在化学反应中生成物的总质量与反应物的总质量不相等。你认为__________的结论正确,请从原子的角度分析,结论正确的理由是________________、________________、______________。
(3)导致其他实验结论错误的原因分别是_____________;___________。如果用_____________的反应验证质量守恒定律,则一定要设计反应在密闭容器中进行实验。
23.如图为实验室制取并收集气体的装置图,请回答下列问题:
(1)写出指定仪器的名称:①______;②______;
(2)实验室用氯酸钾与二氧化锰共热制取干燥的氧气,则选择的制取装置是______,反应的化学方程式为______。
(3)实验室在常温下用块状电石与水反应制取乙炔气体,如果要控制化学反应速率,你认为上图中最适合制取乙炔气体的发生装置是______(填装置序号);如果用E图所示装置收集乙炔,气体应从______(填“a”或“b”)端管口通入。
五、计算题
24.实验室用高锰酸钾制取氧气。先取 32.6g 高锰酸钾固体,加热一段时间后,剩余固体的质量为 29.4g, 请回答下列问题。
(1)生成氧气的质量为_____g;
(2)剩余固体成分有_____种物质;
(3)求剩余固体中二氧化锰的质量分数_____(写出计算过程,结果精确到 0.1%)。
25.酸奶作为世界公认的长寿食品之一,正愈来愈受到人们的喜爱,酸奶中的酸味来自乳酸(化学式为C3H6O3)。
(1)乳酸中C、H、O三种元素的质量比为_______。
(2)乳酸在人体内消化吸收后,最终完全氧化为CO2和H2O。试计算当4.5g乳酸完全氧化,生成H2O的质量为 _______g。(乳酸氧化反应方程式:C3H6O3+3O2═3CO2+3H2O)
(3)为了测定某品牌酸奶中乳酸的含量,某同学取100mL酸奶和100mL蒸馏水于烧杯中,慢慢滴入0.2%的NaOH溶液并不断搅拌,测得当加入NaOH体积10mL时恰好完全反应。请计算该酸奶中乳酸的含量为_______g/L。(已知乳酸和氢氧化钠的反应方程式表示为:C3H6O3+NaOH═C3H5O3Na+H2O,测定所用NaOH溶液的密度为1.0g/mL)
参考答案
1.C 2.B 3.D 4.A 5.C 6.C 7.D 8.C 9.D 10.D 11.C 12.B 13.B 14.C 15.B 16.
17.在二氧化锰的催化作用下过氧化氢分解成水和氧气 H2O2:H2O:O2 为2:2:1 H2O2:H2O:O2 为68:36:32
18.(1) B试管中白色棉花变红
(2) 71 36:5:14:16 50.7% 132
19.
(1) P4 2Fe2+
(2) 3 8
(3)
(4)
20.H2 KClO3 用于医疗急救 CO2
21.
22.
(1) a端上铜丝变黑 玻璃棒a端下沉
(2) 甲 原子种类不变 原子的数目不变 原子质量不变
(3) 乙中反应生成的气体从装置中逸出 丙中空气中的氧气参加了反应 有气体参加、生成
23.
(1) 试管
集气瓶
(2) C
(3) A b
24.
(1)3.2
(2)三(或3)
(3)29.6%
剩余固体中二氧化锰的质量分数为×100%≈29.6%。
答:剩余固体中二氧化锰的质量分数为29.6%。
25.
(1)6:1:8
(2)2.7
(3)0.45
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
