人教版(五四制)八年级全一册化学 第五单元 课题3 利用化学方程式的简单计算 课件(共16张PPT)
文档属性
| 名称 | 人教版(五四制)八年级全一册化学 第五单元 课题3 利用化学方程式的简单计算 课件(共16张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-11 00:00:00 | ||
图片预览






文档简介
(共16张PPT)
课题3 利用化学方程式的简单计算
教学目标
掌握规范的解题格式。
教学重点
养成细心审题的习惯,提高分析问题、解决问题的能力。
高温煅烧碳酸钙(CaCO3)可以制得生石灰(CaO)和二氧化碳。如果高温煅烧50 克碳酸钙,生成多少克二氧化碳?
相对原子质量:C-12 O-16 Ca-40
经验与教训:
注意解题步骤和格式
(细节决定成败)
温故而知新
通关游戏一
需要得到44 L二氧化碳,至少需要煅烧多少克碳酸钙?(二氧化碳的密度约为2.0 g/L)
相对原子质量:C-12 O-16 Ca-40
经验与教训:
①物质的体积不能代入方程式中计算
②公式:质量=密度×体积
③再将质量代入化学方程式中,求其它物质的质量
高温煅烧10克纯度为80%的石灰石(主要成份CaCO3,杂质不参加反应),可得到多少克二氧化碳?
经验与教训:
①混合物的质量不能代入方程式中计算。
②公式:纯净物的质量=混合物的总质量×纯度
③再将纯净物的质量代入化学方程式中,求其它物质的质量
通关游戏二
高温煅烧100克石灰石(主要成分CaCO3,杂质不参加反应),至质量不再减少为止,剩余物质的质量为67克,求
(1)生成二氧化碳的质量为 ;
(2)该石灰石中碳酸钙的质量。
经验与教训:
变化前后减少的质量,就是生成气体的质量。
生成气体的质量=m(反应前)— m(剩余物),
再代入化学方程式中,求其它物质的质量。
通关游戏三
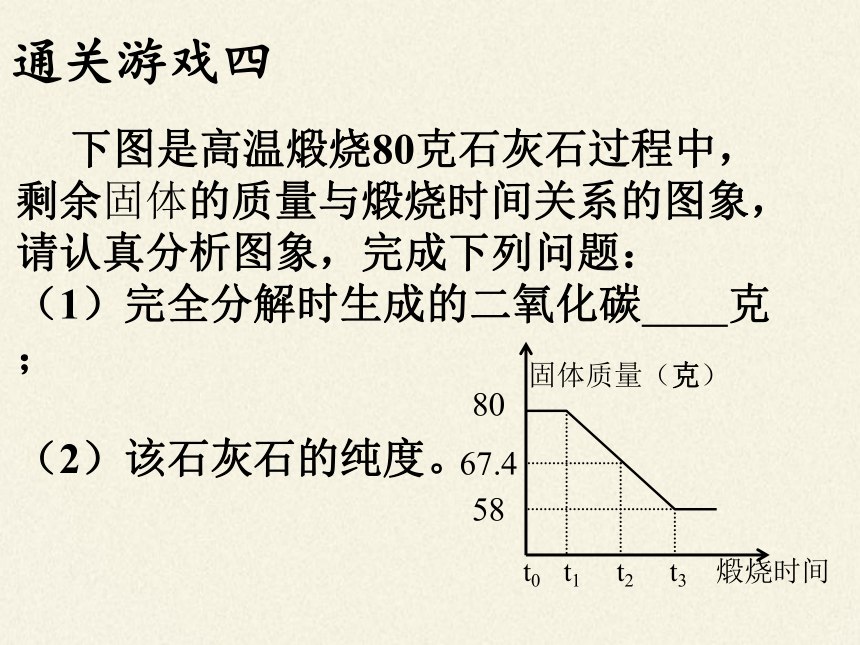
下图是高温煅烧80克石灰石过程中,剩余固体的质量与煅烧时间关系的图象,请认真分析图象,完成下列问题:
(1)完全分解时生成的二氧化碳 克;
(2)该石灰石的纯度。
固体质量(克)
t0 t1 t2 t3 煅烧时间
80
58
67.4
通关游戏四
我的收获,我做主
根据化学方程式计算常见的类型
1、根据方程式中一种纯净物的质量,求方程式中其它物质的质量。
2、已知量是体积或需求体积
体积 质量
3、含杂质的计算
纯净物的质量=混合物的质量×纯度
4、根据质量守恒定律:反应后剩余物减少的质量,就是生成气体的质量。(突破口)
5、根据表格或图形进行数据分析
× ρ
÷ ρ
根据化学方程式计算常见的类型
①已知物质的体积
②已经混合物的
总质量和纯度
③已经变化前、后
物质的总质量
④表格或图像
纯净物的质量
其它物质的质量
代入化学
方程式中
三个要领:
①步骤要完整(5步)
②格式要规范
③得数要准确
三个关键
①准确书写化学方程式
②准确计算相关物质的质量比
③代入的已知量必须是纯净物的质量
收获
①△m=m(反应前)-m(剩余物)
=生成气体的质量
②
③纯净物的质量=总质量×纯度
④质量=密度×体积(m=ρV)
常用到的公式
高温煅烧10克石灰石(主要成分CaCO3,杂质反应),加热煅烧时间与剩余固体质量如下数据。计算:
(1)完全分解时生成的二氧化碳 克;
(2)该石灰石的纯度。
煅烧时间 t0 t1 t2 t3 t4
剩余固体质量/g 10 8.9 7.8 6.7 6.7
打大BOSS
(3)画出剩余固体随时间变化曲线
谢 谢
课题3 利用化学方程式的简单计算
教学目标
掌握规范的解题格式。
教学重点
养成细心审题的习惯,提高分析问题、解决问题的能力。
高温煅烧碳酸钙(CaCO3)可以制得生石灰(CaO)和二氧化碳。如果高温煅烧50 克碳酸钙,生成多少克二氧化碳?
相对原子质量:C-12 O-16 Ca-40
经验与教训:
注意解题步骤和格式
(细节决定成败)
温故而知新
通关游戏一
需要得到44 L二氧化碳,至少需要煅烧多少克碳酸钙?(二氧化碳的密度约为2.0 g/L)
相对原子质量:C-12 O-16 Ca-40
经验与教训:
①物质的体积不能代入方程式中计算
②公式:质量=密度×体积
③再将质量代入化学方程式中,求其它物质的质量
高温煅烧10克纯度为80%的石灰石(主要成份CaCO3,杂质不参加反应),可得到多少克二氧化碳?
经验与教训:
①混合物的质量不能代入方程式中计算。
②公式:纯净物的质量=混合物的总质量×纯度
③再将纯净物的质量代入化学方程式中,求其它物质的质量
通关游戏二
高温煅烧100克石灰石(主要成分CaCO3,杂质不参加反应),至质量不再减少为止,剩余物质的质量为67克,求
(1)生成二氧化碳的质量为 ;
(2)该石灰石中碳酸钙的质量。
经验与教训:
变化前后减少的质量,就是生成气体的质量。
生成气体的质量=m(反应前)— m(剩余物),
再代入化学方程式中,求其它物质的质量。
通关游戏三
下图是高温煅烧80克石灰石过程中,剩余固体的质量与煅烧时间关系的图象,请认真分析图象,完成下列问题:
(1)完全分解时生成的二氧化碳 克;
(2)该石灰石的纯度。
固体质量(克)
t0 t1 t2 t3 煅烧时间
80
58
67.4
通关游戏四
我的收获,我做主
根据化学方程式计算常见的类型
1、根据方程式中一种纯净物的质量,求方程式中其它物质的质量。
2、已知量是体积或需求体积
体积 质量
3、含杂质的计算
纯净物的质量=混合物的质量×纯度
4、根据质量守恒定律:反应后剩余物减少的质量,就是生成气体的质量。(突破口)
5、根据表格或图形进行数据分析
× ρ
÷ ρ
根据化学方程式计算常见的类型
①已知物质的体积
②已经混合物的
总质量和纯度
③已经变化前、后
物质的总质量
④表格或图像
纯净物的质量
其它物质的质量
代入化学
方程式中
三个要领:
①步骤要完整(5步)
②格式要规范
③得数要准确
三个关键
①准确书写化学方程式
②准确计算相关物质的质量比
③代入的已知量必须是纯净物的质量
收获
①△m=m(反应前)-m(剩余物)
=生成气体的质量
②
③纯净物的质量=总质量×纯度
④质量=密度×体积(m=ρV)
常用到的公式
高温煅烧10克石灰石(主要成分CaCO3,杂质反应),加热煅烧时间与剩余固体质量如下数据。计算:
(1)完全分解时生成的二氧化碳 克;
(2)该石灰石的纯度。
煅烧时间 t0 t1 t2 t3 t4
剩余固体质量/g 10 8.9 7.8 6.7 6.7
打大BOSS
(3)画出剩余固体随时间变化曲线
谢 谢
同课章节目录
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的构成
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题1 质量守恒定律
- 课题2 如何正确书写化学方程式
- 课题3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动3 燃烧的条件
- 旧版目录
- 第五单元 物质组成的表示
- 课题2 燃料和热量
- 课题3 使用燃料对环境的影响
