第三单元-到实验室去:配制一定溶质质量分数的溶液练习题2021-2022学年鲁教版九年级化学(含解析)
文档属性
| 名称 | 第三单元-到实验室去:配制一定溶质质量分数的溶液练习题2021-2022学年鲁教版九年级化学(含解析) |
|
|
| 格式 | zip | ||
| 文件大小 | 331.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-10 00:00:00 | ||
图片预览


文档简介
第三单元-到实验室去:配制一定溶质质量分数的溶液练习题2021-2022学年鲁教版九年级化学
一、单选题
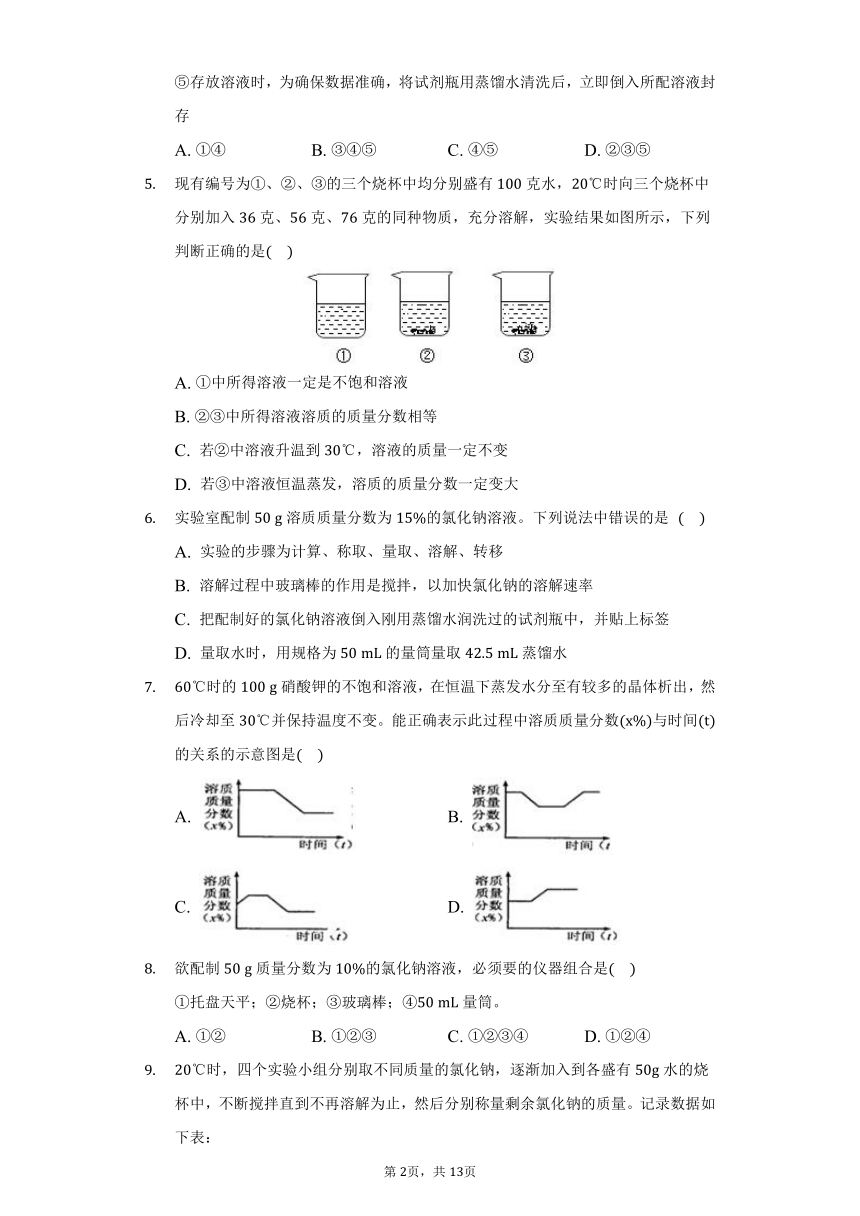
下列配制溶液常见的操作中,正确的是
A. 取用氯化钠 B. 称量氯化钠
C. 量取蒸水 D. 溶解氯化钠
青海玉树地震后,为防止疾病传染,需对灾区喷洒消毒剂,进行医疗卫生防疫.质量分数为的过氧乙酸就是用于环境喷洒和用具浸泡的一种消毒剂.现有市售质量分数为的过氧乙酸,要配制的过氧乙酸,需要市售过氧乙酸的质量为
A. B. C. D.
保持温度不变,小心蒸发不饱和溶液蒸发皿中始终有溶液,则溶液中溶质的质量分数与时间的关系合理的是
A. B.
C. D.
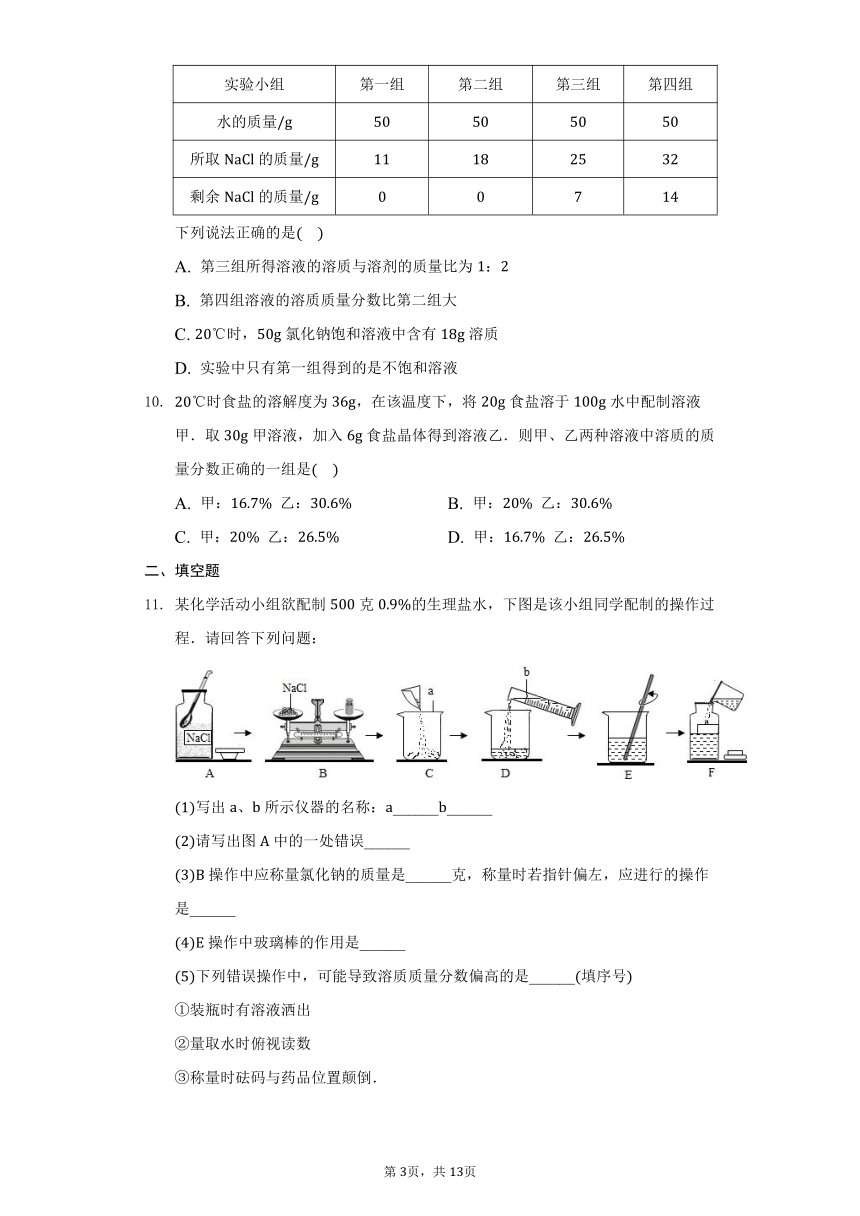
某同学选用氢氧化钠固体与水配制溶质质量分数为的氢氧化钠溶液,下列说法错误的是
需称取氢氧化钠固体
称量前托盘天平应先检查游码是否归零,并调节平衡
用托盘天平称量氢氧化钠固体时,为防止污染托盘,可将氢氧化钠放在纸上称量
选用量筒量取的水
存放溶液时,为确保数据准确,将试剂瓶用蒸馏水清洗后,立即倒入所配溶液封存
A. B. C. D.
现有编号为、、的三个烧杯中均分别盛有克水,时向三个烧杯中分别加入克、克、克的同种物质,充分溶解,实验结果如图所示,下列判断正确的是
A. 中所得溶液一定是不饱和溶液
B. 中所得溶液溶质的质量分数相等
C. 若中溶液升温到,溶液的质量一定不变
D. 若中溶液恒温蒸发,溶质的质量分数一定变大
实验室配制溶质质量分数为的氯化钠溶液。下列说法中错误的是
A. 实验的步骤为计算、称取、量取、溶解、转移
B. 溶解过程中玻璃棒的作用是搅拌,以加快氯化钠的溶解速率
C. 把配制好的氯化钠溶液倒入刚用蒸馏水润洗过的试剂瓶中,并贴上标签
D. 量取水时,用规格为的量筒量取蒸馏水
时的 硝酸钾的不饱和溶液,在恒温下蒸发水分至有较多的晶体析出,然后冷却至并保持温度不变。能正确表示此过程中溶质质量分数与时间的关系的示意图是
A. B.
C. D.
欲配制 质量分数为的氯化钠溶液,必须要的仪器组合是
托盘天平;烧杯;玻璃棒; 量筒。
A. B. C. D.
时,四个实验小组分别取不同质量的氯化钠,逐渐加入到各盛有水的烧杯中,不断搅拌直到不再溶解为止,然后分别称量剩余氯化钠的质量。记录数据如下表:
实验小组 第一组 第二组 第三组 第四组
水的质量
所取的质量
剩余的质量
下列说法正确的是
A. 第三组所得溶液的溶质与溶剂的质量比为:
B. 第四组溶液的溶质质量分数比第二组大
C. 时,氯化钠饱和溶液中含有溶质
D. 实验中只有第一组得到的是不饱和溶液
时食盐的溶解度为,在该温度下,将食盐溶于水中配制溶液甲.取甲溶液,加入食盐晶体得到溶液乙.则甲、乙两种溶液中溶质的质量分数正确的一组是
A. 甲: 乙: B. 甲: 乙:
C. 甲: 乙: D. 甲: 乙:
二、填空题
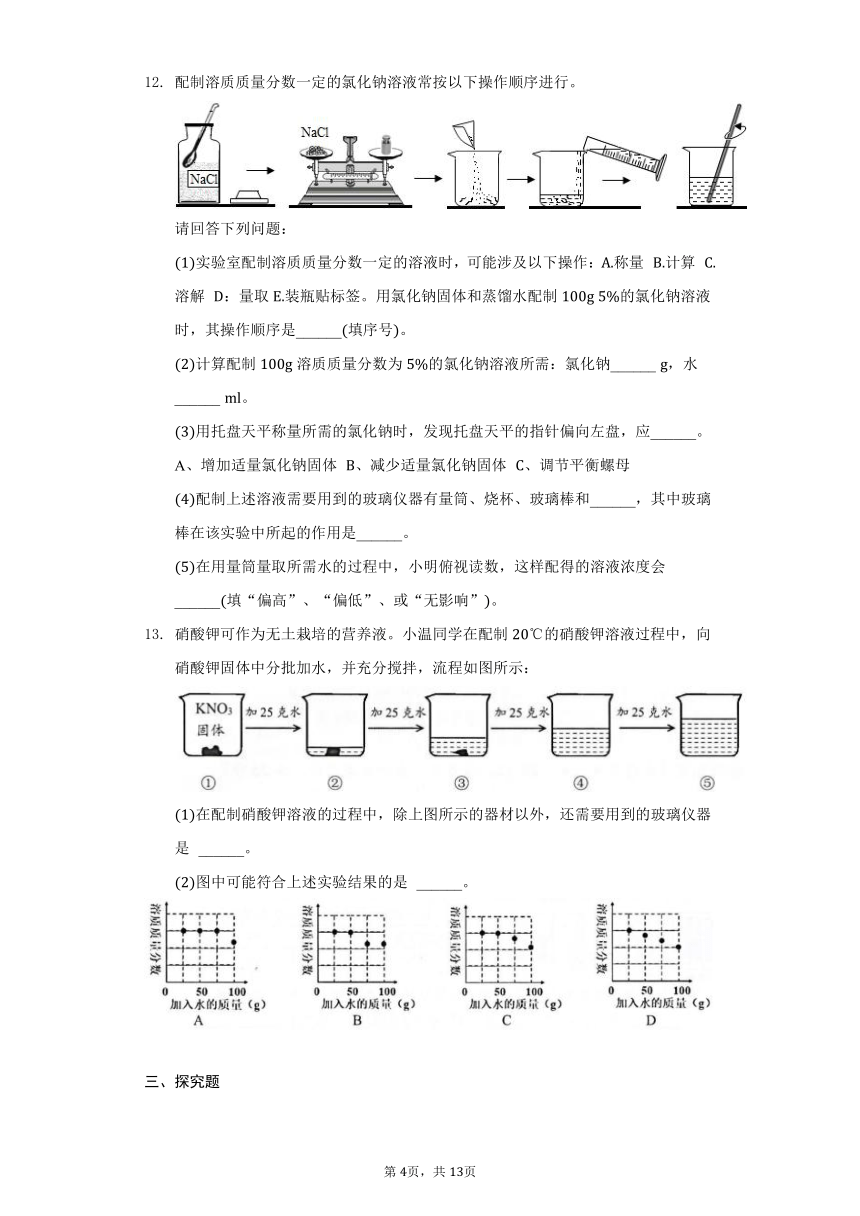
某化学活动小组欲配制克的生理盐水,下图是该小组同学配制的操作过程.请回答下列问题:
写出、所示仪器的名称:____________
请写出图中的一处错误______
操作中应称量氯化钠的质量是______克,称量时若指针偏左,应进行的操作是______
操作中玻璃棒的作用是______
下列错误操作中,可能导致溶质质量分数偏高的是______填序号
装瓶时有溶液洒出
量取水时俯视读数
称量时砝码与药品位置颠倒.
配制溶质质量分数一定的氯化钠溶液常按以下操作顺序进行。
请回答下列问题:
实验室配制溶质质量分数一定的溶液时,可能涉及以下操作:称量 计算 溶解 :量取装瓶贴标签。用氯化钠固体和蒸馏水配制的氯化钠溶液时,其操作顺序是______填序号。
计算配制溶质质量分数为的氯化钠溶液所需:氯化钠______ ,水______ 。
用托盘天平称量所需的氯化钠时,发现托盘天平的指针偏向左盘,应______。
A、增加适量氯化钠固体 、减少适量氯化钠固体 、调节平衡螺母
配制上述溶液需要用到的玻璃仪器有量筒、烧杯、玻璃棒和______,其中玻璃棒在该实验中所起的作用是______。
在用量筒量取所需水的过程中,小明俯视读数,这样配得的溶液浓度会______填“偏高”、“偏低”、或“无影响”。
硝酸钾可作为无土栽培的营养液。小温同学在配制的硝酸钾溶液过程中,向硝酸钾固体中分批加水,并充分搅拌,流程如图所示:
在配制硝酸钾溶液的过程中,除上图所示的器材以外,还需要用到的玻璃仪器是 ______。
图中可能符合上述实验结果的是 ______。
三、探究题
欲配制溶质质量分数为的硝酸铵,实验操作如图所示,请回答下列问题:
量取所需要的水应选择______选填“”、“”或“”量筒。
调平衡后,用托盘天平称量所需的硝酸铵时,发现托盘天平的指针偏向左盘,应______选填序号。
A.增加适量硝酸铵固体
B.减少适量硝酸铵固体
C.调节平衡螺母
D.增加砝码
将硝酸铵和水依次倒入烧杯中,要用玻璃棒搅拌,其目的是______。
用上述图示的序号表示配制溶液的操作顺序______。
在做操作时,烧杯的温度______选填“升高”或“降低”了。
若量取蒸馏水的体积时仰视读数,则该实验小组实际配制的硝酸铵溶液的溶质质量分数比计划配制的溶质质量分数偏______填“高”、“低”。
将制得的硝酸铵溶液装瓶保存时,试剂瓶的标签上应注明等信息______。
的硼酸溶液可用于清洗皮肤的小面积创伤。现配制质量分数为的硼酸溶液,实验操作如下:
称量硼酸固体的质量:在图中分别标出所选砝码的质量和游码的示数。
量取水的体积,用量筒量取______水
溶解:用到的玻璃仪器是______。
装瓶、贴标签。
答案和解析
1.【答案】
【解析】解:、取用固体粉末状药品时,瓶塞要倒放,应用药匙取用,不能用手接触药品,图中瓶塞没有倒放,图中所示操作错误。
B、托盘天平的使用要遵循“左物右码”的原则,图中所示操作砝码与药品位置放反了,图中所示操作错误。
C、量筒读数时视线要与量筒内液体的凹液面的最低处保持水平,图中视线没有对着刻度线的一侧,图中所示操作错误。
D、配制溶液时,溶解操作应在烧杯中进行,用玻璃棒不断搅拌,图中所示操作正确。
故选:。
A、根据固体药品的取用方法进行分析判断。
B、根据托盘天平的使用要遵循“左物右码”的原则进行分析判断。
C、根据量筒读数时视线要与凹液面的最低处保持水平进行分析判断。
D、根据溶解操作的方法,进行分析判断。
本题难度不大,熟悉配制溶液的实验步骤、各操作的注意事项是解答此类试题的关键。
2.【答案】
【解析】解:设需要市售过氧乙酸的质量为.
故选:.
该题属于一道溶液稀释问题的计算题,用的溶液配制的溶液,我们可以向的溶液中加一定质量的水即可,在稀释前后,溶液中溶质的质量不变,了解了这一点,该题便简单易解.
该题是一道溶液稀释问题的计算题,要求学生掌握好解题的规律,即稀释前后溶质的质量不变,本题便可迎刃而解.
3.【答案】
【解析】保持温度不变,氯化钠溶液蒸发水分是由不饱和溶液变为饱和溶液的过程,该过程中溶剂质量减小,溶液中溶质质量分数增大,当氯化钠溶液变为饱和溶液后再蒸发水时,溶液仍为饱和溶液,溶质质量分数将不变,A正确。
4.【答案】
【解析】解:溶质质量溶液质量溶质的质量分数,配制溶质质量分数为的氢氧化钠溶液,需氢氧化钠的质量,故选项说法正确。
称量前托盘天平应先检查游码是否归零,并调节平衡,故选项说法正确。
托盘天平的使用要遵循“左物右码”的原则,且氢氧化钠具有腐蚀性,应放在玻璃器皿中称量,故选项说法错误。
溶剂质量溶液质量溶质质量,所需溶剂的质量为合,应用规格为的量筒量取水的体积,故选项说法错误。
存放溶液时,为确保数据准确,将试剂瓶用蒸馏水清洗后,立即倒入所配溶液封存,会造成实际量取的水的体积偏大,则使溶质质量分数偏小,故选项说法错误。
故选:。
利用溶质质量溶液质量溶质的质量分数,进行分析判断。
根据托盘天平的使用方法,进行分析判断。
根据托盘天平的使用要遵循“左物右码”的原则、氢氧化钠具有腐蚀性,进行分析判断。
根据溶剂质量溶液质量溶质质量,计算出所需水的质量和体积,进而判断所需量筒的量程。
存放溶液时,为确保数据准确,将试剂瓶用蒸馏水清洗后,会造成实际量取的水的体积偏大,进行分析判断。
本题难度不大,明确配制一定溶质质量分数的溶液实验步骤计算、称量、溶解、注意事项等是正确解答本题的关键。
5.【答案】
【解析】解:、依据饱和溶液的概念可知,、中有固体出现,一定是饱和溶液,中没有固体出现,可能是恰好溶解,则可能是饱和溶液;故错误;
B、溶液都是相同温度下的饱和溶液,所以溶液的溶质质量分数一定相等,故正确;
C、烧杯中溶液升温至,溶解度改变,溶液的质量改变,故错误;
D、恒温蒸发溶剂,饱和溶液析出晶体,但溶液仍为饱和溶液,相同温度下的同种物质的饱和溶液溶质质量分数因溶解度相等而相等,溶质质量分数不变,故错误;
故选:。
根据在一定温度和溶剂中,有溶质析出的溶液中,溶质达到最大溶解能力,溶质不会溶解,则溶液一定为饱和溶液,没有固体析出的溶液可能是恰好饱和或不是饱和溶液;在饱和溶液中溶质的质量分数最大且相同进行解答。
本考点考查了溶液中溶质质量分数的比较、饱和溶液与不饱和溶液等,综合性强,要加强记忆,理解应用;本考点主要出现在选择题和填空题中。
6.【答案】
【解析】略
7.【答案】
【解析】解:时的 硝酸钾的不饱和溶液,在恒温下蒸发水分至有较多的晶体析出这一过程中,溶质的质量分数不断变大当达到饱和时溶质质量分数最大且不变,然后冷却至并保持温度不变,这一过程硝酸钾溶解度不断变小,浓度不断变小,达到时,溶质质量分数不再改变。
故选:。
利用硝酸钾溶解度随温度升高而升高的知识,不饱和溶液变成饱和溶液溶质质量分数逐渐变大,但只要是同一温度的饱和溶液溶质质量分数一定不变。
此题是对溶液随外界条件变化的一个全面考察,能很好训练学生对相关知识的分析能力,是一道较为全面的总和题型。
8.【答案】
【解析】解:配制溶质质量分数一定的溶液的基本步骤:计算、称量、量取、溶解、装瓶存放,其中需要用到的仪器有:烧杯、玻璃棒、量筒、胶头滴管、天平、药匙。
故选:。
实验室配制克质量分数为的氢氧化钠溶液的操作步骤分别是:计算、称量、溶解,根据各操作所需要使用的仪器,判断所列仪器是否需要。
本题难度不大,明确配制一定溶质质量分数的溶液实验步骤、所需的仪器是正确解答本题的关键。
9.【答案】
【解析】解:、第三组所得溶液的溶质与溶剂的质量比为:::,该选项说法不正确;
B、第四组溶液的溶质质量分数和第二组溶液的溶质质量分数相等,是因为溶液质量都是,溶质质量都是,该选项说法不正确;
C、时,水中溶解氯化钠恰好饱和,因此氯化钠饱和溶液中含有氯化钠质量:,该选项说法不正确;
D、由表中数据可知,水中溶解氯化钠恰好饱和,因此实验中只有第一组得到的是不饱和溶液,该选项说法正确。
故选:。
根据表中数据可以判断,一定质量的溶剂里达到饱和状态时,溶解的溶质质量;
饱和溶液的溶质质量分数;
溶液中溶质质量分数。
饱和溶液和不饱和溶液之间可以相互转化,要注意理解。
10.【答案】
【解析】解:时的溶解度是,在该温度下,将全部溶于水中,配成溶液甲的溶质质量分数;取甲溶液,依据溶液的均一性可知该溶液溶液中的溶质是中的溶质为,则溶剂的量是,依据该温度下的溶解度可知,溶剂中最多能溶解的氯化钠的质量是,故加入晶体,得到的乙溶液为饱和溶液,故乙溶液的溶质质量分数为;
故选:。
时的溶解度是,则该温度下将溶于水中配成的溶液甲为不饱和溶液;取甲溶液,依据溶液的均一性可知该溶液中的溶质为,则溶剂的量是,依据该温度下的溶解度可知,溶剂中最多能溶解的氯化钠的质量是,故加入晶体,得到的乙溶液为饱和溶液,据此分析解答即可.
根据一定温度下饱和溶液的溶质质量分数为该温度下该物质的溶质质量分数的最大值,利用溶质质量分数与溶解度的关系,可对乙溶液的质量分数做出判断.
11.【答案】烧杯 量筒 瓶塞正放 减少药品 搅拌加速溶解
【解析】解:、所示仪器的名称分别是烧杯和量筒.
故填:烧杯;量筒.
中的瓶塞正方时,容易沾上杂质,是一种错误放置方法.
故填:瓶塞正放.
应称量氯化钠的质量是:,称量时若指针偏左,说明药品过量,应进行的操作是减少药品.
故填:; 减少药品.
操作中玻璃棒的作用是搅拌加速溶解.
故填:搅拌加速溶解.
装瓶时有溶液洒出,不影响质量分数;称量时砝码与药品位置颠倒,使称量的溶质质量偏小,会导致质量分数偏小;
量取水时俯视读数,会使量取的水偏少,会导致质量分数偏大.
故填:.
要熟悉各种仪器的名称、用途;
试剂瓶上的瓶塞取下时应该倒放在桌上;
通过计算可以知道溶质的质量;
玻璃棒的作用有:搅拌、引流、转移物质等;
操作不当会导致配制溶液的质量分数不准确.
配制一定质量分数的溶液时,要注意仪器的使用方法、药品的称量方法、计算等方面的问题,力求面面俱到,万无一失.
12.【答案】 胶头滴管 加速食盐的溶解 偏高
【解析】解:配制溶液的步骤为计算、称量、溶解、装瓶保存;
配制溶液时所需氯化钠的质量为:,水的质量为:,由密度公式可得水的体积为;
天平指针偏向谁,谁的质量就大,所以氯化钠取多了;
配制溶质质量分数为 的氯化钠溶液的仪器有:托盘天平、药匙、量筒、胶头滴管、烧杯、玻璃棒;其中属于玻璃仪器的有:量筒、胶头滴管、烧杯、玻璃棒;玻璃棒的搅拌能加速食盐的溶解。
量取水时俯视凹液面最低处,会使得量取水的体积小于,则所得溶液的溶质质量分数为大于;
故答案为:;;;;胶头滴管,加速溶解;偏高。
据配制溶液的步骤回答;
根据溶质质量分数的计算公式计算解答;
根据天平指针偏向谁谁的质量就大分析解答;
据配制溶液所用仪器和玻璃棒的作用回答;
俯视读数,量取的水偏少,则配制的溶液的溶质的质量分数偏高;
配制溶液两种常见操作:固体溶质加水溶解,配制步骤计算称量溶解装瓶;液体加水稀释,配制步骤计算量取溶解装瓶。
13.【答案】量筒、胶头滴管和玻璃棒
【解析】解:根据图可知,将硝酸钾固体放入烧杯后,需要用量筒和胶头滴管量出规定体积的水,注入烧杯后,再用玻璃棒不断搅拌,最终得到硝酸钾的溶液,因此还需要用到的玻璃仪器为:量筒、胶头滴管和玻璃棒。
根据图可知,在烧杯中注入水和水时,始终存在硝酸钾的固体,因此这时肯定是硝酸钾的饱和溶液。当注入水时,没有硝酸钾固体存在,那么溶液可能饱和也可能不饱和。当注入水时,硝酸钾溶液肯定不饱和。
如果前三次都是硝酸钾在同一温度下的饱和溶液,那么三者的溶质质量分数相同。由于第四次肯定是不饱和溶液,那么它的溶质质量分数肯定小于前三次,故A正确;
如果前两次是硝酸钾的饱和溶液,而后两次都是它的不饱和溶液,那么前两次的溶质质量分数相同,后两次的溶质质星分数都小于前两次。对于后两次而言,溶质的质量相同,但溶剂的质量不断增大,因此溶质质量分数越来越小,故选C。
故选AC。
故答案为:量筒、胶头滴管和玻璃棒;
。
根据配制硝酸钾溶液的过程确定所需的实验器材;
在配制溶液的过程中,如果有未溶的固体存在,那么溶液肯定是饱和的;如果没有未溶的固体存在,那么溶液可能饱和也可能不饱和,据此对溶液的溶质质量分数的变化进行判断即可。
在做此类题时,首先读懂题意,找出题中的叙述与图象的联系,在运用所学的知识结合图象中的关键点进行分析解答,通过该题,要掌握化学中的数形结合的思想。
14.【答案】 加速溶解 降低 低 溶液的名称、溶质的质量分数
【解析】解:欲配制溶质质量分数为的硝酸铵溶液,需要水的质量为,而水的密度为,所以需要量取水的体积为,故应该选择的量筒;
用托盘天平称量药品时,物体放在左盘,而砝码放在右盘,用托盘天平称量所需的硝酸铵时,发现托盘天平的指针偏向左盘,说明取的硝酸铵固体过多,所以应该减少适量硝酸铵固体,故选B;
硝酸铵在溶解时用玻璃棒搅拌能够加速硝酸铵的溶解;
配制溶液的操作步骤是:计算称取固体量去液体溶解,所以正确的操作步骤为:;
硝酸铵溶于水的过程要吸收热量而使溶液的温度降低。
仰视读数,会导致量取的水变多,溶液变稀,实际配制的硝酸铵溶液的溶质质量分数比计划配制的溶质质量分数偏低。
图中标签中填上相应的内容是溶液的名称、溶质的质量分数。
故答案为: ;
;
加速溶解;
;
降低;
低;
溶液的名称、溶质的质量分数。
根据溶液中溶质的质量分数的计算公式进行解答;
根据天平的使用方法来进行解答;
硝酸铵在溶解时用玻璃棒搅拌能够加速硝酸铵的溶解,可以据此解答;
根据溶液配制的过程和步骤进行解答;
硝酸铵溶于水的过程要吸收热量而使溶液的温度降低,可以据此解答;
根据仰视读数,会导致量取的水变多解答;
图中标签中填上相应的内容是溶液的名称、溶质的质量分数。
通过回答本题知道了溶质、溶剂质量的计算方法,用天平称量时的注意事项,掌握了配制溶质质量分数一定的溶液的基本步骤。
15.【答案】 烧杯、玻璃棒
【解析】解:现配制质量分数为的硼酸溶液,需要硼酸的质量为:,需要水的质量为:。
称量硼酸固体的质量:所选砝码的质量为,游码的示数为,如下图:。
由上述计算可知,需要水的质量是,量取水的体积,用量筒量取水;
溶解:用到的玻璃仪器是烧杯、玻璃棒。
故答为:见上图;;烧杯、玻璃棒。
根据溶质质量分数的计算公式计算出需要硼酸固体的质量和水的质量,分析需要的砝码和游码;根据溶解的操作分析用到的玻璃仪器。
本题的难度不大,了解溶液配制的步骤和操作是解答本题的基础知识。
第2页,共2页
第1页,共1页
一、单选题
下列配制溶液常见的操作中,正确的是
A. 取用氯化钠 B. 称量氯化钠
C. 量取蒸水 D. 溶解氯化钠
青海玉树地震后,为防止疾病传染,需对灾区喷洒消毒剂,进行医疗卫生防疫.质量分数为的过氧乙酸就是用于环境喷洒和用具浸泡的一种消毒剂.现有市售质量分数为的过氧乙酸,要配制的过氧乙酸,需要市售过氧乙酸的质量为
A. B. C. D.
保持温度不变,小心蒸发不饱和溶液蒸发皿中始终有溶液,则溶液中溶质的质量分数与时间的关系合理的是
A. B.
C. D.
某同学选用氢氧化钠固体与水配制溶质质量分数为的氢氧化钠溶液,下列说法错误的是
需称取氢氧化钠固体
称量前托盘天平应先检查游码是否归零,并调节平衡
用托盘天平称量氢氧化钠固体时,为防止污染托盘,可将氢氧化钠放在纸上称量
选用量筒量取的水
存放溶液时,为确保数据准确,将试剂瓶用蒸馏水清洗后,立即倒入所配溶液封存
A. B. C. D.
现有编号为、、的三个烧杯中均分别盛有克水,时向三个烧杯中分别加入克、克、克的同种物质,充分溶解,实验结果如图所示,下列判断正确的是
A. 中所得溶液一定是不饱和溶液
B. 中所得溶液溶质的质量分数相等
C. 若中溶液升温到,溶液的质量一定不变
D. 若中溶液恒温蒸发,溶质的质量分数一定变大
实验室配制溶质质量分数为的氯化钠溶液。下列说法中错误的是
A. 实验的步骤为计算、称取、量取、溶解、转移
B. 溶解过程中玻璃棒的作用是搅拌,以加快氯化钠的溶解速率
C. 把配制好的氯化钠溶液倒入刚用蒸馏水润洗过的试剂瓶中,并贴上标签
D. 量取水时,用规格为的量筒量取蒸馏水
时的 硝酸钾的不饱和溶液,在恒温下蒸发水分至有较多的晶体析出,然后冷却至并保持温度不变。能正确表示此过程中溶质质量分数与时间的关系的示意图是
A. B.
C. D.
欲配制 质量分数为的氯化钠溶液,必须要的仪器组合是
托盘天平;烧杯;玻璃棒; 量筒。
A. B. C. D.
时,四个实验小组分别取不同质量的氯化钠,逐渐加入到各盛有水的烧杯中,不断搅拌直到不再溶解为止,然后分别称量剩余氯化钠的质量。记录数据如下表:
实验小组 第一组 第二组 第三组 第四组
水的质量
所取的质量
剩余的质量
下列说法正确的是
A. 第三组所得溶液的溶质与溶剂的质量比为:
B. 第四组溶液的溶质质量分数比第二组大
C. 时,氯化钠饱和溶液中含有溶质
D. 实验中只有第一组得到的是不饱和溶液
时食盐的溶解度为,在该温度下,将食盐溶于水中配制溶液甲.取甲溶液,加入食盐晶体得到溶液乙.则甲、乙两种溶液中溶质的质量分数正确的一组是
A. 甲: 乙: B. 甲: 乙:
C. 甲: 乙: D. 甲: 乙:
二、填空题
某化学活动小组欲配制克的生理盐水,下图是该小组同学配制的操作过程.请回答下列问题:
写出、所示仪器的名称:____________
请写出图中的一处错误______
操作中应称量氯化钠的质量是______克,称量时若指针偏左,应进行的操作是______
操作中玻璃棒的作用是______
下列错误操作中,可能导致溶质质量分数偏高的是______填序号
装瓶时有溶液洒出
量取水时俯视读数
称量时砝码与药品位置颠倒.
配制溶质质量分数一定的氯化钠溶液常按以下操作顺序进行。
请回答下列问题:
实验室配制溶质质量分数一定的溶液时,可能涉及以下操作:称量 计算 溶解 :量取装瓶贴标签。用氯化钠固体和蒸馏水配制的氯化钠溶液时,其操作顺序是______填序号。
计算配制溶质质量分数为的氯化钠溶液所需:氯化钠______ ,水______ 。
用托盘天平称量所需的氯化钠时,发现托盘天平的指针偏向左盘,应______。
A、增加适量氯化钠固体 、减少适量氯化钠固体 、调节平衡螺母
配制上述溶液需要用到的玻璃仪器有量筒、烧杯、玻璃棒和______,其中玻璃棒在该实验中所起的作用是______。
在用量筒量取所需水的过程中,小明俯视读数,这样配得的溶液浓度会______填“偏高”、“偏低”、或“无影响”。
硝酸钾可作为无土栽培的营养液。小温同学在配制的硝酸钾溶液过程中,向硝酸钾固体中分批加水,并充分搅拌,流程如图所示:
在配制硝酸钾溶液的过程中,除上图所示的器材以外,还需要用到的玻璃仪器是 ______。
图中可能符合上述实验结果的是 ______。
三、探究题
欲配制溶质质量分数为的硝酸铵,实验操作如图所示,请回答下列问题:
量取所需要的水应选择______选填“”、“”或“”量筒。
调平衡后,用托盘天平称量所需的硝酸铵时,发现托盘天平的指针偏向左盘,应______选填序号。
A.增加适量硝酸铵固体
B.减少适量硝酸铵固体
C.调节平衡螺母
D.增加砝码
将硝酸铵和水依次倒入烧杯中,要用玻璃棒搅拌,其目的是______。
用上述图示的序号表示配制溶液的操作顺序______。
在做操作时,烧杯的温度______选填“升高”或“降低”了。
若量取蒸馏水的体积时仰视读数,则该实验小组实际配制的硝酸铵溶液的溶质质量分数比计划配制的溶质质量分数偏______填“高”、“低”。
将制得的硝酸铵溶液装瓶保存时,试剂瓶的标签上应注明等信息______。
的硼酸溶液可用于清洗皮肤的小面积创伤。现配制质量分数为的硼酸溶液,实验操作如下:
称量硼酸固体的质量:在图中分别标出所选砝码的质量和游码的示数。
量取水的体积,用量筒量取______水
溶解:用到的玻璃仪器是______。
装瓶、贴标签。
答案和解析
1.【答案】
【解析】解:、取用固体粉末状药品时,瓶塞要倒放,应用药匙取用,不能用手接触药品,图中瓶塞没有倒放,图中所示操作错误。
B、托盘天平的使用要遵循“左物右码”的原则,图中所示操作砝码与药品位置放反了,图中所示操作错误。
C、量筒读数时视线要与量筒内液体的凹液面的最低处保持水平,图中视线没有对着刻度线的一侧,图中所示操作错误。
D、配制溶液时,溶解操作应在烧杯中进行,用玻璃棒不断搅拌,图中所示操作正确。
故选:。
A、根据固体药品的取用方法进行分析判断。
B、根据托盘天平的使用要遵循“左物右码”的原则进行分析判断。
C、根据量筒读数时视线要与凹液面的最低处保持水平进行分析判断。
D、根据溶解操作的方法,进行分析判断。
本题难度不大,熟悉配制溶液的实验步骤、各操作的注意事项是解答此类试题的关键。
2.【答案】
【解析】解:设需要市售过氧乙酸的质量为.
故选:.
该题属于一道溶液稀释问题的计算题,用的溶液配制的溶液,我们可以向的溶液中加一定质量的水即可,在稀释前后,溶液中溶质的质量不变,了解了这一点,该题便简单易解.
该题是一道溶液稀释问题的计算题,要求学生掌握好解题的规律,即稀释前后溶质的质量不变,本题便可迎刃而解.
3.【答案】
【解析】保持温度不变,氯化钠溶液蒸发水分是由不饱和溶液变为饱和溶液的过程,该过程中溶剂质量减小,溶液中溶质质量分数增大,当氯化钠溶液变为饱和溶液后再蒸发水时,溶液仍为饱和溶液,溶质质量分数将不变,A正确。
4.【答案】
【解析】解:溶质质量溶液质量溶质的质量分数,配制溶质质量分数为的氢氧化钠溶液,需氢氧化钠的质量,故选项说法正确。
称量前托盘天平应先检查游码是否归零,并调节平衡,故选项说法正确。
托盘天平的使用要遵循“左物右码”的原则,且氢氧化钠具有腐蚀性,应放在玻璃器皿中称量,故选项说法错误。
溶剂质量溶液质量溶质质量,所需溶剂的质量为合,应用规格为的量筒量取水的体积,故选项说法错误。
存放溶液时,为确保数据准确,将试剂瓶用蒸馏水清洗后,立即倒入所配溶液封存,会造成实际量取的水的体积偏大,则使溶质质量分数偏小,故选项说法错误。
故选:。
利用溶质质量溶液质量溶质的质量分数,进行分析判断。
根据托盘天平的使用方法,进行分析判断。
根据托盘天平的使用要遵循“左物右码”的原则、氢氧化钠具有腐蚀性,进行分析判断。
根据溶剂质量溶液质量溶质质量,计算出所需水的质量和体积,进而判断所需量筒的量程。
存放溶液时,为确保数据准确,将试剂瓶用蒸馏水清洗后,会造成实际量取的水的体积偏大,进行分析判断。
本题难度不大,明确配制一定溶质质量分数的溶液实验步骤计算、称量、溶解、注意事项等是正确解答本题的关键。
5.【答案】
【解析】解:、依据饱和溶液的概念可知,、中有固体出现,一定是饱和溶液,中没有固体出现,可能是恰好溶解,则可能是饱和溶液;故错误;
B、溶液都是相同温度下的饱和溶液,所以溶液的溶质质量分数一定相等,故正确;
C、烧杯中溶液升温至,溶解度改变,溶液的质量改变,故错误;
D、恒温蒸发溶剂,饱和溶液析出晶体,但溶液仍为饱和溶液,相同温度下的同种物质的饱和溶液溶质质量分数因溶解度相等而相等,溶质质量分数不变,故错误;
故选:。
根据在一定温度和溶剂中,有溶质析出的溶液中,溶质达到最大溶解能力,溶质不会溶解,则溶液一定为饱和溶液,没有固体析出的溶液可能是恰好饱和或不是饱和溶液;在饱和溶液中溶质的质量分数最大且相同进行解答。
本考点考查了溶液中溶质质量分数的比较、饱和溶液与不饱和溶液等,综合性强,要加强记忆,理解应用;本考点主要出现在选择题和填空题中。
6.【答案】
【解析】略
7.【答案】
【解析】解:时的 硝酸钾的不饱和溶液,在恒温下蒸发水分至有较多的晶体析出这一过程中,溶质的质量分数不断变大当达到饱和时溶质质量分数最大且不变,然后冷却至并保持温度不变,这一过程硝酸钾溶解度不断变小,浓度不断变小,达到时,溶质质量分数不再改变。
故选:。
利用硝酸钾溶解度随温度升高而升高的知识,不饱和溶液变成饱和溶液溶质质量分数逐渐变大,但只要是同一温度的饱和溶液溶质质量分数一定不变。
此题是对溶液随外界条件变化的一个全面考察,能很好训练学生对相关知识的分析能力,是一道较为全面的总和题型。
8.【答案】
【解析】解:配制溶质质量分数一定的溶液的基本步骤:计算、称量、量取、溶解、装瓶存放,其中需要用到的仪器有:烧杯、玻璃棒、量筒、胶头滴管、天平、药匙。
故选:。
实验室配制克质量分数为的氢氧化钠溶液的操作步骤分别是:计算、称量、溶解,根据各操作所需要使用的仪器,判断所列仪器是否需要。
本题难度不大,明确配制一定溶质质量分数的溶液实验步骤、所需的仪器是正确解答本题的关键。
9.【答案】
【解析】解:、第三组所得溶液的溶质与溶剂的质量比为:::,该选项说法不正确;
B、第四组溶液的溶质质量分数和第二组溶液的溶质质量分数相等,是因为溶液质量都是,溶质质量都是,该选项说法不正确;
C、时,水中溶解氯化钠恰好饱和,因此氯化钠饱和溶液中含有氯化钠质量:,该选项说法不正确;
D、由表中数据可知,水中溶解氯化钠恰好饱和,因此实验中只有第一组得到的是不饱和溶液,该选项说法正确。
故选:。
根据表中数据可以判断,一定质量的溶剂里达到饱和状态时,溶解的溶质质量;
饱和溶液的溶质质量分数;
溶液中溶质质量分数。
饱和溶液和不饱和溶液之间可以相互转化,要注意理解。
10.【答案】
【解析】解:时的溶解度是,在该温度下,将全部溶于水中,配成溶液甲的溶质质量分数;取甲溶液,依据溶液的均一性可知该溶液溶液中的溶质是中的溶质为,则溶剂的量是,依据该温度下的溶解度可知,溶剂中最多能溶解的氯化钠的质量是,故加入晶体,得到的乙溶液为饱和溶液,故乙溶液的溶质质量分数为;
故选:。
时的溶解度是,则该温度下将溶于水中配成的溶液甲为不饱和溶液;取甲溶液,依据溶液的均一性可知该溶液中的溶质为,则溶剂的量是,依据该温度下的溶解度可知,溶剂中最多能溶解的氯化钠的质量是,故加入晶体,得到的乙溶液为饱和溶液,据此分析解答即可.
根据一定温度下饱和溶液的溶质质量分数为该温度下该物质的溶质质量分数的最大值,利用溶质质量分数与溶解度的关系,可对乙溶液的质量分数做出判断.
11.【答案】烧杯 量筒 瓶塞正放 减少药品 搅拌加速溶解
【解析】解:、所示仪器的名称分别是烧杯和量筒.
故填:烧杯;量筒.
中的瓶塞正方时,容易沾上杂质,是一种错误放置方法.
故填:瓶塞正放.
应称量氯化钠的质量是:,称量时若指针偏左,说明药品过量,应进行的操作是减少药品.
故填:; 减少药品.
操作中玻璃棒的作用是搅拌加速溶解.
故填:搅拌加速溶解.
装瓶时有溶液洒出,不影响质量分数;称量时砝码与药品位置颠倒,使称量的溶质质量偏小,会导致质量分数偏小;
量取水时俯视读数,会使量取的水偏少,会导致质量分数偏大.
故填:.
要熟悉各种仪器的名称、用途;
试剂瓶上的瓶塞取下时应该倒放在桌上;
通过计算可以知道溶质的质量;
玻璃棒的作用有:搅拌、引流、转移物质等;
操作不当会导致配制溶液的质量分数不准确.
配制一定质量分数的溶液时,要注意仪器的使用方法、药品的称量方法、计算等方面的问题,力求面面俱到,万无一失.
12.【答案】 胶头滴管 加速食盐的溶解 偏高
【解析】解:配制溶液的步骤为计算、称量、溶解、装瓶保存;
配制溶液时所需氯化钠的质量为:,水的质量为:,由密度公式可得水的体积为;
天平指针偏向谁,谁的质量就大,所以氯化钠取多了;
配制溶质质量分数为 的氯化钠溶液的仪器有:托盘天平、药匙、量筒、胶头滴管、烧杯、玻璃棒;其中属于玻璃仪器的有:量筒、胶头滴管、烧杯、玻璃棒;玻璃棒的搅拌能加速食盐的溶解。
量取水时俯视凹液面最低处,会使得量取水的体积小于,则所得溶液的溶质质量分数为大于;
故答案为:;;;;胶头滴管,加速溶解;偏高。
据配制溶液的步骤回答;
根据溶质质量分数的计算公式计算解答;
根据天平指针偏向谁谁的质量就大分析解答;
据配制溶液所用仪器和玻璃棒的作用回答;
俯视读数,量取的水偏少,则配制的溶液的溶质的质量分数偏高;
配制溶液两种常见操作:固体溶质加水溶解,配制步骤计算称量溶解装瓶;液体加水稀释,配制步骤计算量取溶解装瓶。
13.【答案】量筒、胶头滴管和玻璃棒
【解析】解:根据图可知,将硝酸钾固体放入烧杯后,需要用量筒和胶头滴管量出规定体积的水,注入烧杯后,再用玻璃棒不断搅拌,最终得到硝酸钾的溶液,因此还需要用到的玻璃仪器为:量筒、胶头滴管和玻璃棒。
根据图可知,在烧杯中注入水和水时,始终存在硝酸钾的固体,因此这时肯定是硝酸钾的饱和溶液。当注入水时,没有硝酸钾固体存在,那么溶液可能饱和也可能不饱和。当注入水时,硝酸钾溶液肯定不饱和。
如果前三次都是硝酸钾在同一温度下的饱和溶液,那么三者的溶质质量分数相同。由于第四次肯定是不饱和溶液,那么它的溶质质量分数肯定小于前三次,故A正确;
如果前两次是硝酸钾的饱和溶液,而后两次都是它的不饱和溶液,那么前两次的溶质质量分数相同,后两次的溶质质星分数都小于前两次。对于后两次而言,溶质的质量相同,但溶剂的质量不断增大,因此溶质质量分数越来越小,故选C。
故选AC。
故答案为:量筒、胶头滴管和玻璃棒;
。
根据配制硝酸钾溶液的过程确定所需的实验器材;
在配制溶液的过程中,如果有未溶的固体存在,那么溶液肯定是饱和的;如果没有未溶的固体存在,那么溶液可能饱和也可能不饱和,据此对溶液的溶质质量分数的变化进行判断即可。
在做此类题时,首先读懂题意,找出题中的叙述与图象的联系,在运用所学的知识结合图象中的关键点进行分析解答,通过该题,要掌握化学中的数形结合的思想。
14.【答案】 加速溶解 降低 低 溶液的名称、溶质的质量分数
【解析】解:欲配制溶质质量分数为的硝酸铵溶液,需要水的质量为,而水的密度为,所以需要量取水的体积为,故应该选择的量筒;
用托盘天平称量药品时,物体放在左盘,而砝码放在右盘,用托盘天平称量所需的硝酸铵时,发现托盘天平的指针偏向左盘,说明取的硝酸铵固体过多,所以应该减少适量硝酸铵固体,故选B;
硝酸铵在溶解时用玻璃棒搅拌能够加速硝酸铵的溶解;
配制溶液的操作步骤是:计算称取固体量去液体溶解,所以正确的操作步骤为:;
硝酸铵溶于水的过程要吸收热量而使溶液的温度降低。
仰视读数,会导致量取的水变多,溶液变稀,实际配制的硝酸铵溶液的溶质质量分数比计划配制的溶质质量分数偏低。
图中标签中填上相应的内容是溶液的名称、溶质的质量分数。
故答案为: ;
;
加速溶解;
;
降低;
低;
溶液的名称、溶质的质量分数。
根据溶液中溶质的质量分数的计算公式进行解答;
根据天平的使用方法来进行解答;
硝酸铵在溶解时用玻璃棒搅拌能够加速硝酸铵的溶解,可以据此解答;
根据溶液配制的过程和步骤进行解答;
硝酸铵溶于水的过程要吸收热量而使溶液的温度降低,可以据此解答;
根据仰视读数,会导致量取的水变多解答;
图中标签中填上相应的内容是溶液的名称、溶质的质量分数。
通过回答本题知道了溶质、溶剂质量的计算方法,用天平称量时的注意事项,掌握了配制溶质质量分数一定的溶液的基本步骤。
15.【答案】 烧杯、玻璃棒
【解析】解:现配制质量分数为的硼酸溶液,需要硼酸的质量为:,需要水的质量为:。
称量硼酸固体的质量:所选砝码的质量为,游码的示数为,如下图:。
由上述计算可知,需要水的质量是,量取水的体积,用量筒量取水;
溶解:用到的玻璃仪器是烧杯、玻璃棒。
故答为:见上图;;烧杯、玻璃棒。
根据溶质质量分数的计算公式计算出需要硼酸固体的质量和水的质量,分析需要的砝码和游码;根据溶解的操作分析用到的玻璃仪器。
本题的难度不大,了解溶液配制的步骤和操作是解答本题的基础知识。
第2页,共2页
第1页,共1页
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
