辽宁省丹东市东港第二高级中学2021-2022学年高二上学期11月第二次教学检测化学试卷(PDF版含答案)
文档属性
| 名称 | 辽宁省丹东市东港第二高级中学2021-2022学年高二上学期11月第二次教学检测化学试卷(PDF版含答案) |

|
|
| 格式 | |||
| 文件大小 | 2.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-13 00:00:00 | ||
图片预览

文档简介
2020 级高二年级第二次教学检测
化学试题
注意事项:
1. 答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置。
2. 回答选择题时,选出每小题答案后用铅笔在答题卡上对应题目的答案标号涂黑,如需改动,用橡
皮擦干净后再选涂其它答案标号。回答非选择题时,将答案写在答题纸上,写在本试卷上无效。
可能用到的相对原子质量:H 1 C 12 O 16 Mg 24 S 32 Pb 207
一、单项选择题:本题共 10 个小题,每小题 2 分,共 20 分,每小题只有一个选项符合题目要求。
1.《秋浦歌》中的一首“炉火照天地,红星乱紫烟。赧郎明月夜,歌曲动寒川”描写的是我国古代劳动
人民“冶炼金属”的热烈场面。下列有关金属冶炼的说法错误的是( )
A.应用热还原法可以冶炼铁 B.应用铝热法可以冶炼镁
C.应用电解法可以冶炼铝 D.应用热分解法可以冶炼汞
2.下列关于化学反应与能量的说法正确的是( )
A.风力、流水、原煤、电力、天然气都属于一次能源
B.NaOH 固体溶于水温度升高,是因为发生了放热反应
C.甲烷燃烧放热,是因为破坏反应物化学键所需的能量特别大
D.石墨转化为金刚石是吸热反应,故石墨比金刚石更稳定
3.下列有关测定中和反应反应热实验的说法正确的是( )
A.在一次完整的反应热实验中,温度计至少需要使用两次
B.已知中和热 ΔH= -57.3 kJ·mol-1,该数值不会因酸碱的用量而改变
C.测定中和反应反应热的实验中,混合溶液的温度不再变化时,该温度为终止温度
D.某同学通过实验测出稀盐酸和稀 NaOH 溶液生成 1 mol H2O 反应热 ΔH= -52.3 kJ·mol-1,
造成这一结果的原因不可能是量热计保温效果不好
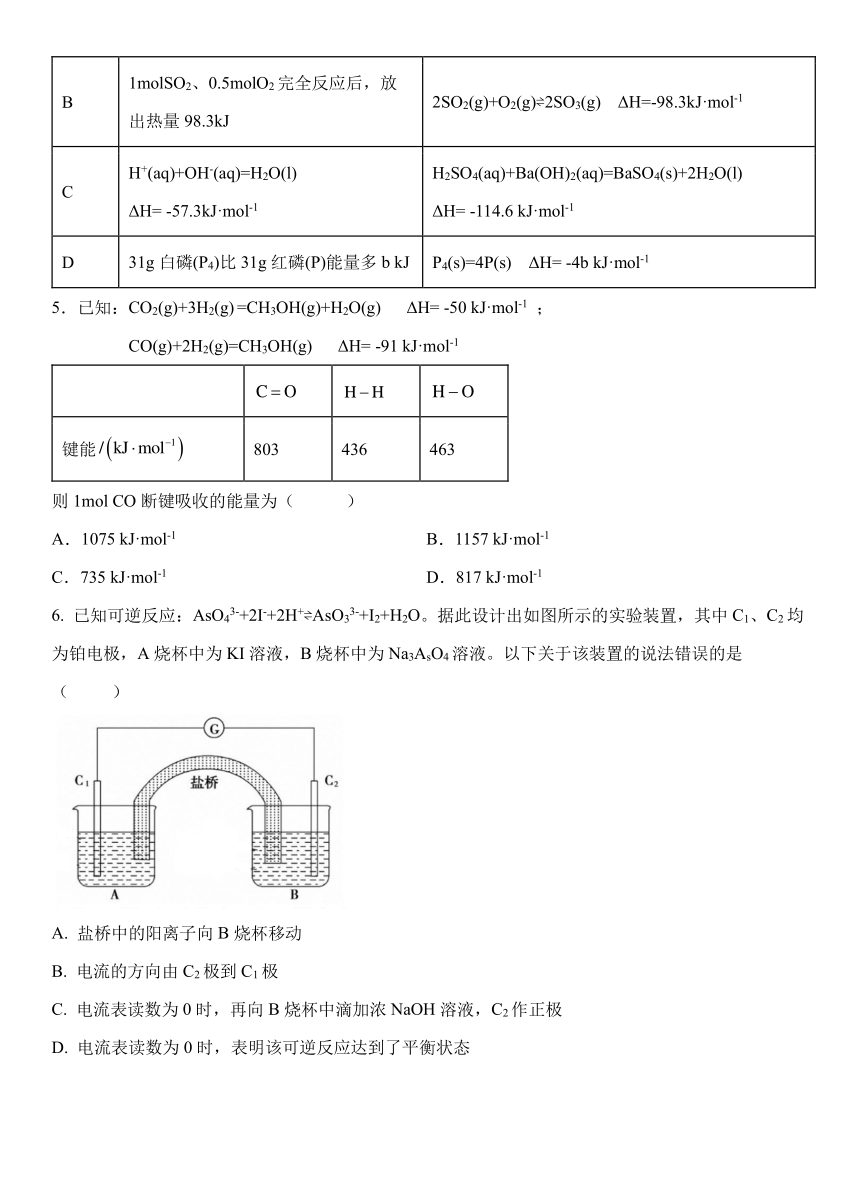
4.下列热化学方程式正确的是( )
选项 已知条件 热化学方程式
A H2的燃烧热为 a kJ·mol-1 H2+Cl2=2HCl ΔH= -a kJ·mol-1
1molSO2、0.5molO2完全反应后,放
B 2SO2(g)+O2(g) 2SO3(g) ΔH=-98.3kJ·mol-1
出热量 98.3kJ
H+(aq)+OH-(aq)=H2O(l) H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l)
C
ΔH= -57.3kJ·mol-1 ΔH= -114.6 kJ·mol-1
D 31g 白磷(P4)比 31g 红磷(P)能量多 b kJ P4(s)=4P(s) ΔH= -4b kJ·mol-1
5.已知:CO2(g)+3H2(g) =CH3OH(g)+H2O(g) ΔH= -50 kJ·mol-1 ;
CO(g)+2H -12(g)=CH3OH(g) ΔH= -91 kJ·mol
C =O H H H O
键能 / (kJ mol 1 ) 803 436 463
则 1mol CO 断键吸收的能量为( )
A.1075 kJ·mol-1 B.1157 kJ·mol-1
C.735 kJ·mol-1 D.817 kJ·mol-1
6. 已知可逆反应:AsO 3-4 +2I-+2H+ AsO 3-3 +I2+H2O。据此设计出如图所示的实验装置,其中 C1、C2 均
为铂电极,A 烧杯中为 KI 溶液,B 烧杯中为 Na3AsO4 溶液。以下关于该装置的说法错误的是
( )
A. 盐桥中的阳离子向 B 烧杯移动
B. 电流的方向由 C2 极到 C1 极
C. 电流表读数为 0 时,再向 B 烧杯中滴加浓 NaOH 溶液,C2作正极
D. 电流表读数为 0 时,表明该可逆反应达到了平衡状态
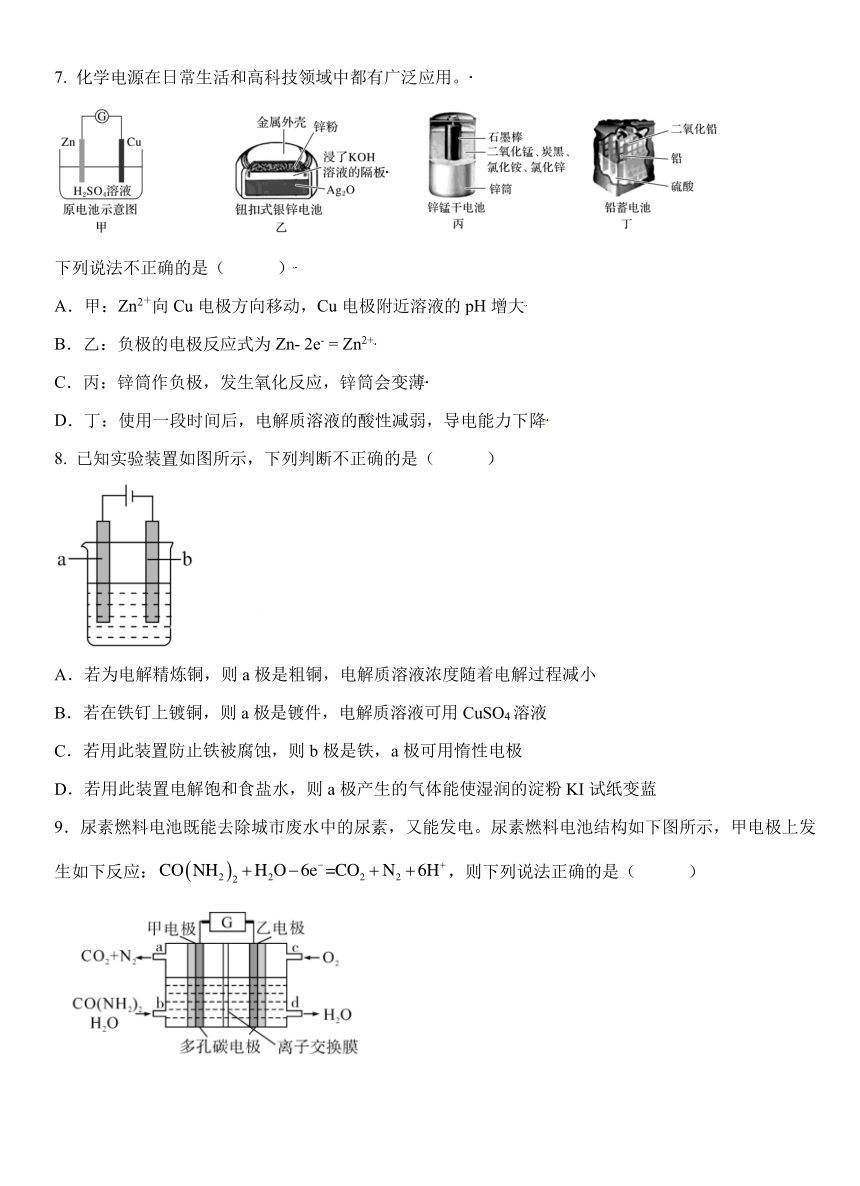
7. 化学电源在日常生活和高科技领域中都有广泛应用。
下列说法不正确的是( )
+
A.甲:Zn2 向 Cu 电极方向移动,Cu 电极附近溶液的 pH 增大
B.乙:负极的电极反应式为 Zn- 2e- = Zn2+
C.丙:锌筒作负极,发生氧化反应,锌筒会变薄
D.丁:使用一段时间后,电解质溶液的酸性减弱,导电能力下降
8. 已知实验装置如图所示,下列判断不正确的是( )
A.若为电解精炼铜,则 a 极是粗铜,电解质溶液浓度随着电解过程减小
B.若在铁钉上镀铜,则 a 极是镀件,电解质溶液可用 CuSO4 溶液
C.若用此装置防止铁被腐蚀,则 b 极是铁,a 极可用惰性电极
D.若用此装置电解饱和食盐水,则 a 极产生的气体能使湿润的淀粉 KI 试纸变蓝
9.尿素燃料电池既能去除城市废水中的尿素,又能发电。尿素燃料电池结构如下图所示,甲电极上发
+
生如下反应:CO(NH2 ) +H2O 6e =CO2 +N2 +6H ,则下列说法正确的是( )2
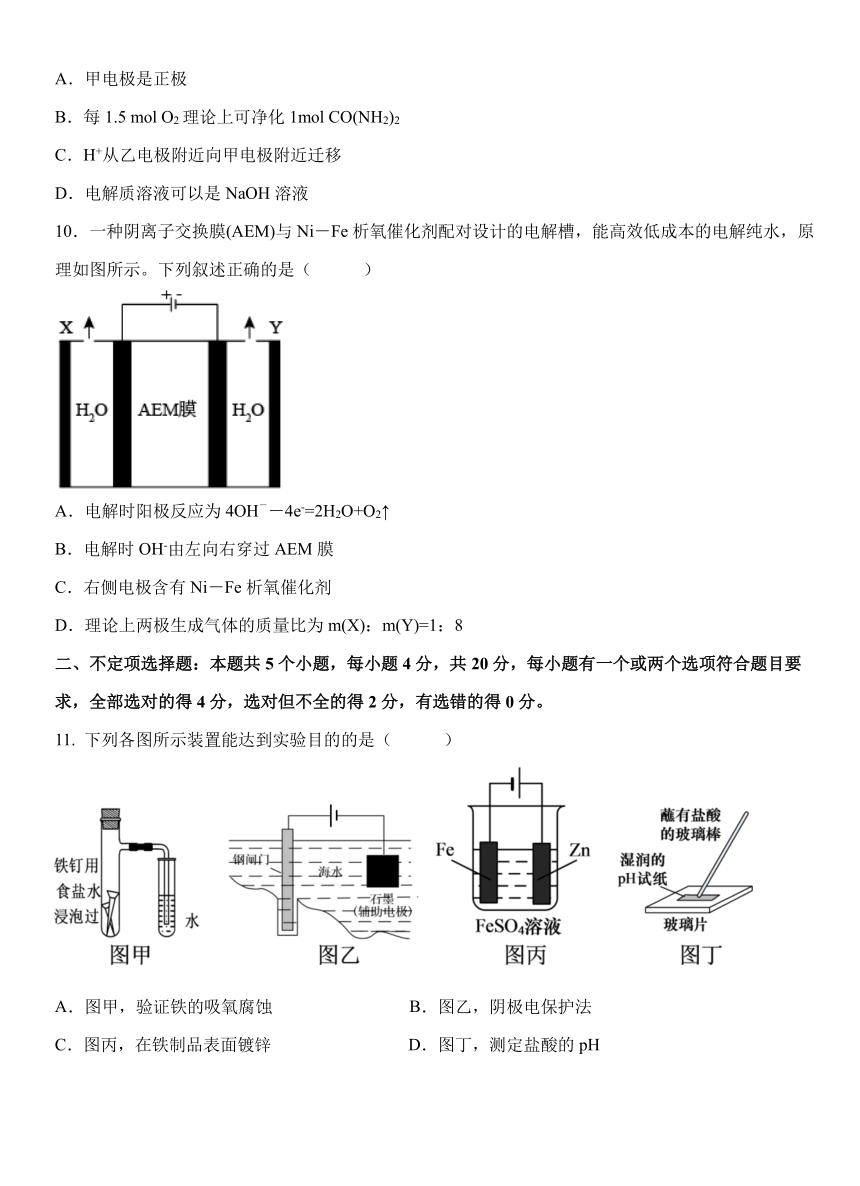
A.甲电极是正极
B.每 1.5 mol O2 理论上可净化 1mol CO(NH2)2
C.H+从乙电极附近向甲电极附近迁移
D.电解质溶液可以是 NaOH 溶液
10.一种阴离子交换膜(AEM)与 Ni-Fe 析氧催化剂配对设计的电解槽,能高效低成本的电解纯水,原
理如图所示。下列叙述正确的是( )
.电解时阳极反应为 -A 4OH -4e-=2H2O+O2↑
B.电解时 OH-由左向右穿过 AEM 膜
C.右侧电极含有 Ni-Fe 析氧催化剂
D.理论上两极生成气体的质量比为 m(X):m(Y)=1:8
二、不定项选择题:本题共 5 个小题,每小题 4 分,共 20 分,每小题有一个或两个选项符合题目要
求,全部选对的得 4 分,选对但不全的得 2 分,有选错的得 0 分。
11. 下列各图所示装置能达到实验目的的是( )
A.图甲,验证铁的吸氧腐蚀 B.图乙,阴极电保护法
C.图丙,在铁制品表面镀锌 D.图丁,测定盐酸的 pH
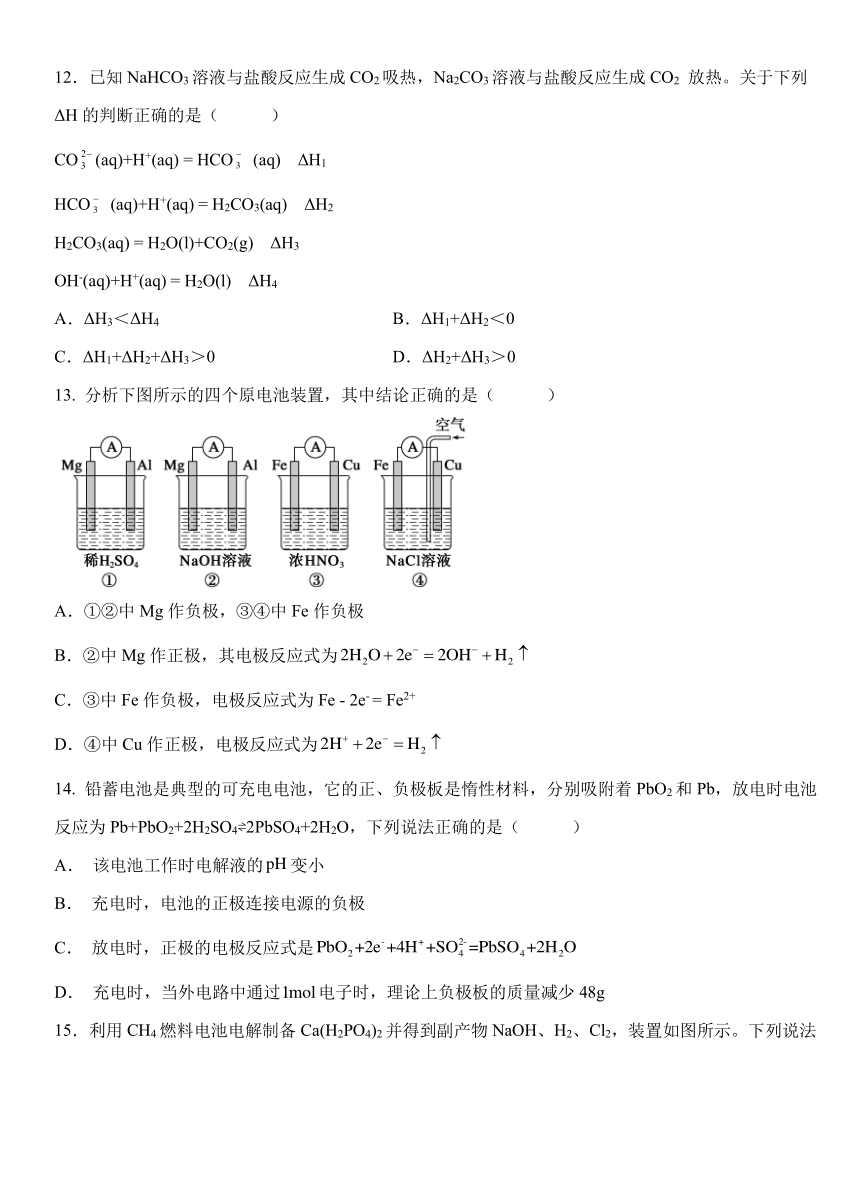
12.已知 NaHCO3 溶液与盐酸反应生成 CO2 吸热,Na2CO3溶液与盐酸反应生成 CO2 放热。关于下列
ΔH 的判断正确的是( )
2
CO +3 (aq)+H (aq) = HCO 3 (aq) ΔH1
HCO 3 (aq)+H
+(aq) = H2CO3(aq) ΔH2
H2CO3(aq) = H2O(l)+CO2(g) ΔH3
OH-(aq)+H+(aq) = H2O(l) ΔH4
A.ΔH3<ΔH4 B.ΔH1+ΔH2<0
C.ΔH1+ΔH2+ΔH3>0 D.ΔH2+ΔH3>0
13. 分析下图所示的四个原电池装置,其中结论正确的是( )
A.①②中 Mg 作负极,③④中 Fe 作负极
B.②中 Mg 作正极,其电极反应式为2H2O+ 2e = 2OH +H2
C.③中 Fe 作负极,电极反应式为 Fe - 2e- = Fe2+
+
D.④中 Cu 作正极,电极反应式为2H + 2e = H2
14. 铅蓄电池是典型的可充电电池,它的正、负极板是惰性材料,分别吸附着 PbO2和 Pb,放电时电池
反应为 Pb+PbO2+2H2SO4 2PbSO4+2H2O,下列说法正确的是( )
A. 该电池工作时电解液的 pH 变小
B. 充电时,电池的正极连接电源的负极
- + 2-
C. 放电时,正极的电极反应式是PbO2 +2e +4H +SO4 =PbSO4 +2H2O
D. 充电时,当外电路中通过1mol电子时,理论上负极板的质量减少 48g
15.利用 CH4 燃料电池电解制备 Ca(H2PO4)2 并得到副产物 NaOH、H2、Cl2,装置如图所示。下列说法
不正确的是( )
A. -a 极反应:CH 8e +4O2 4 =CO2+2H2O
B.A 膜和 C 膜均为阴离子交换膜,B 膜为阳离子交换膜
C.可用铁电极替换阴极的石墨电极
D. a 极上通入标况下 2.24 L 甲烷,理论上产品室可新增 0.8 mol Ca(H2PO4)2
三、非选择题:本题共 5 个大题,共 60 分。
16. (每空 2 分,共 12 分)化学反应伴随能量变化,获取反应能量变化有多条途径。回答下列问题:
(1)理论研究表明,在 101kPa 和 298K 下,HCN(g) = HNC(g)异构化反应过程的能量变化如图所示,计
算可得:HCN(g) = HNC(g) H=_______kJ·mol-1。HCN 与 HNC 稳定性较强的是________。
(2)已知:
化学键种类 C—H N—H
键能(kJ/mol) a b
计算可得:HCN(g) = HNC(g) H=_______kJ·mol-1(用含 a、b 的式子表示)。
(3)已知:4gCH4 完全燃烧生成 CO2(g)、H2O(l)时放出热量 222.5kJ,则表示甲烷燃烧热的热化学方程式
为________________________________________________。
(4)实验室用 50mL0.50mol/L 盐酸、50mL0.55mol/LNaOH 溶液和如图所示装置,进行测定中和热的实
验。
① 实验装置中尚缺少的一种实验用品是__________。
②若测得中和热的数值偏低,请你分析可能的原因是( )
A.测量盐酸的温度后,温度计没有用水冲洗干净
B.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓
C.做本实验的当天室温较高
D.将 50mL0.55mol/L 氢氧化钠溶液取成了 50mL0.55mol/L 的氨水
E. 在量取盐酸时仰视读数
17.(每空 2 分,共 12 分)甲醇是一种重要的化工原料,具有开发和应用的广阔前景。
I. 已知甲醇燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
① CH3OH(g)+H2O(g)=CO2 (g)+3H2 (g) ΔΔHH==4 94.0 kJ m
-1
9.0 kJ·molol-1
② CH3OH(g)+1/2 O2(g)=CO -12(g)+2H2(g) ΔH= -192.9 kJ·mol
又知:③ H2O(g)=H2O(l) ΔΔHH==-4 -44 k4J kmJ·mol
-1
ol-1
则表示甲醇摩尔燃烧焓的热化学方程式为_________________________________________。
II.如图所示,其中甲池的总反应式为 2CH3OH+3O2+4KOH=2K2CO3+6H2O,完成下列问题:
(1)甲池燃料电池的负极反应方程式为____________________________。
(2)写出乙池中电解总反应的化学方程式:_______________________________。
(3)甲池中消耗 224 mL(标准状况下)O2,此时丙池中理论上最多产生__________g 沉淀,此时乙池中溶
液的体积为 400 mL,该溶液的 c(H+)=__________。
(4)若以该甲醇燃料电池为电源,用石墨做电极电解 200mL 含有如下离子的溶液。
2+ + - SO2-离子 Cu H Cl 4
c/mol L-1 0.5 2 2 0.5
电解一段时间后,当两极收集到相同体积(相同条件)的气体时(忽略溶液体积的变化及电极产物可能存
在的溶解现象),电路中转移的电子的物质的量是______________mol。
18.(每空 2 分,共 12 分)钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢铁占世界钢铁年产量的三
分之一。请回答钢铁在腐蚀、防护过程中的有关问题。
(1)在实际生产中,可在铁件的表面镀上锌保护层或锡保护层防止铁被腐蚀。镀层破损后,镀锡铁和
镀锌铁更容易被腐蚀的是___________。(填“镀锡铁”或“镀锌铁”)
(2)下列哪个装置可防止铁棒被腐蚀( )
(3)利用右图装置可以模拟铁的电化学防护。
①若 X 为碳棒,为减缓铁的腐蚀,开关 K 应置于___________处。假设海水中只有 NaCl 溶质,写出此
时总离子反应方程式:_________________________________。
②若 X 为锌,开关 K 置于 M 处,该电化学防护法称为_________________,写出铁电极处的电极反应
式:_______________________________________。
19. (每空 2 分,共 12 分)氯碱工业是以电解饱和食盐水为基础的基本化学工业。如图是某氯碱工业生产
原理示意图:
(1)装置 A 所用食盐水由粗盐水精制而成。精制时,为除去食盐水中的Mg2+ 和Ca2+,要加入的试剂
分别为____________________、____________________(写化学式)。
(2)氯碱工业是高耗能产业,按上图将电解池与燃料电池相组合的新工艺可以节(电)能 30%以上,
相关物料的传输与转化关系如图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。
①图中 Y 是____________________(填化学式);X 与稀 NaOH 溶液反应的离子方程式为
______________________________________。
②比较图示中氢氧化钠的质量分数 a% 与b% 的大小:a _____ b(填“>”“<”或“=”)。
③若用装置 B 作为装置 A 的辅助电源,每当消耗标准状况下氧气的体积为 11.2L 时,则装置 B 可向装
置 A 提供的电量约为__________________________(一个 e 的电量为1.60 10 19 C;计算结果精确到
0.01)。
20. (每空 2 分,共 12 分)电解原理在环保领域有广泛应用,按照要求回答下列问题。
-
(1)工业上,在强碱性条件下用电解法除去废水中的 CN ,装置如图所示:
依次发生的反应有:
- - - -
ⅰ.CN -2e +2OH ===CNO +H2O
- -
ⅱ.2Cl -2e ===Cl2↑
- - - -
ⅲ.3Cl2+2CNO +8OH ===N2+6Cl +2CO23 +4H2O
①a 为电源________(填“正”或“负”)极。
②通电过程中溶液 pH 不断________(填“增大”“减小”或“不变”)。
-
③除去 1 mol CN ,外电路中至少需要转移________ mol 电子。
④为了使电解池连续工作,需要不断补充______________________。(写化学式)
(2)利用如图所示装置(电极均为惰性电极)可吸收 SO2,并用阴极排出的溶液吸收 NO2来解决环境污 染问
题。
①阴极的电极反应式为:________________________________________。
②阳极的电极反应式为:________________________________________。
化学答案
一、 单项选择题
1~5 BDBDA 6~10 CBBBA
二、 不定项选择题
11 A 12 BD 13 B 14 CD 15 BD
三、 非选择题
16. (1) 59.3 HCN
(2) a-b
(3) CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H = - 890 kJ·mol-1
(4) ABD
17. Ⅰ CH3OH(g)+3/2 O2(g) = CO (g)+2H O(l) △H = - 764.7 kJ·mol-12 2
Ⅱ (1) CH3OH - 6e- +8OH- = CO 2- 3 +6H2O
(2)
(3) 1.16 0.1 mol/L
(4) 0.8
18. (1) 镀锡铁
(2) BD
(3) ① N ② 牺牲阳极保护法(牺牲阳极的阴极保护法) O2+4e-+2H2O=4OH-
19. (1) NaOH Na2CO3
(2) ① H2 Cl +2OH- =Cl- +ClO- 2 +H2O ② < ③ 1.93×105 C
20. (1) ① 正 ②减小 ③ 5 ④ NaOH 和 NaCl
(2) ① 2HSO -3 +2H++2e- = S2O 2-4 +2H2O
② SO2+2H - 2- +2O-2e =SO4 +4H
化学试题
注意事项:
1. 答卷前,考生务必将自己的姓名、考生号等填写在答题卡和试卷指定位置。
2. 回答选择题时,选出每小题答案后用铅笔在答题卡上对应题目的答案标号涂黑,如需改动,用橡
皮擦干净后再选涂其它答案标号。回答非选择题时,将答案写在答题纸上,写在本试卷上无效。
可能用到的相对原子质量:H 1 C 12 O 16 Mg 24 S 32 Pb 207
一、单项选择题:本题共 10 个小题,每小题 2 分,共 20 分,每小题只有一个选项符合题目要求。
1.《秋浦歌》中的一首“炉火照天地,红星乱紫烟。赧郎明月夜,歌曲动寒川”描写的是我国古代劳动
人民“冶炼金属”的热烈场面。下列有关金属冶炼的说法错误的是( )
A.应用热还原法可以冶炼铁 B.应用铝热法可以冶炼镁
C.应用电解法可以冶炼铝 D.应用热分解法可以冶炼汞
2.下列关于化学反应与能量的说法正确的是( )
A.风力、流水、原煤、电力、天然气都属于一次能源
B.NaOH 固体溶于水温度升高,是因为发生了放热反应
C.甲烷燃烧放热,是因为破坏反应物化学键所需的能量特别大
D.石墨转化为金刚石是吸热反应,故石墨比金刚石更稳定
3.下列有关测定中和反应反应热实验的说法正确的是( )
A.在一次完整的反应热实验中,温度计至少需要使用两次
B.已知中和热 ΔH= -57.3 kJ·mol-1,该数值不会因酸碱的用量而改变
C.测定中和反应反应热的实验中,混合溶液的温度不再变化时,该温度为终止温度
D.某同学通过实验测出稀盐酸和稀 NaOH 溶液生成 1 mol H2O 反应热 ΔH= -52.3 kJ·mol-1,
造成这一结果的原因不可能是量热计保温效果不好
4.下列热化学方程式正确的是( )
选项 已知条件 热化学方程式
A H2的燃烧热为 a kJ·mol-1 H2+Cl2=2HCl ΔH= -a kJ·mol-1
1molSO2、0.5molO2完全反应后,放
B 2SO2(g)+O2(g) 2SO3(g) ΔH=-98.3kJ·mol-1
出热量 98.3kJ
H+(aq)+OH-(aq)=H2O(l) H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l)
C
ΔH= -57.3kJ·mol-1 ΔH= -114.6 kJ·mol-1
D 31g 白磷(P4)比 31g 红磷(P)能量多 b kJ P4(s)=4P(s) ΔH= -4b kJ·mol-1
5.已知:CO2(g)+3H2(g) =CH3OH(g)+H2O(g) ΔH= -50 kJ·mol-1 ;
CO(g)+2H -12(g)=CH3OH(g) ΔH= -91 kJ·mol
C =O H H H O
键能 / (kJ mol 1 ) 803 436 463
则 1mol CO 断键吸收的能量为( )
A.1075 kJ·mol-1 B.1157 kJ·mol-1
C.735 kJ·mol-1 D.817 kJ·mol-1
6. 已知可逆反应:AsO 3-4 +2I-+2H+ AsO 3-3 +I2+H2O。据此设计出如图所示的实验装置,其中 C1、C2 均
为铂电极,A 烧杯中为 KI 溶液,B 烧杯中为 Na3AsO4 溶液。以下关于该装置的说法错误的是
( )
A. 盐桥中的阳离子向 B 烧杯移动
B. 电流的方向由 C2 极到 C1 极
C. 电流表读数为 0 时,再向 B 烧杯中滴加浓 NaOH 溶液,C2作正极
D. 电流表读数为 0 时,表明该可逆反应达到了平衡状态
7. 化学电源在日常生活和高科技领域中都有广泛应用。
下列说法不正确的是( )
+
A.甲:Zn2 向 Cu 电极方向移动,Cu 电极附近溶液的 pH 增大
B.乙:负极的电极反应式为 Zn- 2e- = Zn2+
C.丙:锌筒作负极,发生氧化反应,锌筒会变薄
D.丁:使用一段时间后,电解质溶液的酸性减弱,导电能力下降
8. 已知实验装置如图所示,下列判断不正确的是( )
A.若为电解精炼铜,则 a 极是粗铜,电解质溶液浓度随着电解过程减小
B.若在铁钉上镀铜,则 a 极是镀件,电解质溶液可用 CuSO4 溶液
C.若用此装置防止铁被腐蚀,则 b 极是铁,a 极可用惰性电极
D.若用此装置电解饱和食盐水,则 a 极产生的气体能使湿润的淀粉 KI 试纸变蓝
9.尿素燃料电池既能去除城市废水中的尿素,又能发电。尿素燃料电池结构如下图所示,甲电极上发
+
生如下反应:CO(NH2 ) +H2O 6e =CO2 +N2 +6H ,则下列说法正确的是( )2
A.甲电极是正极
B.每 1.5 mol O2 理论上可净化 1mol CO(NH2)2
C.H+从乙电极附近向甲电极附近迁移
D.电解质溶液可以是 NaOH 溶液
10.一种阴离子交换膜(AEM)与 Ni-Fe 析氧催化剂配对设计的电解槽,能高效低成本的电解纯水,原
理如图所示。下列叙述正确的是( )
.电解时阳极反应为 -A 4OH -4e-=2H2O+O2↑
B.电解时 OH-由左向右穿过 AEM 膜
C.右侧电极含有 Ni-Fe 析氧催化剂
D.理论上两极生成气体的质量比为 m(X):m(Y)=1:8
二、不定项选择题:本题共 5 个小题,每小题 4 分,共 20 分,每小题有一个或两个选项符合题目要
求,全部选对的得 4 分,选对但不全的得 2 分,有选错的得 0 分。
11. 下列各图所示装置能达到实验目的的是( )
A.图甲,验证铁的吸氧腐蚀 B.图乙,阴极电保护法
C.图丙,在铁制品表面镀锌 D.图丁,测定盐酸的 pH
12.已知 NaHCO3 溶液与盐酸反应生成 CO2 吸热,Na2CO3溶液与盐酸反应生成 CO2 放热。关于下列
ΔH 的判断正确的是( )
2
CO +3 (aq)+H (aq) = HCO 3 (aq) ΔH1
HCO 3 (aq)+H
+(aq) = H2CO3(aq) ΔH2
H2CO3(aq) = H2O(l)+CO2(g) ΔH3
OH-(aq)+H+(aq) = H2O(l) ΔH4
A.ΔH3<ΔH4 B.ΔH1+ΔH2<0
C.ΔH1+ΔH2+ΔH3>0 D.ΔH2+ΔH3>0
13. 分析下图所示的四个原电池装置,其中结论正确的是( )
A.①②中 Mg 作负极,③④中 Fe 作负极
B.②中 Mg 作正极,其电极反应式为2H2O+ 2e = 2OH +H2
C.③中 Fe 作负极,电极反应式为 Fe - 2e- = Fe2+
+
D.④中 Cu 作正极,电极反应式为2H + 2e = H2
14. 铅蓄电池是典型的可充电电池,它的正、负极板是惰性材料,分别吸附着 PbO2和 Pb,放电时电池
反应为 Pb+PbO2+2H2SO4 2PbSO4+2H2O,下列说法正确的是( )
A. 该电池工作时电解液的 pH 变小
B. 充电时,电池的正极连接电源的负极
- + 2-
C. 放电时,正极的电极反应式是PbO2 +2e +4H +SO4 =PbSO4 +2H2O
D. 充电时,当外电路中通过1mol电子时,理论上负极板的质量减少 48g
15.利用 CH4 燃料电池电解制备 Ca(H2PO4)2 并得到副产物 NaOH、H2、Cl2,装置如图所示。下列说法
不正确的是( )
A. -a 极反应:CH 8e +4O2 4 =CO2+2H2O
B.A 膜和 C 膜均为阴离子交换膜,B 膜为阳离子交换膜
C.可用铁电极替换阴极的石墨电极
D. a 极上通入标况下 2.24 L 甲烷,理论上产品室可新增 0.8 mol Ca(H2PO4)2
三、非选择题:本题共 5 个大题,共 60 分。
16. (每空 2 分,共 12 分)化学反应伴随能量变化,获取反应能量变化有多条途径。回答下列问题:
(1)理论研究表明,在 101kPa 和 298K 下,HCN(g) = HNC(g)异构化反应过程的能量变化如图所示,计
算可得:HCN(g) = HNC(g) H=_______kJ·mol-1。HCN 与 HNC 稳定性较强的是________。
(2)已知:
化学键种类 C—H N—H
键能(kJ/mol) a b
计算可得:HCN(g) = HNC(g) H=_______kJ·mol-1(用含 a、b 的式子表示)。
(3)已知:4gCH4 完全燃烧生成 CO2(g)、H2O(l)时放出热量 222.5kJ,则表示甲烷燃烧热的热化学方程式
为________________________________________________。
(4)实验室用 50mL0.50mol/L 盐酸、50mL0.55mol/LNaOH 溶液和如图所示装置,进行测定中和热的实
验。
① 实验装置中尚缺少的一种实验用品是__________。
②若测得中和热的数值偏低,请你分析可能的原因是( )
A.测量盐酸的温度后,温度计没有用水冲洗干净
B.把量筒中的氢氧化钠溶液倒入小烧杯时动作迟缓
C.做本实验的当天室温较高
D.将 50mL0.55mol/L 氢氧化钠溶液取成了 50mL0.55mol/L 的氨水
E. 在量取盐酸时仰视读数
17.(每空 2 分,共 12 分)甲醇是一种重要的化工原料,具有开发和应用的广阔前景。
I. 已知甲醇燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
① CH3OH(g)+H2O(g)=CO2 (g)+3H2 (g) ΔΔHH==4 94.0 kJ m
-1
9.0 kJ·molol-1
② CH3OH(g)+1/2 O2(g)=CO -12(g)+2H2(g) ΔH= -192.9 kJ·mol
又知:③ H2O(g)=H2O(l) ΔΔHH==-4 -44 k4J kmJ·mol
-1
ol-1
则表示甲醇摩尔燃烧焓的热化学方程式为_________________________________________。
II.如图所示,其中甲池的总反应式为 2CH3OH+3O2+4KOH=2K2CO3+6H2O,完成下列问题:
(1)甲池燃料电池的负极反应方程式为____________________________。
(2)写出乙池中电解总反应的化学方程式:_______________________________。
(3)甲池中消耗 224 mL(标准状况下)O2,此时丙池中理论上最多产生__________g 沉淀,此时乙池中溶
液的体积为 400 mL,该溶液的 c(H+)=__________。
(4)若以该甲醇燃料电池为电源,用石墨做电极电解 200mL 含有如下离子的溶液。
2+ + - SO2-离子 Cu H Cl 4
c/mol L-1 0.5 2 2 0.5
电解一段时间后,当两极收集到相同体积(相同条件)的气体时(忽略溶液体积的变化及电极产物可能存
在的溶解现象),电路中转移的电子的物质的量是______________mol。
18.(每空 2 分,共 12 分)钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢铁占世界钢铁年产量的三
分之一。请回答钢铁在腐蚀、防护过程中的有关问题。
(1)在实际生产中,可在铁件的表面镀上锌保护层或锡保护层防止铁被腐蚀。镀层破损后,镀锡铁和
镀锌铁更容易被腐蚀的是___________。(填“镀锡铁”或“镀锌铁”)
(2)下列哪个装置可防止铁棒被腐蚀( )
(3)利用右图装置可以模拟铁的电化学防护。
①若 X 为碳棒,为减缓铁的腐蚀,开关 K 应置于___________处。假设海水中只有 NaCl 溶质,写出此
时总离子反应方程式:_________________________________。
②若 X 为锌,开关 K 置于 M 处,该电化学防护法称为_________________,写出铁电极处的电极反应
式:_______________________________________。
19. (每空 2 分,共 12 分)氯碱工业是以电解饱和食盐水为基础的基本化学工业。如图是某氯碱工业生产
原理示意图:
(1)装置 A 所用食盐水由粗盐水精制而成。精制时,为除去食盐水中的Mg2+ 和Ca2+,要加入的试剂
分别为____________________、____________________(写化学式)。
(2)氯碱工业是高耗能产业,按上图将电解池与燃料电池相组合的新工艺可以节(电)能 30%以上,
相关物料的传输与转化关系如图所示,其中的电极未标出,所用的离子膜都只允许阳离子通过。
①图中 Y 是____________________(填化学式);X 与稀 NaOH 溶液反应的离子方程式为
______________________________________。
②比较图示中氢氧化钠的质量分数 a% 与b% 的大小:a _____ b(填“>”“<”或“=”)。
③若用装置 B 作为装置 A 的辅助电源,每当消耗标准状况下氧气的体积为 11.2L 时,则装置 B 可向装
置 A 提供的电量约为__________________________(一个 e 的电量为1.60 10 19 C;计算结果精确到
0.01)。
20. (每空 2 分,共 12 分)电解原理在环保领域有广泛应用,按照要求回答下列问题。
-
(1)工业上,在强碱性条件下用电解法除去废水中的 CN ,装置如图所示:
依次发生的反应有:
- - - -
ⅰ.CN -2e +2OH ===CNO +H2O
- -
ⅱ.2Cl -2e ===Cl2↑
- - - -
ⅲ.3Cl2+2CNO +8OH ===N2+6Cl +2CO23 +4H2O
①a 为电源________(填“正”或“负”)极。
②通电过程中溶液 pH 不断________(填“增大”“减小”或“不变”)。
-
③除去 1 mol CN ,外电路中至少需要转移________ mol 电子。
④为了使电解池连续工作,需要不断补充______________________。(写化学式)
(2)利用如图所示装置(电极均为惰性电极)可吸收 SO2,并用阴极排出的溶液吸收 NO2来解决环境污 染问
题。
①阴极的电极反应式为:________________________________________。
②阳极的电极反应式为:________________________________________。
化学答案
一、 单项选择题
1~5 BDBDA 6~10 CBBBA
二、 不定项选择题
11 A 12 BD 13 B 14 CD 15 BD
三、 非选择题
16. (1) 59.3 HCN
(2) a-b
(3) CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H = - 890 kJ·mol-1
(4) ABD
17. Ⅰ CH3OH(g)+3/2 O2(g) = CO (g)+2H O(l) △H = - 764.7 kJ·mol-12 2
Ⅱ (1) CH3OH - 6e- +8OH- = CO 2- 3 +6H2O
(2)
(3) 1.16 0.1 mol/L
(4) 0.8
18. (1) 镀锡铁
(2) BD
(3) ① N ② 牺牲阳极保护法(牺牲阳极的阴极保护法) O2+4e-+2H2O=4OH-
19. (1) NaOH Na2CO3
(2) ① H2 Cl +2OH- =Cl- +ClO- 2 +H2O ② < ③ 1.93×105 C
20. (1) ① 正 ②减小 ③ 5 ④ NaOH 和 NaCl
(2) ① 2HSO -3 +2H++2e- = S2O 2-4 +2H2O
② SO2+2H - 2- +2O-2e =SO4 +4H
同课章节目录
