人教版(五四制)八年级全一册化学 第二单元 课题2 氧气第一课时探究O2的性质之旅课件(共17张PPT内嵌视频)
文档属性
| 名称 | 人教版(五四制)八年级全一册化学 第二单元 课题2 氧气第一课时探究O2的性质之旅课件(共17张PPT内嵌视频) |

|
|
| 格式 | pptx | ||
| 文件大小 | 12.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-11 00:00:00 | ||
图片预览





文档简介
(共17张PPT)
观看《科普中国》片段
氧气性质知多少?
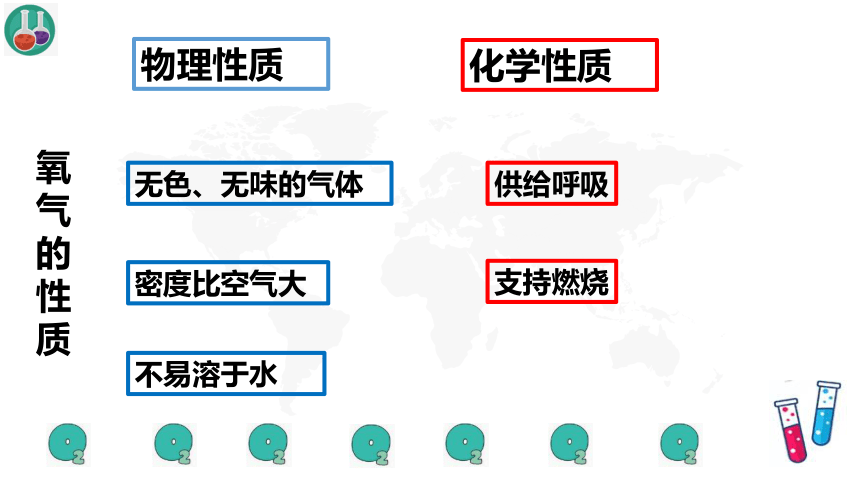
无色、无味的气体
密度比空气大
供给呼吸
支持燃烧
不易溶于水
物理性质
化学性质
氧气的性质
课题2 氧气
(第一课时)
探究O2的性质之旅
在常温下,1L水中只能溶解约30ml氧气。
——氧气不易溶于水。
__________
氧气的物理性质
过氧化氢溶液和二氧化锰
排水法收集:
氧气不易溶于水。
氧气的物理性质
氧气的物理性质
固态氧
氧气
液态氧
(无色、气体)
(淡蓝色、液体)
(淡蓝色、雪花 状固体)
-183℃
-218℃
101KPa
101KPa
氧气的三态变化
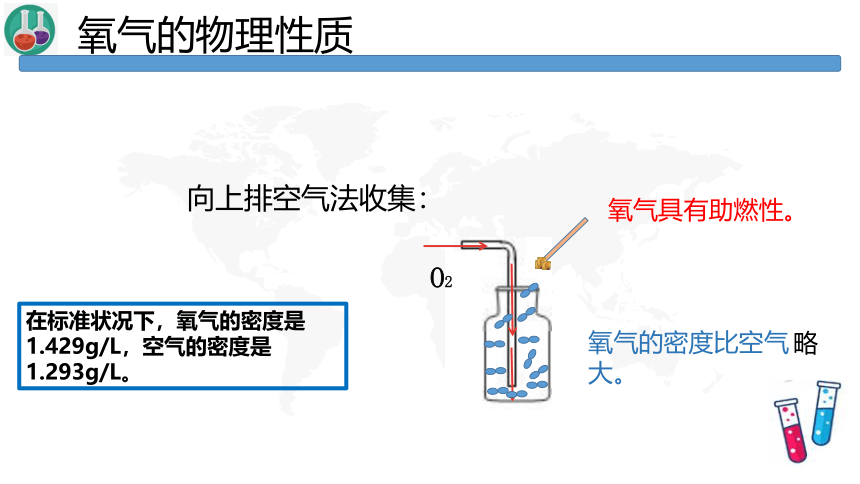
向上排空气法收集:
氧气具有助燃性。
O2
氧气的密度比空气 大。
略
氧气的物理性质
在标准状况下,氧气的密度是1.429g/L,空气的密度是1.293g/L。
反应物 色、态 在空气中燃烧现象 在氧气中燃烧现象
氧气的化学性质:硫与氧气反应
硫
淡黄色固体
淡蓝色火焰,
放出热量,
生成有刺激性气味的气体。
蓝紫色火焰,
放出热量,
生成有刺激性气味的气体。
硫 + 氧气 二氧化硫
点燃
点燃
S + O2 SO2
合作探究:碳与氧气反应
实验用品:木炭、澄清石灰水、酒精灯、火柴、坩埚钳、石棉网、一集气瓶(250ml)的氧气。
实验步骤:(1)用坩埚钳夹取一小块木炭,在酒精灯上加热,观察木炭在空气中燃烧现象。
(2)把烧到发红的木炭由瓶口向下缓慢插入到盛满氧气的1号集气瓶中,观察木炭在氧气里燃烧的现象。
(3)燃烧停止后,用手轻轻触碰集气瓶外壁,并向集气瓶中加入少量澄清石灰水,振荡,观察实验现象。
反应物 色、态 在空气中燃烧现象 在氧气中燃烧现象
氧气的化学性质:碳与氧气反应
碳
黑色
固体
碳 + 氧气 二氧化碳
点燃
点燃
C + O2 CO2
燃烧发红,
放出热量,
生成的气体能使澄清石灰水变浑浊。
剧烈燃烧,发出白光,
放出热量,
生成的气体能使澄清石灰水变浑浊。
合作探究:铁丝与氧气反应
实验用品:两根(已打磨)光亮的铁丝、酒精灯、火柴、坩埚钳、石棉网、一集气瓶的氧气。
实验步骤:(1)取一根细铁丝,用坩埚钳夹住放在酒精灯上加热,观察现象。
(2)取另一根同样的细铁丝,在下端系一根火柴,点燃火柴,待火柴快燃尽时,插入盛有氧气的2号集气瓶中,观察现象。
反应物 颜色、状态 在空气中 在氧气中燃烧现象
合作探究:铁丝与氧气反应
铁
银白色
固体
不能燃烧,只能烧到红热。
剧烈燃烧,火星四射,
放出热量,
生成一种黑色固体。
铁 + 氧气 四氧化三铁
点燃
点燃
Fe + O2 Fe3O4
思考
1.为什么要将铁丝盘成螺旋状?
2.为什么放入集气瓶的那根铁丝下端要系一根火柴?
3.为什么要等火柴即将燃尽时再将铁丝伸入氧气瓶中?
4.为什么集气瓶底部要放少量水?
1.增大铁丝的受热面积和氧气的接触面积。
2.引燃铁丝。
3.防止火柴燃烧消耗过多氧气,影响铁丝和氧气的反应。
4.防止高温熔化物溅落下来炸裂集气瓶底。
讨论
通过以上几个实验,我们可以得出哪些结论?
物质在空气中燃烧主要是与空气中的氧气反应,反应的剧烈程度取决于氧气的含量,氧气含量越高,燃烧越剧烈。
小试牛刀,运用新知
现有四瓶没有标签,无色气体分别为空气、氧气、氮气、二氧化碳中的一种,请同学们设计实验验证。
1.实验用品:
_____________________
2.实验步骤及现象:
___________________________________________________________
___________________________________________________________
___________________________________________________________
___________________________________________________________
3.实验结论:________________________________________________
归纳总结
氧气
物理性质
化学性质
用途
性质
谢谢!
观看《科普中国》片段
氧气性质知多少?
无色、无味的气体
密度比空气大
供给呼吸
支持燃烧
不易溶于水
物理性质
化学性质
氧气的性质
课题2 氧气
(第一课时)
探究O2的性质之旅
在常温下,1L水中只能溶解约30ml氧气。
——氧气不易溶于水。
__________
氧气的物理性质
过氧化氢溶液和二氧化锰
排水法收集:
氧气不易溶于水。
氧气的物理性质
氧气的物理性质
固态氧
氧气
液态氧
(无色、气体)
(淡蓝色、液体)
(淡蓝色、雪花 状固体)
-183℃
-218℃
101KPa
101KPa
氧气的三态变化
向上排空气法收集:
氧气具有助燃性。
O2
氧气的密度比空气 大。
略
氧气的物理性质
在标准状况下,氧气的密度是1.429g/L,空气的密度是1.293g/L。
反应物 色、态 在空气中燃烧现象 在氧气中燃烧现象
氧气的化学性质:硫与氧气反应
硫
淡黄色固体
淡蓝色火焰,
放出热量,
生成有刺激性气味的气体。
蓝紫色火焰,
放出热量,
生成有刺激性气味的气体。
硫 + 氧气 二氧化硫
点燃
点燃
S + O2 SO2
合作探究:碳与氧气反应
实验用品:木炭、澄清石灰水、酒精灯、火柴、坩埚钳、石棉网、一集气瓶(250ml)的氧气。
实验步骤:(1)用坩埚钳夹取一小块木炭,在酒精灯上加热,观察木炭在空气中燃烧现象。
(2)把烧到发红的木炭由瓶口向下缓慢插入到盛满氧气的1号集气瓶中,观察木炭在氧气里燃烧的现象。
(3)燃烧停止后,用手轻轻触碰集气瓶外壁,并向集气瓶中加入少量澄清石灰水,振荡,观察实验现象。
反应物 色、态 在空气中燃烧现象 在氧气中燃烧现象
氧气的化学性质:碳与氧气反应
碳
黑色
固体
碳 + 氧气 二氧化碳
点燃
点燃
C + O2 CO2
燃烧发红,
放出热量,
生成的气体能使澄清石灰水变浑浊。
剧烈燃烧,发出白光,
放出热量,
生成的气体能使澄清石灰水变浑浊。
合作探究:铁丝与氧气反应
实验用品:两根(已打磨)光亮的铁丝、酒精灯、火柴、坩埚钳、石棉网、一集气瓶的氧气。
实验步骤:(1)取一根细铁丝,用坩埚钳夹住放在酒精灯上加热,观察现象。
(2)取另一根同样的细铁丝,在下端系一根火柴,点燃火柴,待火柴快燃尽时,插入盛有氧气的2号集气瓶中,观察现象。
反应物 颜色、状态 在空气中 在氧气中燃烧现象
合作探究:铁丝与氧气反应
铁
银白色
固体
不能燃烧,只能烧到红热。
剧烈燃烧,火星四射,
放出热量,
生成一种黑色固体。
铁 + 氧气 四氧化三铁
点燃
点燃
Fe + O2 Fe3O4
思考
1.为什么要将铁丝盘成螺旋状?
2.为什么放入集气瓶的那根铁丝下端要系一根火柴?
3.为什么要等火柴即将燃尽时再将铁丝伸入氧气瓶中?
4.为什么集气瓶底部要放少量水?
1.增大铁丝的受热面积和氧气的接触面积。
2.引燃铁丝。
3.防止火柴燃烧消耗过多氧气,影响铁丝和氧气的反应。
4.防止高温熔化物溅落下来炸裂集气瓶底。
讨论
通过以上几个实验,我们可以得出哪些结论?
物质在空气中燃烧主要是与空气中的氧气反应,反应的剧烈程度取决于氧气的含量,氧气含量越高,燃烧越剧烈。
小试牛刀,运用新知
现有四瓶没有标签,无色气体分别为空气、氧气、氮气、二氧化碳中的一种,请同学们设计实验验证。
1.实验用品:
_____________________
2.实验步骤及现象:
___________________________________________________________
___________________________________________________________
___________________________________________________________
___________________________________________________________
3.实验结论:________________________________________________
归纳总结
氧气
物理性质
化学性质
用途
性质
谢谢!
同课章节目录
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的构成
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题1 质量守恒定律
- 课题2 如何正确书写化学方程式
- 课题3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动3 燃烧的条件
- 旧版目录
- 第五单元 物质组成的表示
- 课题2 燃料和热量
- 课题3 使用燃料对环境的影响
