4.3质量守恒定律课后练习基础过关—2021-2022学年九年级化学科粤版(2012)上册(含解析)
文档属性
| 名称 | 4.3质量守恒定律课后练习基础过关—2021-2022学年九年级化学科粤版(2012)上册(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 85.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-13 00:00:00 | ||
图片预览




文档简介
第四章生命之源---水4.3质量守恒定律课后练习基础过关九年级化学上册(科粤版2012)
练习
一、单选题,共10小题
1.10 g甲与足量的乙反应,生成8g丙和15g丁,则参加反应的乙的质量是
A.13g B.23g C.18g D.25g
2.自然科学的发展使我们的生活变得丰富多彩。通过化学的学习,你觉得下列情况中不可能实现的是
A.通过化学反应使水直接变成汽油 B.用肥皂水区分硬水和软水
C.用人工的方法合成结晶牛胰岛素 D.通过分离液态空气法得到氧气
3.在化学反应A+B=C+D中,fgA与B反应生成mgC和ngD,则参加反应的B的质量是多少g?
A.m+n B.m-n C.m+n+f D.m+n-f
4.推理是学习化学常用的方法,下列推理正确的是
A.单质由同种元素组成,则只含有一种元素的物质一定是单质
B.化学变化中常伴随发光放热的现象所以有发光放热现象产生时一定发生了化学变化
C.同种元素的质子数相同,则质子数相同的粒子一定属于同种元素
D.蜡烛燃烧生成二氧化碳和水,所以蜡烛组成中一定有碳元素和氢元素
5.下列说法能用质量守恒定律解释的是
A.拧开盛酒精的瓶盖一段时间后质量变小 B.mg水受热变为mg的水蒸气
C.2g氢气和8g氧气反应生成9g水 D.20g食盐溶于80g水得100g食盐水
6.某化合物完全燃烧,需要4.8 g氧气,同时只生成4.4 g二氧化碳和2.7 g 水,则该化合物中
A.只含有碳、氢两种元素 B.只含有碳、氧两种元素
C.含有碳、氢、氧三种元素 D.无法确定
7.下列说法符合质量守恒定律的是
A.2克氢气和8克氧气反应生成10克水
B.12g碳在40g氧气中完全燃烧,则生成的二氧化碳的质量为44g
C.50克酒精和50克水混合得到100克酒精溶液
D.某可燃物完全燃烧生成二氧化碳和水,则可燃物中一定含有碳、氢、氧三种元素
8.下列关于分子、原子和离子的说法不正确的是
A.“花香四溢”说明分子在不断运动
B.化学变化前后原子的种类和数目都不变
C.原子核不都是由质子和中子构成
D.带电的微粒都是离子
9.下列说法正确的是
A.所有原子的原子核都是由质子和中子构成
B.在含有多个电子的原子中离核越近的电子能量越高
C.由同一种元素组成的物质一定是单质,不可能是化合物
D.在物质发生化学变化时,原子的种类不变,元素也不会改变
10.在一密闭容器中,有甲、乙、丙、丁四种物质,在一定条件下存在某个反应,测得反应前后各物质的质量如下表:
物质 甲 乙 丙 丁
反应前质量/g 40 3 8 6
反应后质量/g 4 x 40 10
对该反应,下列描述中正确的是
A.该反应是化合反应 B.该反应不遵守质量守恒定律
C.反应过程中丙和丁的质量比为4:1 D.x=3,乙不一定是催化剂
二、非选择题,共6小题
11.无数实验证明,参加化学反应的各物质的______,等于反应后生成的各物质的______。这个规律叫做质量守恒定律。
12.宏微结合,在宏观、微观和符号之间建立联系,是化学应培养的核心素养。请回答下列问题:
(1)硫酸铜溶液呈蓝色,是因为溶液中含有___________(填离子符号)。
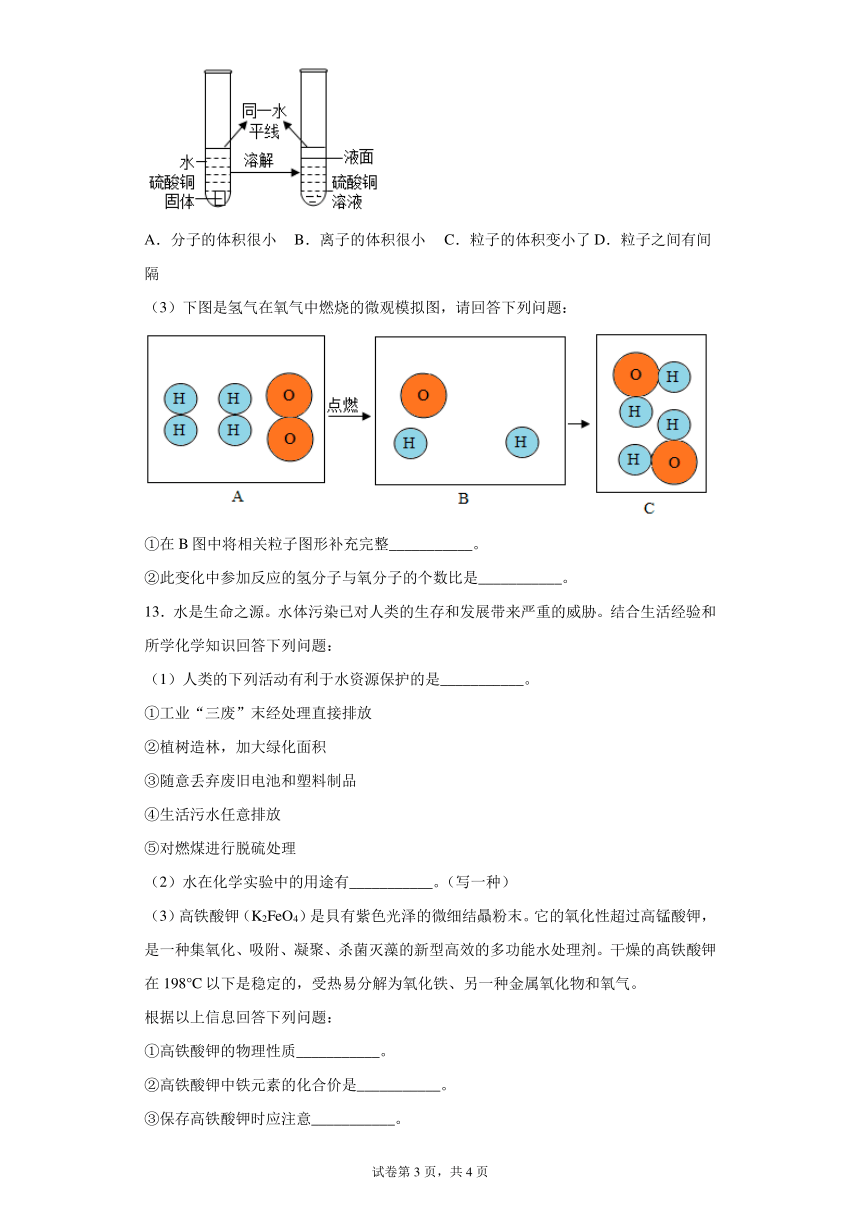
(2)某兴趣小组在做硫酸铜固体溶于水的实验时,观察到如图现象。硫酸铜固体“消失”后液面比原水平线低的微观解释正确的是___________(填选项)
A.分子的体积很小 B.离子的体积很小 C.粒子的体积变小了 D.粒子之间有间隔
(3)下图是氢气在氧气中燃烧的微观模拟图,请回答下列问题:
①在B图中将相关粒子图形补充完整___________。
②此变化中参加反应的氢分子与氧分子的个数比是___________。
13.水是生命之源。水体污染已对人类的生存和发展带来严重的威胁。结合生活经验和所学化学知识回答下列问题:
(1)人类的下列活动有利于水资源保护的是___________。
①工业“三废”末经处理直接排放
②植树造林,加大绿化面积
③随意丢弃废旧电池和塑料制品
④生活污水任意排放
⑤对燃煤进行脱硫处理
(2)水在化学实验中的用途有___________。(写一种)
(3)高铁酸钾(K2FeO4)是貝有紫色光泽的微细结贔粉末。它的氧化性超过高锰酸钾,是一种集氧化、吸附、凝聚、杀菌灭藻的新型高效的多功能水处理剂。干燥的髙铁酸钾在198°C以下是稳定的,受热易分解为氧化铁、另一种金属氧化物和氧气。
根据以上信息回答下列问题:
①高铁酸钾的物理性质___________。
②高铁酸钾中铁元素的化合价是___________。
③保存高铁酸钾时应注意___________。
④写出高铁酸钾受热分解时的符号表达式___________。
14.将36 g水通电完全分解时,得到4 g氢气的同时,可以得到______g氧气;若已知在电解水过程中,共收集到氢气和氧气的质量为1.8 g,则已发生电解的水的质量为______g。
15.化学基础知识是学好化学的关键,请按下列要求填空。
(1)图1是某微粒的结构示意图,其中x=______该微粒在化学反应中易______(填“得”或“失”)电子;写出一条从图2中获得的信息______。
(2)如图3所示是汽车尾气治理过程中某反应的微观示意图,请按要求回答问题。
①图3中体现了在化学变化前后一定不变的是______(填序号)。
A.元素种类 B.原子种类 C分子数目 D原子数目。
②图3中发生反应的符号表达式为______。
16.自来水消毒过程中常会发生如下化学反应,其反应的微观过程可用下图表示:
(表示氯原子,表示氧原子,表示氢原子)
(1)保持A物质化学性质的最小微粒是______(填微粒名称);
(2)分析甲图,请你总结出化学变化的微观本质是______;
(3)请在乙图虚线框内将E物质的分子模型图补画完整。
试卷第1页,共3页
试卷第1页,共3页
参考答案
1.A
【详解】
10g甲与足量的乙反应,生成8g丙和15g丁,由质量守恒定律,参加反应的甲和乙的质量之和等于生成丙和丁的质量之和,则参加反应的乙的质量为8g+15g-10g=13g。
故选:A。
2.A
【详解】
A、由质量守恒定律,反应前后元素种类不变,水中不含碳元素,不能通过化学反应使水直接变成汽油,故选项说法错误;
B、硬水和软水的区别在于所含的钙镁离子的多少,可用肥皂水来区分硬水和软水,加入肥皂水,若产生泡沫较多,则是软水,若产生泡沫较少,则是硬水,故选项说法正确;
C、我国已经成功合成结晶牛胰岛素,可以用人工的方法合成结晶牛胰岛素,故选项说法正确‘
D、氧气和氮气的沸点不同,通过分离液态空气法得到氧气,故选项说法正确。
故选:A。
3.D
【详解】
已知化学反应A+B=C+D 中,若fgA与一定量的B恰好完全反应,生成mgC和ngD;根据质量守恒定律可知参加反应的B的质量为mg+ng-fg=(m+n-f)g。
故选:D 。
4.D
【详解】
A、由同种元素组成的物质不一定是单质,如氧气和臭氧的混合物,选项A错误;
B、化学变化中常伴随发光放热的现象,但有发光放热现象产生时不一定发生了化学变化,如通电的电灯,不属于化学变化,选项B错误;
C、同种元素的原子质子数相同,但是质子数相同的微粒不一定属于同种元素,选项C错误;
D、蜡烛燃烧生成二氧化碳和水,根据质量守恒定律可知,化学反应前后元素的种类不变,所以蜡烛组成中一定有碳元素和氢元素,可能含有氧元素,选项D正确;
故选:D。
5.C
【分析】
质量守恒定律是解释化学反应的定律;
【详解】
A、拧开盛酒精的瓶盖一段时间后质量变小,该变化没有生成新物质,属于物理变化,不能用质量守恒定律解释,错误;
B、mg水受热变为mg的水蒸气,该变化没有生成新物质,属于物理变化,不能用质量守恒定律解释,错误;
C、2g氢气和8g氧气反应生成9g水,该变化是一个化学变化,反应中氢气过量,能用质量守恒定律解释,正确;
D、20g食盐溶于80g水得100g食盐水,该变化没有生成新物质,属于物理变化,不能用质量守恒定律解释,错误;
故选C。
6.C
【分析】
根据质量守恒定律,由生成物可以初步确定该物质中含有碳元素和氢元素,由生成的二氧化碳和水中碳、氢元素的质量和与该物质的质量进行对比,从而确定该物质的组成元素。
【详解】
中含有碳元素的质量为:,水中含有氢元素的质量为:,生成物二氧化碳和水中所含碳、氢元素的质量和为,某化合物的质量为,,该物质中含氧元素的质量为:,则该物质中一定含有碳、氢、氧三种元素。
故选C。
7.B
【详解】
A、氢气和氧气反应的化学方程式为:可知,氢气、氧气、水的质量比为1:8:9,故1克氢气和8克氧气反应生成9克水,故选项说法错误;
B、碳和氧气反应的化学方程式为: 可知,故12份质量的碳和32份质量的氧气反应生成44份质量的二氧化碳,12g碳在40g氧气中完全燃烧也生成44g二氧化碳,氧气剩余,故选项说法正确;
C、50克酒精和50克水混合得到100克酒精溶液,没有新物质生成,属于物理变化,不符合质量守恒定律,故选项说法错误;
D、某可燃物完全燃烧生成二氧化碳和水,CO2和H2O两种物质中含有碳、氢、氧三种元素,根据质量守恒定律,反应前后,元素种类不变,反应物氧气中只含有氧元素,则某化合物中一定含有碳、氢两种元素,可能含有氧元素,故选项说法错误。
故选B。
8.D
【详解】
A. 分子在不断的运动,所以在远处就可以闻到花的香味,故选项正确;
B. 化学变化的实质是分子分成原子,原子重新组合成新的分子,此过程中原子的种类与数目均不改变,故选项正确;
C. 原子核是由质子与中子构成的,但是原子核中不一定都有中子,如氢原子核内只有质子,没有中子,故选项正确;
D. 离子是带电的微粒,但是带电的微粒不一定是离子,如质子、电子也带电,故选项错误。
故选:D。
9.D
【详解】
A、氢原子中没有中子,所以说原子核中一定含有质子,不一定含有中子,选项错误;
B、原子核外电子能量不同,离核越近,电子的能量越低,离核越远,能量越高,选项错误;
C、由同种元素组成的纯净物是单质,由同一种元素组成的物质不一定是纯净物,例如氧气和臭氧在一起属于混合物,选项错误;
D、原子是化学变化中的最小粒子,在物质发生化学变化时,原子的种类不变,元素也不会改变,选项正确。
故选:D。
10.D
【分析】
此类题是根据质量守恒定律进行的相关计算,一般分三步完成:
1、根据质量守恒定律计算出未知的值,的值为:;
2、根据反应前后质量变化确定反应物和生成物,质量减少的为反应物,质量增加的为生成物,甲的质量减小了,是反应物,丙和丁的质量增加了,是生成物;
3、根据反应前后各物质质量的变化,求出反应物反应的质量和生成物生成的质量,即减少的质量和增加的质量,即36g甲完全反应生成32g丙和4g丁。再根据上述信息确定每个选项的正误。
【详解】
A、由分析可知,该反应是由一种物质生成两种物质的反应,是分解反应,故A选项错误;
B、任何化学反应都遵守质量守恒定律,故B选项错误;
C、反应中丙丁的质量比32g:4g=8:1,故C选项错误;
D、催化剂只改变其他物质的反应速率,本身的质量和化学性质在反应前后都不变的物质,由题中信息可得出乙的质量在反应前后没有变化,但无法判断乙的化学性质是否改变和乙是否改变了甲的反应速率,所以乙不一定是该反应的催化剂,故D选项正确。
故选D。
11.总质量 总质量
【详解】
无数实验证明:参加化学反应的各物质的总质量,等于反应后生成的各物质的总质量,这个规律叫作质量守恒定律。
12.
(1)Cu2+
(2)D
(3) 2:1
【分析】
(1)
硫酸铜溶液中含有铜离子、硫酸根离子和水分子,溶液呈蓝色,硫酸溶液中含有氢离子、硫酸根离子和水分子,溶液呈无色,则硫酸铜溶液呈硫酸的原因是溶液中含有铜离子,其符号为Cu2+,故填Cu2+。
(2)
硫酸铜固体溶于水的实验中,硫酸铜固体“消失”后液面比原水平线低是因为分子间有间隔,硫酸铜固体溶于水时,铜离子和硫酸根离子扩散到水分子的间隔中,则硫酸铜溶解后溶液的体积小于溶解前固体与水的体积和,故填D。
(3)
①由图可知,A图中含有2个氢分子和1个氧分子,发生化学变化时,分子先被分成原子,即2个氢分子分成4个氢原子,1个氧分子分成2个氧原子,故B图画为。
②由图可知,A图中含有2个氢分子和1个氧分子,反应后C图中只含有2个水分子,不含氢分子和氧分子,则此变化中参加反应的氢分子与氧分子的个数比为2:1,故填2:1。
13.
(1)②⑤
(2)配制溶液等
(3) 紫色粉末 +6价 防潮避热
【分析】
(1)
①工业“三废”未经处理直接排放会导致环境污染,故①错误;
②植树造林,加大绿化面积,有利于保护环境,故②正确;
③随意丢弃废旧电池和塑料制品,会污染环境,污染地下水资源,故③错误;
③生活污水任意排放,会导致水资源污染,故④错误;
④对然煤进行脱硫处理,减少二氧化硫的排放,故⑤正确;
故答案为:②⑤
(2)
水在化学实验中可以用来作溶剂配制溶液,洗涤仪器,用排水法来收集气体等。
(3)
①颜色状态属于高铁酸钾的物理性质,故答案为:紫色粉末。
②根据在化合物中元素的化合价为0,可得高铁酸钾中铁元素的化合价为(+1)2+x+(-2)4=0,则x=+6。
③因为高铁酸钾在水中或受热的情况下不稳定,容易发生化学反应,所以保存高铁酸钾时应注意防潮避热。
④根据化学反应前后原子的种类和数目不发生改变,则另一种金属氧化物为氧化钾,高铁酸钾受热分解成氧化铁,氧气和氧化钾,故反应的符号表达式为:。
14.32 1.8
【分析】
质量守恒定律是指参加化学反应的各物质的质量总和等于生成的各物质的质量总和。
【详解】
由质量守恒定律可知,将36g水通电完全分解时,得到4g氢气的同时,可以得到氧气的质量为:36g-4g=32g,若已知在电解水过程中,共收集到氢气和氧气的质量为1. 8g,则已发生电解的水的质量为1. 8g,故答案为:32;1. 8。
【点睛】
本题主要考查学生运用质量守恒定律进行推断的能力。
15.
(1) 13 失 原子序数为80、相对原子质量为200.6、元素符号为Hg
(2) ABD CO2+NON2+CO2
【分析】
(1)
根据该微粒的结构示意图可知,图1是原子的结构示意图,原子中质子数=核外电子数,则其中x=2+8+3=13,该微粒最外层电子数小于4,在化学反应中易失电子;
从图2中获得的信息有:汞的原子序数为80,相对原子质量为200.6,元素符号为Hg。
(2)
①由如图3所示的微观示意图可知,反应前有一氧化碳分子和一氧化氮分子,反应后有氮分子、二氧化碳分子。反应前有一个碳原子、两个氧原子、一个氮原子,反应后有一个碳原子、两个氧原子、一个氮原子。因为原子属于元素,所以图3中体现了在化学变化前后一定不变的是元素种类 、原子种类、原子数目,故选ABD。
②图3中发生反应的符号表达式为:CO2+NON2+CO2。
16.
(1)水分子
(2)在化学变化中,分子分成原子,原子结合成新的分子
(3)
【分析】
(1)
由图可知,A物质为水,水由水分子构成,保持A物质化学性质的最小微粒是水分子;
(2)
由图可知,化学变化的微观本质是:在化学变化中,分子分成原子,原子结合成新的分子;
(3)
根据质量守恒定律,化学反应前后,原子的种类和数目不变,反应物中含H、Cl、O的个数分别是2、2、2,生成物中含H、Cl、O的个数分别是2、2、0,故生成物中还应含2个O,每个氧分子由2个氧原子构成,故E物质的分子模型图为: 。答案第1页,共2页
答案第1页,共2页
练习
一、单选题,共10小题
1.10 g甲与足量的乙反应,生成8g丙和15g丁,则参加反应的乙的质量是
A.13g B.23g C.18g D.25g
2.自然科学的发展使我们的生活变得丰富多彩。通过化学的学习,你觉得下列情况中不可能实现的是
A.通过化学反应使水直接变成汽油 B.用肥皂水区分硬水和软水
C.用人工的方法合成结晶牛胰岛素 D.通过分离液态空气法得到氧气
3.在化学反应A+B=C+D中,fgA与B反应生成mgC和ngD,则参加反应的B的质量是多少g?
A.m+n B.m-n C.m+n+f D.m+n-f
4.推理是学习化学常用的方法,下列推理正确的是
A.单质由同种元素组成,则只含有一种元素的物质一定是单质
B.化学变化中常伴随发光放热的现象所以有发光放热现象产生时一定发生了化学变化
C.同种元素的质子数相同,则质子数相同的粒子一定属于同种元素
D.蜡烛燃烧生成二氧化碳和水,所以蜡烛组成中一定有碳元素和氢元素
5.下列说法能用质量守恒定律解释的是
A.拧开盛酒精的瓶盖一段时间后质量变小 B.mg水受热变为mg的水蒸气
C.2g氢气和8g氧气反应生成9g水 D.20g食盐溶于80g水得100g食盐水
6.某化合物完全燃烧,需要4.8 g氧气,同时只生成4.4 g二氧化碳和2.7 g 水,则该化合物中
A.只含有碳、氢两种元素 B.只含有碳、氧两种元素
C.含有碳、氢、氧三种元素 D.无法确定
7.下列说法符合质量守恒定律的是
A.2克氢气和8克氧气反应生成10克水
B.12g碳在40g氧气中完全燃烧,则生成的二氧化碳的质量为44g
C.50克酒精和50克水混合得到100克酒精溶液
D.某可燃物完全燃烧生成二氧化碳和水,则可燃物中一定含有碳、氢、氧三种元素
8.下列关于分子、原子和离子的说法不正确的是
A.“花香四溢”说明分子在不断运动
B.化学变化前后原子的种类和数目都不变
C.原子核不都是由质子和中子构成
D.带电的微粒都是离子
9.下列说法正确的是
A.所有原子的原子核都是由质子和中子构成
B.在含有多个电子的原子中离核越近的电子能量越高
C.由同一种元素组成的物质一定是单质,不可能是化合物
D.在物质发生化学变化时,原子的种类不变,元素也不会改变
10.在一密闭容器中,有甲、乙、丙、丁四种物质,在一定条件下存在某个反应,测得反应前后各物质的质量如下表:
物质 甲 乙 丙 丁
反应前质量/g 40 3 8 6
反应后质量/g 4 x 40 10
对该反应,下列描述中正确的是
A.该反应是化合反应 B.该反应不遵守质量守恒定律
C.反应过程中丙和丁的质量比为4:1 D.x=3,乙不一定是催化剂
二、非选择题,共6小题
11.无数实验证明,参加化学反应的各物质的______,等于反应后生成的各物质的______。这个规律叫做质量守恒定律。
12.宏微结合,在宏观、微观和符号之间建立联系,是化学应培养的核心素养。请回答下列问题:
(1)硫酸铜溶液呈蓝色,是因为溶液中含有___________(填离子符号)。
(2)某兴趣小组在做硫酸铜固体溶于水的实验时,观察到如图现象。硫酸铜固体“消失”后液面比原水平线低的微观解释正确的是___________(填选项)
A.分子的体积很小 B.离子的体积很小 C.粒子的体积变小了 D.粒子之间有间隔
(3)下图是氢气在氧气中燃烧的微观模拟图,请回答下列问题:
①在B图中将相关粒子图形补充完整___________。
②此变化中参加反应的氢分子与氧分子的个数比是___________。
13.水是生命之源。水体污染已对人类的生存和发展带来严重的威胁。结合生活经验和所学化学知识回答下列问题:
(1)人类的下列活动有利于水资源保护的是___________。
①工业“三废”末经处理直接排放
②植树造林,加大绿化面积
③随意丢弃废旧电池和塑料制品
④生活污水任意排放
⑤对燃煤进行脱硫处理
(2)水在化学实验中的用途有___________。(写一种)
(3)高铁酸钾(K2FeO4)是貝有紫色光泽的微细结贔粉末。它的氧化性超过高锰酸钾,是一种集氧化、吸附、凝聚、杀菌灭藻的新型高效的多功能水处理剂。干燥的髙铁酸钾在198°C以下是稳定的,受热易分解为氧化铁、另一种金属氧化物和氧气。
根据以上信息回答下列问题:
①高铁酸钾的物理性质___________。
②高铁酸钾中铁元素的化合价是___________。
③保存高铁酸钾时应注意___________。
④写出高铁酸钾受热分解时的符号表达式___________。
14.将36 g水通电完全分解时,得到4 g氢气的同时,可以得到______g氧气;若已知在电解水过程中,共收集到氢气和氧气的质量为1.8 g,则已发生电解的水的质量为______g。
15.化学基础知识是学好化学的关键,请按下列要求填空。
(1)图1是某微粒的结构示意图,其中x=______该微粒在化学反应中易______(填“得”或“失”)电子;写出一条从图2中获得的信息______。
(2)如图3所示是汽车尾气治理过程中某反应的微观示意图,请按要求回答问题。
①图3中体现了在化学变化前后一定不变的是______(填序号)。
A.元素种类 B.原子种类 C分子数目 D原子数目。
②图3中发生反应的符号表达式为______。
16.自来水消毒过程中常会发生如下化学反应,其反应的微观过程可用下图表示:
(表示氯原子,表示氧原子,表示氢原子)
(1)保持A物质化学性质的最小微粒是______(填微粒名称);
(2)分析甲图,请你总结出化学变化的微观本质是______;
(3)请在乙图虚线框内将E物质的分子模型图补画完整。
试卷第1页,共3页
试卷第1页,共3页
参考答案
1.A
【详解】
10g甲与足量的乙反应,生成8g丙和15g丁,由质量守恒定律,参加反应的甲和乙的质量之和等于生成丙和丁的质量之和,则参加反应的乙的质量为8g+15g-10g=13g。
故选:A。
2.A
【详解】
A、由质量守恒定律,反应前后元素种类不变,水中不含碳元素,不能通过化学反应使水直接变成汽油,故选项说法错误;
B、硬水和软水的区别在于所含的钙镁离子的多少,可用肥皂水来区分硬水和软水,加入肥皂水,若产生泡沫较多,则是软水,若产生泡沫较少,则是硬水,故选项说法正确;
C、我国已经成功合成结晶牛胰岛素,可以用人工的方法合成结晶牛胰岛素,故选项说法正确‘
D、氧气和氮气的沸点不同,通过分离液态空气法得到氧气,故选项说法正确。
故选:A。
3.D
【详解】
已知化学反应A+B=C+D 中,若fgA与一定量的B恰好完全反应,生成mgC和ngD;根据质量守恒定律可知参加反应的B的质量为mg+ng-fg=(m+n-f)g。
故选:D 。
4.D
【详解】
A、由同种元素组成的物质不一定是单质,如氧气和臭氧的混合物,选项A错误;
B、化学变化中常伴随发光放热的现象,但有发光放热现象产生时不一定发生了化学变化,如通电的电灯,不属于化学变化,选项B错误;
C、同种元素的原子质子数相同,但是质子数相同的微粒不一定属于同种元素,选项C错误;
D、蜡烛燃烧生成二氧化碳和水,根据质量守恒定律可知,化学反应前后元素的种类不变,所以蜡烛组成中一定有碳元素和氢元素,可能含有氧元素,选项D正确;
故选:D。
5.C
【分析】
质量守恒定律是解释化学反应的定律;
【详解】
A、拧开盛酒精的瓶盖一段时间后质量变小,该变化没有生成新物质,属于物理变化,不能用质量守恒定律解释,错误;
B、mg水受热变为mg的水蒸气,该变化没有生成新物质,属于物理变化,不能用质量守恒定律解释,错误;
C、2g氢气和8g氧气反应生成9g水,该变化是一个化学变化,反应中氢气过量,能用质量守恒定律解释,正确;
D、20g食盐溶于80g水得100g食盐水,该变化没有生成新物质,属于物理变化,不能用质量守恒定律解释,错误;
故选C。
6.C
【分析】
根据质量守恒定律,由生成物可以初步确定该物质中含有碳元素和氢元素,由生成的二氧化碳和水中碳、氢元素的质量和与该物质的质量进行对比,从而确定该物质的组成元素。
【详解】
中含有碳元素的质量为:,水中含有氢元素的质量为:,生成物二氧化碳和水中所含碳、氢元素的质量和为,某化合物的质量为,,该物质中含氧元素的质量为:,则该物质中一定含有碳、氢、氧三种元素。
故选C。
7.B
【详解】
A、氢气和氧气反应的化学方程式为:可知,氢气、氧气、水的质量比为1:8:9,故1克氢气和8克氧气反应生成9克水,故选项说法错误;
B、碳和氧气反应的化学方程式为: 可知,故12份质量的碳和32份质量的氧气反应生成44份质量的二氧化碳,12g碳在40g氧气中完全燃烧也生成44g二氧化碳,氧气剩余,故选项说法正确;
C、50克酒精和50克水混合得到100克酒精溶液,没有新物质生成,属于物理变化,不符合质量守恒定律,故选项说法错误;
D、某可燃物完全燃烧生成二氧化碳和水,CO2和H2O两种物质中含有碳、氢、氧三种元素,根据质量守恒定律,反应前后,元素种类不变,反应物氧气中只含有氧元素,则某化合物中一定含有碳、氢两种元素,可能含有氧元素,故选项说法错误。
故选B。
8.D
【详解】
A. 分子在不断的运动,所以在远处就可以闻到花的香味,故选项正确;
B. 化学变化的实质是分子分成原子,原子重新组合成新的分子,此过程中原子的种类与数目均不改变,故选项正确;
C. 原子核是由质子与中子构成的,但是原子核中不一定都有中子,如氢原子核内只有质子,没有中子,故选项正确;
D. 离子是带电的微粒,但是带电的微粒不一定是离子,如质子、电子也带电,故选项错误。
故选:D。
9.D
【详解】
A、氢原子中没有中子,所以说原子核中一定含有质子,不一定含有中子,选项错误;
B、原子核外电子能量不同,离核越近,电子的能量越低,离核越远,能量越高,选项错误;
C、由同种元素组成的纯净物是单质,由同一种元素组成的物质不一定是纯净物,例如氧气和臭氧在一起属于混合物,选项错误;
D、原子是化学变化中的最小粒子,在物质发生化学变化时,原子的种类不变,元素也不会改变,选项正确。
故选:D。
10.D
【分析】
此类题是根据质量守恒定律进行的相关计算,一般分三步完成:
1、根据质量守恒定律计算出未知的值,的值为:;
2、根据反应前后质量变化确定反应物和生成物,质量减少的为反应物,质量增加的为生成物,甲的质量减小了,是反应物,丙和丁的质量增加了,是生成物;
3、根据反应前后各物质质量的变化,求出反应物反应的质量和生成物生成的质量,即减少的质量和增加的质量,即36g甲完全反应生成32g丙和4g丁。再根据上述信息确定每个选项的正误。
【详解】
A、由分析可知,该反应是由一种物质生成两种物质的反应,是分解反应,故A选项错误;
B、任何化学反应都遵守质量守恒定律,故B选项错误;
C、反应中丙丁的质量比32g:4g=8:1,故C选项错误;
D、催化剂只改变其他物质的反应速率,本身的质量和化学性质在反应前后都不变的物质,由题中信息可得出乙的质量在反应前后没有变化,但无法判断乙的化学性质是否改变和乙是否改变了甲的反应速率,所以乙不一定是该反应的催化剂,故D选项正确。
故选D。
11.总质量 总质量
【详解】
无数实验证明:参加化学反应的各物质的总质量,等于反应后生成的各物质的总质量,这个规律叫作质量守恒定律。
12.
(1)Cu2+
(2)D
(3) 2:1
【分析】
(1)
硫酸铜溶液中含有铜离子、硫酸根离子和水分子,溶液呈蓝色,硫酸溶液中含有氢离子、硫酸根离子和水分子,溶液呈无色,则硫酸铜溶液呈硫酸的原因是溶液中含有铜离子,其符号为Cu2+,故填Cu2+。
(2)
硫酸铜固体溶于水的实验中,硫酸铜固体“消失”后液面比原水平线低是因为分子间有间隔,硫酸铜固体溶于水时,铜离子和硫酸根离子扩散到水分子的间隔中,则硫酸铜溶解后溶液的体积小于溶解前固体与水的体积和,故填D。
(3)
①由图可知,A图中含有2个氢分子和1个氧分子,发生化学变化时,分子先被分成原子,即2个氢分子分成4个氢原子,1个氧分子分成2个氧原子,故B图画为。
②由图可知,A图中含有2个氢分子和1个氧分子,反应后C图中只含有2个水分子,不含氢分子和氧分子,则此变化中参加反应的氢分子与氧分子的个数比为2:1,故填2:1。
13.
(1)②⑤
(2)配制溶液等
(3) 紫色粉末 +6价 防潮避热
【分析】
(1)
①工业“三废”未经处理直接排放会导致环境污染,故①错误;
②植树造林,加大绿化面积,有利于保护环境,故②正确;
③随意丢弃废旧电池和塑料制品,会污染环境,污染地下水资源,故③错误;
③生活污水任意排放,会导致水资源污染,故④错误;
④对然煤进行脱硫处理,减少二氧化硫的排放,故⑤正确;
故答案为:②⑤
(2)
水在化学实验中可以用来作溶剂配制溶液,洗涤仪器,用排水法来收集气体等。
(3)
①颜色状态属于高铁酸钾的物理性质,故答案为:紫色粉末。
②根据在化合物中元素的化合价为0,可得高铁酸钾中铁元素的化合价为(+1)2+x+(-2)4=0,则x=+6。
③因为高铁酸钾在水中或受热的情况下不稳定,容易发生化学反应,所以保存高铁酸钾时应注意防潮避热。
④根据化学反应前后原子的种类和数目不发生改变,则另一种金属氧化物为氧化钾,高铁酸钾受热分解成氧化铁,氧气和氧化钾,故反应的符号表达式为:。
14.32 1.8
【分析】
质量守恒定律是指参加化学反应的各物质的质量总和等于生成的各物质的质量总和。
【详解】
由质量守恒定律可知,将36g水通电完全分解时,得到4g氢气的同时,可以得到氧气的质量为:36g-4g=32g,若已知在电解水过程中,共收集到氢气和氧气的质量为1. 8g,则已发生电解的水的质量为1. 8g,故答案为:32;1. 8。
【点睛】
本题主要考查学生运用质量守恒定律进行推断的能力。
15.
(1) 13 失 原子序数为80、相对原子质量为200.6、元素符号为Hg
(2) ABD CO2+NON2+CO2
【分析】
(1)
根据该微粒的结构示意图可知,图1是原子的结构示意图,原子中质子数=核外电子数,则其中x=2+8+3=13,该微粒最外层电子数小于4,在化学反应中易失电子;
从图2中获得的信息有:汞的原子序数为80,相对原子质量为200.6,元素符号为Hg。
(2)
①由如图3所示的微观示意图可知,反应前有一氧化碳分子和一氧化氮分子,反应后有氮分子、二氧化碳分子。反应前有一个碳原子、两个氧原子、一个氮原子,反应后有一个碳原子、两个氧原子、一个氮原子。因为原子属于元素,所以图3中体现了在化学变化前后一定不变的是元素种类 、原子种类、原子数目,故选ABD。
②图3中发生反应的符号表达式为:CO2+NON2+CO2。
16.
(1)水分子
(2)在化学变化中,分子分成原子,原子结合成新的分子
(3)
【分析】
(1)
由图可知,A物质为水,水由水分子构成,保持A物质化学性质的最小微粒是水分子;
(2)
由图可知,化学变化的微观本质是:在化学变化中,分子分成原子,原子结合成新的分子;
(3)
根据质量守恒定律,化学反应前后,原子的种类和数目不变,反应物中含H、Cl、O的个数分别是2、2、2,生成物中含H、Cl、O的个数分别是2、2、0,故生成物中还应含2个O,每个氧分子由2个氧原子构成,故E物质的分子模型图为: 。答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
