4.3质量守恒定律课后练习能力提升—2021-2022学年九年级化学科粤版(2012)上册(含解析)
文档属性
| 名称 | 4.3质量守恒定律课后练习能力提升—2021-2022学年九年级化学科粤版(2012)上册(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 69.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-13 00:00:00 | ||
图片预览




文档简介
第四章生命之源---水4.3质量守恒定律课后练习能力提升九年级化学上册(科粤版2012)
练习
一、单选题,共11小题
1.下列说法错误的是
A.化学反应前后,物质的种类一定发生改变 B.化学反应前后,分子的种类一定发生改变
C.化学反应前后,原子的数目一定不发生改变 D.化学反应前后,原子团一定发生改变
2.下列事实符合质量守恒定律的是
A.汽油挥发后质量变小 B.水变成冰后体积变大
C.木材燃烧后质量变小 D.酒精和水混合后质量不变
3.在一个密闭容器中,有甲、乙、丙、丁四种物质在一定条件下充分反应,测得反应前后各物质质量如下表
物质 甲 乙 丙 丁
反应前质量/g 4 2 58 5
反应后质量/g 待测 27 0 19
则该密闭容器中发生的化学反应类型为
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
4.下图表示两种气体发生化学反应的微观示意图,其中相同的球代表同种原子。下列有关说法错误的是
A.该反应属于化合反应 B.反应前后原子的种类和数目都不变
C.生成物是氧化物 D.在化学反应中,分子可以分为原子,而原子不可再分
5.某纯净物3g在氧气中完全燃烧,生成8.8g二氧化碳和5.4g水。下列说法不正确的是
A.该纯净物中含有C、H元素,不含O元素 B.该反应中O2和CO2的质量比为14:11
C.该纯净物中C、H原子的个数比为1:4 D.该反应中O2和H2O的分子数之比为7:6
6.下面是某化学反应的微观模型示意图,据此分析错误的是
A.分子的种类发生变化 B.反应前后原子数目没有变化
C.示意图中的各物质均属于化合物 D.生成物是混合物
7.75克镁、锌、铁的混合物与足量的稀硫酸反应,反应完全后蒸发得到219克固体(已换算成无水硫酸盐),反应中得到氢气的质量
A.3克 B.3.5克 C.4克 D.4.5克
8.下列对化学基本概念的认识,正确的是
A.微粒观:气体单质都是由分子构成
B.分类观:过氧化氢溶液属于氧化物
C.转化观:一氧化碳和二氧化碳在一定条件下可以相互转化
D.守恒观:10克氢气在10克氧气中充分燃烧,生成水的质量为20克
9.在一个密闭容器中有X、Y、Z、Q四种物质,一定条件下充分反应,测得反应前后各物质的质量如下表所示:已知X和Q两种物质的相对分子质量均为M,下列推理中正确的是
X Y Z Q
反应前的质量/g 8 10 1 21
反应后的质量/g 0 21 待测 9
A.反应后物质Z的质量为9g B.反应中物质Y与Q的质量比为1:1
C.反应生成Y的质量为11g D.该反成的化学方程式中,物质X与Q的化学计量数之比为3:2
10.连二亚硫酸钠(Na2S2O4)是重要的化工原料,该物质在潮湿的空气中极不稳定,易分解并引起燃烧,反应的化学方程式为:2Na2S2O4= Na2S2O3 + X + SO2↑。下列说法不正确的是
A.Na2S2O4要在干燥阴凉处密闭保存 B.X中不含氧元素
C.Na2S2O3中S的化合价为+2 D.题干中的反应属于分解反应
11.取两份等质量的xCuCO3· yCu(OH)2固体,在一份中加入过量盐酸,生成6.6gCO2;加热另一份使其完全分解,得到20.0gCuO。则下列关系正确的是
A.y∶x=1∶1 B.y∶x=1∶3 C.y∶x=3∶2 D.y∶x=2∶3
二、非选择题,共5小题
12.无数实验证明,参加化学反应的各物质的______,等于反应后生成的各物质的______。这个规律叫做质量守恒定律。
13.在化学反应前后,下列各项中:①原子的数目,②分子的数目,③原子的种类,④物质的组成,⑤分子的种类,肯定不会改变的是___________;肯定会改变的是___________。
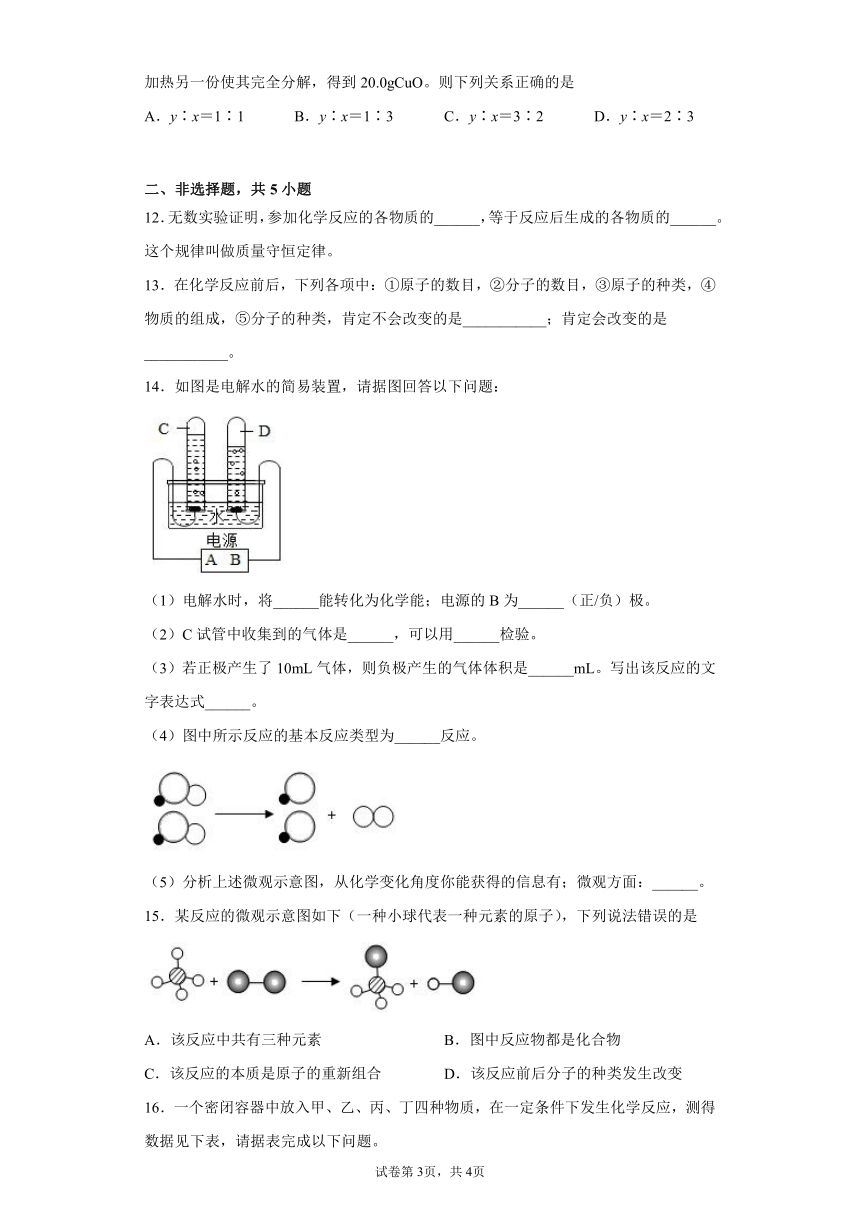
14.如图是电解水的简易装置,请据图回答以下问题:
(1)电解水时,将______能转化为化学能;电源的B为______(正/负)极。
(2)C试管中收集到的气体是______,可以用______检验。
(3)若正极产生了10mL气体,则负极产生的气体体积是______mL。写出该反应的文字表达式______。
(4)图中所示反应的基本反应类型为______反应。
(5)分析上述微观示意图,从化学变化角度你能获得的信息有;微观方面:______。
15.某反应的微观示意图如下(一种小球代表一种元素的原子),下列说法错误的是
A.该反应中共有三种元素 B.图中反应物都是化合物
C.该反应的本质是原子的重新组合 D.该反应前后分子的种类发生改变
16.一个密闭容器中放入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得数据见下表,请据表完成以下问题。
物质 甲 乙 丙 丁
反应前质量/g 8 35 2 x
反应后质量/g 2 7 2 40
(1)表中的x的值为______;
(2)在该反应中,可能是催化剂的物质是______;
(3)该反应的基本反应类型为______(填“化合反应”或“分解反应”);
(4)在该反应过程中,甲和乙的质量之比为______。
试卷第1页,共3页
试卷第1页,共3页
参考答案
1.D
【详解】
A、化学变化中有新物质生成,所以化学反应前后,物质的种类一定发生改变,选项正确;
B、化学变化中有新物质生成,即有新分子生成,所以化学反应前后,分子的种类一定发生改变,选项正确;
C、原子是化学变化中的最小粒子,所以化学反应前后,原子的数目一定不发生改变,选项正确;
D、化学反应前后,原子团不一定发生改变,选项错误。
故选D。
2.C
【详解】
A、汽油挥发后质量变小,是因为汽油的状态发生了改变,无新物质生成,属于物理变化,不符合质量守恒定律, 不符合题意;
B、水变成冰后体积变大,是因为分子之间的间隔变大,无新物质生成,属于物理变化,不符合质量守恒定律,不符合题意;
C、木材燃烧后质量变小,是因为生成了二氧化碳等气体,有新物质生成,属于化学变化,符合质量守恒定律,符合题意;
D、酒精和水混合后质量不变,无新物质生成,属于物理变化,不符合质量守恒定律,不符合题意。
故选C。
3.A
【详解】
反应后丙物质减少了58g,是反应物;乙物质增加了25g,是生成物;丁物质增加了14g,是生成物;根据质量守恒定律可知,甲物质是生成物,生成甲的质量是58g-25g-14g=19g。由分析可知,丙是反应物,甲、乙、丁是生成物,属于分解反应。
故选:A。
4.C
【详解】
A、由图可知,该反应符合“多变一”的特点,属于化合反应,不符合题意;
B、由图及质量守恒定律可知,化学反应前后,原子的种类和数目不变,不符合题意;
C、生成物是由两种元素组成的化合物,可能含氧元素,也可能不含氧元素,故不一定是氧化物,符合题意;
D、由图可知,在化学变化中,分子可分为原子,原子重新组合为新的分子,原子不可再分,不符合题意。
故选C。
5.C
【详解】
A、根据质量守恒定律,化学反应前后,元素的种类和质量不变,生成物中含C、H、O,氧气由氧元素组成,故该纯净物一定含C、H元素,生成二氧化碳中碳元素的质量为,生成水中氢元素的质量为 ,2.4g+0.6g=3g,故该纯净物中不含氧元素,不符合题意;
B、根据质量守恒定律,化学反应前后,物质的总质量不变,故参加反应的氧气的质量为8.8g+5.4g-3g=11.2g,故该反应中,氧气与二氧化碳的质量比为11.2g:8.8g=14:11,不符合题意;
C、该纯净物中C、H原子的个数比为,符合题意;
D、该反应中,氧气和水的分子个数比为,不符合题意。
故选C。
6.C
【详解】
A、该反应有新物质生成,属于化学变化,分子种类发生了改变,不符合题意;
B、由图及质量守恒定律可知,化学反应前后,原子的种类和数目不变,不符合题意;
C、由图可知,反应物中其中一种物质是由同种元素组成的纯净物,属于单质,其它物质均是由不同种元素组成的纯净物,属于化合物,符合题意;
D、生成物是由两种物质组成,属于混合物,不符合题意。
故选C。
7.A
【详解】
由化学方程式, , 可知,固体增加的质量为硫酸根离子的质量。根据硫酸中硫酸根离子与氢离子及氢离子与氢气的关系,设氢气的质量为 x,则
所以反应中得到氢气的质量是3g。故选A。
8.C
【详解】
A、气体单质不一定都是由分子构成,稀有气体是由原子直接构成的,故选项说法错误。
B、过氧化氢溶液中含有过氧化氢、水,属于混合物,故选项说法错误。
C、一氧化碳和二氧化碳在一定条件下可以相互转化,一氧化碳燃烧生成二氧化碳,二氧化碳与碳在高温下反应生成一氧化碳,故选项说法正确。
D、氢气和氧气反应的化学方程式为:可知,氢气、氧气、水的质量比为4:32:36=1:8:9,则10克氢气在10克氧气中充分燃烧,氢气有剩余,生成水的质量一定小于20克,故选项说法错误。
故选:C。
【点睛】
本题难度不大,掌握一氧化碳和二氧化碳的化学性质、氧化物的特征、常见物质的微观构成等是正确解答本题的关键。
9.C
【详解】
A、根据质量守恒定律可知,设待测质量为x,反应前各物质的质量总和等于反应后生成各物质的质量总和,则得:8g + 10g + 1g +21g = 0+ 21g +x+ 9g解得:x= 10g,选项A错误;
B、反应过程中,Y与Q的质量比=(21g -10g):(21g -9g)= 11:12,选项B错误;
C、反应后Y 的质量为21g -10g = 11g,选项C正确;
D、设反应中X与Q的化学计量数α和b,则依据方程式中物质的质量关系可知:,解得 ,则X与Q的计量数之比是2:3,选项D错误。
故选:C。
10.B
【详解】
A、连二亚硫酸钠在潮湿的空气中极不稳定,易分解并引起燃烧,说明该物质化学性质不稳定,应在干燥阴凉处密闭保存,选项A正确;
B、根据反应的化学方程式,反应物中钠、硫、氧原子个数分别为4、4、8,根据反应前后原子种类、数目不变,反应后的生成物中钠、硫、氧原子个数也应该分别为4、4、8,则每个X分子由2个钠原子、1个硫原子和3个氧原子构成,则物质X的化学式为Na2SO3,选项B错误;
C、Na2S2O3中钠元素显+1价,氧元素显-2价,设硫元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1) × 2 + 2x+(-2) × 3 = 0,则x=+2价,选项C正确;
D、该反应是由一种物质生成三种物质,符合“一生多”的特征,属于分解反应,选项D正确;
故选:B
11.D
【详解】
由xCuCO3· yCu(OH)2可知,生成二氧化碳与氧化铜的质量比为
44x:80(x+y)=6.6g:20g
x:y=3:2
故选D。
12.总质量 总质量
【详解】
无数实验证明:参加化学反应的各物质的总质量,等于反应后生成的各物质的总质量,这个规律叫作质量守恒定律。
13.①③ ④⑤
【详解】
根据质量守恒定律,在化学反应前后有6个不变:①物质的总质量不变②元素的种类不变③元素的质量不变④原子的种类不变⑤原子的数目不变⑥原子的质量不变;2个变:①物质的种类②分子的种类;一个可能变:③分子的个数。肯定不会改变的是①③;肯定会改变的是④⑤。
14.
(1) 电 负
(2) 氧气 带火星的木条
(3) 20
(4)分解反应
(5)化学反应前后,原子种类和原子个数都不变
【解析】
(1)
电解水,是在通电的条件下,发生化学反应生成氢气和氧气,故是将电能转化成化学能;电解时正极产生氧气,负极产生氢气,氢气和氧气的体积比为2:1,由图示可以看出,与电源B端产生的气体体积大,故D试管内的气体是氢气,C试管内的气体是氧气,故电源的B端为负极。
(2)
C试管内收集到气体是氧气,氧气有助燃性,能使带火星的木条复燃,故可用带火星的木条检验;
(3)
由于正负极产生气体的体积比为1:2,所以正极产生了10mL气体,负极产生产生20mL气体,反应的文字表达式为:。
(4)
由一种物质反应后生成两种或两种以上其他物质的反应叫做分解反应,图示表示一种分子反应后生成了两种不同的分子,即一种物质反应生成了两种物质,所以属于分解反应。
(5)
由该微观示意图可以得出,化学反应前后,原子的种类和个数都是不变的。
15.B
【详解】
A、从图示看出,该反应中共有三种不同的小球,代表三种不同的原子,故该反应中共有三种元素,故选项说法正确;
B、从图示看出,反应物中有一种是由不同种原子构成的化合物,有一种是由同种原子构成的单质,故选项说法错误;
C、该反应表示的化学反应,化学反应的本质是分子分成原子,原子的重新组合成新分子,故选项说法正确;
D、由微粒的变化可知,该反应前后分子的种类发生改变,故说法正确。
故选B。
16.
(1)6
(2)丙
(3)化合反应
(4)6︰28或3︰14
【分析】
(1)
根据质量守恒,反应前后总质量不变,故8+35+2+x=2+7+2+40,故x=6,故填:6。
(2)
催化剂反应前后质量不变,故丙可能是催化剂,故填:丙。
(3)
甲乙质量减少,是反应物,丁质量增加是生成物,反应多变一属于化合反应,故填:化合反应。
(4)
在该反应过程中,甲和乙的质量之比为(8-2):(35-7)=6:28=3:14,故填:6︰28或3︰14。
答案第1页,共2页
答案第1页,共2页
练习
一、单选题,共11小题
1.下列说法错误的是
A.化学反应前后,物质的种类一定发生改变 B.化学反应前后,分子的种类一定发生改变
C.化学反应前后,原子的数目一定不发生改变 D.化学反应前后,原子团一定发生改变
2.下列事实符合质量守恒定律的是
A.汽油挥发后质量变小 B.水变成冰后体积变大
C.木材燃烧后质量变小 D.酒精和水混合后质量不变
3.在一个密闭容器中,有甲、乙、丙、丁四种物质在一定条件下充分反应,测得反应前后各物质质量如下表
物质 甲 乙 丙 丁
反应前质量/g 4 2 58 5
反应后质量/g 待测 27 0 19
则该密闭容器中发生的化学反应类型为
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
4.下图表示两种气体发生化学反应的微观示意图,其中相同的球代表同种原子。下列有关说法错误的是
A.该反应属于化合反应 B.反应前后原子的种类和数目都不变
C.生成物是氧化物 D.在化学反应中,分子可以分为原子,而原子不可再分
5.某纯净物3g在氧气中完全燃烧,生成8.8g二氧化碳和5.4g水。下列说法不正确的是
A.该纯净物中含有C、H元素,不含O元素 B.该反应中O2和CO2的质量比为14:11
C.该纯净物中C、H原子的个数比为1:4 D.该反应中O2和H2O的分子数之比为7:6
6.下面是某化学反应的微观模型示意图,据此分析错误的是
A.分子的种类发生变化 B.反应前后原子数目没有变化
C.示意图中的各物质均属于化合物 D.生成物是混合物
7.75克镁、锌、铁的混合物与足量的稀硫酸反应,反应完全后蒸发得到219克固体(已换算成无水硫酸盐),反应中得到氢气的质量
A.3克 B.3.5克 C.4克 D.4.5克
8.下列对化学基本概念的认识,正确的是
A.微粒观:气体单质都是由分子构成
B.分类观:过氧化氢溶液属于氧化物
C.转化观:一氧化碳和二氧化碳在一定条件下可以相互转化
D.守恒观:10克氢气在10克氧气中充分燃烧,生成水的质量为20克
9.在一个密闭容器中有X、Y、Z、Q四种物质,一定条件下充分反应,测得反应前后各物质的质量如下表所示:已知X和Q两种物质的相对分子质量均为M,下列推理中正确的是
X Y Z Q
反应前的质量/g 8 10 1 21
反应后的质量/g 0 21 待测 9
A.反应后物质Z的质量为9g B.反应中物质Y与Q的质量比为1:1
C.反应生成Y的质量为11g D.该反成的化学方程式中,物质X与Q的化学计量数之比为3:2
10.连二亚硫酸钠(Na2S2O4)是重要的化工原料,该物质在潮湿的空气中极不稳定,易分解并引起燃烧,反应的化学方程式为:2Na2S2O4= Na2S2O3 + X + SO2↑。下列说法不正确的是
A.Na2S2O4要在干燥阴凉处密闭保存 B.X中不含氧元素
C.Na2S2O3中S的化合价为+2 D.题干中的反应属于分解反应
11.取两份等质量的xCuCO3· yCu(OH)2固体,在一份中加入过量盐酸,生成6.6gCO2;加热另一份使其完全分解,得到20.0gCuO。则下列关系正确的是
A.y∶x=1∶1 B.y∶x=1∶3 C.y∶x=3∶2 D.y∶x=2∶3
二、非选择题,共5小题
12.无数实验证明,参加化学反应的各物质的______,等于反应后生成的各物质的______。这个规律叫做质量守恒定律。
13.在化学反应前后,下列各项中:①原子的数目,②分子的数目,③原子的种类,④物质的组成,⑤分子的种类,肯定不会改变的是___________;肯定会改变的是___________。
14.如图是电解水的简易装置,请据图回答以下问题:
(1)电解水时,将______能转化为化学能;电源的B为______(正/负)极。
(2)C试管中收集到的气体是______,可以用______检验。
(3)若正极产生了10mL气体,则负极产生的气体体积是______mL。写出该反应的文字表达式______。
(4)图中所示反应的基本反应类型为______反应。
(5)分析上述微观示意图,从化学变化角度你能获得的信息有;微观方面:______。
15.某反应的微观示意图如下(一种小球代表一种元素的原子),下列说法错误的是
A.该反应中共有三种元素 B.图中反应物都是化合物
C.该反应的本质是原子的重新组合 D.该反应前后分子的种类发生改变
16.一个密闭容器中放入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得数据见下表,请据表完成以下问题。
物质 甲 乙 丙 丁
反应前质量/g 8 35 2 x
反应后质量/g 2 7 2 40
(1)表中的x的值为______;
(2)在该反应中,可能是催化剂的物质是______;
(3)该反应的基本反应类型为______(填“化合反应”或“分解反应”);
(4)在该反应过程中,甲和乙的质量之比为______。
试卷第1页,共3页
试卷第1页,共3页
参考答案
1.D
【详解】
A、化学变化中有新物质生成,所以化学反应前后,物质的种类一定发生改变,选项正确;
B、化学变化中有新物质生成,即有新分子生成,所以化学反应前后,分子的种类一定发生改变,选项正确;
C、原子是化学变化中的最小粒子,所以化学反应前后,原子的数目一定不发生改变,选项正确;
D、化学反应前后,原子团不一定发生改变,选项错误。
故选D。
2.C
【详解】
A、汽油挥发后质量变小,是因为汽油的状态发生了改变,无新物质生成,属于物理变化,不符合质量守恒定律, 不符合题意;
B、水变成冰后体积变大,是因为分子之间的间隔变大,无新物质生成,属于物理变化,不符合质量守恒定律,不符合题意;
C、木材燃烧后质量变小,是因为生成了二氧化碳等气体,有新物质生成,属于化学变化,符合质量守恒定律,符合题意;
D、酒精和水混合后质量不变,无新物质生成,属于物理变化,不符合质量守恒定律,不符合题意。
故选C。
3.A
【详解】
反应后丙物质减少了58g,是反应物;乙物质增加了25g,是生成物;丁物质增加了14g,是生成物;根据质量守恒定律可知,甲物质是生成物,生成甲的质量是58g-25g-14g=19g。由分析可知,丙是反应物,甲、乙、丁是生成物,属于分解反应。
故选:A。
4.C
【详解】
A、由图可知,该反应符合“多变一”的特点,属于化合反应,不符合题意;
B、由图及质量守恒定律可知,化学反应前后,原子的种类和数目不变,不符合题意;
C、生成物是由两种元素组成的化合物,可能含氧元素,也可能不含氧元素,故不一定是氧化物,符合题意;
D、由图可知,在化学变化中,分子可分为原子,原子重新组合为新的分子,原子不可再分,不符合题意。
故选C。
5.C
【详解】
A、根据质量守恒定律,化学反应前后,元素的种类和质量不变,生成物中含C、H、O,氧气由氧元素组成,故该纯净物一定含C、H元素,生成二氧化碳中碳元素的质量为,生成水中氢元素的质量为 ,2.4g+0.6g=3g,故该纯净物中不含氧元素,不符合题意;
B、根据质量守恒定律,化学反应前后,物质的总质量不变,故参加反应的氧气的质量为8.8g+5.4g-3g=11.2g,故该反应中,氧气与二氧化碳的质量比为11.2g:8.8g=14:11,不符合题意;
C、该纯净物中C、H原子的个数比为,符合题意;
D、该反应中,氧气和水的分子个数比为,不符合题意。
故选C。
6.C
【详解】
A、该反应有新物质生成,属于化学变化,分子种类发生了改变,不符合题意;
B、由图及质量守恒定律可知,化学反应前后,原子的种类和数目不变,不符合题意;
C、由图可知,反应物中其中一种物质是由同种元素组成的纯净物,属于单质,其它物质均是由不同种元素组成的纯净物,属于化合物,符合题意;
D、生成物是由两种物质组成,属于混合物,不符合题意。
故选C。
7.A
【详解】
由化学方程式, , 可知,固体增加的质量为硫酸根离子的质量。根据硫酸中硫酸根离子与氢离子及氢离子与氢气的关系,设氢气的质量为 x,则
所以反应中得到氢气的质量是3g。故选A。
8.C
【详解】
A、气体单质不一定都是由分子构成,稀有气体是由原子直接构成的,故选项说法错误。
B、过氧化氢溶液中含有过氧化氢、水,属于混合物,故选项说法错误。
C、一氧化碳和二氧化碳在一定条件下可以相互转化,一氧化碳燃烧生成二氧化碳,二氧化碳与碳在高温下反应生成一氧化碳,故选项说法正确。
D、氢气和氧气反应的化学方程式为:可知,氢气、氧气、水的质量比为4:32:36=1:8:9,则10克氢气在10克氧气中充分燃烧,氢气有剩余,生成水的质量一定小于20克,故选项说法错误。
故选:C。
【点睛】
本题难度不大,掌握一氧化碳和二氧化碳的化学性质、氧化物的特征、常见物质的微观构成等是正确解答本题的关键。
9.C
【详解】
A、根据质量守恒定律可知,设待测质量为x,反应前各物质的质量总和等于反应后生成各物质的质量总和,则得:8g + 10g + 1g +21g = 0+ 21g +x+ 9g解得:x= 10g,选项A错误;
B、反应过程中,Y与Q的质量比=(21g -10g):(21g -9g)= 11:12,选项B错误;
C、反应后Y 的质量为21g -10g = 11g,选项C正确;
D、设反应中X与Q的化学计量数α和b,则依据方程式中物质的质量关系可知:,解得 ,则X与Q的计量数之比是2:3,选项D错误。
故选:C。
10.B
【详解】
A、连二亚硫酸钠在潮湿的空气中极不稳定,易分解并引起燃烧,说明该物质化学性质不稳定,应在干燥阴凉处密闭保存,选项A正确;
B、根据反应的化学方程式,反应物中钠、硫、氧原子个数分别为4、4、8,根据反应前后原子种类、数目不变,反应后的生成物中钠、硫、氧原子个数也应该分别为4、4、8,则每个X分子由2个钠原子、1个硫原子和3个氧原子构成,则物质X的化学式为Na2SO3,选项B错误;
C、Na2S2O3中钠元素显+1价,氧元素显-2价,设硫元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1) × 2 + 2x+(-2) × 3 = 0,则x=+2价,选项C正确;
D、该反应是由一种物质生成三种物质,符合“一生多”的特征,属于分解反应,选项D正确;
故选:B
11.D
【详解】
由xCuCO3· yCu(OH)2可知,生成二氧化碳与氧化铜的质量比为
44x:80(x+y)=6.6g:20g
x:y=3:2
故选D。
12.总质量 总质量
【详解】
无数实验证明:参加化学反应的各物质的总质量,等于反应后生成的各物质的总质量,这个规律叫作质量守恒定律。
13.①③ ④⑤
【详解】
根据质量守恒定律,在化学反应前后有6个不变:①物质的总质量不变②元素的种类不变③元素的质量不变④原子的种类不变⑤原子的数目不变⑥原子的质量不变;2个变:①物质的种类②分子的种类;一个可能变:③分子的个数。肯定不会改变的是①③;肯定会改变的是④⑤。
14.
(1) 电 负
(2) 氧气 带火星的木条
(3) 20
(4)分解反应
(5)化学反应前后,原子种类和原子个数都不变
【解析】
(1)
电解水,是在通电的条件下,发生化学反应生成氢气和氧气,故是将电能转化成化学能;电解时正极产生氧气,负极产生氢气,氢气和氧气的体积比为2:1,由图示可以看出,与电源B端产生的气体体积大,故D试管内的气体是氢气,C试管内的气体是氧气,故电源的B端为负极。
(2)
C试管内收集到气体是氧气,氧气有助燃性,能使带火星的木条复燃,故可用带火星的木条检验;
(3)
由于正负极产生气体的体积比为1:2,所以正极产生了10mL气体,负极产生产生20mL气体,反应的文字表达式为:。
(4)
由一种物质反应后生成两种或两种以上其他物质的反应叫做分解反应,图示表示一种分子反应后生成了两种不同的分子,即一种物质反应生成了两种物质,所以属于分解反应。
(5)
由该微观示意图可以得出,化学反应前后,原子的种类和个数都是不变的。
15.B
【详解】
A、从图示看出,该反应中共有三种不同的小球,代表三种不同的原子,故该反应中共有三种元素,故选项说法正确;
B、从图示看出,反应物中有一种是由不同种原子构成的化合物,有一种是由同种原子构成的单质,故选项说法错误;
C、该反应表示的化学反应,化学反应的本质是分子分成原子,原子的重新组合成新分子,故选项说法正确;
D、由微粒的变化可知,该反应前后分子的种类发生改变,故说法正确。
故选B。
16.
(1)6
(2)丙
(3)化合反应
(4)6︰28或3︰14
【分析】
(1)
根据质量守恒,反应前后总质量不变,故8+35+2+x=2+7+2+40,故x=6,故填:6。
(2)
催化剂反应前后质量不变,故丙可能是催化剂,故填:丙。
(3)
甲乙质量减少,是反应物,丁质量增加是生成物,反应多变一属于化合反应,故填:化合反应。
(4)
在该反应过程中,甲和乙的质量之比为(8-2):(35-7)=6:28=3:14,故填:6︰28或3︰14。
答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
