4.3质量守恒定律同步练习能力提升—2021-2022学年九年级化学科粤版(2012)上册(含解析)
文档属性
| 名称 | 4.3质量守恒定律同步练习能力提升—2021-2022学年九年级化学科粤版(2012)上册(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 194.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-13 00:00:00 | ||
图片预览




文档简介
第四章生命之源---水4.3质量守恒定律同步练习能力提升九年级化学上册(科粤版2012)
练习
一、单选题,共12小题
1.在反应A+B→C+D中,若15gA与10gB完全反应没有剩余,则生成的C和D的质量总和为
A.15g B.10g C.25 g D.5g
2.举重运动员举重前常用白色的“镁粉”搓手,它质轻、吸水性好,可作防滑剂。“镁粉”的有效成分是碱式碳酸镁(Mg(OH)(CO3)4),其在加热条件下会发生分解,不可能得到的生成物是
A.CO2 B.MgO C.MgCl2 D.O2
3.下列叙述完全符合质量守恒定律的是
A.水结成冰前后,质量保持不变
B.50mL水和50 mL乙醇混合后总体积小于100 mL
C.在100g30%过氧化氢溶液中,含有30g过氧化氢和70g水
D.1.2g碳与3.2g氧气恰好完全反应可生成4.4g二氧化碳
4.在化学反应前后,一定不发生改变的是
A.分子的种类 B.原子的种类 C.分子的质量 D.物质的种类
5.下列说法错误的是
A.原子核一般由质子、中子构成
B.花香四溢主要是因为分子之间有间隔
C.保持水化学性质的最小微粒是水分子
D.化学反应前后原子的种类不会改变
6.氯化钠是重要的化工原料,是氯碱工业的基础。电解饱和食盐水一定不能得到的物质是
A.H2 B.Cl2 C.Na2CO3 D.NaOH
7.推理是学习化学常用的方法,下列推理正确的是
A.单质由同种元素组成,则只含有一种元素的物质一定是单质
B.化学变化中常伴随发光放热的现象所以有发光放热现象产生时一定发生了化学变化
C.同种元素的质子数相同,则质子数相同的粒子一定属于同种元素
D.蜡烛燃烧生成二氧化碳和水,所以蜡烛组成中一定有碳元素和氢元素
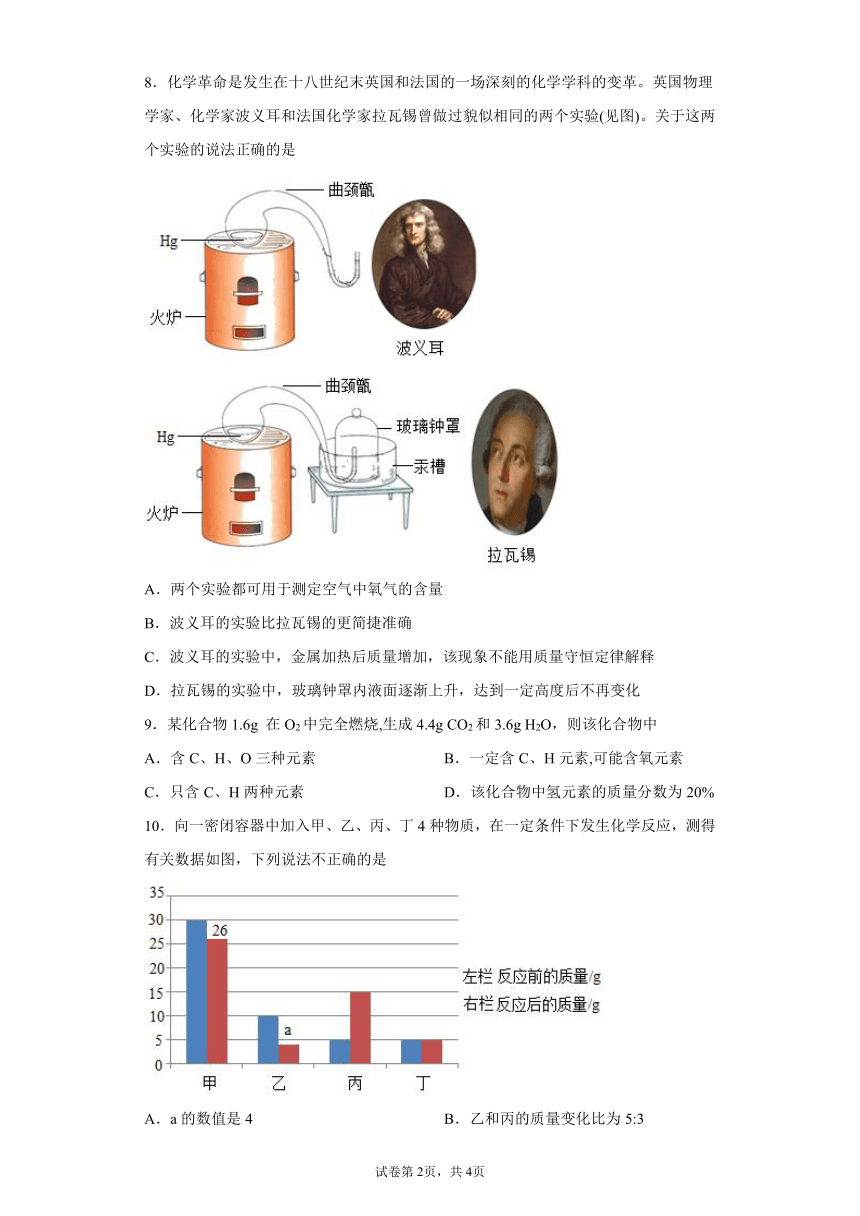
8.化学革命是发生在十八世纪末英国和法国的一场深刻的化学学科的变革。英国物理学家、化学家波义耳和法国化学家拉瓦锡曾做过貌似相同的两个实验(见图)。关于这两个实验的说法正确的是
A.两个实验都可用于测定空气中氧气的含量
B.波义耳的实验比拉瓦锡的更简捷准确
C.波义耳的实验中,金属加热后质量增加,该现象不能用质量守恒定律解释
D.拉瓦锡的实验中,玻璃钟罩内液面逐渐上升,达到一定高度后不再变化
9.某化合物1.6g 在O2中完全燃烧,生成4.4g CO2和3.6g H2O,则该化合物中
A.含C、H、O三种元素 B.一定含C、H元素,可能含氧元素
C.只含C、H两种元素 D.该化合物中氢元素的质量分数为20%
10.向一密闭容器中加入甲、乙、丙、丁4种物质,在一定条件下发生化学反应,测得有关数据如图,下列说法不正确的是
A.a的数值是4 B.乙和丙的质量变化比为5:3
C.该反应是化合反应 D.丁可能是该反应的催化剂
11.宏观辨识与微观探析是化学学习的核心素养。如图所示是某反应的微观示意图,则下列有关说法正确的是
A.该反应属于化合反应
B.该反应中物质的总质量发生改变
C.该反应可以看作是2种单质参加反应生成了1种单质和1种化合物
D.该反应中分子、原子数目都没有发生改变
12.如图是某个化学反应的微观模拟示意图,从图中不能获得的信息是
A.该反应前后一共涉及3种分子
B.该反应前后各种原子的种类没有变化
C.该反应的生成物都是化合物
D.该反应属于分解反应
二、非选择题,共4小题
13.下图是水电解的微观模拟过程。请回答下列问题:
(1)将B中相关粒子的图形补充完整_______,使之符合质量守恒定律。
(2)解释由A→B变化的微观实质是___________。
(3)画出与1个氧分子质子数相同的离子结构示意图__________。
(4)由A→C过程是分解反应,你判断的微观依据是________。
14.将25g氯酸钾和1g二氧化锰的混合物加热至完全分解,得到残余固体质量为16.4g,则产生氧气____g。
15.“见著知微,见微知著”是化学思维方法
(1)从宏观知微观
①50mL水与50mL乙醇混合后,溶液体积小于100mL,微观解释为___________。
②气体X在氧气中燃烧生成氮气和水,X分子中一定含有的原子是______和______(填符号)。
(2)从微观知宏观
①微粒A最外层电子数是___________,在化学反应中容易___________(填“得”或“失”)电子;
②微粒A、B、C、D、E中,对应单质化学性质最稳定的是___________(填编号,下同),属于同一种元素的是___________和___________。
③D元素与地壳中含量最多元素组成化合物的化学式___________ 。
16.下图是汽车尾气中一氧化碳和一氧化氮在催化剂催化作用下发生化学反应的微观示意图。请根据此图回答下列问题:
(1)在A图中将相关粒于图形补充完整:
(2)此变化中未发生改变的微观粒子有:______(填粒子符号)。
(3)已知X粒子与氧离子能形成XY型化合物,且X元素比氧元多一个周期,请写出X粒子的离子符号______。
试卷第1页,共3页
试卷第1页,共3页
参考答案
1.C
【详解】
据质量守恒定律,在化学反应中,参加反应的各物质的质量总和等于反应后生成各物质的质量总和,所以生成C和D的质量总和为15g+10g=25g;
故选:C。
2.C
【详解】
根据质量守恒定律,化学反应前后元素的种类不变,碱式碳酸镁【Mg(OH)(CO3)4】中不含氯元素,故不可能生成MgCl2,故选C。
【点睛】
3.D
【详解】
A、水结成冰前后,质量保持不变,为水的三态变化,为物理变化,不能用质量守恒定律解释;
B、50mL水和50mL乙醇混合后总体积小于100mL,无新物质生成,为物理变化,不能用质量守恒定律解释;
C、在100g过氧化氢溶液中,含有30g过氧化氢和70g水,无新物质生成,不适用质量守恒定律;
D、1.2g碳与3.2g氧气恰好完全反应可生成4.4g二氧化碳,生成物质量=反应物质量之和,符合质量守恒定律。故选D。
【点睛】
质量守恒定律只能解释化学变化,而A、B、C三项中都没有发生化学变化,只是发生了物理变化,因此。质量守恒定律只适合于任何的化学变化。
4.B
【详解】
A、化学变化过程是分子破裂成原子,原子重新组合成新分子的过程,所以化学反应前后分子的种类一定改变,选项不符合题意;
B、化学变化过程是分子破裂成原子,原子重新组合成新分子的过程,所以化学反应前后原子的种类不变,选项符合题意;
C、化学变化过程是分子破裂成原子,原子重新组合成新分子的过程,所以分子的质量一定改变,选项不符合题意;
D、化学反应中有新物质生成,化学反应前后物质的种类一定改变,选项不符合题意。
故选B。
5.B
【详解】
A、原子一般是由质子和中子构成的,说法正确;
B、花香四溢主要是因为分子在不断运动,说法错误;
C、分子是保持物质化学性质的最小微粒,水是由水分子构成,所以保持水化学性质的最小微粒是水分子,说法正确;
D、由质量守恒定律可知,化学反应前后原子的种类不会改变,说法正确。
故选:B。
6.C
【详解】
方法一:电解饱和食盐水的化学方程式:2NaCl+2H2O Cl2↑+H2↑+2NaOH ,电解饱和食盐水可以得到的物质是:Cl2、H2、NaOH,故答案选择C。
方法二:根据质量守恒定律,饱和食盐水中无碳元素,故生成物不可能有碳元素,故答案选择C。
7.D
【详解】
A、由同种元素组成的物质不一定是单质,如氧气和臭氧的混合物,选项A错误;
B、化学变化中常伴随发光放热的现象,但有发光放热现象产生时不一定发生了化学变化,如通电的电灯,不属于化学变化,选项B错误;
C、同种元素的原子质子数相同,但是质子数相同的微粒不一定属于同种元素,选项C错误;
D、蜡烛燃烧生成二氧化碳和水,根据质量守恒定律可知,化学反应前后元素的种类不变,所以蜡烛组成中一定有碳元素和氢元素,可能含有氧元素,选项D正确;
故选:D。
8.D
【详解】
A、波义耳的实验中装置不是密封的,无法测定空气中氧气的含量,不正确;
B、波义耳的实验中装置不是密封的,无法测定空气中氧气的含量,波义耳的实验不如拉瓦锡的准确,不正确;
C、波义耳的实验中,金属加热后质量增加,属于化学变化,该现象能用质量守恒定律解释,不正确;
D、拉瓦锡的实验中,氧气被消耗,玻璃钟罩内液面逐渐上升,达到一定高度后不再变化,是因为氧气完全反应后反应停止,正确。
故选D。
9.C
【分析】
由题可知:某化合物在氧气中燃烧生成二氧化碳和水,根据质量守恒定律可知,化合物中一定含有碳元素和氢元素,且含有的碳元素的质量等于二氧化碳中碳元素的质量: ;含有的氢元素的质量等于水中氢元素的质量: ;所以化合物中碳氢元素的质量和为1.2g+0.4g=1.6g,可知化合物中不含有氧元素。
【详解】
A、由上述分析可知,化合物中一定含有碳元素、氢元素,不含有氧元素,选项A错误;
B、由上述分析可知,化合物中一定含有碳元素、氢元素,不含有氧元素,选项B错误;
C、由上述分析可知,化合物中一定含有碳元素、氢元素,不含有氧元素,选项C正确;
D、该化合物中氢元素的质量分数为,选项D错误;
故选:C
10.B
【详解】
A、根据质量守恒定律,化学反应前后,物质的总质量不变,故30+10+5+5=26+a+15+5,a=4,不符合题意;
B、乙和丙的质量变化比为:(10-4):(15-5)=3:5,符合题意;
C、反应后,甲的质量减小,甲是反应物,乙的质量减小,乙是反应物,丙的质量增加,丙是生成物,丁的质量不变,丁可能是催化剂,也可能是不参与反应的杂质,甲、乙是反应物,丙是生成物,该反应符合“多变一”的特点,属于化合反应,不符合题意;
D、由C的分析可知,丁可能是该反应的催化剂,不符合题意。
故选B。
11.A
【详解】
A、分析微观示意图可知,该反应是由两种单质反应生成一种化合物,故该反应属于化合反应,此选项表述正确;
B、化学反应是分子分成原子,原子又重新组成新的分子的过程,故化学反应前后物质的总质量不变,此选项表述不正确;
C、分析微观示意图可知,该反应是由两种单质参加反应生成了一种化合物,并没有生成新的单质,此选项表述不正确;
D、分析微观示意图可知,该反应的反应物均是由两个原子构成一个分子,而生成物则是由3个原子构成一个分子,故反应前后原子的数目不变,但分子的数目发生了改变,此选项表述不正确。
故选A。
12.C
【详解】
A、反应物中含一种分子,生成物中含两种分子,故该反应前后一共涉及3中分子,此选项表述正确,不符合题意;
B、化学反应前后原子的种类均不发生变化,此选项表述正确,不符合题意;
C、通过示意图可知,反应物属于化合物,生成物中的两种物质都属于单质,此选项表述不正确,符合题意;
D、通过示意图可知,该反应是一种化合物反应后生成两种单质,故该反应属于分解反应,此选项表述正确,不符合题意。
故选C。
【点睛】
13.
(1) ( 补1个氧原子和2个氢原子)
(2)在通电的条件下,水分子分解成氢原子和氧原子
(3)
(4)水分子一种分子反应生成氧分子和氢分子,两种分子(一种分子生成两种分子或水分子生成氢分子和氧分子)
【分析】
(1)
反应前后原子的种类、数目不变,所以B中应补充1个氧原子和2个氢原子,图片为 。
(2)
A到B的过程是水分子拆分成氢氧原子的过程,微观实质是在通电的条件下,水分子分解成氢原子和氧原子。
(3)
1个氧分子含有2个氧原子,1个氧原子有8个质子,所以2个氧原子有16个质子。质子数=原子序数,16号元素是硫元素,硫离子结构示意图为 。
(4)
A→C过程中,水分子一种分子反应生成氧分子和氢分子,两种分子,符合一变多的特点是分解反应。
14.9.6
【详解】
氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,由质量守恒定律,固体混合物减少的质量即为生成氧气的质量;则将25g氯酸钾和1g二氧化锰的混合物加热一段时间后,得到残余固体质量为16.4g,则产生氧气的质量为25g + 1g - 16.4g = 9.6g,故填:9.6g。
15.
(1) 分子间存在间隙 H N
(2) 7 得到 B
C E
Na2O
【详解】
(1)①由于分子间存在间隙,不同种分子彼此进入对方的间隙,使水和乙醇混合后总体积小于二者的体积和;
②化学反应前后元素种类和原子种类都不变,反应后有氮气和水生成,反应前应该存在氮元素、氢元素和氧元素,所以X分子中一定有的是氢原子和氮原子,符号分另为:H和N。
(2)①A微粒最外层电子数为7,大于4,在化学反应中容易得到电子达到稳定结构;
②B为10号元素,其原子的最外层子数为8,对应的单质为氖气,化学性质最稳定,故选B;
质子数决定元素种类,属于同一种元素的为:C和E。
③D元素为钠元素,地壳中含量最多的为氧元素,钠元素化合价为+1价,氧元素为-2价,二都组成的化合物的化学式为:Na2O。
16.
(1)
(2)碳原子、氧原子、氮原子
(3)Mg2+
【分析】
根据题目信息结合微观示意图排除未反应的分子的干扰可写出反应的方程式为2CO+2NON2+2CO2
(1)
由化学方程式可知,A图中还需要补充一个一氧化碳分子;故填: ;
(2)
原子是化学变化中的最小粒子,所以此变化中未发生改变的微观粒子是碳原子、氮原子和氧原子;
(3)
在化合物中,氧元素显-2价,已知X粒子与氧离子能形成XY型化合物,且X元素和比氧元素多一个周期,则X元素显+2价,氧元素位于第二周期,所以X位于第三周期,所以X是镁元素,X粒子是镁离子,其离子符号为Mg2+。答案第1页,共2页
答案第1页,共2页
练习
一、单选题,共12小题
1.在反应A+B→C+D中,若15gA与10gB完全反应没有剩余,则生成的C和D的质量总和为
A.15g B.10g C.25 g D.5g
2.举重运动员举重前常用白色的“镁粉”搓手,它质轻、吸水性好,可作防滑剂。“镁粉”的有效成分是碱式碳酸镁(Mg(OH)(CO3)4),其在加热条件下会发生分解,不可能得到的生成物是
A.CO2 B.MgO C.MgCl2 D.O2
3.下列叙述完全符合质量守恒定律的是
A.水结成冰前后,质量保持不变
B.50mL水和50 mL乙醇混合后总体积小于100 mL
C.在100g30%过氧化氢溶液中,含有30g过氧化氢和70g水
D.1.2g碳与3.2g氧气恰好完全反应可生成4.4g二氧化碳
4.在化学反应前后,一定不发生改变的是
A.分子的种类 B.原子的种类 C.分子的质量 D.物质的种类
5.下列说法错误的是
A.原子核一般由质子、中子构成
B.花香四溢主要是因为分子之间有间隔
C.保持水化学性质的最小微粒是水分子
D.化学反应前后原子的种类不会改变
6.氯化钠是重要的化工原料,是氯碱工业的基础。电解饱和食盐水一定不能得到的物质是
A.H2 B.Cl2 C.Na2CO3 D.NaOH
7.推理是学习化学常用的方法,下列推理正确的是
A.单质由同种元素组成,则只含有一种元素的物质一定是单质
B.化学变化中常伴随发光放热的现象所以有发光放热现象产生时一定发生了化学变化
C.同种元素的质子数相同,则质子数相同的粒子一定属于同种元素
D.蜡烛燃烧生成二氧化碳和水,所以蜡烛组成中一定有碳元素和氢元素
8.化学革命是发生在十八世纪末英国和法国的一场深刻的化学学科的变革。英国物理学家、化学家波义耳和法国化学家拉瓦锡曾做过貌似相同的两个实验(见图)。关于这两个实验的说法正确的是
A.两个实验都可用于测定空气中氧气的含量
B.波义耳的实验比拉瓦锡的更简捷准确
C.波义耳的实验中,金属加热后质量增加,该现象不能用质量守恒定律解释
D.拉瓦锡的实验中,玻璃钟罩内液面逐渐上升,达到一定高度后不再变化
9.某化合物1.6g 在O2中完全燃烧,生成4.4g CO2和3.6g H2O,则该化合物中
A.含C、H、O三种元素 B.一定含C、H元素,可能含氧元素
C.只含C、H两种元素 D.该化合物中氢元素的质量分数为20%
10.向一密闭容器中加入甲、乙、丙、丁4种物质,在一定条件下发生化学反应,测得有关数据如图,下列说法不正确的是
A.a的数值是4 B.乙和丙的质量变化比为5:3
C.该反应是化合反应 D.丁可能是该反应的催化剂
11.宏观辨识与微观探析是化学学习的核心素养。如图所示是某反应的微观示意图,则下列有关说法正确的是
A.该反应属于化合反应
B.该反应中物质的总质量发生改变
C.该反应可以看作是2种单质参加反应生成了1种单质和1种化合物
D.该反应中分子、原子数目都没有发生改变
12.如图是某个化学反应的微观模拟示意图,从图中不能获得的信息是
A.该反应前后一共涉及3种分子
B.该反应前后各种原子的种类没有变化
C.该反应的生成物都是化合物
D.该反应属于分解反应
二、非选择题,共4小题
13.下图是水电解的微观模拟过程。请回答下列问题:
(1)将B中相关粒子的图形补充完整_______,使之符合质量守恒定律。
(2)解释由A→B变化的微观实质是___________。
(3)画出与1个氧分子质子数相同的离子结构示意图__________。
(4)由A→C过程是分解反应,你判断的微观依据是________。
14.将25g氯酸钾和1g二氧化锰的混合物加热至完全分解,得到残余固体质量为16.4g,则产生氧气____g。
15.“见著知微,见微知著”是化学思维方法
(1)从宏观知微观
①50mL水与50mL乙醇混合后,溶液体积小于100mL,微观解释为___________。
②气体X在氧气中燃烧生成氮气和水,X分子中一定含有的原子是______和______(填符号)。
(2)从微观知宏观
①微粒A最外层电子数是___________,在化学反应中容易___________(填“得”或“失”)电子;
②微粒A、B、C、D、E中,对应单质化学性质最稳定的是___________(填编号,下同),属于同一种元素的是___________和___________。
③D元素与地壳中含量最多元素组成化合物的化学式___________ 。
16.下图是汽车尾气中一氧化碳和一氧化氮在催化剂催化作用下发生化学反应的微观示意图。请根据此图回答下列问题:
(1)在A图中将相关粒于图形补充完整:
(2)此变化中未发生改变的微观粒子有:______(填粒子符号)。
(3)已知X粒子与氧离子能形成XY型化合物,且X元素比氧元多一个周期,请写出X粒子的离子符号______。
试卷第1页,共3页
试卷第1页,共3页
参考答案
1.C
【详解】
据质量守恒定律,在化学反应中,参加反应的各物质的质量总和等于反应后生成各物质的质量总和,所以生成C和D的质量总和为15g+10g=25g;
故选:C。
2.C
【详解】
根据质量守恒定律,化学反应前后元素的种类不变,碱式碳酸镁【Mg(OH)(CO3)4】中不含氯元素,故不可能生成MgCl2,故选C。
【点睛】
3.D
【详解】
A、水结成冰前后,质量保持不变,为水的三态变化,为物理变化,不能用质量守恒定律解释;
B、50mL水和50mL乙醇混合后总体积小于100mL,无新物质生成,为物理变化,不能用质量守恒定律解释;
C、在100g过氧化氢溶液中,含有30g过氧化氢和70g水,无新物质生成,不适用质量守恒定律;
D、1.2g碳与3.2g氧气恰好完全反应可生成4.4g二氧化碳,生成物质量=反应物质量之和,符合质量守恒定律。故选D。
【点睛】
质量守恒定律只能解释化学变化,而A、B、C三项中都没有发生化学变化,只是发生了物理变化,因此。质量守恒定律只适合于任何的化学变化。
4.B
【详解】
A、化学变化过程是分子破裂成原子,原子重新组合成新分子的过程,所以化学反应前后分子的种类一定改变,选项不符合题意;
B、化学变化过程是分子破裂成原子,原子重新组合成新分子的过程,所以化学反应前后原子的种类不变,选项符合题意;
C、化学变化过程是分子破裂成原子,原子重新组合成新分子的过程,所以分子的质量一定改变,选项不符合题意;
D、化学反应中有新物质生成,化学反应前后物质的种类一定改变,选项不符合题意。
故选B。
5.B
【详解】
A、原子一般是由质子和中子构成的,说法正确;
B、花香四溢主要是因为分子在不断运动,说法错误;
C、分子是保持物质化学性质的最小微粒,水是由水分子构成,所以保持水化学性质的最小微粒是水分子,说法正确;
D、由质量守恒定律可知,化学反应前后原子的种类不会改变,说法正确。
故选:B。
6.C
【详解】
方法一:电解饱和食盐水的化学方程式:2NaCl+2H2O Cl2↑+H2↑+2NaOH ,电解饱和食盐水可以得到的物质是:Cl2、H2、NaOH,故答案选择C。
方法二:根据质量守恒定律,饱和食盐水中无碳元素,故生成物不可能有碳元素,故答案选择C。
7.D
【详解】
A、由同种元素组成的物质不一定是单质,如氧气和臭氧的混合物,选项A错误;
B、化学变化中常伴随发光放热的现象,但有发光放热现象产生时不一定发生了化学变化,如通电的电灯,不属于化学变化,选项B错误;
C、同种元素的原子质子数相同,但是质子数相同的微粒不一定属于同种元素,选项C错误;
D、蜡烛燃烧生成二氧化碳和水,根据质量守恒定律可知,化学反应前后元素的种类不变,所以蜡烛组成中一定有碳元素和氢元素,可能含有氧元素,选项D正确;
故选:D。
8.D
【详解】
A、波义耳的实验中装置不是密封的,无法测定空气中氧气的含量,不正确;
B、波义耳的实验中装置不是密封的,无法测定空气中氧气的含量,波义耳的实验不如拉瓦锡的准确,不正确;
C、波义耳的实验中,金属加热后质量增加,属于化学变化,该现象能用质量守恒定律解释,不正确;
D、拉瓦锡的实验中,氧气被消耗,玻璃钟罩内液面逐渐上升,达到一定高度后不再变化,是因为氧气完全反应后反应停止,正确。
故选D。
9.C
【分析】
由题可知:某化合物在氧气中燃烧生成二氧化碳和水,根据质量守恒定律可知,化合物中一定含有碳元素和氢元素,且含有的碳元素的质量等于二氧化碳中碳元素的质量: ;含有的氢元素的质量等于水中氢元素的质量: ;所以化合物中碳氢元素的质量和为1.2g+0.4g=1.6g,可知化合物中不含有氧元素。
【详解】
A、由上述分析可知,化合物中一定含有碳元素、氢元素,不含有氧元素,选项A错误;
B、由上述分析可知,化合物中一定含有碳元素、氢元素,不含有氧元素,选项B错误;
C、由上述分析可知,化合物中一定含有碳元素、氢元素,不含有氧元素,选项C正确;
D、该化合物中氢元素的质量分数为,选项D错误;
故选:C
10.B
【详解】
A、根据质量守恒定律,化学反应前后,物质的总质量不变,故30+10+5+5=26+a+15+5,a=4,不符合题意;
B、乙和丙的质量变化比为:(10-4):(15-5)=3:5,符合题意;
C、反应后,甲的质量减小,甲是反应物,乙的质量减小,乙是反应物,丙的质量增加,丙是生成物,丁的质量不变,丁可能是催化剂,也可能是不参与反应的杂质,甲、乙是反应物,丙是生成物,该反应符合“多变一”的特点,属于化合反应,不符合题意;
D、由C的分析可知,丁可能是该反应的催化剂,不符合题意。
故选B。
11.A
【详解】
A、分析微观示意图可知,该反应是由两种单质反应生成一种化合物,故该反应属于化合反应,此选项表述正确;
B、化学反应是分子分成原子,原子又重新组成新的分子的过程,故化学反应前后物质的总质量不变,此选项表述不正确;
C、分析微观示意图可知,该反应是由两种单质参加反应生成了一种化合物,并没有生成新的单质,此选项表述不正确;
D、分析微观示意图可知,该反应的反应物均是由两个原子构成一个分子,而生成物则是由3个原子构成一个分子,故反应前后原子的数目不变,但分子的数目发生了改变,此选项表述不正确。
故选A。
12.C
【详解】
A、反应物中含一种分子,生成物中含两种分子,故该反应前后一共涉及3中分子,此选项表述正确,不符合题意;
B、化学反应前后原子的种类均不发生变化,此选项表述正确,不符合题意;
C、通过示意图可知,反应物属于化合物,生成物中的两种物质都属于单质,此选项表述不正确,符合题意;
D、通过示意图可知,该反应是一种化合物反应后生成两种单质,故该反应属于分解反应,此选项表述正确,不符合题意。
故选C。
【点睛】
13.
(1) ( 补1个氧原子和2个氢原子)
(2)在通电的条件下,水分子分解成氢原子和氧原子
(3)
(4)水分子一种分子反应生成氧分子和氢分子,两种分子(一种分子生成两种分子或水分子生成氢分子和氧分子)
【分析】
(1)
反应前后原子的种类、数目不变,所以B中应补充1个氧原子和2个氢原子,图片为 。
(2)
A到B的过程是水分子拆分成氢氧原子的过程,微观实质是在通电的条件下,水分子分解成氢原子和氧原子。
(3)
1个氧分子含有2个氧原子,1个氧原子有8个质子,所以2个氧原子有16个质子。质子数=原子序数,16号元素是硫元素,硫离子结构示意图为 。
(4)
A→C过程中,水分子一种分子反应生成氧分子和氢分子,两种分子,符合一变多的特点是分解反应。
14.9.6
【详解】
氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,由质量守恒定律,固体混合物减少的质量即为生成氧气的质量;则将25g氯酸钾和1g二氧化锰的混合物加热一段时间后,得到残余固体质量为16.4g,则产生氧气的质量为25g + 1g - 16.4g = 9.6g,故填:9.6g。
15.
(1) 分子间存在间隙 H N
(2) 7 得到 B
C E
Na2O
【详解】
(1)①由于分子间存在间隙,不同种分子彼此进入对方的间隙,使水和乙醇混合后总体积小于二者的体积和;
②化学反应前后元素种类和原子种类都不变,反应后有氮气和水生成,反应前应该存在氮元素、氢元素和氧元素,所以X分子中一定有的是氢原子和氮原子,符号分另为:H和N。
(2)①A微粒最外层电子数为7,大于4,在化学反应中容易得到电子达到稳定结构;
②B为10号元素,其原子的最外层子数为8,对应的单质为氖气,化学性质最稳定,故选B;
质子数决定元素种类,属于同一种元素的为:C和E。
③D元素为钠元素,地壳中含量最多的为氧元素,钠元素化合价为+1价,氧元素为-2价,二都组成的化合物的化学式为:Na2O。
16.
(1)
(2)碳原子、氧原子、氮原子
(3)Mg2+
【分析】
根据题目信息结合微观示意图排除未反应的分子的干扰可写出反应的方程式为2CO+2NON2+2CO2
(1)
由化学方程式可知,A图中还需要补充一个一氧化碳分子;故填: ;
(2)
原子是化学变化中的最小粒子,所以此变化中未发生改变的微观粒子是碳原子、氮原子和氧原子;
(3)
在化合物中,氧元素显-2价,已知X粒子与氧离子能形成XY型化合物,且X元素和比氧元素多一个周期,则X元素显+2价,氧元素位于第二周期,所以X位于第三周期,所以X是镁元素,X粒子是镁离子,其离子符号为Mg2+。答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
