第四章生命之源---水复习与检测同步练习—2021-2022学年九年级化学科粤版(2012)上册(无答案)
文档属性
| 名称 | 第四章生命之源---水复习与检测同步练习—2021-2022学年九年级化学科粤版(2012)上册(无答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 193.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-14 00:00:00 | ||
图片预览


文档简介
第四章生命之源---水复习与检测同步练习能力提升
一、单选题,共11小题
1.推动绿色发展,促进人与自然和谐共生。下列做法合理的是
A.城市生活污水与雨水管网分离 B.河南地区水资源充足,可以不用节约用水
C.农业种植禁止使用农药、化肥,防止水体污染 D.将化工厂废水送入自来水厂净化
2.天然水经一系列操作成为家庭用水的过程中,对水的净化程度最高的操作是
A.吸附 B.过滤 C.沉淀 D.蒸馏
3.一定条件下,在一个密闭容器中发生某反应,测得反应过程中物质的质量如下图所示,下列判断错误的是
A.第二次测定时Y已完全反应 B.若X为氧气,则Y发生氧化反应
C.该反应类型为化合反应 D.该反应中,发生变化的Z与Q质量之比为11:9
4.蜡烛在空气中燃烧,生成二氧化碳和水,可推断蜡烛中一定含有的元素为
A.碳、氢、氧 B.碳、氢 C.碳、氧 D.氢、氧
5.下列说法不能用质量守恒定律解释的是
A.镁带在空气中燃烧生成物的质量比镁带大
B.煤炭在空气中燃烧质量减轻
C.同温同压下,1L氢气与1L氯气在点燃的条件下完全反应生成2L氯化氢气体
D.完全电解20g水得到的氢气和氧气的质量之和仍然是20g
6.下列关于水的天然循环说法正确的是
①水在天然循环过程中实现了水的自身净化
②水的天然循环过程中水分子的大小、间隔和运动速率都发生了改变
③太阳为水的天然循环提供了能量
④水的天然循环完成了水资源的重新分配
⑤水在天然循环中发生了化学变化
A.①③④ B.①②③④ C.①④⑤ D.①②③④⑤
7.甲烷在空气中完全燃烧的微观示意图如下图所示。以下说法错误的是
A.该反应过程中出现了两种氧化物
B.生成物水中氢元素与氧元素的质量比为2:1
C.一个甲烷分子由一个碳原子和四个氢原子构成
D.由微观示意图可知,该反应前、后原子种类不变
8.归纳法是学习化学的重要方法之一,下列图示表述正确的是
A.净化水的方法 B.构成物质的微粒
C.铁元素的质量分数 D.氯元素的化合价
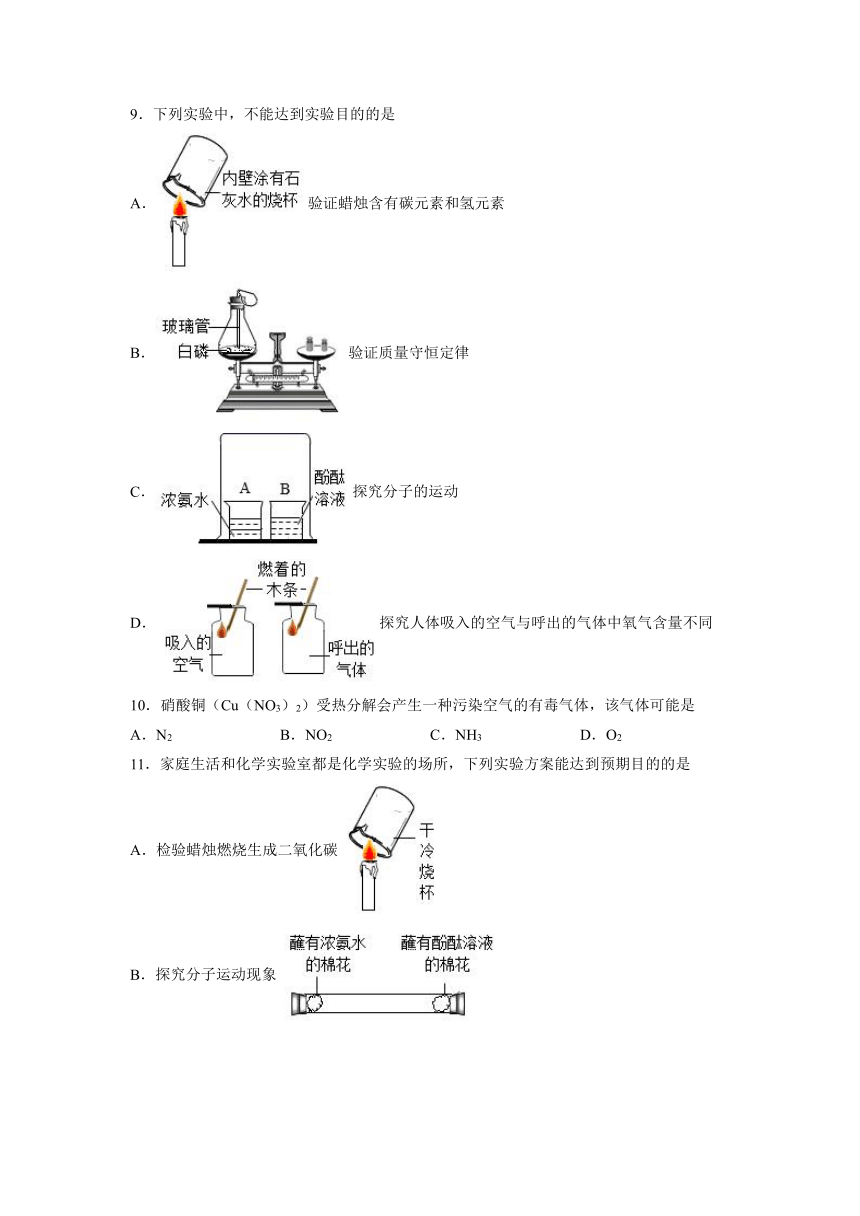
9.下列实验中,不能达到实验目的的是
A.验证蜡烛含有碳元素和氢元素
B.验证质量守恒定律
C.探究分子的运动
D.探究人体吸入的空气与呼出的气体中氧气含量不同
10.硝酸铜(Cu(NO3)2)受热分解会产生一种污染空气的有毒气体,该气体可能是
A.N2 B.NO2 C.NH3 D.O2
11.家庭生活和化学实验室都是化学实验的场所,下列实验方案能达到预期目的的是
A.检验蜡烛燃烧生成二氧化碳
B.探究分子运动现象
C.降低自来水的硬度
D.探究温度对分子运动速率的影响
二、非选择题,共5小题
12.依据所学知识回答问题
(1)如图是“电解水实验”的装置图,b试管内收集的气体是_______,检验该气体的方法是___________。
(2)实验前在水中加入少量硫酸钠的目的是___________。
13.人类的日常生活、工农业生产都与化学密不可分。请回答:
(1)饮用硬度过大的水不利于健康,生活中常用___________方法来降低水的硬度。
(2)按物质组成划分,海水、河水、湖水、井水和矿泉水都属于___________填(“纯净物”或“混合物”);有些村庄打深井取用地下水,检验地下水是硬水还是软水可选用的物质是___________。
14.过滤是分离液体和固体的操作,该实验中需要用到玻璃棒,其作用是________,如果过滤后滤液浑浊,其原因是__________(任意写一条)。
15.学习化学使我们从五彩缤纷的宏观世界步入了充满神奇色彩的微观世界。
(1)请沿用科学家认识事物的方式认识“空气”,根据图1回答:
①从分类角度:空气属于_______(填“混合物”或“纯净物”)。
②从微观角度:用“ ”表示氮原子,用“”表示氧原子。
a.用“”可表示的微粒是_______(填名称)。
b.同温同压下,气体的体积比等于分子数目比。若空气中其他成分忽略不计,图1中可表示空气微观模型的是_______(填字母标号)。
(2)请根据图2写出反应的化学方程式:_______。
16.电解水实验的示意图如下图所示,请完成下列问题:
(1)电解水的符号表达式是___________,该反应属于___________(填“化合反应”“分解反应”)。
(2)与a管中电极相连的是电源的___________(选填“正”或“负”)极,a、b两管中产生气体体积比为___________,a管中产生的气体是___________(填化学式,下同)。b管中产生的气体是___________,它能___________。
(3)下列说法正确的是___________(填字母)。
A.水是由氢气和氧气组成的 B.水是由氢、氧两种元素组成的
C.水是由氢原子和氧原子构成的 D.每个水分子是由2个氢原子和1个氧原子构成的
(4)保持水的化学性质的最小粒子是___________。
一、单选题,共11小题
1.推动绿色发展,促进人与自然和谐共生。下列做法合理的是
A.城市生活污水与雨水管网分离 B.河南地区水资源充足,可以不用节约用水
C.农业种植禁止使用农药、化肥,防止水体污染 D.将化工厂废水送入自来水厂净化
2.天然水经一系列操作成为家庭用水的过程中,对水的净化程度最高的操作是
A.吸附 B.过滤 C.沉淀 D.蒸馏
3.一定条件下,在一个密闭容器中发生某反应,测得反应过程中物质的质量如下图所示,下列判断错误的是
A.第二次测定时Y已完全反应 B.若X为氧气,则Y发生氧化反应
C.该反应类型为化合反应 D.该反应中,发生变化的Z与Q质量之比为11:9
4.蜡烛在空气中燃烧,生成二氧化碳和水,可推断蜡烛中一定含有的元素为
A.碳、氢、氧 B.碳、氢 C.碳、氧 D.氢、氧
5.下列说法不能用质量守恒定律解释的是
A.镁带在空气中燃烧生成物的质量比镁带大
B.煤炭在空气中燃烧质量减轻
C.同温同压下,1L氢气与1L氯气在点燃的条件下完全反应生成2L氯化氢气体
D.完全电解20g水得到的氢气和氧气的质量之和仍然是20g
6.下列关于水的天然循环说法正确的是
①水在天然循环过程中实现了水的自身净化
②水的天然循环过程中水分子的大小、间隔和运动速率都发生了改变
③太阳为水的天然循环提供了能量
④水的天然循环完成了水资源的重新分配
⑤水在天然循环中发生了化学变化
A.①③④ B.①②③④ C.①④⑤ D.①②③④⑤
7.甲烷在空气中完全燃烧的微观示意图如下图所示。以下说法错误的是
A.该反应过程中出现了两种氧化物
B.生成物水中氢元素与氧元素的质量比为2:1
C.一个甲烷分子由一个碳原子和四个氢原子构成
D.由微观示意图可知,该反应前、后原子种类不变
8.归纳法是学习化学的重要方法之一,下列图示表述正确的是
A.净化水的方法 B.构成物质的微粒
C.铁元素的质量分数 D.氯元素的化合价
9.下列实验中,不能达到实验目的的是
A.验证蜡烛含有碳元素和氢元素
B.验证质量守恒定律
C.探究分子的运动
D.探究人体吸入的空气与呼出的气体中氧气含量不同
10.硝酸铜(Cu(NO3)2)受热分解会产生一种污染空气的有毒气体,该气体可能是
A.N2 B.NO2 C.NH3 D.O2
11.家庭生活和化学实验室都是化学实验的场所,下列实验方案能达到预期目的的是
A.检验蜡烛燃烧生成二氧化碳
B.探究分子运动现象
C.降低自来水的硬度
D.探究温度对分子运动速率的影响
二、非选择题,共5小题
12.依据所学知识回答问题
(1)如图是“电解水实验”的装置图,b试管内收集的气体是_______,检验该气体的方法是___________。
(2)实验前在水中加入少量硫酸钠的目的是___________。
13.人类的日常生活、工农业生产都与化学密不可分。请回答:
(1)饮用硬度过大的水不利于健康,生活中常用___________方法来降低水的硬度。
(2)按物质组成划分,海水、河水、湖水、井水和矿泉水都属于___________填(“纯净物”或“混合物”);有些村庄打深井取用地下水,检验地下水是硬水还是软水可选用的物质是___________。
14.过滤是分离液体和固体的操作,该实验中需要用到玻璃棒,其作用是________,如果过滤后滤液浑浊,其原因是__________(任意写一条)。
15.学习化学使我们从五彩缤纷的宏观世界步入了充满神奇色彩的微观世界。
(1)请沿用科学家认识事物的方式认识“空气”,根据图1回答:
①从分类角度:空气属于_______(填“混合物”或“纯净物”)。
②从微观角度:用“ ”表示氮原子,用“”表示氧原子。
a.用“”可表示的微粒是_______(填名称)。
b.同温同压下,气体的体积比等于分子数目比。若空气中其他成分忽略不计,图1中可表示空气微观模型的是_______(填字母标号)。
(2)请根据图2写出反应的化学方程式:_______。
16.电解水实验的示意图如下图所示,请完成下列问题:
(1)电解水的符号表达式是___________,该反应属于___________(填“化合反应”“分解反应”)。
(2)与a管中电极相连的是电源的___________(选填“正”或“负”)极,a、b两管中产生气体体积比为___________,a管中产生的气体是___________(填化学式,下同)。b管中产生的气体是___________,它能___________。
(3)下列说法正确的是___________(填字母)。
A.水是由氢气和氧气组成的 B.水是由氢、氧两种元素组成的
C.水是由氢原子和氧原子构成的 D.每个水分子是由2个氢原子和1个氧原子构成的
(4)保持水的化学性质的最小粒子是___________。
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
