6.1 金刚石、石墨和C60 同步练习--2021-2022学年九年级化学人教版上册(word版 含答案)
文档属性
| 名称 | 6.1 金刚石、石墨和C60 同步练习--2021-2022学年九年级化学人教版上册(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 155.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-15 00:00:00 | ||
图片预览


文档简介
2021——2022学年度人教版九年级化学上册 第六单元碳和碳的化合物 课题1 金刚石、石墨和C60 同步练习
一、选择题
1.下列物质的用途及其依据的性质对应正确的是
A.金刚石用于制造钻石——金刚石硬度大
B.石墨用作电池的电极——石墨是一种黑色固体
C.氮气作粮食瓜果的保护气——氮气化学性质稳定
D.氧气可用于医疗急救——氧气具有助燃性
2.下列实验现象的描述中,正确的是( )
A.铁丝在空气中燃烧,火星四射,生成黑色固体 B.红磷在空气中燃烧产生大量的白雾
C.硫在氧气中燃烧,发出淡蓝色火焰 D.高温下木炭还原氧化铜时,黑色粉末逐渐变成红色
3.下图是金刚石、石墨、C60、碳纳米管结构示意图。下列关于这四种物质的说法中不正确的是
A.都是由碳元素组成的单质 B.碳原子的排列方式不同
C.完全燃烧后的产物都是CO2 D.都是由碳原子构成的,具有相同的性质
4.石墨烯是由碳元素组成的、性能非常优良的纳米材料,具有超强导电、导热的性能。关于石墨烯的认识错误的是
A.完全燃烧生成二氧化碳 B.可作散热材料
C.可用作新型电池材料 D.是一种化合物
5.下列说法正确的是
A.H2S、H2、H2O、H2SO4四种物质中都含有两个氢原子
B.我们使用的铅笔笔芯是金属铅制成的
C.化学性质相似的两种元素其原子的最外层电子数一定相同
D.KMnO4和K2MnO4中含有不相同的原子团
6.在反应中,体现出具有还原性的物质是
A.C B.CuO C.Cu D.CO2
7.欲除去氧化铜粉末中混有的少量木炭粉,可采用的方法是
A.将混合物隔绝空气加强热 B.采用先加水溶解然后过滤的方法
C.将H2不断通过灼热的混合物 D.将O2不断通过灼热的混合物
8.关于碳的化学性质不正确的是( )
A.温度越高,碳的活动性越强 B.高温时碳能与二氧化碳反应
C.碳在氧气中充分燃烧是放热反应,而不充分燃烧时是吸热反应 D.碳在常温下能长时间保存不变质
9.“中国高铁,世界第一”,高铁列车车体材料使用了含镍不锈钢,工业上火法炼镍的原理是。下列相关说法错误的是
A.该反应中C发生还原反应 B.碳在该反应中表现出还原性
C.含镍不锈钢中还含有铁和碳 D.气体产物中可能有CO
10.“碳海绵”具备高弹性和疏松多孔的结构,主要成分是石墨烯和碳纳米管(两者都是碳单质)。关于“碳海绵”的说法中不正确的是
A.属于混合物,充分燃烧生成CO2 B.具有吸附性,属于物理性质
C.在一定条件下可以还原氧化铜 D.与石墨、金刚石互称为同素异形体
11.科学家发现由C60制取的化合物M具有抑制艾滋病毒的作用,下列叙述错误的是 ( )
A.由C60制取M的过程中发生了化学变化
B.化合物M中含有碳元素
C.C60中的碳原子比石墨中的大
D.C60在空气中燃烧生成二氧化碳的反应是化合反应
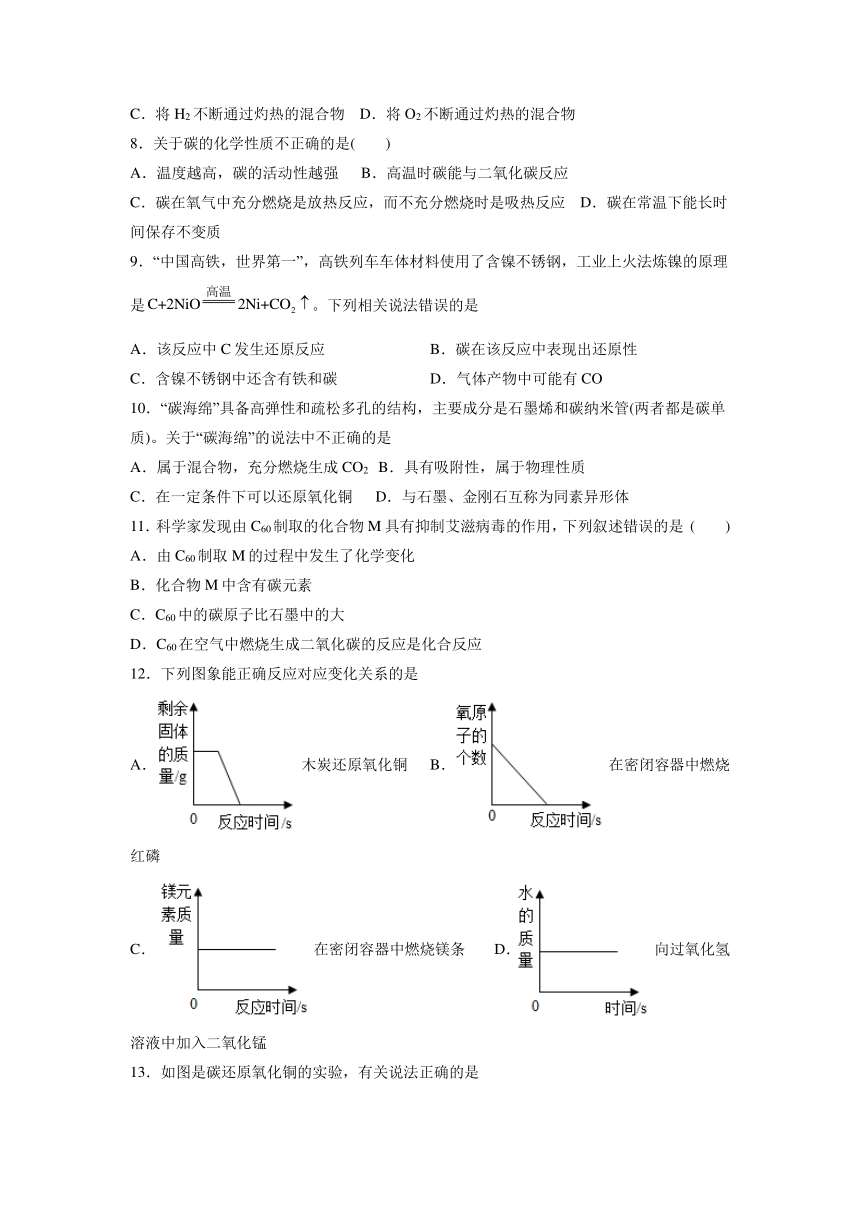
12.下列图象能正确反应对应变化关系的是
A.木炭还原氧化铜 B.在密闭容器中燃烧红磷
C.在密闭容器中燃烧镁条 D.向过氧化氢溶液中加入二氧化锰
13.如图是碳还原氧化铜的实验,有关说法正确的是
A.该实验体现了碳的氧化性
B.反应开始的标志是:导管口有气泡产生
C.该反应的实验现象是黑色固体变红色,澄清石灰水变浑浊
D.实验结束时应先熄灭酒精灯,待试管冷却后再将导管从澄清石灰水中移出
14.如图表示一定量的木炭和氧化铁固体混合物受热过程中,某变量y随加热时间的变化趋势,其中纵坐标y表示
A.固体的质量 B.固体中氧化铁的质量 C.固体中铁元素的质量分数 D.二氧化碳的质量
二、填空题
15.化学来源于生活,服务于生活。请你用学过的化学知识回答下列问题。
(1)净化水的操作有:①静置、②过滤、③蒸馏,其中单一操作净化程度最高的是__(填序号)。
(2)用活性炭除去冰箱里的异味,是利用其_______性。
(3)6000L氧气在加压的情况下可装入容积为40L的钢瓶中,从分子的角度解释其原因_____。
(4)炒菜用到的食盐的主要成分NaCl是由_______(填“离子”、“分子”或“原子”)构成的。
16.向盛有红棕色二氧化氮气体的集气瓶中投入几块烘烤过的木炭,发现红棕色消失,说明木炭具有________作用。用墨汁书写或绘画的字画能从古代保存至今而不褪色,是因为常温下碳的化学性质________。石墨和C60的物理性质存在明显差异的原因是________。
17.Cu可以形成化合价为+2 和+1 的化合物。其中+1 价化合物称为亚铜化合物。
(1)写出氧化亚铜的化学式________。
(2)高温时,氧化铜可被木炭还原为铜,反应的化学方程式是______。
(3)氧化亚铜是一种红色粉末。加热时,氧化亚铜能与氧气发生化合反应,反应的化学方程式是___________。
18.金刚石、石墨都是由碳元素组成的单质,但是由于他们的______不同,因此它们的______存在差异
19.中国科学技术大学的钱逸泰教授等以CCl4和金属钠为原料,在700℃下隔绝空气反应得到了纳米级金刚石粉末和化合物X。该成果被科学家们喻为“稻草变黄金”。回答下列问题:
(1)CCl4中碳元素的化合价为___________;化合物X的化学式是___________。
(2)该反应需要隔绝空气进行的原因是___________。
20.写出下列反应的化学方程式:
(1)硫在氧气中燃烧_________。
(2)碳在高温下还原氧化铜_________。
(3)实验室用过氧化氢溶液和二氧化锰制氧气_________。
三、简答题
21.请从微观角度解释下列问题:
(1)吸烟者常给周围的人带来被动吸烟的危害.
(2)金刚石和石墨物理性质差异很大.
(3)水通电分解的过程中一定不变的微粒有哪些?
22.用木炭还原氧化铜的实验如图.
(1)酒精灯加灯罩的目的 ______ ;
(2)加热一段时间后,可观察到的现象________________、_________________________
(3)请你写出①②试管中发生反应的化学方程式:
① _________________________________ ② ________________________
23.活性炭有良好的吸附性能,可用于防毒面具材料的制备。为研究活性炭在不同条件下对氯气(Cl2)的吸附性能,(吸附量越大,吸附性能越好),科学工作者们做了系列实验得到如下图所示的结果。分析图示可得到的结论是________。
24.除去CO2中混有的少量CO,可将混合气体通过______,反应的化学方程式是______。
四、综合应用题
25.依据文意内容,回答下列问题。
多孔活性炭具有较好的吸附性能,是一种优良的催化剂载体材料,广泛应用于各行各业,其生产一直以煤、竹子、木材等宝贵资源为原料。随着可持续发展理念的不断深入,越来越多的研究者尝试以清洁廉价的资源作为原料(如白酒糟),制备多孔活性炭。
白酒糟是酿酒过程的副产物,富含纤维素((C6H10O5)n)。以白酒糟为原料生产多孔活性炭的过程主要包括干燥、炭化、活化三步。炭化过程是将干燥的白酒糟在充满氮气的环境中,加热至650℃,将其中的纤维素转化为炭质原料(主要成为单质碳)。活化过程是以水蒸气或CO2为活化剂,在一定条件下使其在炭质原料内部发生反应,生成气体,形成孔隙结构,制备多孔活性炭。
也有研究者在其他条件相同的情况下,通过实验测定所得多孔活性炭对碘的吸附值与水蒸气、CO2用量的关系分别如图1、2所示。
尽管以白酒糟为原料,制备多孔活性炭材料的技术仍有许多问题有待于进一步探索、解决,但已有研究为富含纤维素工业残渣的利用提供了可能途径。
(1)以白酒糟为原料制备多孔活性炭的优点是_________。
(2)纤维素中碳、氢元素质量比为_________。
(3)炭化过程中需要在充满氮气的环境中,此处氮气的作用是_______。
(4)分析图1得出的结论是_______。
(5)由图1、图2可知,为了达到最佳吸附效果,应选用的活化剂是______。(填“水蒸气”或“二氧化碳”)
【参考答案】
1.C 2.D 3.D 4.D 5.D 6.A 7.D 8.C 9.A 10.D 11.C 12.C 13.C 14.C
15.(1)③
(2)吸附
(3)分子之间存在间隔
(4)离子
16.吸附 不活泼 碳原子的排列方式不同
17.(1)Cu2O
(2)
(3)
18.原子排列方式 物理性质
19.+4 NaCl 防止反应生成的金刚石在高温下和氧气发生反应
20.
21.(1)分子是在不断的运动的;(2)碳原子的排列方式不同;(3)氢原子和氧原子.
22.集中火焰,提高温度 固体黑色变红色 澄清石灰水变 浑浊
23.在压强一定的条件下,温度越低,活性炭对氯气的吸附性能越好(在温度一定的条件下,压强越大,活性炭对氯气的吸附性能越好)(活性炭对氯气的吸附性能受温度和压强的影响)(在实验研究的范围内,压强越大,温度越低,活性炭对氯气的吸附性能越好)
24.灼热的氧化铜 CuO+COCu+CO2
25.(1)白酒糟是清洁廉价的资源,能够变废为宝
(2)36:5
(3)作保护气,防止碳与氧气接触
(4)不是水蒸气用量越多,制得的多孔活性炭的吸附性能越好(合理即可)
(5)水蒸气
一、选择题
1.下列物质的用途及其依据的性质对应正确的是
A.金刚石用于制造钻石——金刚石硬度大
B.石墨用作电池的电极——石墨是一种黑色固体
C.氮气作粮食瓜果的保护气——氮气化学性质稳定
D.氧气可用于医疗急救——氧气具有助燃性
2.下列实验现象的描述中,正确的是( )
A.铁丝在空气中燃烧,火星四射,生成黑色固体 B.红磷在空气中燃烧产生大量的白雾
C.硫在氧气中燃烧,发出淡蓝色火焰 D.高温下木炭还原氧化铜时,黑色粉末逐渐变成红色
3.下图是金刚石、石墨、C60、碳纳米管结构示意图。下列关于这四种物质的说法中不正确的是
A.都是由碳元素组成的单质 B.碳原子的排列方式不同
C.完全燃烧后的产物都是CO2 D.都是由碳原子构成的,具有相同的性质
4.石墨烯是由碳元素组成的、性能非常优良的纳米材料,具有超强导电、导热的性能。关于石墨烯的认识错误的是
A.完全燃烧生成二氧化碳 B.可作散热材料
C.可用作新型电池材料 D.是一种化合物
5.下列说法正确的是
A.H2S、H2、H2O、H2SO4四种物质中都含有两个氢原子
B.我们使用的铅笔笔芯是金属铅制成的
C.化学性质相似的两种元素其原子的最外层电子数一定相同
D.KMnO4和K2MnO4中含有不相同的原子团
6.在反应中,体现出具有还原性的物质是
A.C B.CuO C.Cu D.CO2
7.欲除去氧化铜粉末中混有的少量木炭粉,可采用的方法是
A.将混合物隔绝空气加强热 B.采用先加水溶解然后过滤的方法
C.将H2不断通过灼热的混合物 D.将O2不断通过灼热的混合物
8.关于碳的化学性质不正确的是( )
A.温度越高,碳的活动性越强 B.高温时碳能与二氧化碳反应
C.碳在氧气中充分燃烧是放热反应,而不充分燃烧时是吸热反应 D.碳在常温下能长时间保存不变质
9.“中国高铁,世界第一”,高铁列车车体材料使用了含镍不锈钢,工业上火法炼镍的原理是。下列相关说法错误的是
A.该反应中C发生还原反应 B.碳在该反应中表现出还原性
C.含镍不锈钢中还含有铁和碳 D.气体产物中可能有CO
10.“碳海绵”具备高弹性和疏松多孔的结构,主要成分是石墨烯和碳纳米管(两者都是碳单质)。关于“碳海绵”的说法中不正确的是
A.属于混合物,充分燃烧生成CO2 B.具有吸附性,属于物理性质
C.在一定条件下可以还原氧化铜 D.与石墨、金刚石互称为同素异形体
11.科学家发现由C60制取的化合物M具有抑制艾滋病毒的作用,下列叙述错误的是 ( )
A.由C60制取M的过程中发生了化学变化
B.化合物M中含有碳元素
C.C60中的碳原子比石墨中的大
D.C60在空气中燃烧生成二氧化碳的反应是化合反应
12.下列图象能正确反应对应变化关系的是
A.木炭还原氧化铜 B.在密闭容器中燃烧红磷
C.在密闭容器中燃烧镁条 D.向过氧化氢溶液中加入二氧化锰
13.如图是碳还原氧化铜的实验,有关说法正确的是
A.该实验体现了碳的氧化性
B.反应开始的标志是:导管口有气泡产生
C.该反应的实验现象是黑色固体变红色,澄清石灰水变浑浊
D.实验结束时应先熄灭酒精灯,待试管冷却后再将导管从澄清石灰水中移出
14.如图表示一定量的木炭和氧化铁固体混合物受热过程中,某变量y随加热时间的变化趋势,其中纵坐标y表示
A.固体的质量 B.固体中氧化铁的质量 C.固体中铁元素的质量分数 D.二氧化碳的质量
二、填空题
15.化学来源于生活,服务于生活。请你用学过的化学知识回答下列问题。
(1)净化水的操作有:①静置、②过滤、③蒸馏,其中单一操作净化程度最高的是__(填序号)。
(2)用活性炭除去冰箱里的异味,是利用其_______性。
(3)6000L氧气在加压的情况下可装入容积为40L的钢瓶中,从分子的角度解释其原因_____。
(4)炒菜用到的食盐的主要成分NaCl是由_______(填“离子”、“分子”或“原子”)构成的。
16.向盛有红棕色二氧化氮气体的集气瓶中投入几块烘烤过的木炭,发现红棕色消失,说明木炭具有________作用。用墨汁书写或绘画的字画能从古代保存至今而不褪色,是因为常温下碳的化学性质________。石墨和C60的物理性质存在明显差异的原因是________。
17.Cu可以形成化合价为+2 和+1 的化合物。其中+1 价化合物称为亚铜化合物。
(1)写出氧化亚铜的化学式________。
(2)高温时,氧化铜可被木炭还原为铜,反应的化学方程式是______。
(3)氧化亚铜是一种红色粉末。加热时,氧化亚铜能与氧气发生化合反应,反应的化学方程式是___________。
18.金刚石、石墨都是由碳元素组成的单质,但是由于他们的______不同,因此它们的______存在差异
19.中国科学技术大学的钱逸泰教授等以CCl4和金属钠为原料,在700℃下隔绝空气反应得到了纳米级金刚石粉末和化合物X。该成果被科学家们喻为“稻草变黄金”。回答下列问题:
(1)CCl4中碳元素的化合价为___________;化合物X的化学式是___________。
(2)该反应需要隔绝空气进行的原因是___________。
20.写出下列反应的化学方程式:
(1)硫在氧气中燃烧_________。
(2)碳在高温下还原氧化铜_________。
(3)实验室用过氧化氢溶液和二氧化锰制氧气_________。
三、简答题
21.请从微观角度解释下列问题:
(1)吸烟者常给周围的人带来被动吸烟的危害.
(2)金刚石和石墨物理性质差异很大.
(3)水通电分解的过程中一定不变的微粒有哪些?
22.用木炭还原氧化铜的实验如图.
(1)酒精灯加灯罩的目的 ______ ;
(2)加热一段时间后,可观察到的现象________________、_________________________
(3)请你写出①②试管中发生反应的化学方程式:
① _________________________________ ② ________________________
23.活性炭有良好的吸附性能,可用于防毒面具材料的制备。为研究活性炭在不同条件下对氯气(Cl2)的吸附性能,(吸附量越大,吸附性能越好),科学工作者们做了系列实验得到如下图所示的结果。分析图示可得到的结论是________。
24.除去CO2中混有的少量CO,可将混合气体通过______,反应的化学方程式是______。
四、综合应用题
25.依据文意内容,回答下列问题。
多孔活性炭具有较好的吸附性能,是一种优良的催化剂载体材料,广泛应用于各行各业,其生产一直以煤、竹子、木材等宝贵资源为原料。随着可持续发展理念的不断深入,越来越多的研究者尝试以清洁廉价的资源作为原料(如白酒糟),制备多孔活性炭。
白酒糟是酿酒过程的副产物,富含纤维素((C6H10O5)n)。以白酒糟为原料生产多孔活性炭的过程主要包括干燥、炭化、活化三步。炭化过程是将干燥的白酒糟在充满氮气的环境中,加热至650℃,将其中的纤维素转化为炭质原料(主要成为单质碳)。活化过程是以水蒸气或CO2为活化剂,在一定条件下使其在炭质原料内部发生反应,生成气体,形成孔隙结构,制备多孔活性炭。
也有研究者在其他条件相同的情况下,通过实验测定所得多孔活性炭对碘的吸附值与水蒸气、CO2用量的关系分别如图1、2所示。
尽管以白酒糟为原料,制备多孔活性炭材料的技术仍有许多问题有待于进一步探索、解决,但已有研究为富含纤维素工业残渣的利用提供了可能途径。
(1)以白酒糟为原料制备多孔活性炭的优点是_________。
(2)纤维素中碳、氢元素质量比为_________。
(3)炭化过程中需要在充满氮气的环境中,此处氮气的作用是_______。
(4)分析图1得出的结论是_______。
(5)由图1、图2可知,为了达到最佳吸附效果,应选用的活化剂是______。(填“水蒸气”或“二氧化碳”)
【参考答案】
1.C 2.D 3.D 4.D 5.D 6.A 7.D 8.C 9.A 10.D 11.C 12.C 13.C 14.C
15.(1)③
(2)吸附
(3)分子之间存在间隔
(4)离子
16.吸附 不活泼 碳原子的排列方式不同
17.(1)Cu2O
(2)
(3)
18.原子排列方式 物理性质
19.+4 NaCl 防止反应生成的金刚石在高温下和氧气发生反应
20.
21.(1)分子是在不断的运动的;(2)碳原子的排列方式不同;(3)氢原子和氧原子.
22.集中火焰,提高温度 固体黑色变红色 澄清石灰水变 浑浊
23.在压强一定的条件下,温度越低,活性炭对氯气的吸附性能越好(在温度一定的条件下,压强越大,活性炭对氯气的吸附性能越好)(活性炭对氯气的吸附性能受温度和压强的影响)(在实验研究的范围内,压强越大,温度越低,活性炭对氯气的吸附性能越好)
24.灼热的氧化铜 CuO+COCu+CO2
25.(1)白酒糟是清洁廉价的资源,能够变废为宝
(2)36:5
(3)作保护气,防止碳与氧气接触
(4)不是水蒸气用量越多,制得的多孔活性炭的吸附性能越好(合理即可)
(5)水蒸气
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
