高中化学人教版(2019)必修第一册3.1铁及其化合物(共21张ppt)
文档属性
| 名称 | 高中化学人教版(2019)必修第一册3.1铁及其化合物(共21张ppt) |  | |
| 格式 | zip | ||
| 文件大小 | 15.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-17 22:22:36 | ||
图片预览








文档简介
(共21张PPT)
金属材料
第一节 铁及其化合物
同学们认不认识图片中的东西?
这种东西叫做“陨铁”
是一种来自外太空的陨石,含有大量的铁单质
早在4000多年前,人类就已经利用陨铁开始制造工具。
早期人类为什么不直接用地球上的铁单质直接创造工具呢?
自然界只存在化合态的铁元素,并没有铁单质。
美丽的张掖七彩丹霞地貌中的红土富含Fe2O3
慢慢的,人类掌握了冶铁技术
出土于甘肃灵台的春秋时期的秦国铜柄铁剑
同学们是否还记得炼铁的化学原理吗?
Fe2O3+3CO=高温=2Fe+3CO2
一、铁的单质
1.物理性质
铁具有良好的延展性和导热性。能够导电,导电性不如铜和铝,能够被磁铁吸引。
2.化学性质
铁的化学性质怎样呢?
一、铁的单质
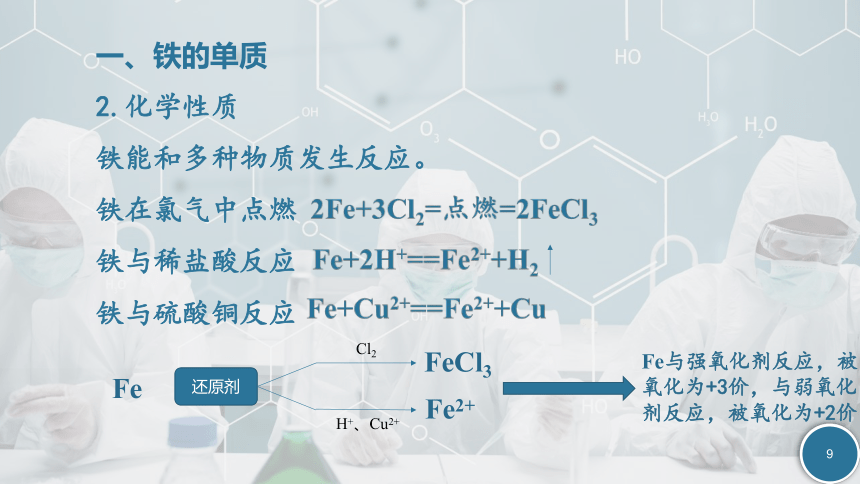
2.化学性质
铁能和多种物质发生反应。
铁在氯气中点燃
铁与稀盐酸反应
铁与硫酸铜反应
Fe
还原剂
Cl2
H+、Cu2+
FeCl3
Fe2+
Fe与强氧化剂反应,被氧化为+3价,与弱氧化剂反应,被氧化为+2价
一、铁的单质
2.化学性质
思考:铁与单质硫反应会产物是什么,写出化学方程式
Fe+S=加热=FeS
一、铁的单质
2.化学性质
活泼金属可以与水反应,那么铁是否能于水反应呢?
生活经验告诉我们,常温下,铁不会和水反应。
钢铁厂提示:
在进行钢水浇铸过程中,模具必须要进行干燥处理,这是为什么呢?
一、铁的单质
2.化学性质
铁与水蒸气在高温时发生反应,生成四氧化三铁和氢气
二、铁的化合物
1.铁的氧化物
铁元素共有3种氧化物,分别是FeO、Fe2O3、Fe3O4。
FeO是一种黑色的粉末,不太稳定
Fe2O3是一种红棕色粉末,俗称铁红,常用作涂料等颜料。
Fe3O4是一种复杂的化合物,也是具有磁性的黑色晶体,俗称磁性氧化物。
二、铁的化合物
1.铁的氧化物
FeO
Fe2O3
Fe3O4
碱性氧化物
+2、+3
FeO·Fe2O3
二、铁的化合物
1.铁的氧化物
1mol铁单质与水蒸气高温下反应转移8/3mol电子
二、铁的化合物
2.铁的氢氧化物
铁有两种氢氧化物,Fe(OH)2、 Fe(OH)3
那么,如何制备这两种氢氧化物呢?
Fe(OH)2 Fe(OH)3
操作 向FeSO4中滴加NaOH溶液 向FeCl3中滴加NaOH溶液
现象
离子方程式
实验结论
Fe(OH)2 Fe(OH)3
颜色
溶解度
与盐酸的离子方程式
稳定性
(2)氢氧化铁和氢氧化亚铁的性质比较
思考与讨论:白色的氢氧化亚铁在制备时很容易会被氧气氧化变为氢氧化铁,那么如何防止这种变质呢?
金属材料
第一节 铁及其化合物
同学们认不认识图片中的东西?
这种东西叫做“陨铁”
是一种来自外太空的陨石,含有大量的铁单质
早在4000多年前,人类就已经利用陨铁开始制造工具。
早期人类为什么不直接用地球上的铁单质直接创造工具呢?
自然界只存在化合态的铁元素,并没有铁单质。
美丽的张掖七彩丹霞地貌中的红土富含Fe2O3
慢慢的,人类掌握了冶铁技术
出土于甘肃灵台的春秋时期的秦国铜柄铁剑
同学们是否还记得炼铁的化学原理吗?
Fe2O3+3CO=高温=2Fe+3CO2
一、铁的单质
1.物理性质
铁具有良好的延展性和导热性。能够导电,导电性不如铜和铝,能够被磁铁吸引。
2.化学性质
铁的化学性质怎样呢?
一、铁的单质
2.化学性质
铁能和多种物质发生反应。
铁在氯气中点燃
铁与稀盐酸反应
铁与硫酸铜反应
Fe
还原剂
Cl2
H+、Cu2+
FeCl3
Fe2+
Fe与强氧化剂反应,被氧化为+3价,与弱氧化剂反应,被氧化为+2价
一、铁的单质
2.化学性质
思考:铁与单质硫反应会产物是什么,写出化学方程式
Fe+S=加热=FeS
一、铁的单质
2.化学性质
活泼金属可以与水反应,那么铁是否能于水反应呢?
生活经验告诉我们,常温下,铁不会和水反应。
钢铁厂提示:
在进行钢水浇铸过程中,模具必须要进行干燥处理,这是为什么呢?
一、铁的单质
2.化学性质
铁与水蒸气在高温时发生反应,生成四氧化三铁和氢气
二、铁的化合物
1.铁的氧化物
铁元素共有3种氧化物,分别是FeO、Fe2O3、Fe3O4。
FeO是一种黑色的粉末,不太稳定
Fe2O3是一种红棕色粉末,俗称铁红,常用作涂料等颜料。
Fe3O4是一种复杂的化合物,也是具有磁性的黑色晶体,俗称磁性氧化物。
二、铁的化合物
1.铁的氧化物
FeO
Fe2O3
Fe3O4
碱性氧化物
+2、+3
FeO·Fe2O3
二、铁的化合物
1.铁的氧化物
1mol铁单质与水蒸气高温下反应转移8/3mol电子
二、铁的化合物
2.铁的氢氧化物
铁有两种氢氧化物,Fe(OH)2、 Fe(OH)3
那么,如何制备这两种氢氧化物呢?
Fe(OH)2 Fe(OH)3
操作 向FeSO4中滴加NaOH溶液 向FeCl3中滴加NaOH溶液
现象
离子方程式
实验结论
Fe(OH)2 Fe(OH)3
颜色
溶解度
与盐酸的离子方程式
稳定性
(2)氢氧化铁和氢氧化亚铁的性质比较
思考与讨论:白色的氢氧化亚铁在制备时很容易会被氧气氧化变为氢氧化铁,那么如何防止这种变质呢?
