5.2如何正确书写化学方程式课后练习--2021-2022学年九年级化学人教版上册(含解析)
文档属性
| 名称 | 5.2如何正确书写化学方程式课后练习--2021-2022学年九年级化学人教版上册(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 164.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-17 00:00:00 | ||
图片预览




文档简介
第五单元化学方程式课题2如何正确书写化学方程式课后练习基础过关九年级化学上册(人教版)
练习
一、单选题,共12小题
1.化学方程式不能提供的信息是
A.通过什么条件反应 B.哪些物质参加反应
C.各物质之间的质量比 D.化学反应速率的快慢
2.下列化学方程式书写正确的是
A.2P+5O2P2O5
B.2KMnO4K2MnO4 + MnO2 + O2
C.2CO + O22CO2
D.CO2+Ca(OH)2=CaCO3+H2O
3.多功能水处理剂高铁酸钾受热会发生分解:,则R是
A.FeO B.Fe2O3 C.Fe D.Fe3O4
4.在化学反应SO2+2X=3S↓+2H2O中,X的化学式为
A.S B.H2 C.HS D.H2S
5.下列化学方程式中,书写正确的是
A.2P+5O2P2O5 B.C+O2CO2
C.2CO+O2=2CO2 D.H2O2H2↑+O2↑
6.MnO2不仅可作催化剂,还可作重要的氧化剂,如用于实验室制取氯气,化学方程式为MnO2+4XMnCl2+2H2O+Cl2↑,则物质X的化学式为
A.ClO2 B.H2O2 C.HClO D.HCl
7.下列化学方程式书写正确的是
A. B.
C. D.
8.已知某反应的化学方程式为:,则X的化学式为
A.SO2 B.SO3 C.H2SO3 D.H2SO4
9.关于反应 2SO2+O22SO3,说法错误的是
A.V2O5在反应前后化学性质不变 B.二氧化硫加氧气反应生成三氧化硫
C.参加反应的 SO2与 O2的质量比为 4:1 D.反应中 SO2 作还原剂,具有还原性
10.四位同学正在讨论某一个化学方程式的意义,他们所描述的化学方程式是
A. B.
C. D.
11.用“”和“”分别代表A2和B2两种物质,二者反应的微观示意图如图。有关说法不正确的是
该反应属于化合反应
B.参加反应的A2与B2的分子个数比为3:1
反应后各元素种类不改变
D.反应后的生成了二种新的分子
二、非选择题,共5小题
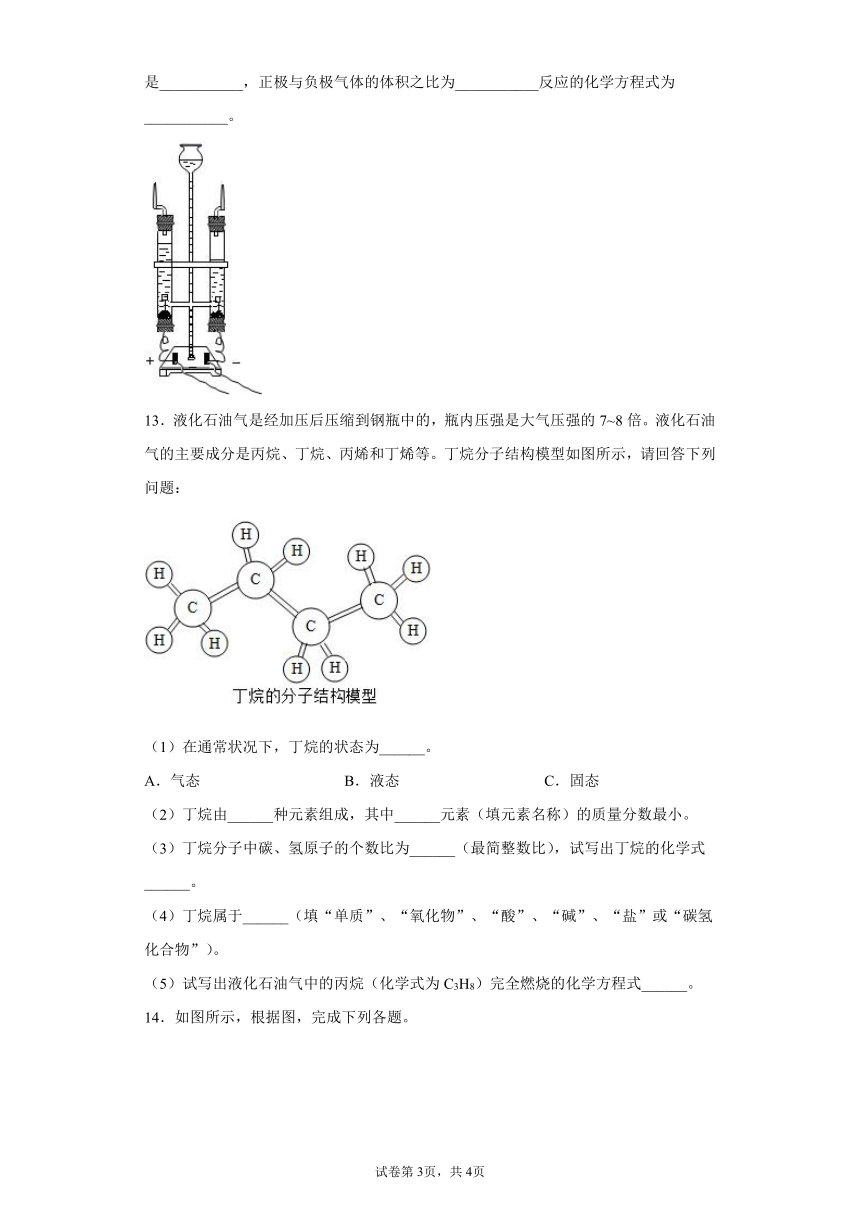
12.水是生命之源,电解水实验如图所示,与直流电源正极相连的玻璃管中生成的气体是___________,正极与负极气体的体积之比为___________反应的化学方程式为___________。
13.液化石油气是经加压后压缩到钢瓶中的,瓶内压强是大气压强的7~8倍。液化石油气的主要成分是丙烷、丁烷、丙烯和丁烯等。丁烷分子结构模型如图所示,请回答下列问题:
(1)在通常状况下,丁烷的状态为______。
A.气态 B.液态 C.固态
(2)丁烷由______种元素组成,其中______元素(填元素名称)的质量分数最小。
(3)丁烷分子中碳、氢原子的个数比为______(最简整数比),试写出丁烷的化学式______。
(4)丁烷属于______(填“单质”、“氧化物”、“酸”、“碱”、“盐”或“碳氢化合物”)。
(5)试写出液化石油气中的丙烷(化学式为C3H8)完全燃烧的化学方程式______。
14.如图所示,根据图,完成下列各题。
(1)上图中属于原子的是______,属于阳离子的是______。(填番号)其单质是由原子构成的是______。。E和F属于同种______,其原因是______。属于不同种______。D微粒的符号为______。A和C形成化合物的化学式为______。
(2)往燃烧很旺的火炉中撒几滴水,发现煤燃烧得更旺,其原因是碳在高温下与水蒸气反应,生成了一氧化碳和氢气,写出该反应的化学方程式:______。
(3)镁条在空气中燃烧,不仅生成氧化镁、氮化镁,还有少量镁与二氧化碳反应生成另一种单质和镁的氧化物。
①已知氮化镁中氮元素的化合价为-3价,请你写出氮化镁的化学式______;
②写出镁与二氧化碳反应的化学方程式______;
③任写出一个镁参加的化合反应的化学方程式______。
15.水是生命之源,自来水消毒过程中发生化学反应的微观示意图如下请回答下列问题。
(1)写出图甲反应的化学方程式_______。
(2)写出上图E的化学式_______。
(3)ClO2中氯元素的化合价为_______,所属物质类别是_______。
(4)通过上述微观过程得出的结论:_______。
(5)饮用硬度过大的水不利于人体健康,生活中常用_______的方法降低水的硬度。
试卷第2页,共2页
试卷第1页,共1页
参考答案
1.D
【详解】
A、根据化学方程式可知能表示反应条件;
B、根据化学方程式可知参加反应的反应物;
C、根据化学方程式可知各反应物和生成物的微观粒子个数比、质量比;
D、根据化学方程式不能判断化学反应的快慢。
故选:D。
2.C
【分析】
根据化学方程式判断正误的方法需考虑:应用的原理是否正确;化学式书写是否正确;是否配平;反应条件是否正确;↑和↓的标注是否正确。
【详解】略
3.B
【详解】
根据反应的化学方程式,反应物中钾、铁、氧原子个数分别为8、4、16,反应后的生成物中钾、铁、氧原子个数分别为8、0、10,根据反应前后原子种类、数目不变,则2R中含有4个铁原子和6个氧原子,每个R分子由2个铁原子和3个氧原子构成,则物质R的化学式为Fe2O3。
故选:B。
4.D
【详解】
根据质量守恒定律,化学反应前后原子种类和个数都不变,反应前硫、氧、氢的原子个数分别为:1、2、0;反应后硫、氧、氢的原子个数分别为:3、2、4,所以反应前还少两个硫原子、四个氢原子,故2X中含有两个硫原子和四个氢原子,所以X的化学式为H2S。
故选D。
5.B
【详解】
A、磷在氧气中燃烧生成五氧化二磷,该化学方程式没有配平,正确的化学方程式为:4P+5O22P2O5,书写错误;
B、碳在氧气中燃烧生成二氧化碳,该化学方程式完全正确;
C、一氧化碳在氧气中燃烧生成二氧化碳,该化学方程式缺少反应条件,正确的化学方程式为:2CO+O22CO2,书写错误;
D、过氧化氢在二氧化锰催化作用下分解生成水和氧气,该化学方程式反应物的化学式书写错误,正确的化学方程式为:2H2O22H2O+O2↑,书写错误。
故选:B。
6.D
【详解】
根据质量守恒定律,化学反应前后,原子的种类和数目不变,反应物中含Mn、O、Cl、H的个数分别是1、2、0、0,生成物中含Mn、O、Cl、H的个数分别是1、2、4、4,故反应物中还应含4个Cl、4个H,故X的化学式为HCl。
故选D。
7.C
【详解】
A、磷与氧气在点燃条件下反应生成五氧化二磷,正确的反应方程式为,故错误;
B、镁在氧气中燃烧生成氧化镁,正确的反应方程式为,故错误;
C、碳在氧气中燃烧生成二氧化碳,反应的化学方程式为,故正确;
D、加热条件下,氯酸钾在二氧化锰催化作用下反应生成氯化钾和氧气,正确的反应方程式为,故错误。
故选:C。
8.A
【详解】
根据质量守恒定律,化学反应前后原子的种类、个数、质量不变,由化学反应方程式可得:反应前不算X,有4个H和2个S;而反应后共有3个S、4个H、2个O。因此用反应后原子个数-反应前原子个数为X分子的原子构成,即X是由1个S和2个O构成,因此X的化学式为SO2,故选A。
9.B
【详解】
A:二氧化硫与氧气在五氧化二钒做催化剂加热的条件下,生成三氧化硫。由于五氧化二钒是催化剂,因此,五氧化二钒在化学反应前后质量和化学性质不变。A正确。
B:该化学反应读成:二氧化硫与氧气在五氧化二钒做催化剂加热的条件下,生成三氧化硫。所以,B错误。
C:根据化学方程式可知参加反应的 SO2与 O2的质量比为2×(32+16×2):16×2=4:1 。所以,C正确。
D:二氧化硫与氧气在五氧化二钒做催化剂加热的条件下,生成三氧化硫。氧气是氧化剂,二氧化硫是还原剂。还原剂具有还原性。D正确。
综上所述:选择B。
10.A
【详解】
由两种或两种以上物质生成一种物质的反应叫化合反应,由题中信息可知,四个方程式对应的反应都是化合反应,反应均在点燃条件下进行;化学方程式中化学式前边的数为化学计量数,所以A中计量数之比为1:1:1,B中计量数之比为2:1:2,C中计量数之比为1:1:2,D中计量数之比为2:1:2,且A中各物质的质量比为:12:32:44=3:8:11。
故选A。
11.D
【分析】
由反应的微观示意图可知,反应的化学方程式为。
【详解】
A、由反应的微观示意图可知,反应的化学方程式为,该反应由两种物质反应生成一种物质,属于化合反应,故A正确;
B、反应的化学方程式为,参加反应的A2与B2的分子个数比为3∶1,故B正确;
C、由质量守恒定律可知,化学反应后各元素种类不改变,故C正确;
D、反应的化学方程式为,生成物只含有一种分子,故D不正确。故选D。
12.氧气 1:2
【分析】
水在通电的条件下可以分解生成氧气和氢气;正极得到氧气,负极得到氢气,两者体积比为1:2;
【详解】
与直流电源正极相连的玻璃管中生成的气体是氧气,正极与负极气体的体积之比为1:2;反应水通电生成氢气和氧气,。
13.
(1)A
(2) 2 氢
(3) 2︰5 C4H10
(4)碳氢化合物
(5)C3H8 + 5O2 3CO2 + 4H2O
【分析】
(1)
液化石油气是经加压后压缩到钢瓶中的,瓶内压强是大气压强的7~8倍。液化石油气的主要成分是丙烷、丁烷、丙烯和丁烯等。在通常状况下,丁烷的状态为气态,故选:A;
(2)
根据丁烷分子结构模型可知,丁烷化学式为C4H10,丁烷由碳、氢2种元素组成。两种元素质量比=(12×4):(1×10)=24:5,所以其中氢元素的质量分数最小;
(3)
根据丁烷分子结构模型可知,丁烷化学式为C4H10,丁烷分子中碳、氢原子的个数比=4:10=2:5,丁烷的化学式C4H10;
(4)
根据丁烷的化学式可知,丁烷是由碳元素和氢元素组成的化合物,丁烷属于碳氢化合物;
(5)
液化石油气中的丙烷(化学式为C3H8)完全燃烧生成水和二氧化碳,反应的化学方程式为:C3H8 + 5O2 3CO2 + 4H2O。
14.
(1) ABCE D BCD 元素 质子数相同 微粒 Mg2+ Na2O
(2)C+H2OCO+H2
(3) Mg3N2 2Mg+CO22MgO+C 2Mg+O22MgO
【分析】
(1)
原子中核电荷数=核外电子数,阳离子核电荷数大于核外电子数,故ABCE属于原子;D属于阳离子,稀有气体和金属都是由原子构成的,B是稀有气体元素,CD表示的金属元素,单质由原子构成,BCD的单质都由原子构成;E和F因是质子数相同但电子数不同,属于同种元素的不同种微粒。D微粒的符号为Mg2+,A和C形成化合物的化学式为Na2O,故填:ABCE;D;BCD元素;质子数相同;微粒;Mg2+;Na2O。
(2)
碳在高温下与水蒸气反应,生成了一氧化碳和氢气,故填:C+H2OCO+H2。
(3)
①已知氮化镁中氮元素的化合价为-3价,根据化合价代数和为零,氮化镁的化学式Mg3N2,故填:Mg3N2。
②写出镁与二氧化碳反应生成氧化镁和碳,化学方程式2Mg+CO22MgO+C,故填:2Mg+CO22MgO+C。
③镁和氧气反应生成氧化镁,属于化合反应,故填:2Mg+O22MgO。
15.(1)
【分析】
(1)
图甲是A水和B氯气反应生成C氯化氢和DHClO,化学方程式为Cl2+H2O=HCl+HClO。
(2)
E表示氧气,化学式O2。
(3)
化合物中各元素的化合价代数和为0,氧元素为-2价,所以氯元素是+4价,该物质是由2种元素组成,其中一种是氧元素的化合物,是氧化物或化合物。
(4)
从图甲与图乙可知,化学变化中分子改变,原子不变。在化学变化中分子可分,而原子不可分,原子重新组合成新物质的分子。
(5)
生活中常用加热煮沸的方法降低水的硬度,加热过程中,水中的钙镁离子部分转化为水垢析出,从而降低水的硬度。答案第1页,共2页
答案第1页,共2页
练习
一、单选题,共12小题
1.化学方程式不能提供的信息是
A.通过什么条件反应 B.哪些物质参加反应
C.各物质之间的质量比 D.化学反应速率的快慢
2.下列化学方程式书写正确的是
A.2P+5O2P2O5
B.2KMnO4K2MnO4 + MnO2 + O2
C.2CO + O22CO2
D.CO2+Ca(OH)2=CaCO3+H2O
3.多功能水处理剂高铁酸钾受热会发生分解:,则R是
A.FeO B.Fe2O3 C.Fe D.Fe3O4
4.在化学反应SO2+2X=3S↓+2H2O中,X的化学式为
A.S B.H2 C.HS D.H2S
5.下列化学方程式中,书写正确的是
A.2P+5O2P2O5 B.C+O2CO2
C.2CO+O2=2CO2 D.H2O2H2↑+O2↑
6.MnO2不仅可作催化剂,还可作重要的氧化剂,如用于实验室制取氯气,化学方程式为MnO2+4XMnCl2+2H2O+Cl2↑,则物质X的化学式为
A.ClO2 B.H2O2 C.HClO D.HCl
7.下列化学方程式书写正确的是
A. B.
C. D.
8.已知某反应的化学方程式为:,则X的化学式为
A.SO2 B.SO3 C.H2SO3 D.H2SO4
9.关于反应 2SO2+O22SO3,说法错误的是
A.V2O5在反应前后化学性质不变 B.二氧化硫加氧气反应生成三氧化硫
C.参加反应的 SO2与 O2的质量比为 4:1 D.反应中 SO2 作还原剂,具有还原性
10.四位同学正在讨论某一个化学方程式的意义,他们所描述的化学方程式是
A. B.
C. D.
11.用“”和“”分别代表A2和B2两种物质,二者反应的微观示意图如图。有关说法不正确的是
该反应属于化合反应
B.参加反应的A2与B2的分子个数比为3:1
反应后各元素种类不改变
D.反应后的生成了二种新的分子
二、非选择题,共5小题
12.水是生命之源,电解水实验如图所示,与直流电源正极相连的玻璃管中生成的气体是___________,正极与负极气体的体积之比为___________反应的化学方程式为___________。
13.液化石油气是经加压后压缩到钢瓶中的,瓶内压强是大气压强的7~8倍。液化石油气的主要成分是丙烷、丁烷、丙烯和丁烯等。丁烷分子结构模型如图所示,请回答下列问题:
(1)在通常状况下,丁烷的状态为______。
A.气态 B.液态 C.固态
(2)丁烷由______种元素组成,其中______元素(填元素名称)的质量分数最小。
(3)丁烷分子中碳、氢原子的个数比为______(最简整数比),试写出丁烷的化学式______。
(4)丁烷属于______(填“单质”、“氧化物”、“酸”、“碱”、“盐”或“碳氢化合物”)。
(5)试写出液化石油气中的丙烷(化学式为C3H8)完全燃烧的化学方程式______。
14.如图所示,根据图,完成下列各题。
(1)上图中属于原子的是______,属于阳离子的是______。(填番号)其单质是由原子构成的是______。。E和F属于同种______,其原因是______。属于不同种______。D微粒的符号为______。A和C形成化合物的化学式为______。
(2)往燃烧很旺的火炉中撒几滴水,发现煤燃烧得更旺,其原因是碳在高温下与水蒸气反应,生成了一氧化碳和氢气,写出该反应的化学方程式:______。
(3)镁条在空气中燃烧,不仅生成氧化镁、氮化镁,还有少量镁与二氧化碳反应生成另一种单质和镁的氧化物。
①已知氮化镁中氮元素的化合价为-3价,请你写出氮化镁的化学式______;
②写出镁与二氧化碳反应的化学方程式______;
③任写出一个镁参加的化合反应的化学方程式______。
15.水是生命之源,自来水消毒过程中发生化学反应的微观示意图如下请回答下列问题。
(1)写出图甲反应的化学方程式_______。
(2)写出上图E的化学式_______。
(3)ClO2中氯元素的化合价为_______,所属物质类别是_______。
(4)通过上述微观过程得出的结论:_______。
(5)饮用硬度过大的水不利于人体健康,生活中常用_______的方法降低水的硬度。
试卷第2页,共2页
试卷第1页,共1页
参考答案
1.D
【详解】
A、根据化学方程式可知能表示反应条件;
B、根据化学方程式可知参加反应的反应物;
C、根据化学方程式可知各反应物和生成物的微观粒子个数比、质量比;
D、根据化学方程式不能判断化学反应的快慢。
故选:D。
2.C
【分析】
根据化学方程式判断正误的方法需考虑:应用的原理是否正确;化学式书写是否正确;是否配平;反应条件是否正确;↑和↓的标注是否正确。
【详解】略
3.B
【详解】
根据反应的化学方程式,反应物中钾、铁、氧原子个数分别为8、4、16,反应后的生成物中钾、铁、氧原子个数分别为8、0、10,根据反应前后原子种类、数目不变,则2R中含有4个铁原子和6个氧原子,每个R分子由2个铁原子和3个氧原子构成,则物质R的化学式为Fe2O3。
故选:B。
4.D
【详解】
根据质量守恒定律,化学反应前后原子种类和个数都不变,反应前硫、氧、氢的原子个数分别为:1、2、0;反应后硫、氧、氢的原子个数分别为:3、2、4,所以反应前还少两个硫原子、四个氢原子,故2X中含有两个硫原子和四个氢原子,所以X的化学式为H2S。
故选D。
5.B
【详解】
A、磷在氧气中燃烧生成五氧化二磷,该化学方程式没有配平,正确的化学方程式为:4P+5O22P2O5,书写错误;
B、碳在氧气中燃烧生成二氧化碳,该化学方程式完全正确;
C、一氧化碳在氧气中燃烧生成二氧化碳,该化学方程式缺少反应条件,正确的化学方程式为:2CO+O22CO2,书写错误;
D、过氧化氢在二氧化锰催化作用下分解生成水和氧气,该化学方程式反应物的化学式书写错误,正确的化学方程式为:2H2O22H2O+O2↑,书写错误。
故选:B。
6.D
【详解】
根据质量守恒定律,化学反应前后,原子的种类和数目不变,反应物中含Mn、O、Cl、H的个数分别是1、2、0、0,生成物中含Mn、O、Cl、H的个数分别是1、2、4、4,故反应物中还应含4个Cl、4个H,故X的化学式为HCl。
故选D。
7.C
【详解】
A、磷与氧气在点燃条件下反应生成五氧化二磷,正确的反应方程式为,故错误;
B、镁在氧气中燃烧生成氧化镁,正确的反应方程式为,故错误;
C、碳在氧气中燃烧生成二氧化碳,反应的化学方程式为,故正确;
D、加热条件下,氯酸钾在二氧化锰催化作用下反应生成氯化钾和氧气,正确的反应方程式为,故错误。
故选:C。
8.A
【详解】
根据质量守恒定律,化学反应前后原子的种类、个数、质量不变,由化学反应方程式可得:反应前不算X,有4个H和2个S;而反应后共有3个S、4个H、2个O。因此用反应后原子个数-反应前原子个数为X分子的原子构成,即X是由1个S和2个O构成,因此X的化学式为SO2,故选A。
9.B
【详解】
A:二氧化硫与氧气在五氧化二钒做催化剂加热的条件下,生成三氧化硫。由于五氧化二钒是催化剂,因此,五氧化二钒在化学反应前后质量和化学性质不变。A正确。
B:该化学反应读成:二氧化硫与氧气在五氧化二钒做催化剂加热的条件下,生成三氧化硫。所以,B错误。
C:根据化学方程式可知参加反应的 SO2与 O2的质量比为2×(32+16×2):16×2=4:1 。所以,C正确。
D:二氧化硫与氧气在五氧化二钒做催化剂加热的条件下,生成三氧化硫。氧气是氧化剂,二氧化硫是还原剂。还原剂具有还原性。D正确。
综上所述:选择B。
10.A
【详解】
由两种或两种以上物质生成一种物质的反应叫化合反应,由题中信息可知,四个方程式对应的反应都是化合反应,反应均在点燃条件下进行;化学方程式中化学式前边的数为化学计量数,所以A中计量数之比为1:1:1,B中计量数之比为2:1:2,C中计量数之比为1:1:2,D中计量数之比为2:1:2,且A中各物质的质量比为:12:32:44=3:8:11。
故选A。
11.D
【分析】
由反应的微观示意图可知,反应的化学方程式为。
【详解】
A、由反应的微观示意图可知,反应的化学方程式为,该反应由两种物质反应生成一种物质,属于化合反应,故A正确;
B、反应的化学方程式为,参加反应的A2与B2的分子个数比为3∶1,故B正确;
C、由质量守恒定律可知,化学反应后各元素种类不改变,故C正确;
D、反应的化学方程式为,生成物只含有一种分子,故D不正确。故选D。
12.氧气 1:2
【分析】
水在通电的条件下可以分解生成氧气和氢气;正极得到氧气,负极得到氢气,两者体积比为1:2;
【详解】
与直流电源正极相连的玻璃管中生成的气体是氧气,正极与负极气体的体积之比为1:2;反应水通电生成氢气和氧气,。
13.
(1)A
(2) 2 氢
(3) 2︰5 C4H10
(4)碳氢化合物
(5)C3H8 + 5O2 3CO2 + 4H2O
【分析】
(1)
液化石油气是经加压后压缩到钢瓶中的,瓶内压强是大气压强的7~8倍。液化石油气的主要成分是丙烷、丁烷、丙烯和丁烯等。在通常状况下,丁烷的状态为气态,故选:A;
(2)
根据丁烷分子结构模型可知,丁烷化学式为C4H10,丁烷由碳、氢2种元素组成。两种元素质量比=(12×4):(1×10)=24:5,所以其中氢元素的质量分数最小;
(3)
根据丁烷分子结构模型可知,丁烷化学式为C4H10,丁烷分子中碳、氢原子的个数比=4:10=2:5,丁烷的化学式C4H10;
(4)
根据丁烷的化学式可知,丁烷是由碳元素和氢元素组成的化合物,丁烷属于碳氢化合物;
(5)
液化石油气中的丙烷(化学式为C3H8)完全燃烧生成水和二氧化碳,反应的化学方程式为:C3H8 + 5O2 3CO2 + 4H2O。
14.
(1) ABCE D BCD 元素 质子数相同 微粒 Mg2+ Na2O
(2)C+H2OCO+H2
(3) Mg3N2 2Mg+CO22MgO+C 2Mg+O22MgO
【分析】
(1)
原子中核电荷数=核外电子数,阳离子核电荷数大于核外电子数,故ABCE属于原子;D属于阳离子,稀有气体和金属都是由原子构成的,B是稀有气体元素,CD表示的金属元素,单质由原子构成,BCD的单质都由原子构成;E和F因是质子数相同但电子数不同,属于同种元素的不同种微粒。D微粒的符号为Mg2+,A和C形成化合物的化学式为Na2O,故填:ABCE;D;BCD元素;质子数相同;微粒;Mg2+;Na2O。
(2)
碳在高温下与水蒸气反应,生成了一氧化碳和氢气,故填:C+H2OCO+H2。
(3)
①已知氮化镁中氮元素的化合价为-3价,根据化合价代数和为零,氮化镁的化学式Mg3N2,故填:Mg3N2。
②写出镁与二氧化碳反应生成氧化镁和碳,化学方程式2Mg+CO22MgO+C,故填:2Mg+CO22MgO+C。
③镁和氧气反应生成氧化镁,属于化合反应,故填:2Mg+O22MgO。
15.(1)
【分析】
(1)
图甲是A水和B氯气反应生成C氯化氢和DHClO,化学方程式为Cl2+H2O=HCl+HClO。
(2)
E表示氧气,化学式O2。
(3)
化合物中各元素的化合价代数和为0,氧元素为-2价,所以氯元素是+4价,该物质是由2种元素组成,其中一种是氧元素的化合物,是氧化物或化合物。
(4)
从图甲与图乙可知,化学变化中分子改变,原子不变。在化学变化中分子可分,而原子不可分,原子重新组合成新物质的分子。
(5)
生活中常用加热煮沸的方法降低水的硬度,加热过程中,水中的钙镁离子部分转化为水垢析出,从而降低水的硬度。答案第1页,共2页
答案第1页,共2页
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
