第五单元 定量研究化学反应测试题—2021-2022学年鲁教版化学九年级上册(word版 含答案)
文档属性
| 名称 | 第五单元 定量研究化学反应测试题—2021-2022学年鲁教版化学九年级上册(word版 含答案) |  | |
| 格式 | docx | ||
| 文件大小 | 210.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-18 17:57:52 | ||
图片预览


文档简介
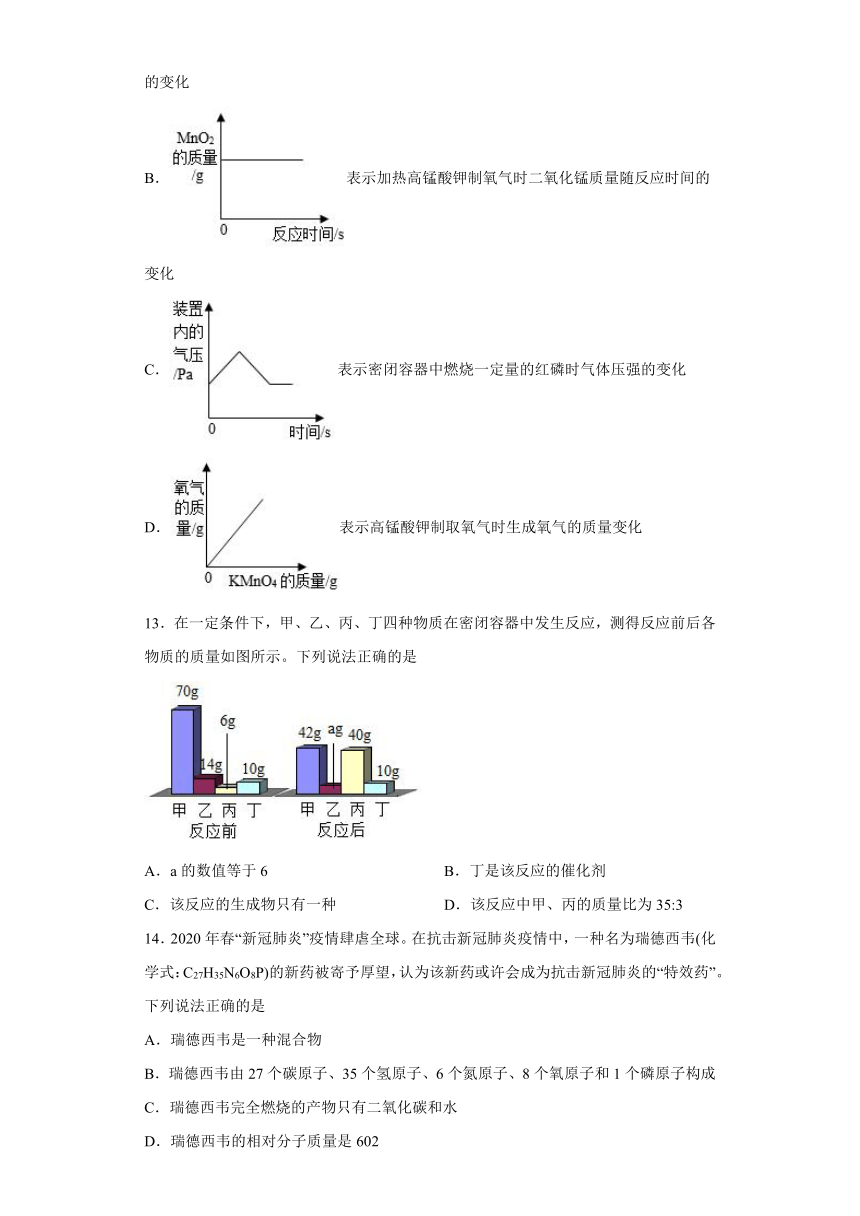
第五单元《定量研究化学反应》测试题
一、单选题
1.2021年9月15日,第十四届全运会开幕式在陕西西安奥体中心体育场举行,主火炬经传递后,最终由00后奥运冠军杨倩点燃圣火,火炬一般使用的燃料是丙烷(C3H8),其燃烧的化学方程式为: ,其中x、y分别是
A.1和5 B.7和3 C.1和3 D.5和3
2.建立宏观和微观之间的联系是化学独有的思维方式。若用“”表示氢原子,“”表示氧原子,下图四种变化中能体现“水蒸发”的微观本质的是
A. B.
C. D.
3.“502胶”是一种快干胶,易溶于酒精,其主要成分为a-氰基丙烯酸乙酯(C6H7NO2),在空气中微量水催化下发生化学反应,迅速固化而将物粘牢。下列有关其说法不正确的是
A.a-氰基丙烯酸乙酯是一种含氧化合物
B.a-氰基丙烯酸乙酯中C、H元素质量比为72:7
C.a-氰基丙烯酸乙酯和蜡烛完全燃烧的产物相同
D.粘在手上的“502”胶水可以用酒精清除
4.化学方程式书写正确的是
A. B.
C. D.
5.M物质与氧气反应生成一氧化氮和水。下列推断中正确的是
A.M中含氮元素和氢元素,可能含氧元素 B.M中只含氮元素和氢元素
C.M中含氮、氢、氧三种元素 D.无法确定M的组成
6.科研人员发现维生素P能封住病毒的侵占途径。已知维生素P的化学式为C27H30O16,关于维生素P的叙述中正确的是
A.维生素P是一种氧化物
B.维生素P是由27个碳原子、30个氢原子和16个氧原子构成
C.维生素P相对分子质量为610g
D.将维生素P在足量的氧气中充分燃烧,产物为CO2和H2O
7.正确的化学方程式是
A.3Fe+2O2Fe3O4 B.C+O2CO2↑
C.Mg+O2MgO2 D.H2O2=2H2↑+O2↑
8.有关催化剂的说法错误的是
A.反应前后本身质量不变 B.反应前后化学性质不变
C.一般加快化学反应速率 D.元素相对原子质量改变
9.下列推理或归纳合理的是
A.在化合物中金属元素一定显正价,非金属元素一定都显负价
B.分子、原子都是不带电的微粒,不带电的微粒不是分子就是原子
C.化学变化中常伴随发光放热现象,所以发光放热一定发生了化学变化
D.单质是由一种元素组成的纯净物,则由一种元素组成的纯净物一定是单质
10.下列关于物质及变化的认识,正确的是
A.任何变化都遵循质量守恒定律
B.化学变化有可能创造出世界上原来不存在的物质
C.有发光、放热现象的变化一定是化学变化
D.只有通过化学变化才能获得物质和能量
11.我国古代典籍中有“银针验毒”的记载,其反应原理之一是 。下列有关该反应的说法不正确的是
A.X的化学式是Ag2S B.反应前后元素种类不变
C.反应前后银元素的化合价不变 D.H2S中硫元素为-2价
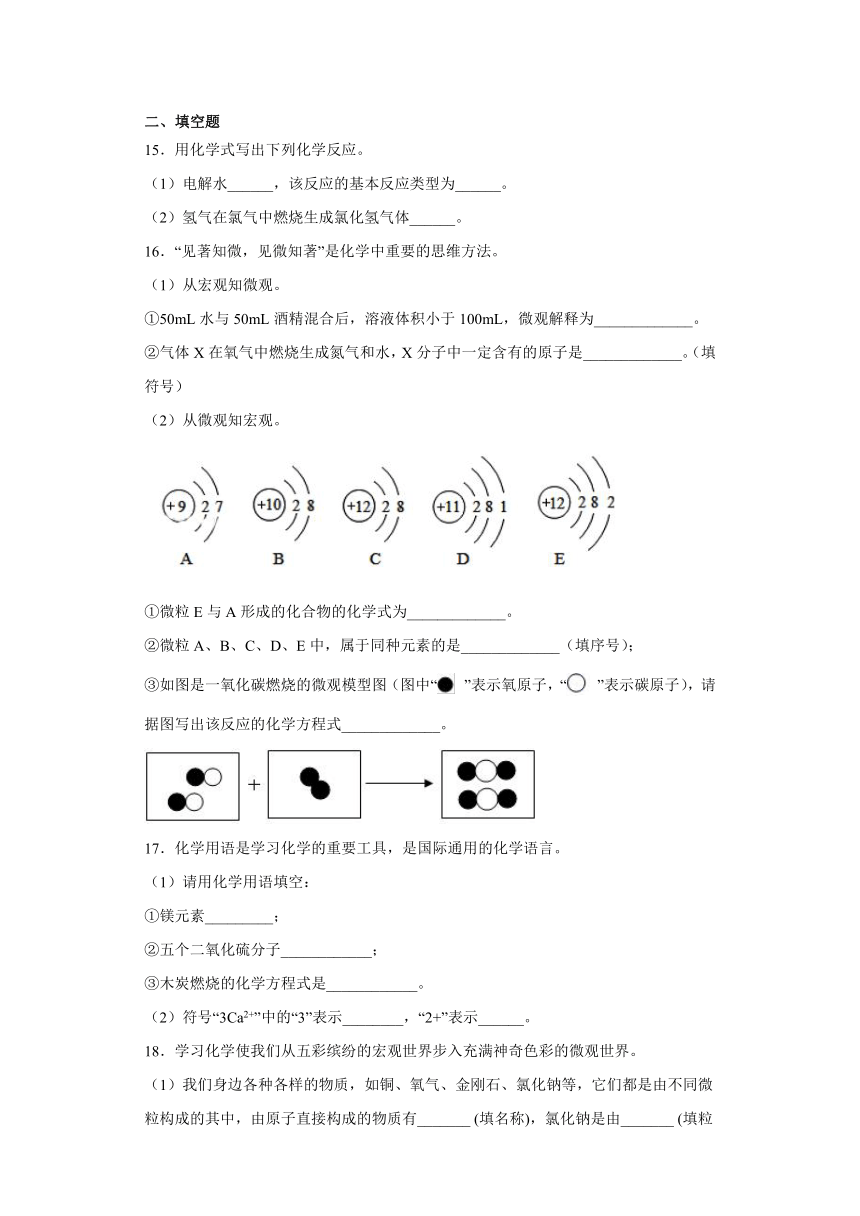
12.下列图象符合其描述情况的是
A.表示敞口容器中加热一定量镁条时固体质量随加热时间的变化
B.表示加热高锰酸钾制氧气时二氧化锰质量随反应时间的变化
C.表示密闭容器中燃烧一定量的红磷时气体压强的变化
D.表示高锰酸钾制取氧气时生成氧气的质量变化
13.在一定条件下,甲、乙、丙、丁四种物质在密闭容器中发生反应,测得反应前后各物质的质量如图所示。下列说法正确的是
A.a的数值等于6 B.丁是该反应的催化剂
C.该反应的生成物只有一种 D.该反应中甲、丙的质量比为35:3
14.2020年春“新冠肺炎”疫情肆虐全球。在抗击新冠肺炎疫情中,一种名为瑞德西韦(化学式:C27H35N6O8P)的新药被寄予厚望,认为该新药或许会成为抗击新冠肺炎的“特效药”。下列说法正确的是
A.瑞德西韦是一种混合物
B.瑞德西韦由27个碳原子、35个氢原子、6个氮原子、8个氧原子和1个磷原子构成
C.瑞德西韦完全燃烧的产物只有二氧化碳和水
D.瑞德西韦的相对分子质量是602
二、填空题
15.用化学式写出下列化学反应。
(1)电解水______,该反应的基本反应类型为______。
(2)氢气在氯气中燃烧生成氯化氢气体______。
16.“见著知微,见微知著”是化学中重要的思维方法。
(1)从宏观知微观。
①50mL水与50mL酒精混合后,溶液体积小于100mL,微观解释为_____________。
②气体X在氧气中燃烧生成氮气和水,X分子中一定含有的原子是_____________。(填符号)
(2)从微观知宏观。
①微粒E与A形成的化合物的化学式为_____________。
②微粒A、B、C、D、E中,属于同种元素的是_____________(填序号);
③如图是一氧化碳燃烧的微观模型图(图中“ ”表示氧原子,“ ”表示碳原子),请据图写出该反应的化学方程式_____________。
17.化学用语是学习化学的重要工具,是国际通用的化学语言。
(1)请用化学用语填空:
①镁元素_________;
②五个二氧化硫分子____________;
③木炭燃烧的化学方程式是____________。
(2)符号“3Ca2+”中的“3”表示________,“2+”表示______。
18.学习化学使我们从五彩缤纷的宏观世界步入充满神奇色彩的微观世界。
(1)我们身边各种各样的物质,如铜、氧气、金刚石、氯化钠等,它们都是由不同微粒构成的其中,由原子直接构成的物质有_______ (填名称),氯化钠是由_______ (填粒子符号)构成的。
(2)学习“原子的构成”之后,小张幻想自己变成一个进入原子内部的微粒,写了如下短文。
我想象中的原子结构
进入镁原子,我发现①原子是由原子核与核外电子构成的,②原子核相比较原子的体积竟然那么小,③12 个电子在原子核外做高速运动,④我试着去搬动它们,发现电子的质量与原子核的质量差不多…
小张对原子结构的认识有些是错误的,指出文中的错误______ (填句子前的序号)。请帮助小张画出镁原子的结构示意图______,请以镁原子为例,谈一谈原子结构与元素化学性质的关系______。
(3)氢气在氯气中燃烧生成氯化氢,下图是该变化的微观示意图
根据图示,写出该反应的化学方程式____________。图中方框内表示纯净物的是_______ (填字母序号)。请写出图中转化①和转化②的微观实质_______。
三、推断题
19. A~H八种物质,有下图所示关系:其中A是暗紫色的固体,D能使带火星的木条复燃,H是一种有刺激性气味的气体,试推断:
(1)请你根据上述信息,回答:
A的名称 _______ 、B的作用___________、D化学符号___________。
(2)写出反应①③的化学反应方程式,并指出反应的基本类型(化合、分解反应):
①__________,属于 __________反应;
③___________,属于___________反应。
20.小明取暗紫色粉末A进行实验,实验过程如图,其中固体C在化学反应②、③前后质量和化学性质都不变。请回答下列问题。
(1)写出下列物质的名称:A______;F______。
(2)C在上图的关系中扮演了两个角色,分别为______和______。
(3)写出下列反应的文字表达式(或符号表达式);③______。④______。
(4)反应①②③④中,属于分解反应的是______。
四、实验题
21.下图是实验室制取气体的常用装置。
(1)实验室用KMnO4制取O2应选用的一套发生和收集装置为________(填字母代号);该反应的化学方程式为______________。
2017年5月,我国宣布首次海域“可燃冰”试采成功。“可燃冰”主要含有甲烷水合物。
(2)实验室里加热醋酸钠和碱石灰的固体混合物可制取甲烷,请将右面方框中该气体的发生装置图补画完整__________。
22.如图是某班同学验证质量守恒定律的两个实验片段。
(1)A图是测定红磷燃烧前后质量的变化情况实验。试回答下列问题:
①锥形瓶底部铺少量细沙的目的是___________;
②实验过程中可观察到锥形瓶内红磷燃烧有大量白烟,气球___________;
③写出红磷燃烧的化学方程式___________;
④充分反应后,能证明质量守恒定律的现象是___________。
(2)B图装置测定稀盐酸与碳酸钠反应前后质量的变化情况实验,反应前天平平衡,然后将稀盐酸倒入烧杯中与碳酸钠充分反应后,再称量,观察到反应后天平不平衡,天平指针向___________偏转(填“左”或“右”)。该反应___________质量守恒定律(填“遵守”或“不遵守”)。反应后天平不平衡的原因是___________。
(3)由质量守恒定律可知,化学反应前后,一定不变的是___________(填序号)。
①原子种类 ②原子数目 ③分子种类 ④分子数目 ⑤元素种类 ⑥物质种类
五、计算题
23.用电解水的方法制取氧气,现在要制取16kg氧气,需要电解多少水?小红的解题过程如下,请判断小红的解题过程是否正确,如不正确请改正。(可能用到的相对原子质量 H:1 O:16)
解:设需要电解水的质量为x
答:需电解水18kg。
24.工业上,高温煅烧石灰石可制得生石灰和二氧化碳,如果要制取5.6t的氧化钙,需要碳酸钙的质量是多少?
参考答案
1.D 2.B 3.C 4.D 5.A 6.D 7.A 8.D 9.D 10.B 11.C 12.D 13.C 14.D
15.(1) 分解反应 (2)
16.(1) 分子间有间隔 N、H
(2) MgF2 CE
17.(1) Mg 5SO2
(2) 3个钙离子 每个钙离子带两个单位的正电荷
18.(1) 铜、金刚石 Na+和Cl-
(2) ④
镁原子最外层上有2个电子,由于小于4个,化学性质比较活泼,在化学反应中易失2个电子,形成阳离子
(3)
C 氯气分子和氢气分子分成氯原子和氢原子,氢原子和氯原子重新组合生成氯化氢分子
19.(1) 高锰酸钾 作催化剂 O2
(2) 2KMnO4K2MnO4+MnO2+O2↑ 分解 S+O2SO2 化合
20.(1) 高锰酸钾 氯酸钾
(2) 生成物 催化剂
(3) 过氧化氢水+氧气,或H2O2H2O+O2 铁+氧气四氧化三铁,或Fe+O2Fe3O4 (4)①②③
21.(1) AD或AE
(2)
22.(1) 防止红磷燃烧放热炸裂瓶底 先膨胀后缩小 天平仍保持平衡
(2) 右 遵守 生成气体逸散,总质量变小
(3)①②⑤
23.不正确。改正答案如下:
解:设需要电解水的质量为x
答:需电解水质量为18kg。
24.10t
解:设需要碳酸钙质量为x。
x=10t
答:需要碳酸钙10t。
一、单选题
1.2021年9月15日,第十四届全运会开幕式在陕西西安奥体中心体育场举行,主火炬经传递后,最终由00后奥运冠军杨倩点燃圣火,火炬一般使用的燃料是丙烷(C3H8),其燃烧的化学方程式为: ,其中x、y分别是
A.1和5 B.7和3 C.1和3 D.5和3
2.建立宏观和微观之间的联系是化学独有的思维方式。若用“”表示氢原子,“”表示氧原子,下图四种变化中能体现“水蒸发”的微观本质的是
A. B.
C. D.
3.“502胶”是一种快干胶,易溶于酒精,其主要成分为a-氰基丙烯酸乙酯(C6H7NO2),在空气中微量水催化下发生化学反应,迅速固化而将物粘牢。下列有关其说法不正确的是
A.a-氰基丙烯酸乙酯是一种含氧化合物
B.a-氰基丙烯酸乙酯中C、H元素质量比为72:7
C.a-氰基丙烯酸乙酯和蜡烛完全燃烧的产物相同
D.粘在手上的“502”胶水可以用酒精清除
4.化学方程式书写正确的是
A. B.
C. D.
5.M物质与氧气反应生成一氧化氮和水。下列推断中正确的是
A.M中含氮元素和氢元素,可能含氧元素 B.M中只含氮元素和氢元素
C.M中含氮、氢、氧三种元素 D.无法确定M的组成
6.科研人员发现维生素P能封住病毒的侵占途径。已知维生素P的化学式为C27H30O16,关于维生素P的叙述中正确的是
A.维生素P是一种氧化物
B.维生素P是由27个碳原子、30个氢原子和16个氧原子构成
C.维生素P相对分子质量为610g
D.将维生素P在足量的氧气中充分燃烧,产物为CO2和H2O
7.正确的化学方程式是
A.3Fe+2O2Fe3O4 B.C+O2CO2↑
C.Mg+O2MgO2 D.H2O2=2H2↑+O2↑
8.有关催化剂的说法错误的是
A.反应前后本身质量不变 B.反应前后化学性质不变
C.一般加快化学反应速率 D.元素相对原子质量改变
9.下列推理或归纳合理的是
A.在化合物中金属元素一定显正价,非金属元素一定都显负价
B.分子、原子都是不带电的微粒,不带电的微粒不是分子就是原子
C.化学变化中常伴随发光放热现象,所以发光放热一定发生了化学变化
D.单质是由一种元素组成的纯净物,则由一种元素组成的纯净物一定是单质
10.下列关于物质及变化的认识,正确的是
A.任何变化都遵循质量守恒定律
B.化学变化有可能创造出世界上原来不存在的物质
C.有发光、放热现象的变化一定是化学变化
D.只有通过化学变化才能获得物质和能量
11.我国古代典籍中有“银针验毒”的记载,其反应原理之一是 。下列有关该反应的说法不正确的是
A.X的化学式是Ag2S B.反应前后元素种类不变
C.反应前后银元素的化合价不变 D.H2S中硫元素为-2价
12.下列图象符合其描述情况的是
A.表示敞口容器中加热一定量镁条时固体质量随加热时间的变化
B.表示加热高锰酸钾制氧气时二氧化锰质量随反应时间的变化
C.表示密闭容器中燃烧一定量的红磷时气体压强的变化
D.表示高锰酸钾制取氧气时生成氧气的质量变化
13.在一定条件下,甲、乙、丙、丁四种物质在密闭容器中发生反应,测得反应前后各物质的质量如图所示。下列说法正确的是
A.a的数值等于6 B.丁是该反应的催化剂
C.该反应的生成物只有一种 D.该反应中甲、丙的质量比为35:3
14.2020年春“新冠肺炎”疫情肆虐全球。在抗击新冠肺炎疫情中,一种名为瑞德西韦(化学式:C27H35N6O8P)的新药被寄予厚望,认为该新药或许会成为抗击新冠肺炎的“特效药”。下列说法正确的是
A.瑞德西韦是一种混合物
B.瑞德西韦由27个碳原子、35个氢原子、6个氮原子、8个氧原子和1个磷原子构成
C.瑞德西韦完全燃烧的产物只有二氧化碳和水
D.瑞德西韦的相对分子质量是602
二、填空题
15.用化学式写出下列化学反应。
(1)电解水______,该反应的基本反应类型为______。
(2)氢气在氯气中燃烧生成氯化氢气体______。
16.“见著知微,见微知著”是化学中重要的思维方法。
(1)从宏观知微观。
①50mL水与50mL酒精混合后,溶液体积小于100mL,微观解释为_____________。
②气体X在氧气中燃烧生成氮气和水,X分子中一定含有的原子是_____________。(填符号)
(2)从微观知宏观。
①微粒E与A形成的化合物的化学式为_____________。
②微粒A、B、C、D、E中,属于同种元素的是_____________(填序号);
③如图是一氧化碳燃烧的微观模型图(图中“ ”表示氧原子,“ ”表示碳原子),请据图写出该反应的化学方程式_____________。
17.化学用语是学习化学的重要工具,是国际通用的化学语言。
(1)请用化学用语填空:
①镁元素_________;
②五个二氧化硫分子____________;
③木炭燃烧的化学方程式是____________。
(2)符号“3Ca2+”中的“3”表示________,“2+”表示______。
18.学习化学使我们从五彩缤纷的宏观世界步入充满神奇色彩的微观世界。
(1)我们身边各种各样的物质,如铜、氧气、金刚石、氯化钠等,它们都是由不同微粒构成的其中,由原子直接构成的物质有_______ (填名称),氯化钠是由_______ (填粒子符号)构成的。
(2)学习“原子的构成”之后,小张幻想自己变成一个进入原子内部的微粒,写了如下短文。
我想象中的原子结构
进入镁原子,我发现①原子是由原子核与核外电子构成的,②原子核相比较原子的体积竟然那么小,③12 个电子在原子核外做高速运动,④我试着去搬动它们,发现电子的质量与原子核的质量差不多…
小张对原子结构的认识有些是错误的,指出文中的错误______ (填句子前的序号)。请帮助小张画出镁原子的结构示意图______,请以镁原子为例,谈一谈原子结构与元素化学性质的关系______。
(3)氢气在氯气中燃烧生成氯化氢,下图是该变化的微观示意图
根据图示,写出该反应的化学方程式____________。图中方框内表示纯净物的是_______ (填字母序号)。请写出图中转化①和转化②的微观实质_______。
三、推断题
19. A~H八种物质,有下图所示关系:其中A是暗紫色的固体,D能使带火星的木条复燃,H是一种有刺激性气味的气体,试推断:
(1)请你根据上述信息,回答:
A的名称 _______ 、B的作用___________、D化学符号___________。
(2)写出反应①③的化学反应方程式,并指出反应的基本类型(化合、分解反应):
①__________,属于 __________反应;
③___________,属于___________反应。
20.小明取暗紫色粉末A进行实验,实验过程如图,其中固体C在化学反应②、③前后质量和化学性质都不变。请回答下列问题。
(1)写出下列物质的名称:A______;F______。
(2)C在上图的关系中扮演了两个角色,分别为______和______。
(3)写出下列反应的文字表达式(或符号表达式);③______。④______。
(4)反应①②③④中,属于分解反应的是______。
四、实验题
21.下图是实验室制取气体的常用装置。
(1)实验室用KMnO4制取O2应选用的一套发生和收集装置为________(填字母代号);该反应的化学方程式为______________。
2017年5月,我国宣布首次海域“可燃冰”试采成功。“可燃冰”主要含有甲烷水合物。
(2)实验室里加热醋酸钠和碱石灰的固体混合物可制取甲烷,请将右面方框中该气体的发生装置图补画完整__________。
22.如图是某班同学验证质量守恒定律的两个实验片段。
(1)A图是测定红磷燃烧前后质量的变化情况实验。试回答下列问题:
①锥形瓶底部铺少量细沙的目的是___________;
②实验过程中可观察到锥形瓶内红磷燃烧有大量白烟,气球___________;
③写出红磷燃烧的化学方程式___________;
④充分反应后,能证明质量守恒定律的现象是___________。
(2)B图装置测定稀盐酸与碳酸钠反应前后质量的变化情况实验,反应前天平平衡,然后将稀盐酸倒入烧杯中与碳酸钠充分反应后,再称量,观察到反应后天平不平衡,天平指针向___________偏转(填“左”或“右”)。该反应___________质量守恒定律(填“遵守”或“不遵守”)。反应后天平不平衡的原因是___________。
(3)由质量守恒定律可知,化学反应前后,一定不变的是___________(填序号)。
①原子种类 ②原子数目 ③分子种类 ④分子数目 ⑤元素种类 ⑥物质种类
五、计算题
23.用电解水的方法制取氧气,现在要制取16kg氧气,需要电解多少水?小红的解题过程如下,请判断小红的解题过程是否正确,如不正确请改正。(可能用到的相对原子质量 H:1 O:16)
解:设需要电解水的质量为x
答:需电解水18kg。
24.工业上,高温煅烧石灰石可制得生石灰和二氧化碳,如果要制取5.6t的氧化钙,需要碳酸钙的质量是多少?
参考答案
1.D 2.B 3.C 4.D 5.A 6.D 7.A 8.D 9.D 10.B 11.C 12.D 13.C 14.D
15.(1) 分解反应 (2)
16.(1) 分子间有间隔 N、H
(2) MgF2 CE
17.(1) Mg 5SO2
(2) 3个钙离子 每个钙离子带两个单位的正电荷
18.(1) 铜、金刚石 Na+和Cl-
(2) ④
镁原子最外层上有2个电子,由于小于4个,化学性质比较活泼,在化学反应中易失2个电子,形成阳离子
(3)
C 氯气分子和氢气分子分成氯原子和氢原子,氢原子和氯原子重新组合生成氯化氢分子
19.(1) 高锰酸钾 作催化剂 O2
(2) 2KMnO4K2MnO4+MnO2+O2↑ 分解 S+O2SO2 化合
20.(1) 高锰酸钾 氯酸钾
(2) 生成物 催化剂
(3) 过氧化氢水+氧气,或H2O2H2O+O2 铁+氧气四氧化三铁,或Fe+O2Fe3O4 (4)①②③
21.(1) AD或AE
(2)
22.(1) 防止红磷燃烧放热炸裂瓶底 先膨胀后缩小 天平仍保持平衡
(2) 右 遵守 生成气体逸散,总质量变小
(3)①②⑤
23.不正确。改正答案如下:
解:设需要电解水的质量为x
答:需电解水质量为18kg。
24.10t
解:设需要碳酸钙质量为x。
x=10t
答:需要碳酸钙10t。
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
