第五单元定量研究化学反应测试题 --2021-2022学年九年级化学鲁教版上册(有答案)
文档属性
| 名称 | 第五单元定量研究化学反应测试题 --2021-2022学年九年级化学鲁教版上册(有答案) |  | |
| 格式 | docx | ||
| 文件大小 | 168.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-18 22:59:53 | ||
图片预览



文档简介
第五单元《定量研究化学反应》测试题
一、单选题
1.下列化学反应的符号表达式正确的是
A. B.
C. D.
2.化学方程式中蕴含着丰富的化学反应信息,从化学方程式 中获得的信息,错误的是
A.反应物有两种 B.生成物有两种
C.反应中有水生成 D.反应条件是点燃
3.用氯酸钾和二氧化锰的混合物制取氧气,固体混合物的质量变化如图。下列分析中错误的是
A.P点处固体成分是氯酸钾、氯化钾和二氧化锰
B.在0-t1时段,固体混合物质量不变,说明没有氧气产生
C.在0-t2时段,MnO2在固体混合物中的质量分数始终不变
D.若忽略实验误差,则反应结束时能收集到(a-b)g氧气
4.在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下发生化学反应一段时间后,测得有关数据如下表所示,测关于此反应认识不正确的是
物质 甲 乙 丙 丁
反应前质量/g 18 1 22 32
一段时间后质量/g x 26 22 12
A.丙物质可能是该反应的催化剂 B.X的值为13
C.参加反应的甲、丁两物质的质量比为1:4 D.该反应可用甲+乙→丁表示
5.下列说法中正确的是
A.氢气和氧气生成水,说明水是由氢、氧两种元素组成的
B.电解水生成氢气和氧气,说明水是由氢气和氧气组成的
C.天然水和水都是纯净物
D.水和过氧化氢的组成元素一样,所以化学性质也一样
6.甲醛是室内装修时产生的主要污染物。用下面的化学反应可检测室内甲醛含量是否超标:,根据质量守恒定律确定R的化学式为
A.CHO B.CHO2 C.CH2O D.C2H4O
7.为了使人们及时发现煤气泄漏,常在每期中加入有特殊气味的乙硫醇C2H5SH,其燃烧的化学方程式为:,则X的化学式
A.S B.SO2 C.SO3 D.CO
8.下列化学方程式书写正确的是
A. B.
C. D.
9.如下图是某密闭容器中物质变化过程的微观示意图。下列说法正确的是
A.上述变化I、II、III中,属于化合反应的是I和II
B.变化I中,一定不变的微粒只有碳原子
C.变化III中总体积变大是因为分子本身变大了
D.该反应中涉及的变化可表示为
10.甲烷在空气中完全燃烧的微观示意图如下图所示。以下说法错误的是
A.该反应过程中出现了两种氧化物
B.生成物水中氢元素与氧元素的质量比为2:1
C.一个甲烷分子由一个碳原子和四个氢原子构成
D.由微观示意图可知,该反应前、后原子种类不变
11.运载火箭的动力可由高氯酸铵(NH4ClO4)分解提供,化学方程式为2NH4ClO4=N2+Cl2+4X+2O2↑。下列有关说法不正确的是
A.X的化学式为H2O
B.该反应属于分解反应
C.NH4C1O4中氯元素的化合价为+7
D.反应生成氮气和氧气的质量比为7 : 8
12.已知2A+3B=2C+3D,2.3gA和4.8gB恰好完全反应,生成4.4gC。又知D的相对分子质量为18,则A的相对分子质量为
A.23 B.46 C.92 D.96
13.某化合物可发生如下反应:M + 3H22Fe + 3H2O,则该化合物的化学式为
A.FeO B.FeCO3 C.Fe2O3 D.Fe3O4
14.密闭容器中有一定质量的甲、乙、丙、丁四种物质,在一定条件下反应一段时 间后,测得各物质的质量如表所示:有关说法正确的是
物质 甲 乙 丙 丁
反应前的质量/g 8.0 16.8 3.4 2.0
反应后的质量/g 11.4 10 X 2.0
A.该反应中甲与乙的质量比是 57:50 B.x=3.4
C.该反应属于分解反应 D.丁一定是催化剂
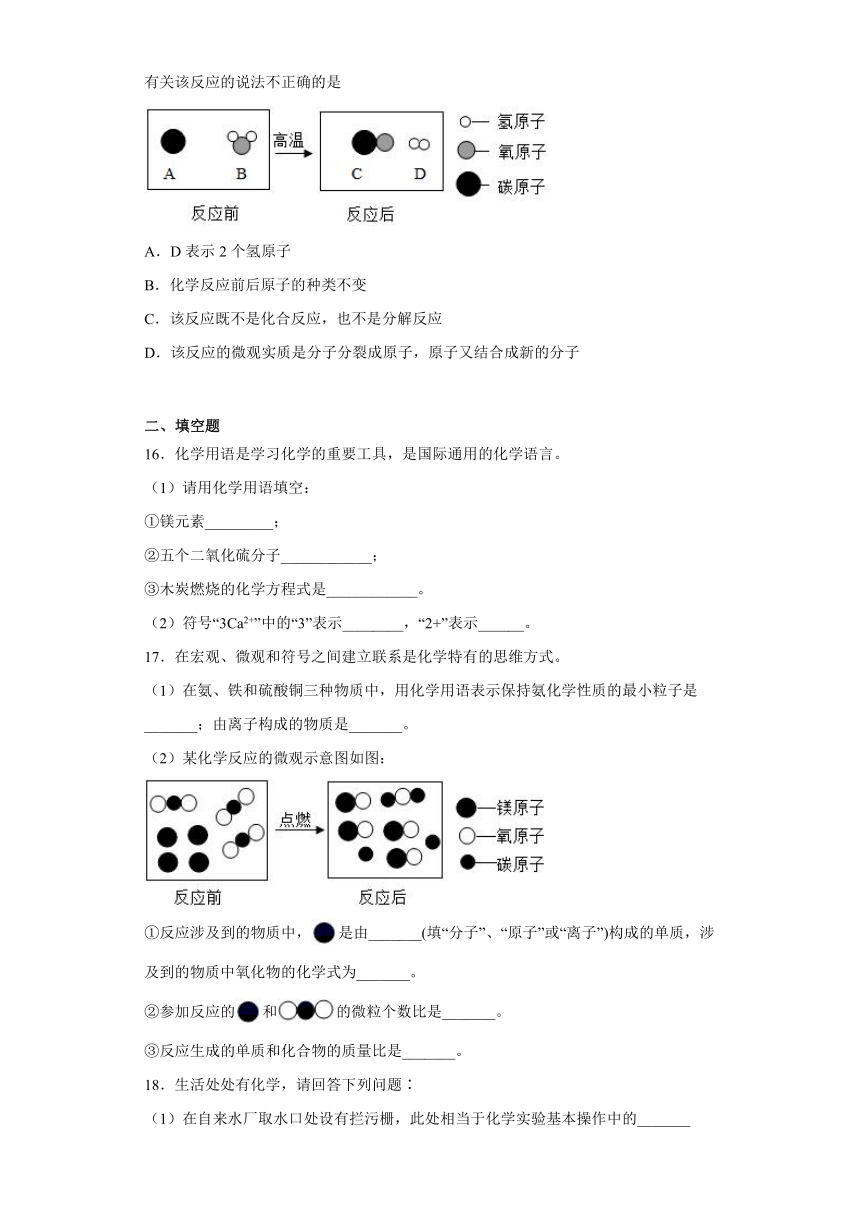
15.工业上常将煤洗选加工后用于制备水煤气,其主要反应的微观过程如图所示。下列有关该反应的说法不正确的是
A.D表示2个氢原子
B.化学反应前后原子的种类不变
C.该反应既不是化合反应,也不是分解反应
D.该反应的微观实质是分子分裂成原子,原子又结合成新的分子
二、填空题
16.化学用语是学习化学的重要工具,是国际通用的化学语言。
(1)请用化学用语填空:
①镁元素_________;
②五个二氧化硫分子____________;
③木炭燃烧的化学方程式是____________。
(2)符号“3Ca2+”中的“3”表示________,“2+”表示______。
17.在宏观、微观和符号之间建立联系是化学特有的思维方式。
(1)在氨、铁和硫酸铜三种物质中,用化学用语表示保持氨化学性质的最小粒子是_______;由离子构成的物质是_______。
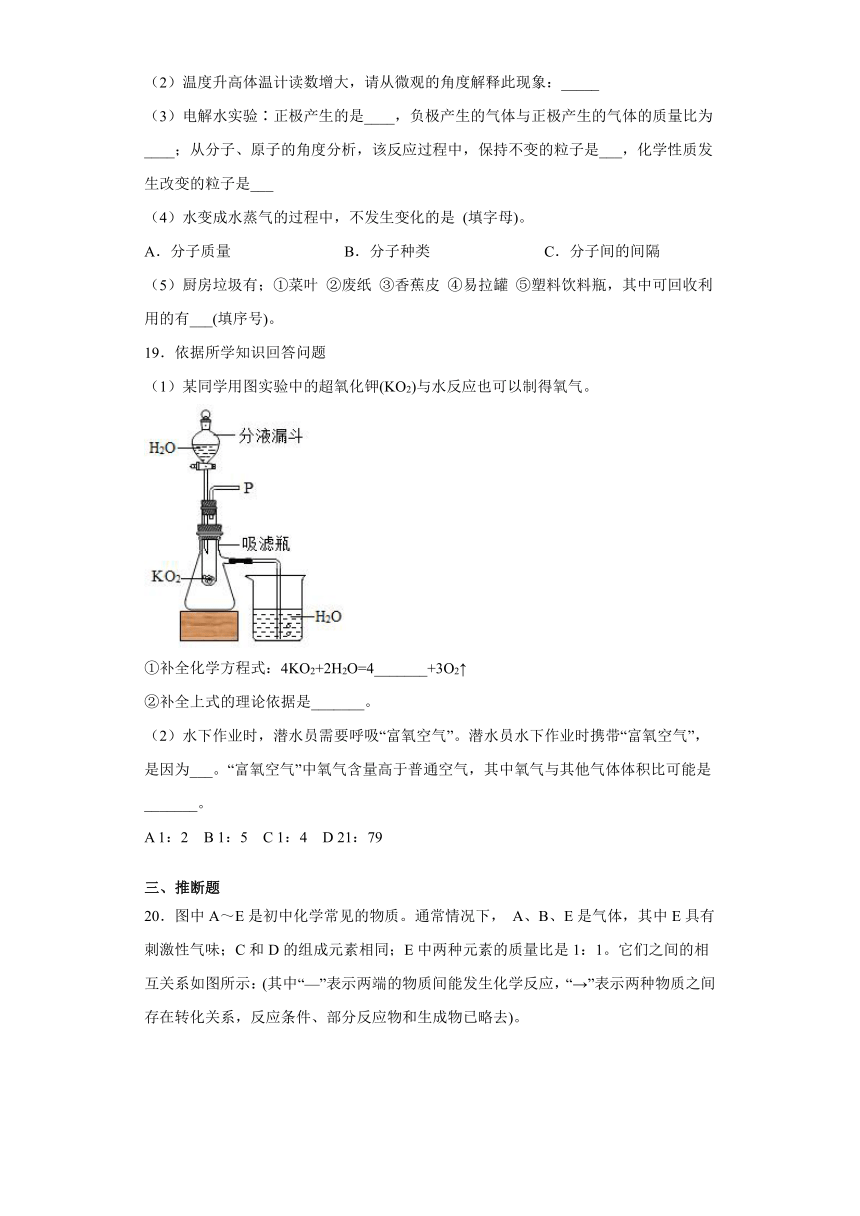
(2)某化学反应的微观示意图如图:
①反应涉及到的物质中,是由_______(填“分子”、“原子”或“离子”)构成的单质,涉及到的物质中氧化物的化学式为_______。
②参加反应的和的微粒个数比是_______。
③反应生成的单质和化合物的质量比是_______。
18.生活处处有化学,请回答下列问题∶
(1)在自来水厂取水口处设有拦污栅,此处相当于化学实验基本操作中的_______
(2)温度升高体温计读数增大,请从微观的角度解释此现象:_____
(3)电解水实验∶正极产生的是____,负极产生的气体与正极产生的气体的质量比为____;从分子、原子的角度分析,该反应过程中,保持不变的粒子是___,化学性质发生改变的粒子是___
(4)水变成水蒸气的过程中,不发生变化的是 (填字母)。
A.分子质量 B.分子种类 C.分子间的间隔
(5)厨房垃圾有;①菜叶 ②废纸 ③香蕉皮 ④易拉罐 ⑤塑料饮料瓶,其中可回收利用的有___(填序号)。
19.依据所学知识回答问题
(1)某同学用图实验中的超氧化钾(KO2)与水反应也可以制得氧气。
①补全化学方程式:4KO2+2H2O=4_______+3O2↑
②补全上式的理论依据是_______。
(2)水下作业时,潜水员需要呼吸“富氧空气”。潜水员水下作业时携带“富氧空气”,是因为___。“富氧空气”中氧气含量高于普通空气,其中氧气与其他气体体积比可能是_______。
A 1:2 B 1:5 C 1:4 D 21:79
三、推断题
20.图中A~E是初中化学常见的物质。通常情况下, A、B、E是气体,其中E具有刺激性气味;C和D的组成元素相同;E中两种元素的质量比是1:1。它们之间的相互关系如图所示:(其中“—”表示两端的物质间能发生化学反应,“→”表示两种物质之间存在转化关系,反应条件、部分反应物和生成物已略去)。
(1)A物质的化学式是____;E物质的化学式是____。
(2)写出下列反应的化学方程式:
①C→B的反应:________。
②D→C的反应:________。
21.A、B、C、D、E、F、G、H八种物质,有如图所示关系:其中A是一种暗紫色固体,B、G都是黑色固体,D 能使带火星的木条复燃,E、F都是无色液体,H是一种能使澄清石灰水变浑浊的气体。
请回答下列问题:
(1)物质C是________(写名称);
(2)写出反应②③的化学方程式,并指出反应的基本类型:
②______;属于______反应;
③______;属于_______反应。
四、实验题
22.实验室常用气体的发生和收集装置如下图所示,回答下列问题:
(1)写出上图装置中标将序号的仪器名称:①______,②______。
(2)实验室常用过氧化氢溶液和二氧化锰混合制取氧气,发生反应的化学方程式为______,选用的发生装置是______(填字母代号,下同); 要收集纯净的氧气,应该选用的收集装置是______,若用该装置收集的氧气也不纯,原因可能是______。
(3)做铁丝燃烧实验时,集气瓶出现了炸裂,可能的原因是______。
(4)制取氧气的反应结束后,欲分离反应后混合物中的二氧化锰,可采用______的方法,这种分离方法的原理是利用混合物中各物质______不同。
(5)某化学兴趣小组用块状固体硫化亚铁(FeS)与稀硫酸反应来制取硫化氢 (H2S)气体。硫化氢的密度比空气大,能溶于水形成氢硫酸。根据以上信息推断: 实验室制取硫化氢应选用的发生装置和收集装置组合是______。
23.下列是实验室制取氧气的一些装置,请回答有关问题:
(1)写出a、b仪器的名称:a___________,b___________。
(2)实验室采用高锰酸钾制取氧气,应选用的发生装置是___________(填编号),试管口要放一团棉花,其作用是___________,用E装置收集氧气,当气泡___________冒出时开始收集,该反应的化学方程式是___________ 。
(3)采用过氧化氢制取氧气,如需随时控制生成气体的量并节约药品,发生装置最好选用___________(填仪器编号),如用F装置收集氧气,检验氧气是否收集满的方法是___________。
(4)如果F装置中充满水时,也可以作为氧气的收集装置,则氧气应从___________(填“c”或“d”)端通入。
五、计算题
24.氢气是最理想的燃料,具有放热量高、无污染的优点。计算:
(1)10kg氢气完全燃烧可生成水的质量是多少?
(2)消耗氧气的质量至少是多少?
参考答案
1.C 2.D 3.C 4.D 5.A 6.C 7.B 8.C 9.D 10.B 11.D 12.A 13.C 14.C 15.A
16.(1) Mg 5SO2
(2) 3个钙离子 每个钙离子带两个单位的正电荷
17.(1) NH3 CuSO4
(2) 原子 CO2、MgO 2:1 3:20
18.(1)过滤
(2)温度升高后,微粒之间的间隔变大了
(3) 氧气 1:8 氢原子、氧原子 水分子
(4)AB
(5)②④⑤
19.(1) KOH 质量守恒定律
(2) 氧气能供给呼吸 A
20.O2 SO2 2H2O2H2↑+O2↑ 2H2O22H2O+O2↑
21.锰酸钾 2H2O22H2O+O2↑ 分解反应 C+O2CO2 化合反应
22.(1) 分液漏斗 水槽
(2) B E 气泡未均匀连续冒出时就开始收集
(3)集气瓶底没有放沙或水
(4) 过滤 颗粒大小
(5)BC
23.(1) 试管 锥形瓶
(2) A 防止高锰酸钾粉末进入导管 连续并比较均匀
(3) B 将带火星的木条放在d处,若木条复燃,则收集满
(4)d
24.(1)设生成水的质量为y,消耗氧气的质量为x
解得:x=80kg,y=90kg
答:生成水的质量是90kg。
(2)根据题(1)可知,消耗氧气的质量为80kg
答:消耗氧气的质量至少是80kg。
一、单选题
1.下列化学反应的符号表达式正确的是
A. B.
C. D.
2.化学方程式中蕴含着丰富的化学反应信息,从化学方程式 中获得的信息,错误的是
A.反应物有两种 B.生成物有两种
C.反应中有水生成 D.反应条件是点燃
3.用氯酸钾和二氧化锰的混合物制取氧气,固体混合物的质量变化如图。下列分析中错误的是
A.P点处固体成分是氯酸钾、氯化钾和二氧化锰
B.在0-t1时段,固体混合物质量不变,说明没有氧气产生
C.在0-t2时段,MnO2在固体混合物中的质量分数始终不变
D.若忽略实验误差,则反应结束时能收集到(a-b)g氧气
4.在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下发生化学反应一段时间后,测得有关数据如下表所示,测关于此反应认识不正确的是
物质 甲 乙 丙 丁
反应前质量/g 18 1 22 32
一段时间后质量/g x 26 22 12
A.丙物质可能是该反应的催化剂 B.X的值为13
C.参加反应的甲、丁两物质的质量比为1:4 D.该反应可用甲+乙→丁表示
5.下列说法中正确的是
A.氢气和氧气生成水,说明水是由氢、氧两种元素组成的
B.电解水生成氢气和氧气,说明水是由氢气和氧气组成的
C.天然水和水都是纯净物
D.水和过氧化氢的组成元素一样,所以化学性质也一样
6.甲醛是室内装修时产生的主要污染物。用下面的化学反应可检测室内甲醛含量是否超标:,根据质量守恒定律确定R的化学式为
A.CHO B.CHO2 C.CH2O D.C2H4O
7.为了使人们及时发现煤气泄漏,常在每期中加入有特殊气味的乙硫醇C2H5SH,其燃烧的化学方程式为:,则X的化学式
A.S B.SO2 C.SO3 D.CO
8.下列化学方程式书写正确的是
A. B.
C. D.
9.如下图是某密闭容器中物质变化过程的微观示意图。下列说法正确的是
A.上述变化I、II、III中,属于化合反应的是I和II
B.变化I中,一定不变的微粒只有碳原子
C.变化III中总体积变大是因为分子本身变大了
D.该反应中涉及的变化可表示为
10.甲烷在空气中完全燃烧的微观示意图如下图所示。以下说法错误的是
A.该反应过程中出现了两种氧化物
B.生成物水中氢元素与氧元素的质量比为2:1
C.一个甲烷分子由一个碳原子和四个氢原子构成
D.由微观示意图可知,该反应前、后原子种类不变
11.运载火箭的动力可由高氯酸铵(NH4ClO4)分解提供,化学方程式为2NH4ClO4=N2+Cl2+4X+2O2↑。下列有关说法不正确的是
A.X的化学式为H2O
B.该反应属于分解反应
C.NH4C1O4中氯元素的化合价为+7
D.反应生成氮气和氧气的质量比为7 : 8
12.已知2A+3B=2C+3D,2.3gA和4.8gB恰好完全反应,生成4.4gC。又知D的相对分子质量为18,则A的相对分子质量为
A.23 B.46 C.92 D.96
13.某化合物可发生如下反应:M + 3H22Fe + 3H2O,则该化合物的化学式为
A.FeO B.FeCO3 C.Fe2O3 D.Fe3O4
14.密闭容器中有一定质量的甲、乙、丙、丁四种物质,在一定条件下反应一段时 间后,测得各物质的质量如表所示:有关说法正确的是
物质 甲 乙 丙 丁
反应前的质量/g 8.0 16.8 3.4 2.0
反应后的质量/g 11.4 10 X 2.0
A.该反应中甲与乙的质量比是 57:50 B.x=3.4
C.该反应属于分解反应 D.丁一定是催化剂
15.工业上常将煤洗选加工后用于制备水煤气,其主要反应的微观过程如图所示。下列有关该反应的说法不正确的是
A.D表示2个氢原子
B.化学反应前后原子的种类不变
C.该反应既不是化合反应,也不是分解反应
D.该反应的微观实质是分子分裂成原子,原子又结合成新的分子
二、填空题
16.化学用语是学习化学的重要工具,是国际通用的化学语言。
(1)请用化学用语填空:
①镁元素_________;
②五个二氧化硫分子____________;
③木炭燃烧的化学方程式是____________。
(2)符号“3Ca2+”中的“3”表示________,“2+”表示______。
17.在宏观、微观和符号之间建立联系是化学特有的思维方式。
(1)在氨、铁和硫酸铜三种物质中,用化学用语表示保持氨化学性质的最小粒子是_______;由离子构成的物质是_______。
(2)某化学反应的微观示意图如图:
①反应涉及到的物质中,是由_______(填“分子”、“原子”或“离子”)构成的单质,涉及到的物质中氧化物的化学式为_______。
②参加反应的和的微粒个数比是_______。
③反应生成的单质和化合物的质量比是_______。
18.生活处处有化学,请回答下列问题∶
(1)在自来水厂取水口处设有拦污栅,此处相当于化学实验基本操作中的_______
(2)温度升高体温计读数增大,请从微观的角度解释此现象:_____
(3)电解水实验∶正极产生的是____,负极产生的气体与正极产生的气体的质量比为____;从分子、原子的角度分析,该反应过程中,保持不变的粒子是___,化学性质发生改变的粒子是___
(4)水变成水蒸气的过程中,不发生变化的是 (填字母)。
A.分子质量 B.分子种类 C.分子间的间隔
(5)厨房垃圾有;①菜叶 ②废纸 ③香蕉皮 ④易拉罐 ⑤塑料饮料瓶,其中可回收利用的有___(填序号)。
19.依据所学知识回答问题
(1)某同学用图实验中的超氧化钾(KO2)与水反应也可以制得氧气。
①补全化学方程式:4KO2+2H2O=4_______+3O2↑
②补全上式的理论依据是_______。
(2)水下作业时,潜水员需要呼吸“富氧空气”。潜水员水下作业时携带“富氧空气”,是因为___。“富氧空气”中氧气含量高于普通空气,其中氧气与其他气体体积比可能是_______。
A 1:2 B 1:5 C 1:4 D 21:79
三、推断题
20.图中A~E是初中化学常见的物质。通常情况下, A、B、E是气体,其中E具有刺激性气味;C和D的组成元素相同;E中两种元素的质量比是1:1。它们之间的相互关系如图所示:(其中“—”表示两端的物质间能发生化学反应,“→”表示两种物质之间存在转化关系,反应条件、部分反应物和生成物已略去)。
(1)A物质的化学式是____;E物质的化学式是____。
(2)写出下列反应的化学方程式:
①C→B的反应:________。
②D→C的反应:________。
21.A、B、C、D、E、F、G、H八种物质,有如图所示关系:其中A是一种暗紫色固体,B、G都是黑色固体,D 能使带火星的木条复燃,E、F都是无色液体,H是一种能使澄清石灰水变浑浊的气体。
请回答下列问题:
(1)物质C是________(写名称);
(2)写出反应②③的化学方程式,并指出反应的基本类型:
②______;属于______反应;
③______;属于_______反应。
四、实验题
22.实验室常用气体的发生和收集装置如下图所示,回答下列问题:
(1)写出上图装置中标将序号的仪器名称:①______,②______。
(2)实验室常用过氧化氢溶液和二氧化锰混合制取氧气,发生反应的化学方程式为______,选用的发生装置是______(填字母代号,下同); 要收集纯净的氧气,应该选用的收集装置是______,若用该装置收集的氧气也不纯,原因可能是______。
(3)做铁丝燃烧实验时,集气瓶出现了炸裂,可能的原因是______。
(4)制取氧气的反应结束后,欲分离反应后混合物中的二氧化锰,可采用______的方法,这种分离方法的原理是利用混合物中各物质______不同。
(5)某化学兴趣小组用块状固体硫化亚铁(FeS)与稀硫酸反应来制取硫化氢 (H2S)气体。硫化氢的密度比空气大,能溶于水形成氢硫酸。根据以上信息推断: 实验室制取硫化氢应选用的发生装置和收集装置组合是______。
23.下列是实验室制取氧气的一些装置,请回答有关问题:
(1)写出a、b仪器的名称:a___________,b___________。
(2)实验室采用高锰酸钾制取氧气,应选用的发生装置是___________(填编号),试管口要放一团棉花,其作用是___________,用E装置收集氧气,当气泡___________冒出时开始收集,该反应的化学方程式是___________ 。
(3)采用过氧化氢制取氧气,如需随时控制生成气体的量并节约药品,发生装置最好选用___________(填仪器编号),如用F装置收集氧气,检验氧气是否收集满的方法是___________。
(4)如果F装置中充满水时,也可以作为氧气的收集装置,则氧气应从___________(填“c”或“d”)端通入。
五、计算题
24.氢气是最理想的燃料,具有放热量高、无污染的优点。计算:
(1)10kg氢气完全燃烧可生成水的质量是多少?
(2)消耗氧气的质量至少是多少?
参考答案
1.C 2.D 3.C 4.D 5.A 6.C 7.B 8.C 9.D 10.B 11.D 12.A 13.C 14.C 15.A
16.(1) Mg 5SO2
(2) 3个钙离子 每个钙离子带两个单位的正电荷
17.(1) NH3 CuSO4
(2) 原子 CO2、MgO 2:1 3:20
18.(1)过滤
(2)温度升高后,微粒之间的间隔变大了
(3) 氧气 1:8 氢原子、氧原子 水分子
(4)AB
(5)②④⑤
19.(1) KOH 质量守恒定律
(2) 氧气能供给呼吸 A
20.O2 SO2 2H2O2H2↑+O2↑ 2H2O22H2O+O2↑
21.锰酸钾 2H2O22H2O+O2↑ 分解反应 C+O2CO2 化合反应
22.(1) 分液漏斗 水槽
(2) B E 气泡未均匀连续冒出时就开始收集
(3)集气瓶底没有放沙或水
(4) 过滤 颗粒大小
(5)BC
23.(1) 试管 锥形瓶
(2) A 防止高锰酸钾粉末进入导管 连续并比较均匀
(3) B 将带火星的木条放在d处,若木条复燃,则收集满
(4)d
24.(1)设生成水的质量为y,消耗氧气的质量为x
解得:x=80kg,y=90kg
答:生成水的质量是90kg。
(2)根据题(1)可知,消耗氧气的质量为80kg
答:消耗氧气的质量至少是80kg。
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
