2.2物质的转化规律(1)
图片预览




文档简介
(共19张PPT)
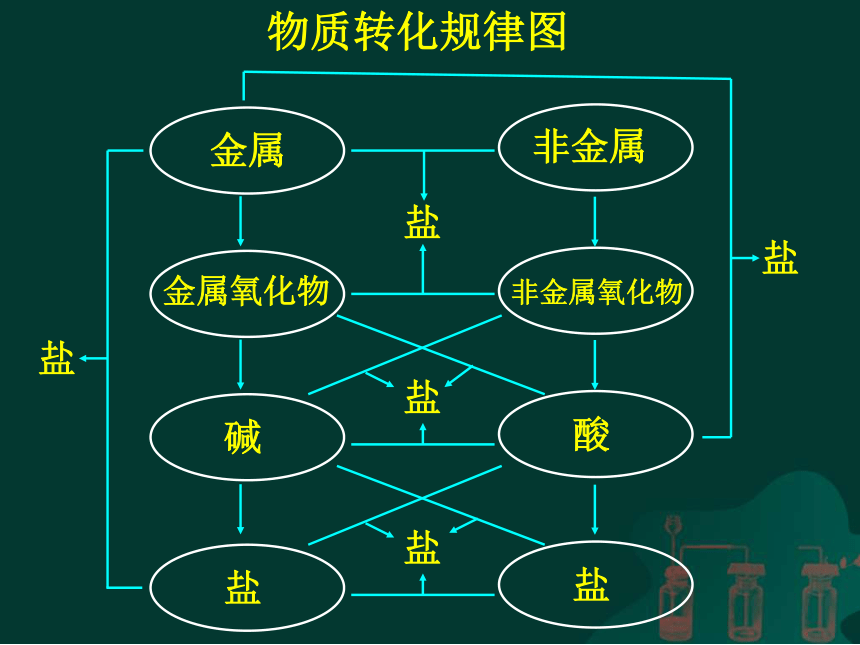
物质转化的规律
金属
金属氧化物
碱
盐
非金属
非金属氧化物
酸
盐
盐
盐
盐
盐
盐
物质转化规律图
一、非金属单质与其化合物的转化
实验:硫黄燃烧
观察外观:硫黄 是一种淡黄色的固体。
实验现象:硫在空气中燃烧,发出淡蓝色的火焰;在氧气中燃烧,发出明亮的蓝紫色火焰,生成的气体具有刺激性气味。
点燃
S+O2 ==== SO2
归纳:非金属单质能与氧气反应生成非金属氧化物
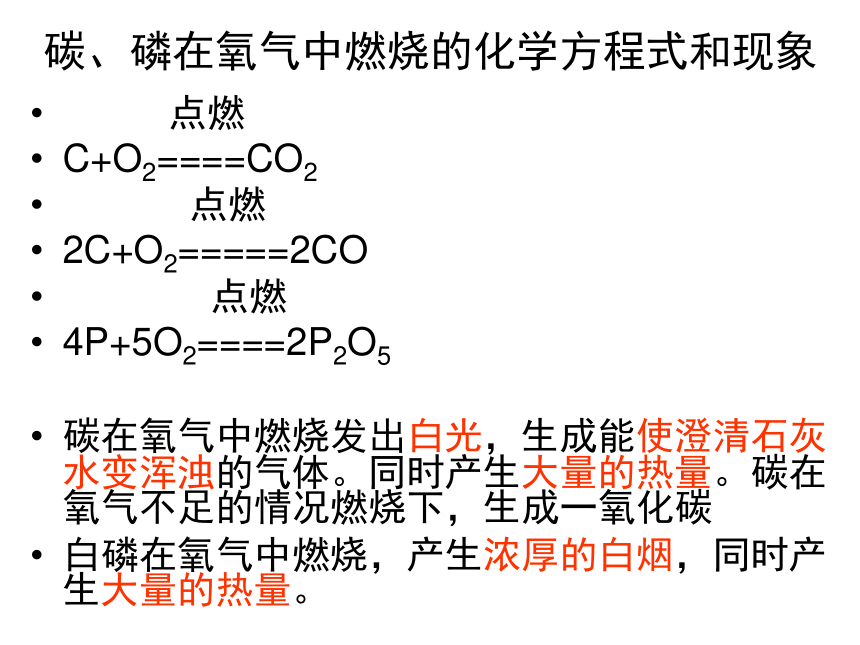
碳、磷在氧气中燃烧的化学方程式和现象
点燃
C+O2====CO2
点燃
2C+O2=====2CO
点燃
4P+5O2====2P2O5
碳在氧气中燃烧发出白光,生成能使澄清石灰水变浑浊的气体。同时产生大量的热量。碳在氧气不足的情况燃烧下,生成一氧化碳
白磷在氧气中燃烧,产生浓厚的白烟,同时产生大量的热量。
转化规律的运用
1、燃料燃烧:氢气燃烧、碳燃烧
点燃
C+O2====CO2
点燃
2C+O2=====2CO
点燃
2H2+O2====2H2O
2、用于除去气体中的氧气,
思考:白炽灯内少量氧气如何除去
白炽灯内加入少量磷,可除去灯泡内的少量氧气,防止钨丝氧化熔断。
点燃
4P+5O2====2P2O5
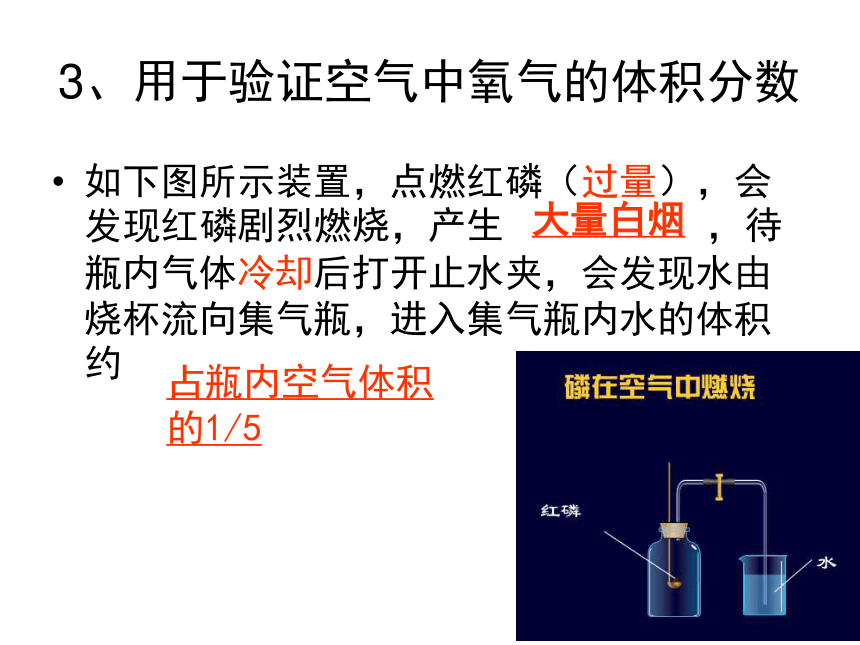
3、用于验证空气中氧气的体积分数
如下图所示装置,点燃红磷(过量),会发现红磷剧烈燃烧,产生 ,待瓶内气体冷却后打开止水夹,会发现水由烧杯流向集气瓶,进入集气瓶内水的体积约
大量白烟
占瓶内空气体积的1/5
CO2 +H2O=H2CO3
碳酸使蓝色石蕊试液变红色。
H2CO3 = H2O + CO2↑
碳酸不稳定,易分解。
二、非金属氧化物与酸间的相互转化
实验:取二支试管,分别加入蒸馏水,然后向其中一支通入二氧化碳气体,再分别滴入几滴石蕊试液。观察实验现象
实验现象:通入二氧化碳的那支试管中的紫色石蕊试液变红色
结论:CO2+H2O = H2CO3
将变红的那支试管加热,观察实验现象
实验现象:原来变红的溶液重新变为紫色。
结论: H2CO3 = CO2+H2O
归纳:非金属氧化物与酸间的相互转化规律:
非金属氧化物 水 酸
注意:二氧化硅不能与水反应生成硅酸,一氧化碳也不与水反应。
(SiO2+H2O →不反应)
练习
1、N2O5 +H2O=
2、SO2 +H20=
3、SO3 +H2O=
4、P2O5 +H2O=
注意:在转化过程中要特别注意化合价的问题。非金属氧化物与酸间的相互转化中化合价是不变的。
思考:
A、将下列物质放入水中,哪一种物质的与水反应会使溶液的PH值下降:二氧化硫、二氧化硅、氧化钙;
B、8克三氧化硫溶解于92克水中所得溶液的溶质质量分数是8%吗?
6.4克二氧化硫溶于93.6克水中,所得溶液溶质的质量分数为多少?
思 考
解:
由于SO2与H2O反应得到H2SO3,所以溶质是H2SO3。设H2SO3的质量分数为x
SO2 + H2O = H2SO3
64 82
(6.4g+93.6g)x
6.4g
三、酸与盐之间的转化
实验:向稀硫酸中分别倒入氧化铜、氢氧化铜、碳酸铜中,观察实验现象
实验现象:三种不溶于水的物质慢慢消失,并有蓝色溶液生成。
结论:
Cu(OH)2+H2SO4 = CuSO4+2H2O
CuO+H2SO4 = CuSO4+H2O
CuCO3+ H2SO4 = CuSO4+H2O+CO2↑
非金属氧化物
非金属
酸
盐
C
CO2
H2CO3
CaCO3
C + O2 = CO2
点燃
CO2 + H2O = H2CO3
H2CO3 +Ca(OH)2 = CaCO3↓+2H2O
非金属
非金属氧化物
酸
盐
S
SO2
H2SO3
Na2SO3
S + O2 = SO2
点燃
SO2 + H2O = H2SO3
H2SO3 + 2NaOH = Na2SO3 + H2O
非金属氧化物
非金属
酸
盐
P
P2O5
H3PO4
Ca3(PO4)2
4P + 5O2 = 2P2O5
点燃
P2O5 + 3H2O = 2H3PO4
2H3PO4+3Ca(OH)2=Ca3(PO4)2↓+6H2O
(红色)
(白色)
(白色)
非金属氧化物
非金属
酸
盐
非金属+氧气→非金属氧化物
非金属氧化物+水→含氧酸
酸→非金属氧化物+水
某些金属+某些酸→盐+氢气
酸+金属氧化物→盐+水
酸+碱→盐+水
酸+某些盐→另一种酸+另一种盐
例:写出以盐酸为原料制取氯化锌的化学反应方程式。
Zn+2HCl = ZnCl2+H2↑
ZnO+2HCl = ZnCl2+H2O
Zn(OH)2+2HCl = ZnCl2+2H2O
ZnCO3+2HCl = ZnCl2+ H2O+CO2↑
思考:以硫酸为原料制取硫酸镁,你能有几种方法?
物质转化的规律
金属
金属氧化物
碱
盐
非金属
非金属氧化物
酸
盐
盐
盐
盐
盐
盐
物质转化规律图
一、非金属单质与其化合物的转化
实验:硫黄燃烧
观察外观:硫黄 是一种淡黄色的固体。
实验现象:硫在空气中燃烧,发出淡蓝色的火焰;在氧气中燃烧,发出明亮的蓝紫色火焰,生成的气体具有刺激性气味。
点燃
S+O2 ==== SO2
归纳:非金属单质能与氧气反应生成非金属氧化物
碳、磷在氧气中燃烧的化学方程式和现象
点燃
C+O2====CO2
点燃
2C+O2=====2CO
点燃
4P+5O2====2P2O5
碳在氧气中燃烧发出白光,生成能使澄清石灰水变浑浊的气体。同时产生大量的热量。碳在氧气不足的情况燃烧下,生成一氧化碳
白磷在氧气中燃烧,产生浓厚的白烟,同时产生大量的热量。
转化规律的运用
1、燃料燃烧:氢气燃烧、碳燃烧
点燃
C+O2====CO2
点燃
2C+O2=====2CO
点燃
2H2+O2====2H2O
2、用于除去气体中的氧气,
思考:白炽灯内少量氧气如何除去
白炽灯内加入少量磷,可除去灯泡内的少量氧气,防止钨丝氧化熔断。
点燃
4P+5O2====2P2O5
3、用于验证空气中氧气的体积分数
如下图所示装置,点燃红磷(过量),会发现红磷剧烈燃烧,产生 ,待瓶内气体冷却后打开止水夹,会发现水由烧杯流向集气瓶,进入集气瓶内水的体积约
大量白烟
占瓶内空气体积的1/5
CO2 +H2O=H2CO3
碳酸使蓝色石蕊试液变红色。
H2CO3 = H2O + CO2↑
碳酸不稳定,易分解。
二、非金属氧化物与酸间的相互转化
实验:取二支试管,分别加入蒸馏水,然后向其中一支通入二氧化碳气体,再分别滴入几滴石蕊试液。观察实验现象
实验现象:通入二氧化碳的那支试管中的紫色石蕊试液变红色
结论:CO2+H2O = H2CO3
将变红的那支试管加热,观察实验现象
实验现象:原来变红的溶液重新变为紫色。
结论: H2CO3 = CO2+H2O
归纳:非金属氧化物与酸间的相互转化规律:
非金属氧化物 水 酸
注意:二氧化硅不能与水反应生成硅酸,一氧化碳也不与水反应。
(SiO2+H2O →不反应)
练习
1、N2O5 +H2O=
2、SO2 +H20=
3、SO3 +H2O=
4、P2O5 +H2O=
注意:在转化过程中要特别注意化合价的问题。非金属氧化物与酸间的相互转化中化合价是不变的。
思考:
A、将下列物质放入水中,哪一种物质的与水反应会使溶液的PH值下降:二氧化硫、二氧化硅、氧化钙;
B、8克三氧化硫溶解于92克水中所得溶液的溶质质量分数是8%吗?
6.4克二氧化硫溶于93.6克水中,所得溶液溶质的质量分数为多少?
思 考
解:
由于SO2与H2O反应得到H2SO3,所以溶质是H2SO3。设H2SO3的质量分数为x
SO2 + H2O = H2SO3
64 82
(6.4g+93.6g)x
6.4g
三、酸与盐之间的转化
实验:向稀硫酸中分别倒入氧化铜、氢氧化铜、碳酸铜中,观察实验现象
实验现象:三种不溶于水的物质慢慢消失,并有蓝色溶液生成。
结论:
Cu(OH)2+H2SO4 = CuSO4+2H2O
CuO+H2SO4 = CuSO4+H2O
CuCO3+ H2SO4 = CuSO4+H2O+CO2↑
非金属氧化物
非金属
酸
盐
C
CO2
H2CO3
CaCO3
C + O2 = CO2
点燃
CO2 + H2O = H2CO3
H2CO3 +Ca(OH)2 = CaCO3↓+2H2O
非金属
非金属氧化物
酸
盐
S
SO2
H2SO3
Na2SO3
S + O2 = SO2
点燃
SO2 + H2O = H2SO3
H2SO3 + 2NaOH = Na2SO3 + H2O
非金属氧化物
非金属
酸
盐
P
P2O5
H3PO4
Ca3(PO4)2
4P + 5O2 = 2P2O5
点燃
P2O5 + 3H2O = 2H3PO4
2H3PO4+3Ca(OH)2=Ca3(PO4)2↓+6H2O
(红色)
(白色)
(白色)
非金属氧化物
非金属
酸
盐
非金属+氧气→非金属氧化物
非金属氧化物+水→含氧酸
酸→非金属氧化物+水
某些金属+某些酸→盐+氢气
酸+金属氧化物→盐+水
酸+碱→盐+水
酸+某些盐→另一种酸+另一种盐
例:写出以盐酸为原料制取氯化锌的化学反应方程式。
Zn+2HCl = ZnCl2+H2↑
ZnO+2HCl = ZnCl2+H2O
Zn(OH)2+2HCl = ZnCl2+2H2O
ZnCO3+2HCl = ZnCl2+ H2O+CO2↑
思考:以硫酸为原料制取硫酸镁,你能有几种方法?
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
