人教版(五四制)九年级全一册化学 第二单元 课题2 溶解度 第二课时(课件)(20张PPT)
文档属性
| 名称 | 人教版(五四制)九年级全一册化学 第二单元 课题2 溶解度 第二课时(课件)(20张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 18.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-19 00:00:00 | ||
图片预览








文档简介
(共20张PPT)
溶解度(第二课时)
如何比较两种物质的溶解能力大小
20 ℃
40 ℃
NaCl
KNO3
20g水
100g水
NaCl
KNO3
10gNaCl
10gKNO3
20g水
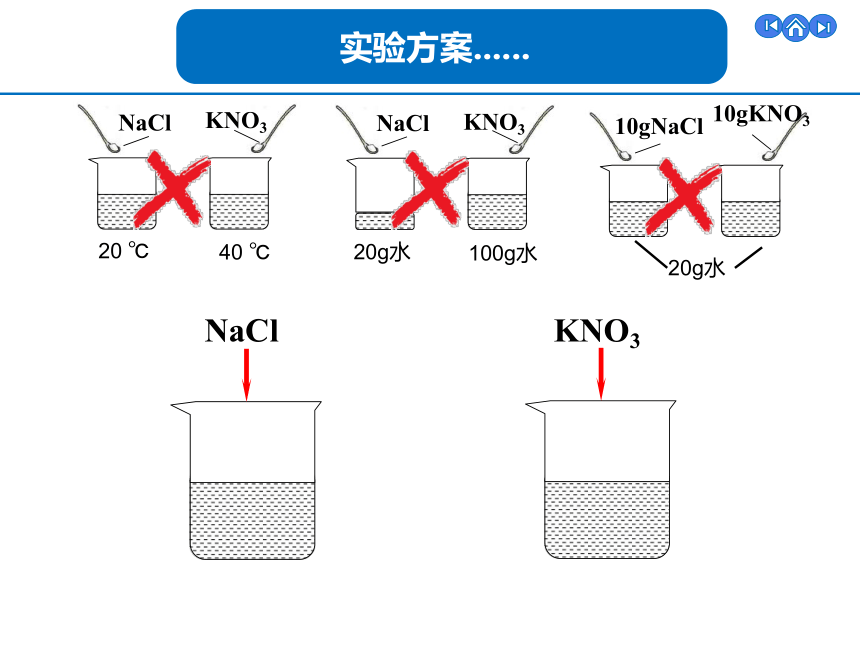
实验方案......
NaCl
KNO3
定义:
在一定温度下,
某固态物质在100g溶剂里
达到饱和状态时
所溶解的溶质质量
,单位:g。
一、固体物质的溶解度(S)
化学上,为了方便比较物质的溶解能力,引入了溶解度的概念。
固体物质的溶解度(S)
①在20 ℃时, NaCl在水中溶解度为36g,所以在20 ℃时,100 g水中最多溶解36g的NaCl。
根据固体物质的溶解度定义,判断下列说法是否正确
注意:描述溶解度一定要指明温度
②在20 ℃时,NaCl在水中溶解度为36g,所以100 g水中溶解了36gNaCl,溶液一定达到饱和。
溶解度与溶质、溶剂的 有关,与其质量无关
温馨提示
同一种物质的溶解度只要 不变,溶解度就是个定值。
③31.6gKNO3溶解在100g水中恰好得到饱和溶液,所以KNO3的溶解度为31.6g。
④在20 ℃时,10g水中最多能溶解3.16g KNO3,所以20 ℃时KNO3的溶解度是31.6g。
固体物质的溶解度(S)
根据固体物质的溶解度定义,判断下列说法是否正确
本身性质
温度
固体物质的溶解度(S)
( )( ) ( ) ( )
0.01 1 10 20 ℃ S/g
、 、 、
易溶
难溶
微溶
可溶
易溶
难溶
微溶
可溶
溶解度与溶解性的关系
定性
定量
温度/℃ 0 10 20 30 40 50 60 70 80 85 90 100
溶解度/g NaCl 35.7 35.8 36.0 36.3 36.6 37.0 37.3 37.8 38.4 39.0 39.8
KNO3 13.3 20.9 31.6 45.8 63.9 85.5 110 138 169 202 246
二、溶解度的表示方法
1.溶解度数据表
溶解度随温度变化的表示方法
溶解度的表示方法
温度/℃ 0 10 20 30 40 50 60 70 80 85 90 100
溶解度/g KNO3 13.3 20.9 31.6 45.8 63.9 85.5 110 138 169 202 246
185
2.溶解度曲线
溶解度的表示方法
温度℃ 0 10 20 30 40 50 60 70 80 85 90 100
溶解度/g KNO3 13.3 20.9 31.6 45.8 63.9 85.5 110 138 169 202 246
185
饱和
(有固体剩余)
C
饱和
A
不饱和
B
溶解度的表示方法
两条线交点有何含义?
60℃时,a,b两物质的溶解度相等,均为52g
溶解度的表示方法
陡升型
平缓型
观察两组溶解度曲线图片,溶解度随温度变化有何规律?
Ca(OH)2的溶解度曲线
下降型
溶解度的表示方法
讨论:两种溶解度的表示方法有什么不同?
三、溶解度曲线的应用
1、要使硝酸钾从其饱和溶液中析出晶体,最好用什么方法?为什么?
硝酸钾
氯化钠
温度℃
溶解度(g)
结晶方法
2、海水晒盐用的什么方法结晶?为什么?
溶解度曲线的应用
物质的分离提纯
硝酸钾固体中含有少量氯化钠,提纯硝酸钾流程图
混合物
加热
适量水
热饱和
溶液
降温
结晶
过滤
滤渣:KNO3固体
滤液:NaCl
KNO3
你能说出该方法的原理吗?
溶解度数据表
定义
一定温度
总结
固体物质的溶解度
溶解度曲线图
100g溶剂
饱和状态
单位:g
表示
方法
感
谢
聆
听
溶解度(第二课时)
如何比较两种物质的溶解能力大小
20 ℃
40 ℃
NaCl
KNO3
20g水
100g水
NaCl
KNO3
10gNaCl
10gKNO3
20g水
实验方案......
NaCl
KNO3
定义:
在一定温度下,
某固态物质在100g溶剂里
达到饱和状态时
所溶解的溶质质量
,单位:g。
一、固体物质的溶解度(S)
化学上,为了方便比较物质的溶解能力,引入了溶解度的概念。
固体物质的溶解度(S)
①在20 ℃时, NaCl在水中溶解度为36g,所以在20 ℃时,100 g水中最多溶解36g的NaCl。
根据固体物质的溶解度定义,判断下列说法是否正确
注意:描述溶解度一定要指明温度
②在20 ℃时,NaCl在水中溶解度为36g,所以100 g水中溶解了36gNaCl,溶液一定达到饱和。
溶解度与溶质、溶剂的 有关,与其质量无关
温馨提示
同一种物质的溶解度只要 不变,溶解度就是个定值。
③31.6gKNO3溶解在100g水中恰好得到饱和溶液,所以KNO3的溶解度为31.6g。
④在20 ℃时,10g水中最多能溶解3.16g KNO3,所以20 ℃时KNO3的溶解度是31.6g。
固体物质的溶解度(S)
根据固体物质的溶解度定义,判断下列说法是否正确
本身性质
温度
固体物质的溶解度(S)
( )( ) ( ) ( )
0.01 1 10 20 ℃ S/g
、 、 、
易溶
难溶
微溶
可溶
易溶
难溶
微溶
可溶
溶解度与溶解性的关系
定性
定量
温度/℃ 0 10 20 30 40 50 60 70 80 85 90 100
溶解度/g NaCl 35.7 35.8 36.0 36.3 36.6 37.0 37.3 37.8 38.4 39.0 39.8
KNO3 13.3 20.9 31.6 45.8 63.9 85.5 110 138 169 202 246
二、溶解度的表示方法
1.溶解度数据表
溶解度随温度变化的表示方法
溶解度的表示方法
温度/℃ 0 10 20 30 40 50 60 70 80 85 90 100
溶解度/g KNO3 13.3 20.9 31.6 45.8 63.9 85.5 110 138 169 202 246
185
2.溶解度曲线
溶解度的表示方法
温度℃ 0 10 20 30 40 50 60 70 80 85 90 100
溶解度/g KNO3 13.3 20.9 31.6 45.8 63.9 85.5 110 138 169 202 246
185
饱和
(有固体剩余)
C
饱和
A
不饱和
B
溶解度的表示方法
两条线交点有何含义?
60℃时,a,b两物质的溶解度相等,均为52g
溶解度的表示方法
陡升型
平缓型
观察两组溶解度曲线图片,溶解度随温度变化有何规律?
Ca(OH)2的溶解度曲线
下降型
溶解度的表示方法
讨论:两种溶解度的表示方法有什么不同?
三、溶解度曲线的应用
1、要使硝酸钾从其饱和溶液中析出晶体,最好用什么方法?为什么?
硝酸钾
氯化钠
温度℃
溶解度(g)
结晶方法
2、海水晒盐用的什么方法结晶?为什么?
溶解度曲线的应用
物质的分离提纯
硝酸钾固体中含有少量氯化钠,提纯硝酸钾流程图
混合物
加热
适量水
热饱和
溶液
降温
结晶
过滤
滤渣:KNO3固体
滤液:NaCl
KNO3
你能说出该方法的原理吗?
溶解度数据表
定义
一定温度
总结
固体物质的溶解度
溶解度曲线图
100g溶剂
饱和状态
单位:g
表示
方法
感
谢
聆
听
同课章节目录
- 第一单元 金属和金属材料
- 课题1 金属材料
- 课题2 金属的化学性质
- 课题3 金属资源的利用和保护
- 实验活动1 金属的物理性质和某些化学性质
- 第二单元 溶液
- 课题1 溶液的形成
- 课题2 溶解度
- 课题3 溶液的浓度
- 实验活动2 一定溶质质量分数的氯化钠溶液的配制
- 第三单元 酸和碱
- 课题1 常见的酸和碱
- 课题2 酸和碱的中和反应
- 实验活动3 酸、碱的化学性质
- 实验活动4 溶液酸碱性的检验
- 第四单元 盐 化肥
- 课题1 生活中常见的盐
- 课题2 化学肥料
- 实验活动5 粗盐中难溶性杂志的去除
- 第五单元 化学与生活
- 课题1 人类重要的营养物质
- 课题2 化学元素与人体健康
- 课题3 有机合成材料
- 旧版目录
- 课题3 溶质的质量分数
- 课题2 酸和碱之间会发生什么反应
