实验活动2二氧化碳的实验室制取与性质课后练习--2021-2022学年九年级化学人教版上册(有答案)
文档属性
| 名称 | 实验活动2二氧化碳的实验室制取与性质课后练习--2021-2022学年九年级化学人教版上册(有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 190.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-19 00:00:00 | ||
图片预览


文档简介
2021——2022学年度人教版九年级化学上册 实验活动2二氧化碳的实验室制取与性质 课后练习
一、选择题
1.下列说法正确的是( )
A.二氧化碳无毒,可以供给呼吸
B.用澄清石灰水浸泡鸡蛋可以保鲜
C.某物质完全燃烧后生成二氧化碳,则该物质一定是由碳、氧元素组成的
D.将燃着的木条伸入充满某气体的集气瓶中,木条熄灭,则该气体一定是二氧化碳
2.下列实验现象描述正确的是( )
A.红磷燃烧后生成大量白雾 B.铁丝伸入盛有氧气的集气瓶中剧烈燃烧
C.CO燃烧时,发出蓝色的火焰 D.二氧化碳气体能使干燥的石蕊试液染成的小花变红
3.化学实验中常用到木条,下列实验中木条的使用不能达到目的是( )
A.用带火星的木条检验氧气 B.用小木条比较酒精灯火焰各层的温度
C.将燃着的木条放在集气瓶口,检验二氧化碳是否集满 D.用燃着的木条区别氨气和二氧化碳
4.要除去二氧化碳气体中混有的一氧化碳气体,最好的方法是:( )
A.使气体通过灼热的焦炭 B.使气流缓慢的通过足量的澄清石灰水
C.使气体通过灼热的氧化铜 D.通入氧气流点燃
5.下列有关化学反应的说法不正确的是( )
A.化学反应前后,元素的化合价可能会发生改变
B.2gH2与18gO2充分反应可生成20g水,这符合质量守恒定律
C.一氧化碳燃烧,反应物的化学计量数之比:v(CO):v(O2):=2:1
D.二氧化碳灭火实验能说明二氧化碳不助燃、不可燃、密度大于空气
6.期末复习阶段,某同学梳理了以下知识:①具有相同质子数的粒子属于同种元素;②催化剂一定能加快化学反应的速率;③由同种元素组成的物质一定是单质;④物质与氧气发生的反应属于氧化反应;⑤最外层电子数是8个电子的相对稳定结构的粒子不一定是稀有气体的原子;⑥二氧化碳能灭火是因为不能燃烧也不能支持燃烧且密度比空气大,而用水灭火是因为可降低可燃物的着火点。其中你认为正确的个数是( )
A.2 B.3 C.4 D.5
7.有关如图实验的说法中,正确的是( )
A.观察到高处蜡烛先熄灭 B.观察到二氧化碳为无色气体
C.该实验证明二氧化碳密度比空气小 D.蜡烛熄灭的原因是温度降低到蜡烛着火点以下
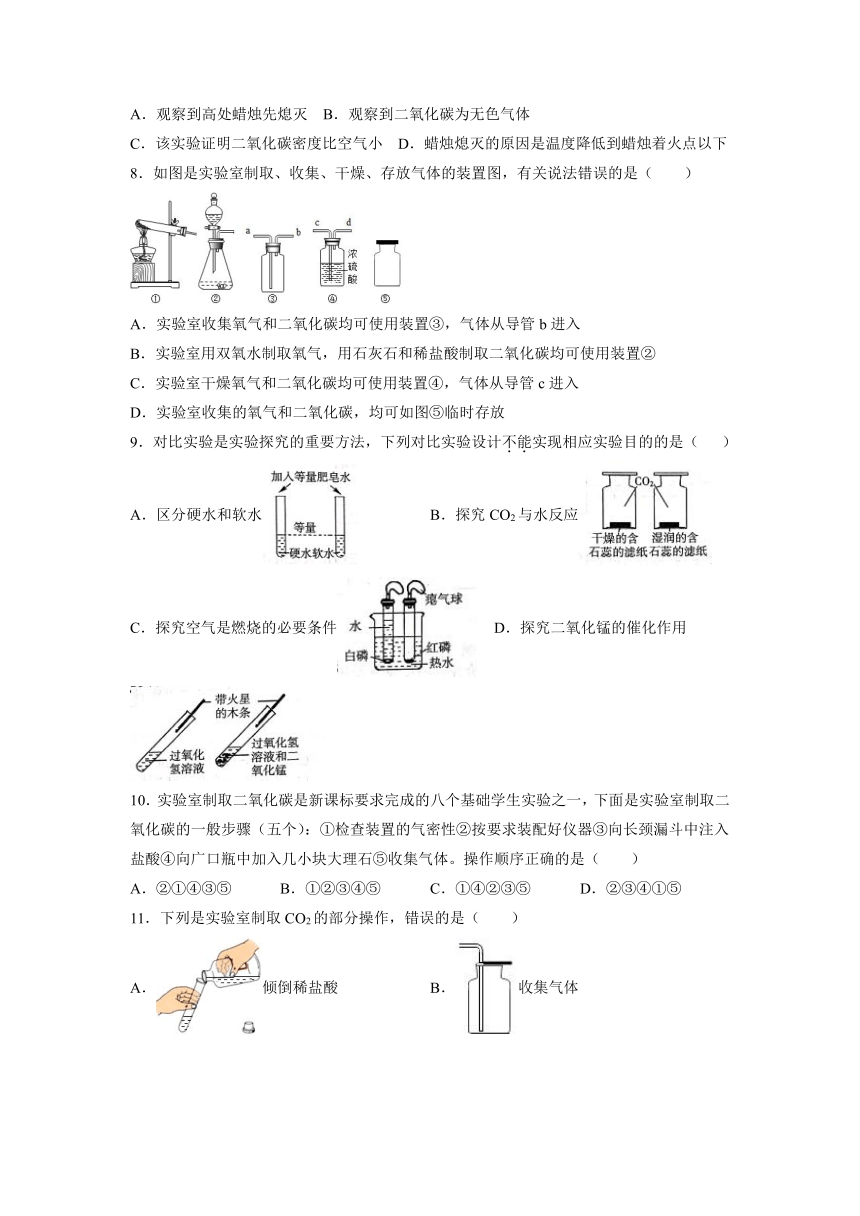
8.如图是实验室制取、收集、干燥、存放气体的装置图,有关说法错误的是( )
A.实验室收集氧气和二氧化碳均可使用装置③,气体从导管b进入
B.实验室用双氧水制取氧气,用石灰石和稀盐酸制取二氧化碳均可使用装置②
C.实验室干燥氧气和二氧化碳均可使用装置④,气体从导管c进入
D.实验室收集的氧气和二氧化碳,均可如图⑤临时存放
9.对比实验是实验探究的重要方法,下列对比实验设计不能实现相应实验目的的是( )
A.区分硬水和软水 B.探究CO2与水反应
C.探究空气是燃烧的必要条件 D.探究二氧化锰的催化作用
10.实验室制取二氧化碳是新课标要求完成的八个基础学生实验之一,下面是实验室制取二氧化碳的一般步骤(五个):①检查装置的气密性②按要求装配好仪器③向长颈漏斗中注入盐酸④向广口瓶中加入几小块大理石⑤收集气体。操作顺序正确的是( )
A.②①④③⑤ B.①②③④⑤ C.①④②③⑤ D.②③④①⑤
11.下列是实验室制取CO2的部分操作,错误的是( )
A.倾倒稀盐酸 B.收集气体
C.检查气密性 D.验满
12.现有甲乙丙三种气体,如下图,将乙气体倒入放有填充空气气球的一个空烧杯里,发现气球飘起来了,把分别盛满甲、丙气体的试管倒插入盛有水的烧杯中,一段时间后,观察到如图所示的现象,对甲、乙、丙气体的分析正确的是
A.甲气体可以用排水法收集 B.丙气体只能用排气法收集
C.若乙气体可以用排气法收集,则一定是向下排空气法 D.不能确定乙气体是否可以用排水法收集
13.如图为改良版的“验证二氧化碳化学性质”的实验装置。用一根铁丝穿4片紫色石蕊试纸,按图示将稀硫酸和水滴加到相应的试纸上,下列说法错误的是
A.图中1、3变为红色,2、4不变色
B.若将稀硫酸换成稀醋酸也可以得到正确的实验结果
C.该实验证明二氧化碳能与石蕊发生反应生成红色物质
D.该实验的优点是将四个实验改成一个实验,对比性强
14.气体X可能含有氢气、一氧化碳和二氧化碳中的一种或几种。将气体X依次通过灼热氧化铜和澄清石灰水,观察到黑色固体变红、澄清石灰水变浑浊,气体X组成的可能性有
A.2种 B.3种 C.4种 D.5种
二、填空题
15.写出下列反应的化学方程式:
(1)碳在氧气中充分燃烧_____
(2)实验室用双氧水制氧气_____
(3)二氧化碳与水反应_____
16.如图所示实验中,①、④为用紫色石蕊溶液润湿的棉球,②、③为用石蕊溶液染成紫色的干燥棉球。实验现象是:④比①先变红,②、③始终不变红。
(1)由此可得出CO2的相关性质有_____
A 不能燃烧,也不支持燃烧 B 能与水反应
C 能与石蕊反应 D 密度比空气大
(2)②、③棉花球不变红的原因是_____。
17.向盛有紫色石蕊试液的试管中通入适量的CO2,紫色石蕊试液变为____色,其反应的化学方程式为:__________________________,将反应后的溶液加热,则溶液最终变为______色。
18.将一个充满CO2的试管倒插在澄清石灰水的烧杯里,可观察到的现象是:________;________.
19.燃着的两支短蜡烛放在两个高低阶梯上,沿着烧杯倾倒二氧化碳,观察 到_____.这说明二氧化碳的两个性质,即_____、_____.
20.已知A、B、C、D、E是初中化学常见的五种不同物质,A、E是空气中常见的气体,其中A在空气中的含量为21%,B在常温下为液体。(说明:“—”表示相连的两种物质能发生化学反应,“→”表示相连的两种物质能向箭头所指方向转化)。试根据如图所示的关系回答下列问题:
写出有关物质的化学式:C_______,D_____,E_________。
三、简答题
21.今年5月中俄签署了东线天然气合作协议.天然气不充分燃烧时会产生炭黑或一氧化碳.
(1)CO具有可燃性,写出其在工业上的一种具体用途_____.
(2)CO与CO2可以相互转化.用化学方程式为_____.
(3)将CO2通入紫色石蕊溶液中,溶液变红的原因是(用化学方程式表示)_____.
22.为了研究动物的呼吸作用,某兴趣小组设计了如图所示装置进行探究。同学们观察到实验过程中红墨水向左移动,澄清石灰水变浑浊,实验结束后,把燃着的木条放到瓶中,木条熄灭。这些现象说明动物呼吸入________气体,呼出_________气体。
23.如图所示,在一去盖塑料瓶上打3个孔,在一根细铁丝上穿2张用紫色石蕊溶液浸泡过的纸条(其中一干、一湿)放入塑料瓶中,在塑料瓶外点燃高低两支蜡烛,火焰分别与高低两个孔持平,通入CO2。
(1)两张纸条出现的现象是______,其原因是______。
(2)低蜡烛先熄灭,高蜡烛后熄灭,说明二氧化碳具有的性质是______。
24.碳及其化合物在生产、生活中应用广泛。
(1)二氧化碳是植物光合作用的原料,检验二氧化碳发生反应的化学方程式为______________。
(2)电石的主要成分碳化钙(CaC2),遇水发生剧烈反应,放出热量,生成乙炔(C2H2)气体和另一种化合物,反应的化学方程式为_____________。
四、综合应用题
25.请根据本小题A、B两图回答下列问题。
(1)仪器a的名称是________________________。
(2)锥形瓶内的反应进行较长时间后,用燃着的火柴放在集气瓶口,火焰仍不熄灭的原因是 ___________________。
(3)如B图所示,将一瓶二氧化碳气体慢慢倒入放着蜡烛的烧杯中,发现上层蜡烛先熄灭, 试解释原因。答:_________________。
(4)某化学兴趣小组为了测定当地矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水。)有关实验数据如下表:
反应前 反应后
实验数据 烧杯和稀盐酸的质量 石灰石样品的质量 烧杯及剩余物的质量
150 g 12 g 157.6 g
①根据质量守恒定律可知,反应中生成二氧化碳的质量为___________________。
② 求该石灰石中碳酸钙的质量为___________________。
③求该石灰石中碳酸钙的质量分数为___________________。
【参考答案】
1.B 2.C 3.D 4.C 5.B 6.A 7.B 8.A 9.C 10.A 11.D 12.D 13.C 14.D
15.
16.BD 二氧化碳不能与石蕊反应
17.红 CO2+H2O===H2CO3 紫
18.澄清石灰水变浑浊;试管内的液面上升
19.底层蜡烛先熄灭密度比空气的较大不燃烧,也不支持燃烧
20.H2 H2O2 CO2
21.作燃料; CO2+C高温2CO、2CO+O2点燃2CO2(合理即可); CO2+H2O═H2CO3.
22.氧气 ; 二氧化碳
23.干纸条无明显变化,湿纸条变红 二氧化碳与水反应生成碳酸 不支持燃烧、不能燃烧、密度比空气大
24.CO2+Ca(OH)2=== CaCO3↓+H2O CaC2+2H2O=== Ca(OH)2+C2H2↑
25.长颈漏斗 气体从长颈漏斗逸出(装置气密性不好) 二氧化碳气体直接倒在上层火焰上 4.4g 10g 83.3%
一、选择题
1.下列说法正确的是( )
A.二氧化碳无毒,可以供给呼吸
B.用澄清石灰水浸泡鸡蛋可以保鲜
C.某物质完全燃烧后生成二氧化碳,则该物质一定是由碳、氧元素组成的
D.将燃着的木条伸入充满某气体的集气瓶中,木条熄灭,则该气体一定是二氧化碳
2.下列实验现象描述正确的是( )
A.红磷燃烧后生成大量白雾 B.铁丝伸入盛有氧气的集气瓶中剧烈燃烧
C.CO燃烧时,发出蓝色的火焰 D.二氧化碳气体能使干燥的石蕊试液染成的小花变红
3.化学实验中常用到木条,下列实验中木条的使用不能达到目的是( )
A.用带火星的木条检验氧气 B.用小木条比较酒精灯火焰各层的温度
C.将燃着的木条放在集气瓶口,检验二氧化碳是否集满 D.用燃着的木条区别氨气和二氧化碳
4.要除去二氧化碳气体中混有的一氧化碳气体,最好的方法是:( )
A.使气体通过灼热的焦炭 B.使气流缓慢的通过足量的澄清石灰水
C.使气体通过灼热的氧化铜 D.通入氧气流点燃
5.下列有关化学反应的说法不正确的是( )
A.化学反应前后,元素的化合价可能会发生改变
B.2gH2与18gO2充分反应可生成20g水,这符合质量守恒定律
C.一氧化碳燃烧,反应物的化学计量数之比:v(CO):v(O2):=2:1
D.二氧化碳灭火实验能说明二氧化碳不助燃、不可燃、密度大于空气
6.期末复习阶段,某同学梳理了以下知识:①具有相同质子数的粒子属于同种元素;②催化剂一定能加快化学反应的速率;③由同种元素组成的物质一定是单质;④物质与氧气发生的反应属于氧化反应;⑤最外层电子数是8个电子的相对稳定结构的粒子不一定是稀有气体的原子;⑥二氧化碳能灭火是因为不能燃烧也不能支持燃烧且密度比空气大,而用水灭火是因为可降低可燃物的着火点。其中你认为正确的个数是( )
A.2 B.3 C.4 D.5
7.有关如图实验的说法中,正确的是( )
A.观察到高处蜡烛先熄灭 B.观察到二氧化碳为无色气体
C.该实验证明二氧化碳密度比空气小 D.蜡烛熄灭的原因是温度降低到蜡烛着火点以下
8.如图是实验室制取、收集、干燥、存放气体的装置图,有关说法错误的是( )
A.实验室收集氧气和二氧化碳均可使用装置③,气体从导管b进入
B.实验室用双氧水制取氧气,用石灰石和稀盐酸制取二氧化碳均可使用装置②
C.实验室干燥氧气和二氧化碳均可使用装置④,气体从导管c进入
D.实验室收集的氧气和二氧化碳,均可如图⑤临时存放
9.对比实验是实验探究的重要方法,下列对比实验设计不能实现相应实验目的的是( )
A.区分硬水和软水 B.探究CO2与水反应
C.探究空气是燃烧的必要条件 D.探究二氧化锰的催化作用
10.实验室制取二氧化碳是新课标要求完成的八个基础学生实验之一,下面是实验室制取二氧化碳的一般步骤(五个):①检查装置的气密性②按要求装配好仪器③向长颈漏斗中注入盐酸④向广口瓶中加入几小块大理石⑤收集气体。操作顺序正确的是( )
A.②①④③⑤ B.①②③④⑤ C.①④②③⑤ D.②③④①⑤
11.下列是实验室制取CO2的部分操作,错误的是( )
A.倾倒稀盐酸 B.收集气体
C.检查气密性 D.验满
12.现有甲乙丙三种气体,如下图,将乙气体倒入放有填充空气气球的一个空烧杯里,发现气球飘起来了,把分别盛满甲、丙气体的试管倒插入盛有水的烧杯中,一段时间后,观察到如图所示的现象,对甲、乙、丙气体的分析正确的是
A.甲气体可以用排水法收集 B.丙气体只能用排气法收集
C.若乙气体可以用排气法收集,则一定是向下排空气法 D.不能确定乙气体是否可以用排水法收集
13.如图为改良版的“验证二氧化碳化学性质”的实验装置。用一根铁丝穿4片紫色石蕊试纸,按图示将稀硫酸和水滴加到相应的试纸上,下列说法错误的是
A.图中1、3变为红色,2、4不变色
B.若将稀硫酸换成稀醋酸也可以得到正确的实验结果
C.该实验证明二氧化碳能与石蕊发生反应生成红色物质
D.该实验的优点是将四个实验改成一个实验,对比性强
14.气体X可能含有氢气、一氧化碳和二氧化碳中的一种或几种。将气体X依次通过灼热氧化铜和澄清石灰水,观察到黑色固体变红、澄清石灰水变浑浊,气体X组成的可能性有
A.2种 B.3种 C.4种 D.5种
二、填空题
15.写出下列反应的化学方程式:
(1)碳在氧气中充分燃烧_____
(2)实验室用双氧水制氧气_____
(3)二氧化碳与水反应_____
16.如图所示实验中,①、④为用紫色石蕊溶液润湿的棉球,②、③为用石蕊溶液染成紫色的干燥棉球。实验现象是:④比①先变红,②、③始终不变红。
(1)由此可得出CO2的相关性质有_____
A 不能燃烧,也不支持燃烧 B 能与水反应
C 能与石蕊反应 D 密度比空气大
(2)②、③棉花球不变红的原因是_____。
17.向盛有紫色石蕊试液的试管中通入适量的CO2,紫色石蕊试液变为____色,其反应的化学方程式为:__________________________,将反应后的溶液加热,则溶液最终变为______色。
18.将一个充满CO2的试管倒插在澄清石灰水的烧杯里,可观察到的现象是:________;________.
19.燃着的两支短蜡烛放在两个高低阶梯上,沿着烧杯倾倒二氧化碳,观察 到_____.这说明二氧化碳的两个性质,即_____、_____.
20.已知A、B、C、D、E是初中化学常见的五种不同物质,A、E是空气中常见的气体,其中A在空气中的含量为21%,B在常温下为液体。(说明:“—”表示相连的两种物质能发生化学反应,“→”表示相连的两种物质能向箭头所指方向转化)。试根据如图所示的关系回答下列问题:
写出有关物质的化学式:C_______,D_____,E_________。
三、简答题
21.今年5月中俄签署了东线天然气合作协议.天然气不充分燃烧时会产生炭黑或一氧化碳.
(1)CO具有可燃性,写出其在工业上的一种具体用途_____.
(2)CO与CO2可以相互转化.用化学方程式为_____.
(3)将CO2通入紫色石蕊溶液中,溶液变红的原因是(用化学方程式表示)_____.
22.为了研究动物的呼吸作用,某兴趣小组设计了如图所示装置进行探究。同学们观察到实验过程中红墨水向左移动,澄清石灰水变浑浊,实验结束后,把燃着的木条放到瓶中,木条熄灭。这些现象说明动物呼吸入________气体,呼出_________气体。
23.如图所示,在一去盖塑料瓶上打3个孔,在一根细铁丝上穿2张用紫色石蕊溶液浸泡过的纸条(其中一干、一湿)放入塑料瓶中,在塑料瓶外点燃高低两支蜡烛,火焰分别与高低两个孔持平,通入CO2。
(1)两张纸条出现的现象是______,其原因是______。
(2)低蜡烛先熄灭,高蜡烛后熄灭,说明二氧化碳具有的性质是______。
24.碳及其化合物在生产、生活中应用广泛。
(1)二氧化碳是植物光合作用的原料,检验二氧化碳发生反应的化学方程式为______________。
(2)电石的主要成分碳化钙(CaC2),遇水发生剧烈反应,放出热量,生成乙炔(C2H2)气体和另一种化合物,反应的化学方程式为_____________。
四、综合应用题
25.请根据本小题A、B两图回答下列问题。
(1)仪器a的名称是________________________。
(2)锥形瓶内的反应进行较长时间后,用燃着的火柴放在集气瓶口,火焰仍不熄灭的原因是 ___________________。
(3)如B图所示,将一瓶二氧化碳气体慢慢倒入放着蜡烛的烧杯中,发现上层蜡烛先熄灭, 试解释原因。答:_________________。
(4)某化学兴趣小组为了测定当地矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水。)有关实验数据如下表:
反应前 反应后
实验数据 烧杯和稀盐酸的质量 石灰石样品的质量 烧杯及剩余物的质量
150 g 12 g 157.6 g
①根据质量守恒定律可知,反应中生成二氧化碳的质量为___________________。
② 求该石灰石中碳酸钙的质量为___________________。
③求该石灰石中碳酸钙的质量分数为___________________。
【参考答案】
1.B 2.C 3.D 4.C 5.B 6.A 7.B 8.A 9.C 10.A 11.D 12.D 13.C 14.D
15.
16.BD 二氧化碳不能与石蕊反应
17.红 CO2+H2O===H2CO3 紫
18.澄清石灰水变浑浊;试管内的液面上升
19.底层蜡烛先熄灭密度比空气的较大不燃烧,也不支持燃烧
20.H2 H2O2 CO2
21.作燃料; CO2+C高温2CO、2CO+O2点燃2CO2(合理即可); CO2+H2O═H2CO3.
22.氧气 ; 二氧化碳
23.干纸条无明显变化,湿纸条变红 二氧化碳与水反应生成碳酸 不支持燃烧、不能燃烧、密度比空气大
24.CO2+Ca(OH)2=== CaCO3↓+H2O CaC2+2H2O=== Ca(OH)2+C2H2↑
25.长颈漏斗 气体从长颈漏斗逸出(装置气密性不好) 二氧化碳气体直接倒在上层火焰上 4.4g 10g 83.3%
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
