人教版化学九年级下册 10.1.2 酸的化学性质 同步课件(14张PPT)
文档属性
| 名称 | 人教版化学九年级下册 10.1.2 酸的化学性质 同步课件(14张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.3MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-12-07 00:00:00 | ||
图片预览




文档简介
(共14张PPT)
空白演示
单击输入您的封面副标题
九年级化学下册(RJ)
教学课件
第十单元 酸和碱
课题1 常见的酸和碱
第2课时 酸的化学性质
在不借用试剂的前提下,你可以使紫色的石蕊变成红色吗
紫色石蕊试液为什么变色?
除了碳酸,还有其他物质能使紫色石蕊试液变红吗?
石蕊试液
导入新课
1.知道稀盐酸和稀硫酸能使指示剂变色;
2.知道金属与稀盐酸、稀硫酸反应;
3.知道稀酸与金属氧化物反应。
学习目标
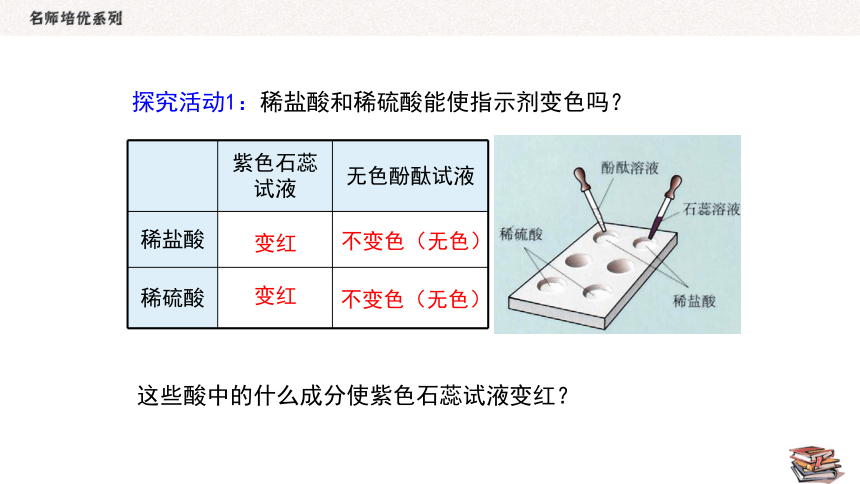
探究活动1:稀盐酸和稀硫酸能使指示剂变色吗?
这些酸中的什么成分使紫色石蕊试液变红?
紫色石蕊试液 无色酚酞试液
稀盐酸
稀硫酸
变红
变红
不变色(无色)
不变色(无色)
思考:现有两瓶未贴标签的稀盐酸和氯化钠溶液,如何区分?
小结:
NaCl溶液中有Cl-,而NaCl溶液不能使石蕊溶液变红,那么也不是Cl-的作用;应该是酸中的H+使石蕊溶液变红。
温馨提示:氯化钠溶液呈中性
你能否将这种方法推广一下,区别稀硫酸和硫酸钠溶液,为什么?
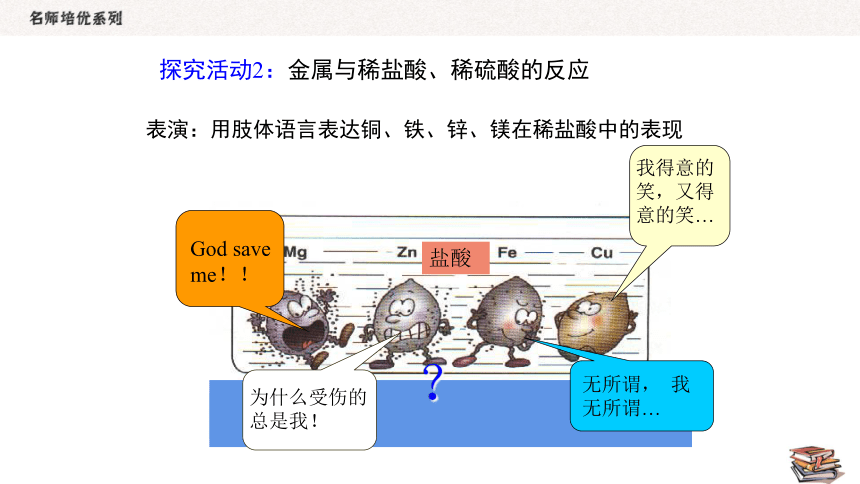
探究活动2:金属与稀盐酸、稀硫酸的反应
表演:用肢体语言表达铜、铁、锌、镁在稀盐酸中的表现
盐酸
God save me!!
无所谓, 我无所谓…
我得意的笑,又得意的笑…
为什么受伤的总是我!
?
与稀盐酸反应 与稀硫酸反应
镁
锌
铁
结论:酸能与较活泼的金属反应产生氢气
Mg +2 HCl = MgCl2 + H2↑
Zn +2 HCl = ZnCl2 + H2↑
Zn + H2SO4 = Zn SO4 + H2↑
Mg + H2SO4 = MgSO4 + H2↑
Fe + H2SO4 = Fe SO4 + H2↑
Fe +2 HCl = FeCl2 + H2↑
思考:
硫酸厂有一辆运输过浓硫酸的铁罐车(常温下,浓硫酸使铁表面生成一层致密的氧化膜,阻止铁与浓硫酸进一步反应),某新上岗的工人违反操作规定,边吸烟边用水冲洗该铁罐车,结果发生了爆炸事故。请以该厂技术员的身份分析一下发生爆炸的原因。
如何用化学方法清除铁锈?
探究活动3:稀酸与金属氧化物反应
温馨提示:应当实事求是的汇报实验现象,即是实验失败,也可以从失败的实验中得到教训。
小结:当酸不足或适量时,铁锈与酸反应;当酸过量时,与铁锈反应剩余的酸就会继续与铁反应。
从实验、观察、汇报及大家讨论中,你得到什么启示?
稀酸与金属氧化物的反应
现象 化学方程式
铁锈 + 稀盐酸
铁锈 + 稀硫酸
Fe2O3+6HCl=2FeCl3+3H2O
铁钉表面的铁锈被除去,溶液变为黄色
铁钉表面的铁锈被除去,溶液变为黄色
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
结论: 酸能与金属氧化物反应
思考:利用酸清除铁锈时,能否将金属制品长时间浸泡在酸中,为什么?
盐酸和硫酸为什么有这些相似的化学性质
交流讨论
HCl=H++Cl-
H2SO4=2H+ + SO4 2-
利用酸的性质做些什么
证据
性质
用途
拓展延伸
你能归纳出稀盐酸和稀硫酸有哪些相似的化学性质吗
③稀硫酸、盐酸都能与金属氧化物
反应,并生成水
①稀硫酸、稀盐酸都能与指示剂作用
②稀硫酸、稀盐酸都能与活动性较强
的金属发生置换反应,放出氢气
酸的化学性质
课堂小结
空白演示
单击输入您的封面副标题
九年级化学下册(RJ)
教学课件
第十单元 酸和碱
课题1 常见的酸和碱
第2课时 酸的化学性质
在不借用试剂的前提下,你可以使紫色的石蕊变成红色吗
紫色石蕊试液为什么变色?
除了碳酸,还有其他物质能使紫色石蕊试液变红吗?
石蕊试液
导入新课
1.知道稀盐酸和稀硫酸能使指示剂变色;
2.知道金属与稀盐酸、稀硫酸反应;
3.知道稀酸与金属氧化物反应。
学习目标
探究活动1:稀盐酸和稀硫酸能使指示剂变色吗?
这些酸中的什么成分使紫色石蕊试液变红?
紫色石蕊试液 无色酚酞试液
稀盐酸
稀硫酸
变红
变红
不变色(无色)
不变色(无色)
思考:现有两瓶未贴标签的稀盐酸和氯化钠溶液,如何区分?
小结:
NaCl溶液中有Cl-,而NaCl溶液不能使石蕊溶液变红,那么也不是Cl-的作用;应该是酸中的H+使石蕊溶液变红。
温馨提示:氯化钠溶液呈中性
你能否将这种方法推广一下,区别稀硫酸和硫酸钠溶液,为什么?
探究活动2:金属与稀盐酸、稀硫酸的反应
表演:用肢体语言表达铜、铁、锌、镁在稀盐酸中的表现
盐酸
God save me!!
无所谓, 我无所谓…
我得意的笑,又得意的笑…
为什么受伤的总是我!
?
与稀盐酸反应 与稀硫酸反应
镁
锌
铁
结论:酸能与较活泼的金属反应产生氢气
Mg +2 HCl = MgCl2 + H2↑
Zn +2 HCl = ZnCl2 + H2↑
Zn + H2SO4 = Zn SO4 + H2↑
Mg + H2SO4 = MgSO4 + H2↑
Fe + H2SO4 = Fe SO4 + H2↑
Fe +2 HCl = FeCl2 + H2↑
思考:
硫酸厂有一辆运输过浓硫酸的铁罐车(常温下,浓硫酸使铁表面生成一层致密的氧化膜,阻止铁与浓硫酸进一步反应),某新上岗的工人违反操作规定,边吸烟边用水冲洗该铁罐车,结果发生了爆炸事故。请以该厂技术员的身份分析一下发生爆炸的原因。
如何用化学方法清除铁锈?
探究活动3:稀酸与金属氧化物反应
温馨提示:应当实事求是的汇报实验现象,即是实验失败,也可以从失败的实验中得到教训。
小结:当酸不足或适量时,铁锈与酸反应;当酸过量时,与铁锈反应剩余的酸就会继续与铁反应。
从实验、观察、汇报及大家讨论中,你得到什么启示?
稀酸与金属氧化物的反应
现象 化学方程式
铁锈 + 稀盐酸
铁锈 + 稀硫酸
Fe2O3+6HCl=2FeCl3+3H2O
铁钉表面的铁锈被除去,溶液变为黄色
铁钉表面的铁锈被除去,溶液变为黄色
Fe2O3+3H2SO4=Fe2(SO4)3+3H2O
结论: 酸能与金属氧化物反应
思考:利用酸清除铁锈时,能否将金属制品长时间浸泡在酸中,为什么?
盐酸和硫酸为什么有这些相似的化学性质
交流讨论
HCl=H++Cl-
H2SO4=2H+ + SO4 2-
利用酸的性质做些什么
证据
性质
用途
拓展延伸
你能归纳出稀盐酸和稀硫酸有哪些相似的化学性质吗
③稀硫酸、盐酸都能与金属氧化物
反应,并生成水
①稀硫酸、稀盐酸都能与指示剂作用
②稀硫酸、稀盐酸都能与活动性较强
的金属发生置换反应,放出氢气
酸的化学性质
课堂小结
同课章节目录
