人教版化学九年级下册 9.1.1溶质的质量分数 同步课件(20张PPT)
文档属性
| 名称 | 人教版化学九年级下册 9.1.1溶质的质量分数 同步课件(20张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.9MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-12-07 00:00:00 | ||
图片预览







文档简介
(共20张PPT)
空白演示
单击输入您的封面副标题
九年级化学下册(RJ)
教学课件
第九单元 溶液
课题3 溶液的浓度
第1课时 溶质的质量分数
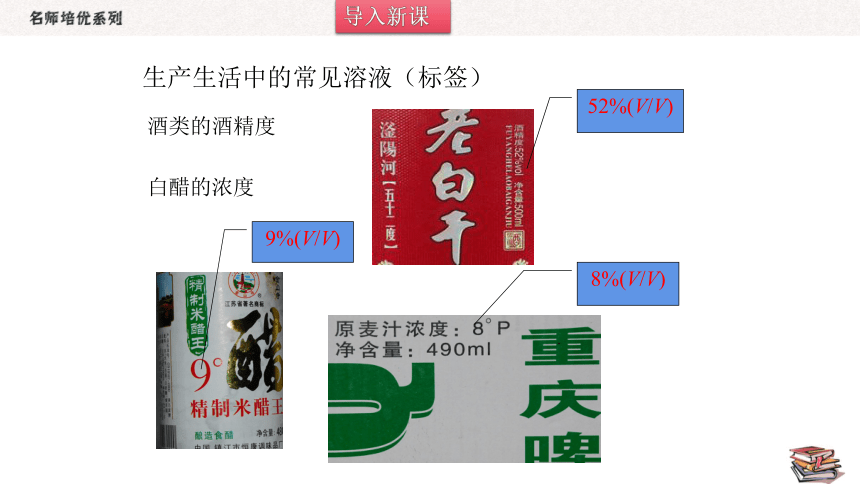
生产生活中的常见溶液(标签)
9%(V/V)
8%(V/V)
52%(V/V)
酒类的酒精度
白醋的浓度
导入新课
10%(m/V)
葡萄糖注射液的浓度
0.9%(m/V)
生理盐水中NaCl的含量
饮料中各种营养成分的含量(每100ml溶液中含某成分的质量)
化学试剂中溶质的含量(每100g溶液中含溶质的质量)
1.掌握溶液中溶质的质量分数的概念;
2.会计算有关溶质的质量分数。
学习目标
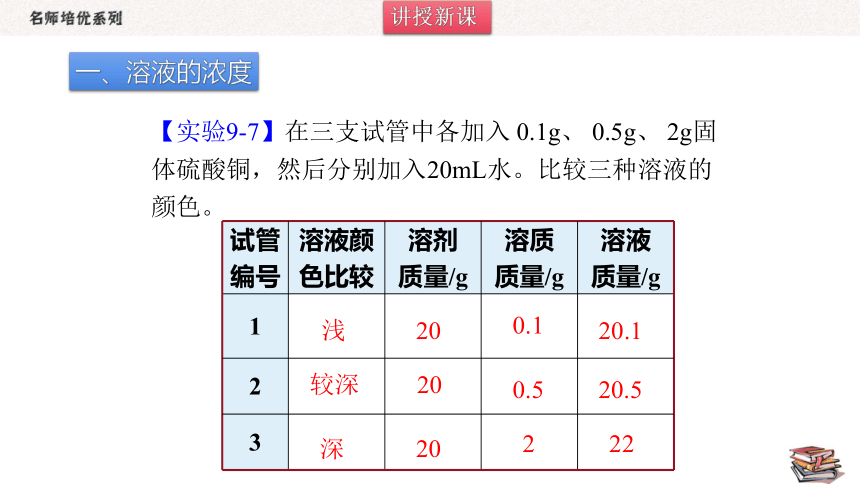
【实验9-7】在三支试管中各加入 0.1g、 0.5g、 2g固体硫酸铜,然后分别加入20mL水。比较三种溶液的颜色。
试管 编号 溶液颜 色比较 溶剂 质量/g 溶质 质量/g 溶液
质量/g
1
2
3
浅
较深
深
20
20
20
0.1
0.5
2
20.1
20.5
22
一、溶液的浓度
讲授新课
淡蓝 蓝色 深蓝
对于有色溶液来说,根据颜色的深浅可以区分溶液是浓还是稀。但这种方法比较粗略,不能准确地表明一定量的溶液里究竟含有多少溶质。
通过观察颜色来判断溶液的浓稀,仅仅是判断溶液浓稀粗略的方法。
我们应该学习商家向消费者介绍产品那样明确地表示出溶液的组成。其中表示溶液组成的方法有多种,这里主要认识溶质的质量分数。
讨论
溶质的质量分数
1.定义:溶质质量与溶液质量之比
2.公式:
溶质质量 = 溶液质量× 溶质的质量分数
溶质的质量分数
溶质的质量 /
溶液质量
=
=
溶液质量
溶质质量
溶质的质量分数
单位要统一
%
×100
+
=
溶剂质量
溶质质量
溶质质量
×100%
0.05%
2.44%
试管 编号 溶液颜 色比较 溶 剂 质量/g 溶 质 质量/g 溶 液 质量/g 溶质的质量分数
1
2
3
浅
较深
深
20
20
20
0.1
0.5
2
20.1
20.5
22
比一比 算一算
结论:一般而言,有色溶液的颜色深些其溶质的质量分数大些。
9.09%
【实验9-8】在室温下,根据下表规定的质量配制氯化钠溶液,观察现象(能否全部溶解),并计算溶液中溶质的质量分数。
溶质质量/g 溶剂(水)质量/g 现 象 溶液中溶质的质量分数
10
90
20
80
10%
20%
氯化钠溶解
氯化钠溶解
已知200C时,氯化钠的溶解度是36g。有人说:“200C时氯化钠饱和溶液中溶质的质量分数为36%”这种说法对吗?为什么?
溶质质量/g 溶剂质量/g 溶液质量/g
36 100 136
36g
136g
100%
×
=26.5%
溶质 质量 溶剂 质量 溶液 质量 溶液中溶质的质量分数
A 20g 100g
B 10g 90g
C 200g 20%
D 15g 10%
比一比 看谁算得快
溶质的质量=溶液的质量×溶质的质量分数
溶液的质量=溶质的质量+溶剂的质量
80g
20%
100g
10%
40g
160g
150g
135g
例1:在农业生产中,常需要用质量分数为16%的氯化钠溶液来选种。现要配制150kg这种溶液,需要氯化钠和水的质量各是多少?
解:
溶质质量
溶液质量
溶质的质量分数=
100%
溶质质量
=溶液质量
×溶质的质量分数
=150kg
×16%
=24kg
溶剂质量
=溶液质量
-溶质质量
=150kg
-24kg
=126kg
或= 150kg ×(1-16% )=126kg。
答:略。
二、溶质的质量分数的简单计算
×
例2: 化学实验室现在有98%的浓硫酸,但在实验中常需要用较稀的硫酸溶液。要把50g质量分数为98%的浓硫酸稀释为质量分数为20%的硫酸溶液,需要多少克水?
分析:解决这道题的关键是什么?
解:
溶液稀释前后溶质的质量不变
设稀释后溶液的质量为x。
50g× 98%= x × 20%
x=245g
需要水的质量=245g-50g=195g
答:需要水的质量为195g。
有关溶液稀释问题的计算
解题依据:溶液稀释前后,溶质的质量不变。
若有某溶液Ag,其溶质的质量分数为a%,稀释后得到溶质质量分数为b%的溶液Bg。则有:
Ag×a% = Bg×b%
(稀释前 (稀释后)
小结
① 溶质的质量分数表示溶质质量与溶液质量之比,并不是溶质质量与溶剂质量之比。
②溶质的质量分数一般用百分数表示。
③溶质的质量分数计算式中溶质质量与溶液质量的单位必须统一。
④计算式中溶质质量是指被溶解的那部分溶质的质量,没有被溶解的那部分溶质质量不能计算在内。
注意
饱和溶液的
溶质质量分数=
溶解度
100g+溶解度
溶质的质量分数36% 是指:每 100g溶液中含有36g溶质。
溶质t 0C时溶解度36g是指: 在t 0C 时,100g水最多溶解该溶质36g。
溶质质量分数与溶解度的联系和区别
×100%
1.什么是溶质的质量分数?
2.溶质质量分数与溶解度的联系和区别:
一定温度下:某物质的饱和溶液的溶质质量分数
溶解度
100g+溶解度
溶质的质量分数=
%
×100
+
=
溶剂质量
溶质质量
溶质质量
溶质的质量分数
×100%
课堂小结
空白演示
单击输入您的封面副标题
九年级化学下册(RJ)
教学课件
第九单元 溶液
课题3 溶液的浓度
第1课时 溶质的质量分数
生产生活中的常见溶液(标签)
9%(V/V)
8%(V/V)
52%(V/V)
酒类的酒精度
白醋的浓度
导入新课
10%(m/V)
葡萄糖注射液的浓度
0.9%(m/V)
生理盐水中NaCl的含量
饮料中各种营养成分的含量(每100ml溶液中含某成分的质量)
化学试剂中溶质的含量(每100g溶液中含溶质的质量)
1.掌握溶液中溶质的质量分数的概念;
2.会计算有关溶质的质量分数。
学习目标
【实验9-7】在三支试管中各加入 0.1g、 0.5g、 2g固体硫酸铜,然后分别加入20mL水。比较三种溶液的颜色。
试管 编号 溶液颜 色比较 溶剂 质量/g 溶质 质量/g 溶液
质量/g
1
2
3
浅
较深
深
20
20
20
0.1
0.5
2
20.1
20.5
22
一、溶液的浓度
讲授新课
淡蓝 蓝色 深蓝
对于有色溶液来说,根据颜色的深浅可以区分溶液是浓还是稀。但这种方法比较粗略,不能准确地表明一定量的溶液里究竟含有多少溶质。
通过观察颜色来判断溶液的浓稀,仅仅是判断溶液浓稀粗略的方法。
我们应该学习商家向消费者介绍产品那样明确地表示出溶液的组成。其中表示溶液组成的方法有多种,这里主要认识溶质的质量分数。
讨论
溶质的质量分数
1.定义:溶质质量与溶液质量之比
2.公式:
溶质质量 = 溶液质量× 溶质的质量分数
溶质的质量分数
溶质的质量 /
溶液质量
=
=
溶液质量
溶质质量
溶质的质量分数
单位要统一
%
×100
+
=
溶剂质量
溶质质量
溶质质量
×100%
0.05%
2.44%
试管 编号 溶液颜 色比较 溶 剂 质量/g 溶 质 质量/g 溶 液 质量/g 溶质的质量分数
1
2
3
浅
较深
深
20
20
20
0.1
0.5
2
20.1
20.5
22
比一比 算一算
结论:一般而言,有色溶液的颜色深些其溶质的质量分数大些。
9.09%
【实验9-8】在室温下,根据下表规定的质量配制氯化钠溶液,观察现象(能否全部溶解),并计算溶液中溶质的质量分数。
溶质质量/g 溶剂(水)质量/g 现 象 溶液中溶质的质量分数
10
90
20
80
10%
20%
氯化钠溶解
氯化钠溶解
已知200C时,氯化钠的溶解度是36g。有人说:“200C时氯化钠饱和溶液中溶质的质量分数为36%”这种说法对吗?为什么?
溶质质量/g 溶剂质量/g 溶液质量/g
36 100 136
36g
136g
100%
×
=26.5%
溶质 质量 溶剂 质量 溶液 质量 溶液中溶质的质量分数
A 20g 100g
B 10g 90g
C 200g 20%
D 15g 10%
比一比 看谁算得快
溶质的质量=溶液的质量×溶质的质量分数
溶液的质量=溶质的质量+溶剂的质量
80g
20%
100g
10%
40g
160g
150g
135g
例1:在农业生产中,常需要用质量分数为16%的氯化钠溶液来选种。现要配制150kg这种溶液,需要氯化钠和水的质量各是多少?
解:
溶质质量
溶液质量
溶质的质量分数=
100%
溶质质量
=溶液质量
×溶质的质量分数
=150kg
×16%
=24kg
溶剂质量
=溶液质量
-溶质质量
=150kg
-24kg
=126kg
或= 150kg ×(1-16% )=126kg。
答:略。
二、溶质的质量分数的简单计算
×
例2: 化学实验室现在有98%的浓硫酸,但在实验中常需要用较稀的硫酸溶液。要把50g质量分数为98%的浓硫酸稀释为质量分数为20%的硫酸溶液,需要多少克水?
分析:解决这道题的关键是什么?
解:
溶液稀释前后溶质的质量不变
设稀释后溶液的质量为x。
50g× 98%= x × 20%
x=245g
需要水的质量=245g-50g=195g
答:需要水的质量为195g。
有关溶液稀释问题的计算
解题依据:溶液稀释前后,溶质的质量不变。
若有某溶液Ag,其溶质的质量分数为a%,稀释后得到溶质质量分数为b%的溶液Bg。则有:
Ag×a% = Bg×b%
(稀释前 (稀释后)
小结
① 溶质的质量分数表示溶质质量与溶液质量之比,并不是溶质质量与溶剂质量之比。
②溶质的质量分数一般用百分数表示。
③溶质的质量分数计算式中溶质质量与溶液质量的单位必须统一。
④计算式中溶质质量是指被溶解的那部分溶质的质量,没有被溶解的那部分溶质质量不能计算在内。
注意
饱和溶液的
溶质质量分数=
溶解度
100g+溶解度
溶质的质量分数36% 是指:每 100g溶液中含有36g溶质。
溶质t 0C时溶解度36g是指: 在t 0C 时,100g水最多溶解该溶质36g。
溶质质量分数与溶解度的联系和区别
×100%
1.什么是溶质的质量分数?
2.溶质质量分数与溶解度的联系和区别:
一定温度下:某物质的饱和溶液的溶质质量分数
溶解度
100g+溶解度
溶质的质量分数=
%
×100
+
=
溶剂质量
溶质质量
溶质质量
溶质的质量分数
×100%
课堂小结
同课章节目录
