2021-2022学年高二上学期人教版(2019)化学选择性必修3第一章《有机化合物的结构特点与研究方法》测试题(word版含答案)
文档属性
| 名称 | 2021-2022学年高二上学期人教版(2019)化学选择性必修3第一章《有机化合物的结构特点与研究方法》测试题(word版含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 316.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-19 00:00:00 | ||
图片预览


文档简介
第3章《有机化合物的结构特点与研究方法》测试题
一、单选题(共12题)
1.下列物质不能做为碘水萃取剂的是
A.苯 B.汽油 C.四氯化碳 D.酒精
2.某烷烃的分子式为C4H10,其一氯代物最多有
A.2种 B.3种 C.4种 D.5种
3.下列各组微粒中,互为同素异形体的是
A.C和C B.红磷和白磷 C.H2O和H2O2 D.正丁烷和异丁烷
4.下列说法正确的是
A.间二甲苯和苯互为同系物 B.和互为同位素
C.和互为同素异形体 D.石墨和石墨烯互为同分异构体
5.有机化合物含有的官能团有
A.4种 B.5种 C.6种 D.7种
6.鉴别环己醇()和3,3-二甲基丁醛,可采用化学方法或物理方法,下列方法中不能对二者进行鉴别的是
A.利用金属钠或金属钾 B.利用质谱法
C.利用红外光谱法 D.利用核磁共振氢谱
7.充分燃烧0.1mol气态烃A,在标准状况下生成6.72LCO2和5.4gH2O,则烃A是
A.C4H6 B.C3H6 C.C2H6 D.C2H2
8.分析表中各项的排布规律,按此规律排布第26项应为
1 2 3 4 5 6 7 8 9 10 …
C2H4 C2H6 C2H6O C2H6O2 C3H6 C3H8 C3H8O C3H6O2 C4H8 C4H10 …
A.C7H16 B.C7H14O2 C.C8H18 D.C8H18O
9.分子式为的有机物共有(不含立体异构)
A.5种 B.6种 C.7种 D.8种
10.随着科学技术的发展,诞生了更多可靠的化学检验方法,下列说法错误的是
A.利用原子光谱上的特征谱线鉴定元素时,吸收光谱特点是亮线暗背景
B.应用质谱仪可以测定分子的结构
C.应用红外光谱仪可以测定分子的立体构型
D.18O可用于同位素跟踪法研究某些有机反应的机理
11.下列化学用语的表示正确的是
A.羟基的电子式: B.苯的结构简式:
C.质量数为18的氧原子:18O D.乙酸的结构式:
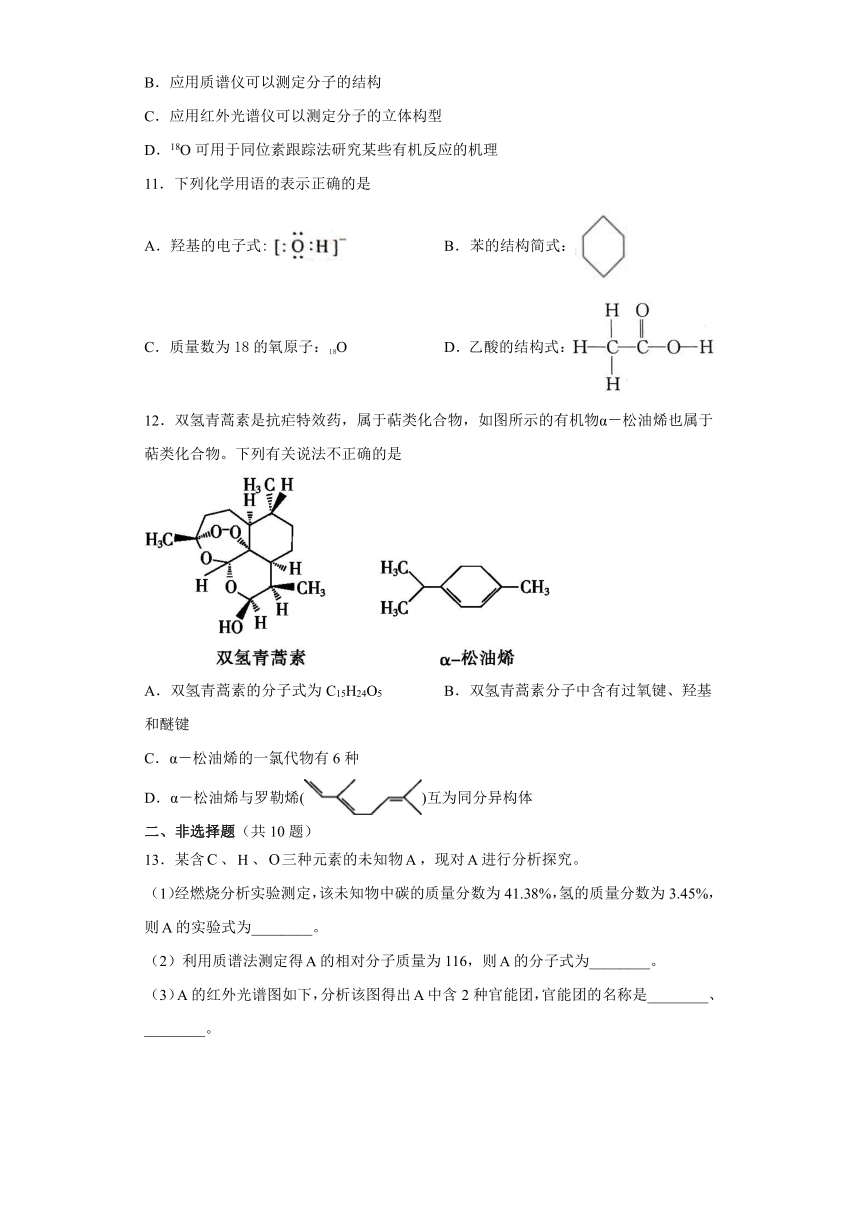
12.双氢青蒿素是抗疟特效药,属于萜类化合物,如图所示的有机物α-松油烯也属于萜类化合物。下列有关说法不正确的是
A.双氢青蒿素的分子式为C15H24O5 B.双氢青蒿素分子中含有过氧键、羟基和醚键
C.α-松油烯的一氯代物有6种
D.α-松油烯与罗勒烯()互为同分异构体
二、非选择题(共10题)
13.某含、、三种元素的未知物,现对进行分析探究。
(1)经燃烧分析实验测定,该未知物中碳的质量分数为41.38%,氢的质量分数为3.45%,则的实验式为________。
(2)利用质谱法测定得的相对分子质量为116,则的分子式为________。
(3)的红外光谱图如下,分析该图得出中含2种官能团,官能团的名称是________、________。
(4)的核磁共振氢谱图如下,综合分析的结构简式为________。
14.有A、B、C、D、E、F六种短周期主族元素,原子序数由A到F逐渐增大。①A是短周期元素中原子半径最小的元素②B元素最外层电子数是次外层电子数的2倍。 ③C的阴离子和D的阳离子与氖原子的电子层结构相同。④在通常状况下,C的单质是气体,0.1molC的气体与足量的氢气完全反应共有0.4mol电子转移。⑤D的单质在点燃时与C的单质充分反应,生成淡黄色的固体,此淡黄色固体能与BC2反应可生成C的单质。⑥E的气态氢化物与其最高价含氧酸间能发生氧化还原反应。请写出:
(1)B元素的最高价氧化物的结构式_____________。
(2)符合分子式B4A10的所有同分异构结构简式______________________________。
(3)C、D、E、F简单离子半径由大到小的顺序 ______________ (用离子符号表示)。
(4)E元素的低价氧化物与F的单质的水溶液反应的离子方程式为______________。
(5)D与E能形成2:1的化合物,用电子式表示该化合物的形成过程______________。
(6)元素E与元素F相比,非金属性较强的是___________(用元素符号表示),下列表述中能证 明这一事实的是_________________(填选项序号)。
a.常温下E的单质和F的单质状态不同
b.F的氢化物比E的氢化物稳定
c.一定条件下E和F的单质都能与钠反应
d.E的最高价含氧酸酸性弱于F的最高价含氧酸
e.F的单质能与E氢化物反应生成E单质
15.Ⅰ.如图所示是几种烷烃的球棍模型,试回答下列问题:
(1)A、B、C三者的关系是___。
(2)A的分子式为___,C的名称为___。
(3)写出C的同分异构体的结构简式:___。
Ⅱ.(4)如图均能表示甲烷的分子结构,其中更能反映其真实的存在状况的是___(填字母)。
A.甲烷分子的结构示意图
B.甲烷分子的电子式
C.甲烷分子的球棍模型
D.甲烷分子的比例模型
(5)化合物A是合成天然橡胶的单体,分子式为C5H8。A的结构简式为___,化学名称是___。
(6)某3.0g有机物X,完全燃烧后生成3.6g水和3.36LCO2(标准状况),已知该有机物的蒸气对氢气的相对密度为30,则该有机物的分子式:___。
16.核磁共振(NMR)是研究有机物结构的有力手段之一,在所研究的化合物分子中,每一个结构中的等性氢原子的1H—NMR谱中都给出了相应的峰(信号),谱中峰的强度与结构中的等性氢原子数成正比。现有某种有机物,通过元素分析得到的数据为C∶85.71%,H∶14.29%(质量分数),质谱数据表明它的相对分子质量为84。
(1)该化合物的分子式为___________。
(2)已知该物质可能存在多种结构,A、B、C是其中的三种,请根据下列要求填空:
①A是链状化合物与氢气加成产物分子中有三个甲基,则A的可能结构有___________种(不考虑立体异构)。
②B是链状化合物,1H—NMR谱中只有一个信号,则B的结构简式为___________。
17.下列反应曾用于检测司机是否酒后驾驶:2+3CH3CH2OH+16H++13H2O→4[Cr(H2O)6]3++CH3COOH
(1)基态Cr3+核外电子排布式为_______;配离子[Cr(H2O)6]3+中,与Cr3+形成配位键的原子是_______;(填元素符号)。
(2)CH3COOH中C原子轨道杂化类型分别为_______、_______;1molCH3COOH分子中含有σ键的数目为_______;
(3)H2O与CH3CH2OH可以任意比例互溶,除因为它们都是极性分子外,还因为_______。
(4)CH3CH2OH核磁共振氢谱中有_______个不同的吸收峰。
18.将某镧系元素的无水氯化物和异丙基醇钠在异丙醇中回流,得淡蓝色溶液。该溶液经蒸发浓缩、真空干燥,所得固体在甲苯中低温重结晶,析出淡蓝色针状品体A,A为稀土离子的配合物,加热至300℃也不分解。进一步分析表征结果如下:
Ⅰ.溶液电导测定显示,A为1:1电离类型,只有一种外界离子。称取6.354g晶体A,溶解后加入足量硝酸银溶液,得到0.4778g乳白色沉淀B。
Ⅱ.A的元素分析结果为:C,32.02%;H,6.17%;0,14.35%;均为质量分数。
Ⅲ.单晶X射线衍射分析显示,A的结构中:氯仅有一种环境;稀土离子所处环境完全等同,它与配体结合形成多聚团簇,每个离子周围有5个氧原子:氧原子均参与配位且有3种类型(端基、边桥基和面桥基)。
(1)计算A的摩尔质量__________。
(2)通过计算,推出A的化学式__________。
(3)写出配合物结构中端基氧、边桥基氧和面桥基氧的数目__________。
19.在+3D2→+3H2的反应中,使用的催化剂是。
(1)指出上述催化剂中Ta的配位数_______,氧化数_______。
(2)说明该催化剂不能直接参加催化反应的理由_______。
(3)试用反应方程武将质给催化剂转变成活性催化剂,并指出该反应的类型_______。
20.为了测定某有机物A的结构,做如下实验:
①将2.3 g该有机物完全燃烧,生成0.1 mol CO2和2.7 g水;
②用质谱仪测定其相对分子质量,得如图1所示的质谱图;
③用核磁共振仪处理该化合物,得到如图2所示图谱,图中三个峰的面积之比是1:2:3。
试回答下列问题:
(1)有机物A的相对分子质量是________。
(2)有机物A的分子式是________。
(3)写出有机物A的结构简式:_______________。
21.为了测定某有机物A的结构,做如下实验:
①将2.3g该有机物完全燃烧,生成0.1molCO2和2.7g水;
②用质谱仪测定其相对分子质量,得如图1所示的质谱图;
③用核磁共振仪处理该化合物,得到如图2所示图谱,图中三个峰的面积之比是1:2:3。
试回答下列问题:
(1)有机物A的相对分子质量是_______;
(2)有机物A的最简式分子式是_______,分子式是_______
(3)写出有机物A的结构简式:_______。
(4)写出有机物A的一种同分异构体结构简式:_______。
22.某烃在标准状况下的密度为3.215 g/L,现取3.6 g该烃完全燃烧,将全部产物依次通入足量的浓硫酸和碱石灰,浓硫酸增重5.4 g,碱石灰增重11 g,求:
(1)该烃分子的摩尔质量为________。
(2)确定该烃的分子式为___________。
(3)已知该烃的一氯代物只有一种,写出该烃的结构简式_________。
参考答案
1.D 2.C 3.B 4.A 5.B 6.B 7.B 8.C 9.C 10.D 11.D 12.C
13.CHO C4H4O4 羧基 碳碳双键 HOOC CH=CH COOH
14.O=C=O CH3(CH2)2CH3 、CH(CH3)3 S2->CI->O2->Na+ SO2 + Cl2 + 2H2O = 4H+ + SO42- +2Cl- Cl b、d 、e
15.同系物 C2H6 正丁烷 (CH3)2CHCH3 D 异戊二烯或2-甲基-1,3-丁二烯 C3H8O
16.(1)
(2) 7 (CH3)2C=C(CH3)2
17.(1) 1s22s22p63s23p63d3或[Ar]3d3 O
(2) sp3 sp2 7NA
(3)H2O与CH3CH2OH之间可以形成氢键
(4)3
18. 6个端基、9个边桥基、2个面桥基
19.(1) 9 +5
(2)因为该催化剂已经是18电子构型了,属于惰性催化剂,不能进行氧化加成反应
(3)→ +H2;还原消去反应
20.46 C2H6O CH3CH2OH
21.46 C2H6O C2H6O CH3CH2OH CH3OCH3
22.72 g·mol-1 C5H12
一、单选题(共12题)
1.下列物质不能做为碘水萃取剂的是
A.苯 B.汽油 C.四氯化碳 D.酒精
2.某烷烃的分子式为C4H10,其一氯代物最多有
A.2种 B.3种 C.4种 D.5种
3.下列各组微粒中,互为同素异形体的是
A.C和C B.红磷和白磷 C.H2O和H2O2 D.正丁烷和异丁烷
4.下列说法正确的是
A.间二甲苯和苯互为同系物 B.和互为同位素
C.和互为同素异形体 D.石墨和石墨烯互为同分异构体
5.有机化合物含有的官能团有
A.4种 B.5种 C.6种 D.7种
6.鉴别环己醇()和3,3-二甲基丁醛,可采用化学方法或物理方法,下列方法中不能对二者进行鉴别的是
A.利用金属钠或金属钾 B.利用质谱法
C.利用红外光谱法 D.利用核磁共振氢谱
7.充分燃烧0.1mol气态烃A,在标准状况下生成6.72LCO2和5.4gH2O,则烃A是
A.C4H6 B.C3H6 C.C2H6 D.C2H2
8.分析表中各项的排布规律,按此规律排布第26项应为
1 2 3 4 5 6 7 8 9 10 …
C2H4 C2H6 C2H6O C2H6O2 C3H6 C3H8 C3H8O C3H6O2 C4H8 C4H10 …
A.C7H16 B.C7H14O2 C.C8H18 D.C8H18O
9.分子式为的有机物共有(不含立体异构)
A.5种 B.6种 C.7种 D.8种
10.随着科学技术的发展,诞生了更多可靠的化学检验方法,下列说法错误的是
A.利用原子光谱上的特征谱线鉴定元素时,吸收光谱特点是亮线暗背景
B.应用质谱仪可以测定分子的结构
C.应用红外光谱仪可以测定分子的立体构型
D.18O可用于同位素跟踪法研究某些有机反应的机理
11.下列化学用语的表示正确的是
A.羟基的电子式: B.苯的结构简式:
C.质量数为18的氧原子:18O D.乙酸的结构式:
12.双氢青蒿素是抗疟特效药,属于萜类化合物,如图所示的有机物α-松油烯也属于萜类化合物。下列有关说法不正确的是
A.双氢青蒿素的分子式为C15H24O5 B.双氢青蒿素分子中含有过氧键、羟基和醚键
C.α-松油烯的一氯代物有6种
D.α-松油烯与罗勒烯()互为同分异构体
二、非选择题(共10题)
13.某含、、三种元素的未知物,现对进行分析探究。
(1)经燃烧分析实验测定,该未知物中碳的质量分数为41.38%,氢的质量分数为3.45%,则的实验式为________。
(2)利用质谱法测定得的相对分子质量为116,则的分子式为________。
(3)的红外光谱图如下,分析该图得出中含2种官能团,官能团的名称是________、________。
(4)的核磁共振氢谱图如下,综合分析的结构简式为________。
14.有A、B、C、D、E、F六种短周期主族元素,原子序数由A到F逐渐增大。①A是短周期元素中原子半径最小的元素②B元素最外层电子数是次外层电子数的2倍。 ③C的阴离子和D的阳离子与氖原子的电子层结构相同。④在通常状况下,C的单质是气体,0.1molC的气体与足量的氢气完全反应共有0.4mol电子转移。⑤D的单质在点燃时与C的单质充分反应,生成淡黄色的固体,此淡黄色固体能与BC2反应可生成C的单质。⑥E的气态氢化物与其最高价含氧酸间能发生氧化还原反应。请写出:
(1)B元素的最高价氧化物的结构式_____________。
(2)符合分子式B4A10的所有同分异构结构简式______________________________。
(3)C、D、E、F简单离子半径由大到小的顺序 ______________ (用离子符号表示)。
(4)E元素的低价氧化物与F的单质的水溶液反应的离子方程式为______________。
(5)D与E能形成2:1的化合物,用电子式表示该化合物的形成过程______________。
(6)元素E与元素F相比,非金属性较强的是___________(用元素符号表示),下列表述中能证 明这一事实的是_________________(填选项序号)。
a.常温下E的单质和F的单质状态不同
b.F的氢化物比E的氢化物稳定
c.一定条件下E和F的单质都能与钠反应
d.E的最高价含氧酸酸性弱于F的最高价含氧酸
e.F的单质能与E氢化物反应生成E单质
15.Ⅰ.如图所示是几种烷烃的球棍模型,试回答下列问题:
(1)A、B、C三者的关系是___。
(2)A的分子式为___,C的名称为___。
(3)写出C的同分异构体的结构简式:___。
Ⅱ.(4)如图均能表示甲烷的分子结构,其中更能反映其真实的存在状况的是___(填字母)。
A.甲烷分子的结构示意图
B.甲烷分子的电子式
C.甲烷分子的球棍模型
D.甲烷分子的比例模型
(5)化合物A是合成天然橡胶的单体,分子式为C5H8。A的结构简式为___,化学名称是___。
(6)某3.0g有机物X,完全燃烧后生成3.6g水和3.36LCO2(标准状况),已知该有机物的蒸气对氢气的相对密度为30,则该有机物的分子式:___。
16.核磁共振(NMR)是研究有机物结构的有力手段之一,在所研究的化合物分子中,每一个结构中的等性氢原子的1H—NMR谱中都给出了相应的峰(信号),谱中峰的强度与结构中的等性氢原子数成正比。现有某种有机物,通过元素分析得到的数据为C∶85.71%,H∶14.29%(质量分数),质谱数据表明它的相对分子质量为84。
(1)该化合物的分子式为___________。
(2)已知该物质可能存在多种结构,A、B、C是其中的三种,请根据下列要求填空:
①A是链状化合物与氢气加成产物分子中有三个甲基,则A的可能结构有___________种(不考虑立体异构)。
②B是链状化合物,1H—NMR谱中只有一个信号,则B的结构简式为___________。
17.下列反应曾用于检测司机是否酒后驾驶:2+3CH3CH2OH+16H++13H2O→4[Cr(H2O)6]3++CH3COOH
(1)基态Cr3+核外电子排布式为_______;配离子[Cr(H2O)6]3+中,与Cr3+形成配位键的原子是_______;(填元素符号)。
(2)CH3COOH中C原子轨道杂化类型分别为_______、_______;1molCH3COOH分子中含有σ键的数目为_______;
(3)H2O与CH3CH2OH可以任意比例互溶,除因为它们都是极性分子外,还因为_______。
(4)CH3CH2OH核磁共振氢谱中有_______个不同的吸收峰。
18.将某镧系元素的无水氯化物和异丙基醇钠在异丙醇中回流,得淡蓝色溶液。该溶液经蒸发浓缩、真空干燥,所得固体在甲苯中低温重结晶,析出淡蓝色针状品体A,A为稀土离子的配合物,加热至300℃也不分解。进一步分析表征结果如下:
Ⅰ.溶液电导测定显示,A为1:1电离类型,只有一种外界离子。称取6.354g晶体A,溶解后加入足量硝酸银溶液,得到0.4778g乳白色沉淀B。
Ⅱ.A的元素分析结果为:C,32.02%;H,6.17%;0,14.35%;均为质量分数。
Ⅲ.单晶X射线衍射分析显示,A的结构中:氯仅有一种环境;稀土离子所处环境完全等同,它与配体结合形成多聚团簇,每个离子周围有5个氧原子:氧原子均参与配位且有3种类型(端基、边桥基和面桥基)。
(1)计算A的摩尔质量__________。
(2)通过计算,推出A的化学式__________。
(3)写出配合物结构中端基氧、边桥基氧和面桥基氧的数目__________。
19.在+3D2→+3H2的反应中,使用的催化剂是。
(1)指出上述催化剂中Ta的配位数_______,氧化数_______。
(2)说明该催化剂不能直接参加催化反应的理由_______。
(3)试用反应方程武将质给催化剂转变成活性催化剂,并指出该反应的类型_______。
20.为了测定某有机物A的结构,做如下实验:
①将2.3 g该有机物完全燃烧,生成0.1 mol CO2和2.7 g水;
②用质谱仪测定其相对分子质量,得如图1所示的质谱图;
③用核磁共振仪处理该化合物,得到如图2所示图谱,图中三个峰的面积之比是1:2:3。
试回答下列问题:
(1)有机物A的相对分子质量是________。
(2)有机物A的分子式是________。
(3)写出有机物A的结构简式:_______________。
21.为了测定某有机物A的结构,做如下实验:
①将2.3g该有机物完全燃烧,生成0.1molCO2和2.7g水;
②用质谱仪测定其相对分子质量,得如图1所示的质谱图;
③用核磁共振仪处理该化合物,得到如图2所示图谱,图中三个峰的面积之比是1:2:3。
试回答下列问题:
(1)有机物A的相对分子质量是_______;
(2)有机物A的最简式分子式是_______,分子式是_______
(3)写出有机物A的结构简式:_______。
(4)写出有机物A的一种同分异构体结构简式:_______。
22.某烃在标准状况下的密度为3.215 g/L,现取3.6 g该烃完全燃烧,将全部产物依次通入足量的浓硫酸和碱石灰,浓硫酸增重5.4 g,碱石灰增重11 g,求:
(1)该烃分子的摩尔质量为________。
(2)确定该烃的分子式为___________。
(3)已知该烃的一氯代物只有一种,写出该烃的结构简式_________。
参考答案
1.D 2.C 3.B 4.A 5.B 6.B 7.B 8.C 9.C 10.D 11.D 12.C
13.CHO C4H4O4 羧基 碳碳双键 HOOC CH=CH COOH
14.O=C=O CH3(CH2)2CH3 、CH(CH3)3 S2->CI->O2->Na+ SO2 + Cl2 + 2H2O = 4H+ + SO42- +2Cl- Cl b、d 、e
15.同系物 C2H6 正丁烷 (CH3)2CHCH3 D 异戊二烯或2-甲基-1,3-丁二烯 C3H8O
16.(1)
(2) 7 (CH3)2C=C(CH3)2
17.(1) 1s22s22p63s23p63d3或[Ar]3d3 O
(2) sp3 sp2 7NA
(3)H2O与CH3CH2OH之间可以形成氢键
(4)3
18. 6个端基、9个边桥基、2个面桥基
19.(1) 9 +5
(2)因为该催化剂已经是18电子构型了,属于惰性催化剂,不能进行氧化加成反应
(3)→ +H2;还原消去反应
20.46 C2H6O CH3CH2OH
21.46 C2H6O C2H6O CH3CH2OH CH3OCH3
22.72 g·mol-1 C5H12
