第五单元 定量研究化学反应测试题—2021-2022学年九年级化学鲁教版上册(word版 含答案)
文档属性
| 名称 | 第五单元 定量研究化学反应测试题—2021-2022学年九年级化学鲁教版上册(word版 含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 158.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-20 00:00:00 | ||
图片预览



文档简介
第五单元《定量研究化学反应》测试题
一、单选题
1.为及时发现燃气泄漏,常在燃气中加入少量有特殊气味的乙醇硫(C2H5SH),乙醇硫也可以充分燃烧,化学方程式为:。下列关于X的说法正确的是
A.常温下X是无色无味的气体 B.X属于单质
C.X中两种元素的原子个数比为1:2 D.X不是空气污染物
2.下列说法正确的是
A.物质在空气中加热发生反应后,生成物的总质量必定等于反应物的总质量
B.蜡烛燃烧后质量减小,说明质量守恒定律不是普遍规律
C.细铁丝在氧气中燃烧后,生成物的质量比原来细铁丝的质量大,因此这个反应不遵守质量守恒定律
D.水结冰前后质量不变,因此这个变化遵守质量守恒定律
3.已知某物质R在空气中燃烧的表达式为:R+O2H2O+CO2,则有关R中元素组成说法正确的是
A.只含碳元素 B.一定含碳元素和氧元素
C.一定含有氧元素 D.一定含碳元素和氢元素,可能含有氧元素
4.化学概念的正确理解,是学好化学的关键,下列说法错误的是
A.单质是由同种元素组成的物质
B.O2、CO2、SO2三种物质中,都含有氧元素
C.原子和离子可以通过得失电子相互转化
D.电解水的实验说明在化学变化中,分子改变了,但原子种类和数目没变
5.对于方程式 的意义或读法正确是
A.铝加氧气等于氧化铝 B.铝和氧气反应生成氧化铝
C.4个铝原子和3个氧分子等于2个氧化铝分子 D.化学反应中各物质的质量比为27:32:102
6.下列四种物质完全分解后制得氧气的质量相同,消耗最多的物质是
A.H2O2 B.H2O C.KClO3 D.KMnO4
7.中药当归、白芷中富含的紫花前胡醇(化学式为C14H14O4),能增强人体免疫力。下列关于紫花前胡醇叙述错误的是
A.由14个碳原子、14个氢原子和4个氧原子构成 B.由三种元素组成
C.C、H、O的原子个数比为7:7:2 D.在空气中燃烧可能生成CO2
8.在化学反应前后,一定改变的是:①原子种类②原子数目③原子质量④分子种类⑤分子数目⑥元素种类⑦物质种类⑧元素质量
A.④⑤⑦ B.①②③ C.⑥⑧ D.④⑦
9.下图所示是氢气燃烧的微观示意图,下列叙述正确的是
A.反应前后分子的数目不变 B.参加反应的氧气与氢气的质量比为8:1
C.分子是化学变化中的最小粒子 D.该反应属于分解反应
10.实验探究是学习化学的重要方法。下列实验中,能达到相应目的的是
A.探究吸入的空气和呼出气体中CO2含量不同:将燃着的木条分别伸入等体积的两种气体中
B.探究石蜡中是否含有氢元素:点燃石蜡并在火焰上方罩一个干而冷的烧杯
C.探究水泥块能否作H2O2分解的催化剂:比较水泥块加入H2O2溶液前后产生气泡的快慢
D.探究化学反应前后物质的质量关系:比较烧杯中碳酸钠粉末和稀盐酸反应前后的总质量
11.6.4g某物质在氧气中燃烧,恰好生成2.8g一氧化碳,4.4g二氧化碳和7.2g水,关于该物质有下列判断:①一定含碳元素和氢元素;②一定不含氧元素:③可能含氧元素:①一定含氧元素:⑤分子中C、H原子个数比为1:8,其中正确的是
A.①② B.①③ C.①④ D.①④⑤
12.Pt-Al2O3-Ba催化净化汽车尾气反应过程的模型如图所示。下列说法错误的是
A.反应物是CO、NO2 B.该反应的生成物无污染
C.该反应为化合反应 D.Pt在反应前后质量不变
13.我国古代典籍中有“银针验毒”的记载,其反应原理之一是 。下列有关该反应的说法不正确的是
A.X的化学式是Ag2S B.反应前后元素种类不变
C.反应前后银元素的化合价不变 D.H2S中硫元素为-2价
14.2021年10月16日,长征二号F十三运载火箭在酒泉卫星发射中心点火起飞。氢氧发动机是火箭常用推进装置之一,反应原理可用化学方程式表示为,下列说法中,错误的是
A.氢气和氧气在点燃的条件下生成水 B.该反应中,氢气发生了氧化反应
C.2g氢气和lg氧气反应可生成3g水 D.反应前后氢、氧元素化合价都改变
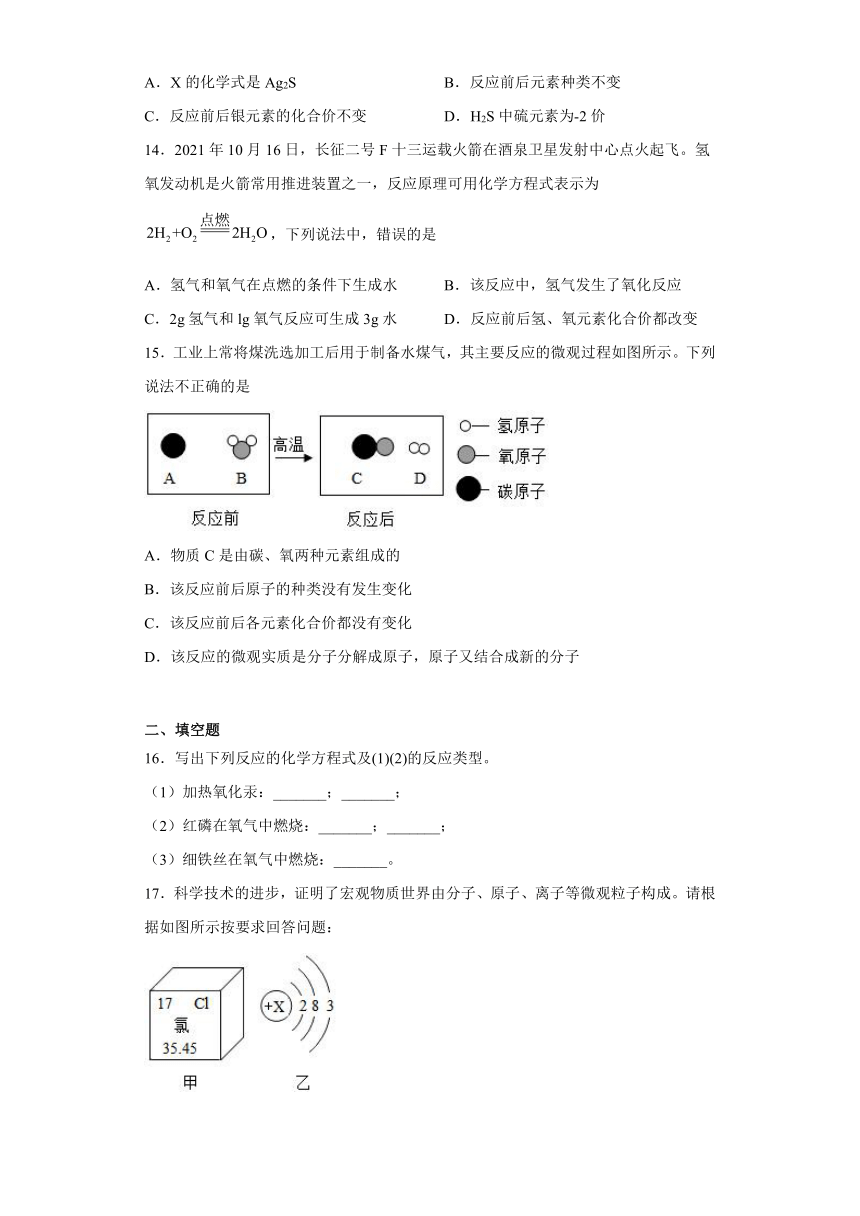
15.工业上常将煤洗选加工后用于制备水煤气,其主要反应的微观过程如图所示。下列说法不正确的是
A.物质C是由碳、氧两种元素组成的
B.该反应前后原子的种类没有发生变化
C.该反应前后各元素化合价都没有变化
D.该反应的微观实质是分子分解成原子,原子又结合成新的分子
二、填空题
16.写出下列反应的化学方程式及(1)(2)的反应类型。
(1)加热氧化汞:_______;_______;
(2)红磷在氧气中燃烧:_______;_______;
(3)细铁丝在氧气中燃烧:_______。
17.科学技术的进步,证明了宏观物质世界由分子、原子、离子等微观粒子构成。请根据如图所示按要求回答问题:
(1)图甲是氯元素在元素周期表中的信息,氯元素的相对原子质量是______,属于第_____周期元素。
(2)图乙是铝原子的结构示意图,则X的数值是____,该原子形成的阳离子符号是________。
(3)图丙是某化学反应的微观示意图,请写出该反应的化学方程式为______,该反应类型属于_______反应。
18.在宏观、微观和符号之间建立联系是化学特有的思维方式。
(1)在氨、铁和硫酸铜三种物质中,用化学用语表示保持氨化学性质的最小粒子是_______;由离子构成的物质是_______。
(2)某化学反应的微观示意图如图:
①反应涉及到的物质中,是由_______(填“分子”、“原子”或“离子”)构成的单质,涉及到的物质中氧化物的化学式为_______。
②参加反应的和的微粒个数比是_______。
③反应生成的单质和化合物的质量比是_______。
19.化学用语是学习和研究化学的重要工具,也是建立宏观、微观联系的重要桥梁。
(1)请用化学用语填空:
①地壳中含量最多的金属元素______;
②氢氧化钙______;
③两个钠离子______;
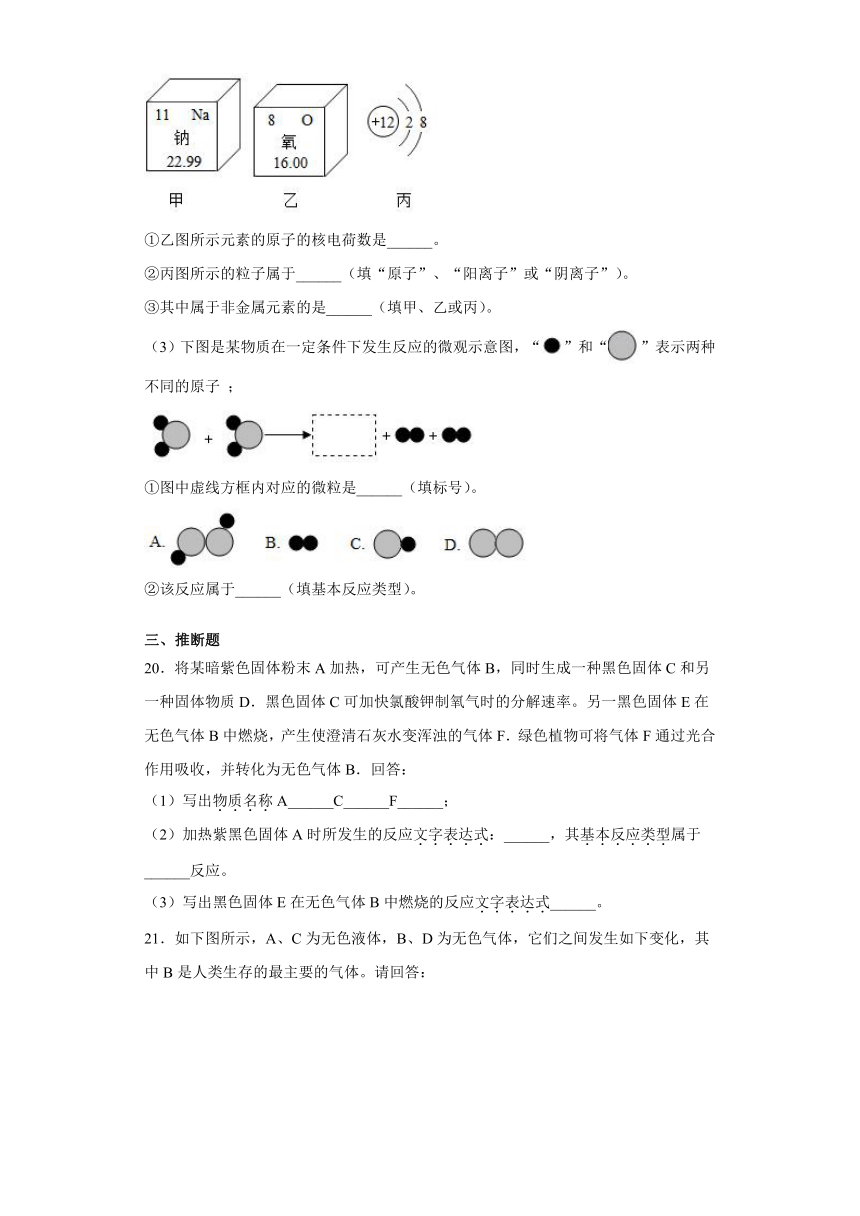
(2)下图所示为某些元素和原子结构的部分信息。
①乙图所示元素的原子的核电荷数是______。
②丙图所示的粒子属于______(填“原子”、“阳离子”或“阴离子”)。
③其中属于非金属元素的是______(填甲、乙或丙)。
(3)下图是某物质在一定条件下发生反应的微观示意图,“”和“”表示两种不同的原子 ;
①图中虚线方框内对应的微粒是______(填标号)。
②该反应属于______(填基本反应类型)。
三、推断题
20.将某暗紫色固体粉末A加热,可产生无色气体B,同时生成一种黑色固体C和另一种固体物质D.黑色固体C可加快氯酸钾制氧气时的分解速率。另一黑色固体E在无色气体B中燃烧,产生使澄清石灰水变浑浊的气体F.绿色植物可将气体F通过光合作用吸收,并转化为无色气体B.回答:
(1)写出物质名称A______C______F______;
(2)加热紫黑色固体A时所发生的反应文字表达式:______,其基本反应类型属于______反应。
(3)写出黑色固体E在无色气体B中燃烧的反应文字表达式______。
21.如下图所示,A、C为无色液体,B、D为无色气体,它们之间发生如下变化,其中B是人类生存的最主要的气体。请回答:
(1)D的化学式为________;
(2)反应①的化学方程式为______;该反应属于______(填基本反应类型名称)。
(3)物质B的用途________。
四、实验题
22.实验室制取气体所需装置如图所示,请回答以下问题:
(1)写出仪器 a 和 b 的名称:a________________,b_________________。
(2)利用 A 装置制取氧气的符号表达式为____________________;利用 B 装置制取氧气的符号表达式为____________________。
(3)其中 A 装置中试管口略向下倾斜的目的是____________________,在进行制取氧气的操作时,加入药品之前必须进行的一步操作是__________________________,收集比较纯净的氧气最好选用___________________装置(填字母序号)。
(4)下表是某同学利用氯酸钾和二氧化锰制取氧气时测定的实验数据:
MnO2与KClO3的质量比 1:40 1:20 1:10 1:5 1:3 1:2 2:3 1:1 2:1
生成1L O2所需的时间(s) 124 79 50 54 75 93 106 153 240
①据上表可知二氧化锰与氯酸钾的质量比为________________时,反应速率最快;
②二氧化锰的用量过少时产生氧气的速率很慢,可能原因是___________________;
③通过上述数据分析可知,在化学反应中催化剂的用量_________________(填“是”或“不是”)越多越好。
(5)如图 2 所示的装置,用排水法收集氧气,气体应该从_______________端(填字母序号)通入;用排空气法收集氧气,气体应该从_________________端(填字母序号)进入。
23.某化学课外小组同学,用如图所示实验验证质量守恒定律。
(1)某甲同学用A装置探究质量守恒定律,实验步骤如下:
如图将烧杯放在天平上用砝码平衡,然后倾斜烧杯使硫酸铜溶液与铁钉接触,一段时间后再把烧杯放在天平上。
①发生反应的化学方程式为_______
②最后天平的指针(填序号)_______(a.偏左 b.偏右 c.不偏转 d.无法预测)。
(2)乙同学用B装置研究质量守恒定律,实验步骤如下:
如图将烧杯放在天平上用砝码平衡,然后倾斜烧杯使盐酸与碳酸钠粉末接触,一段时间后再把烧杯放在天平上。发现天平的指针偏右。
①造成天平的指针向右偏转的原因是_______。
②若将本实验中的烧杯替换成带有气球的锥形瓶,如上图C所示,其他操作不变,最后天平仍不平衡,可能原因是____。若利用有气体参加或有气体生成的化学反应来设计实验验证质量守恒定律一般应在____容器中进行。
五、计算题
24.化学兴趣小组为测定某铜锌合金中成分金属的含量,称取10g样品放入烧杯中,向其中加入足量稀硫酸,测得反应后烧杯中物质的总质量(m)与反应时间(t)的关系如下表:
反应时间t/s t0 t1 t2 t3 t4 t5
反应后烧杯总质量m/g 110.00 109.94 109.90 109.88 109.80 109.80
请计算:
(1)生成H2的质量为________g;
(2)请计算铜锌合金中铜的质量分数。
25.有一固体为KMnO4和MnO2的混合物,为测定混合物中KMnO4的质量,某同学取样35.0g,对固体充分加热,并在不同时刻测定试管内剩余固体物质的质量(如下表):
反应时间/min 1.0 2.0 3.0 4.0 5.0
剩余固体质量/g 34.2 33.4 32.6 31.8 31.8
分析表中数据,完成下列问题:
(1)反应到___________min时反应完毕。
(2)反应后生成氧气的质量是___________g。
(3)该样品中KMnO4的质量。
参考答案
1.C 2.A 3.D 4.A 5.B 6.D 7.A 8.D 9.B 10.B 11.C 12.C 13.C 14.C 15.C
16.(1) 2HgO 2Hg+O2↑ 分解反应
(2) 4P+5O22P2O5 化合反应
(3)3Fe+2O2Fe3O4
17.(1)35.45 3三
(2) 13 Al3+
(3) 化合
18.(1) NH3 CuSO4
(2) 原子 CO2、MgO 2:1 3:20
19.(1) Al Ca(OH)2 2Na+
(2) 8 阳离子 乙
(3) D 分解反应
20.(1) 高锰酸钾 二氧化锰 二氧化碳
(2) 高锰酸钾锰酸钾+二氧化锰+氧气 分解
(3)碳+氧气二氧化碳
21.H2 2H2O2 2H2O+O2↑ 分解反应 供给呼吸(合理即可)
22.(1) 水槽 锥形瓶
(2) KMnO4K2MnO4+MnO2+O2 H2O2H2O+O2
(3) 防止冷凝水回流,炸裂试管 检查装置的气密性 C
(4) 1:10 氯酸钾没有与二氧化锰充分接触 不是
(5) B A
23.(1) Fe+CuSO4=FeSO4+Cu c
(2) 碳酸钠和盐酸反应生成的二氧化碳气体逸散到空气中 气球中的二氧化碳气体产生了浮力 密闭
24.(1)0.20g(2)35%
解:样品中锌的质量为x
解得x=6.5g
所以铜锌合金中铜的质量分数=
答:铜锌合金中铜的质量分数为35%。
25.(1)40
(2)3.2
(3)解:设样品中高锰酸钾的质量为x
=
x=31.6g
答:样品中高锰酸钾的质量为31.6g。
一、单选题
1.为及时发现燃气泄漏,常在燃气中加入少量有特殊气味的乙醇硫(C2H5SH),乙醇硫也可以充分燃烧,化学方程式为:。下列关于X的说法正确的是
A.常温下X是无色无味的气体 B.X属于单质
C.X中两种元素的原子个数比为1:2 D.X不是空气污染物
2.下列说法正确的是
A.物质在空气中加热发生反应后,生成物的总质量必定等于反应物的总质量
B.蜡烛燃烧后质量减小,说明质量守恒定律不是普遍规律
C.细铁丝在氧气中燃烧后,生成物的质量比原来细铁丝的质量大,因此这个反应不遵守质量守恒定律
D.水结冰前后质量不变,因此这个变化遵守质量守恒定律
3.已知某物质R在空气中燃烧的表达式为:R+O2H2O+CO2,则有关R中元素组成说法正确的是
A.只含碳元素 B.一定含碳元素和氧元素
C.一定含有氧元素 D.一定含碳元素和氢元素,可能含有氧元素
4.化学概念的正确理解,是学好化学的关键,下列说法错误的是
A.单质是由同种元素组成的物质
B.O2、CO2、SO2三种物质中,都含有氧元素
C.原子和离子可以通过得失电子相互转化
D.电解水的实验说明在化学变化中,分子改变了,但原子种类和数目没变
5.对于方程式 的意义或读法正确是
A.铝加氧气等于氧化铝 B.铝和氧气反应生成氧化铝
C.4个铝原子和3个氧分子等于2个氧化铝分子 D.化学反应中各物质的质量比为27:32:102
6.下列四种物质完全分解后制得氧气的质量相同,消耗最多的物质是
A.H2O2 B.H2O C.KClO3 D.KMnO4
7.中药当归、白芷中富含的紫花前胡醇(化学式为C14H14O4),能增强人体免疫力。下列关于紫花前胡醇叙述错误的是
A.由14个碳原子、14个氢原子和4个氧原子构成 B.由三种元素组成
C.C、H、O的原子个数比为7:7:2 D.在空气中燃烧可能生成CO2
8.在化学反应前后,一定改变的是:①原子种类②原子数目③原子质量④分子种类⑤分子数目⑥元素种类⑦物质种类⑧元素质量
A.④⑤⑦ B.①②③ C.⑥⑧ D.④⑦
9.下图所示是氢气燃烧的微观示意图,下列叙述正确的是
A.反应前后分子的数目不变 B.参加反应的氧气与氢气的质量比为8:1
C.分子是化学变化中的最小粒子 D.该反应属于分解反应
10.实验探究是学习化学的重要方法。下列实验中,能达到相应目的的是
A.探究吸入的空气和呼出气体中CO2含量不同:将燃着的木条分别伸入等体积的两种气体中
B.探究石蜡中是否含有氢元素:点燃石蜡并在火焰上方罩一个干而冷的烧杯
C.探究水泥块能否作H2O2分解的催化剂:比较水泥块加入H2O2溶液前后产生气泡的快慢
D.探究化学反应前后物质的质量关系:比较烧杯中碳酸钠粉末和稀盐酸反应前后的总质量
11.6.4g某物质在氧气中燃烧,恰好生成2.8g一氧化碳,4.4g二氧化碳和7.2g水,关于该物质有下列判断:①一定含碳元素和氢元素;②一定不含氧元素:③可能含氧元素:①一定含氧元素:⑤分子中C、H原子个数比为1:8,其中正确的是
A.①② B.①③ C.①④ D.①④⑤
12.Pt-Al2O3-Ba催化净化汽车尾气反应过程的模型如图所示。下列说法错误的是
A.反应物是CO、NO2 B.该反应的生成物无污染
C.该反应为化合反应 D.Pt在反应前后质量不变
13.我国古代典籍中有“银针验毒”的记载,其反应原理之一是 。下列有关该反应的说法不正确的是
A.X的化学式是Ag2S B.反应前后元素种类不变
C.反应前后银元素的化合价不变 D.H2S中硫元素为-2价
14.2021年10月16日,长征二号F十三运载火箭在酒泉卫星发射中心点火起飞。氢氧发动机是火箭常用推进装置之一,反应原理可用化学方程式表示为,下列说法中,错误的是
A.氢气和氧气在点燃的条件下生成水 B.该反应中,氢气发生了氧化反应
C.2g氢气和lg氧气反应可生成3g水 D.反应前后氢、氧元素化合价都改变
15.工业上常将煤洗选加工后用于制备水煤气,其主要反应的微观过程如图所示。下列说法不正确的是
A.物质C是由碳、氧两种元素组成的
B.该反应前后原子的种类没有发生变化
C.该反应前后各元素化合价都没有变化
D.该反应的微观实质是分子分解成原子,原子又结合成新的分子
二、填空题
16.写出下列反应的化学方程式及(1)(2)的反应类型。
(1)加热氧化汞:_______;_______;
(2)红磷在氧气中燃烧:_______;_______;
(3)细铁丝在氧气中燃烧:_______。
17.科学技术的进步,证明了宏观物质世界由分子、原子、离子等微观粒子构成。请根据如图所示按要求回答问题:
(1)图甲是氯元素在元素周期表中的信息,氯元素的相对原子质量是______,属于第_____周期元素。
(2)图乙是铝原子的结构示意图,则X的数值是____,该原子形成的阳离子符号是________。
(3)图丙是某化学反应的微观示意图,请写出该反应的化学方程式为______,该反应类型属于_______反应。
18.在宏观、微观和符号之间建立联系是化学特有的思维方式。
(1)在氨、铁和硫酸铜三种物质中,用化学用语表示保持氨化学性质的最小粒子是_______;由离子构成的物质是_______。
(2)某化学反应的微观示意图如图:
①反应涉及到的物质中,是由_______(填“分子”、“原子”或“离子”)构成的单质,涉及到的物质中氧化物的化学式为_______。
②参加反应的和的微粒个数比是_______。
③反应生成的单质和化合物的质量比是_______。
19.化学用语是学习和研究化学的重要工具,也是建立宏观、微观联系的重要桥梁。
(1)请用化学用语填空:
①地壳中含量最多的金属元素______;
②氢氧化钙______;
③两个钠离子______;
(2)下图所示为某些元素和原子结构的部分信息。
①乙图所示元素的原子的核电荷数是______。
②丙图所示的粒子属于______(填“原子”、“阳离子”或“阴离子”)。
③其中属于非金属元素的是______(填甲、乙或丙)。
(3)下图是某物质在一定条件下发生反应的微观示意图,“”和“”表示两种不同的原子 ;
①图中虚线方框内对应的微粒是______(填标号)。
②该反应属于______(填基本反应类型)。
三、推断题
20.将某暗紫色固体粉末A加热,可产生无色气体B,同时生成一种黑色固体C和另一种固体物质D.黑色固体C可加快氯酸钾制氧气时的分解速率。另一黑色固体E在无色气体B中燃烧,产生使澄清石灰水变浑浊的气体F.绿色植物可将气体F通过光合作用吸收,并转化为无色气体B.回答:
(1)写出物质名称A______C______F______;
(2)加热紫黑色固体A时所发生的反应文字表达式:______,其基本反应类型属于______反应。
(3)写出黑色固体E在无色气体B中燃烧的反应文字表达式______。
21.如下图所示,A、C为无色液体,B、D为无色气体,它们之间发生如下变化,其中B是人类生存的最主要的气体。请回答:
(1)D的化学式为________;
(2)反应①的化学方程式为______;该反应属于______(填基本反应类型名称)。
(3)物质B的用途________。
四、实验题
22.实验室制取气体所需装置如图所示,请回答以下问题:
(1)写出仪器 a 和 b 的名称:a________________,b_________________。
(2)利用 A 装置制取氧气的符号表达式为____________________;利用 B 装置制取氧气的符号表达式为____________________。
(3)其中 A 装置中试管口略向下倾斜的目的是____________________,在进行制取氧气的操作时,加入药品之前必须进行的一步操作是__________________________,收集比较纯净的氧气最好选用___________________装置(填字母序号)。
(4)下表是某同学利用氯酸钾和二氧化锰制取氧气时测定的实验数据:
MnO2与KClO3的质量比 1:40 1:20 1:10 1:5 1:3 1:2 2:3 1:1 2:1
生成1L O2所需的时间(s) 124 79 50 54 75 93 106 153 240
①据上表可知二氧化锰与氯酸钾的质量比为________________时,反应速率最快;
②二氧化锰的用量过少时产生氧气的速率很慢,可能原因是___________________;
③通过上述数据分析可知,在化学反应中催化剂的用量_________________(填“是”或“不是”)越多越好。
(5)如图 2 所示的装置,用排水法收集氧气,气体应该从_______________端(填字母序号)通入;用排空气法收集氧气,气体应该从_________________端(填字母序号)进入。
23.某化学课外小组同学,用如图所示实验验证质量守恒定律。
(1)某甲同学用A装置探究质量守恒定律,实验步骤如下:
如图将烧杯放在天平上用砝码平衡,然后倾斜烧杯使硫酸铜溶液与铁钉接触,一段时间后再把烧杯放在天平上。
①发生反应的化学方程式为_______
②最后天平的指针(填序号)_______(a.偏左 b.偏右 c.不偏转 d.无法预测)。
(2)乙同学用B装置研究质量守恒定律,实验步骤如下:
如图将烧杯放在天平上用砝码平衡,然后倾斜烧杯使盐酸与碳酸钠粉末接触,一段时间后再把烧杯放在天平上。发现天平的指针偏右。
①造成天平的指针向右偏转的原因是_______。
②若将本实验中的烧杯替换成带有气球的锥形瓶,如上图C所示,其他操作不变,最后天平仍不平衡,可能原因是____。若利用有气体参加或有气体生成的化学反应来设计实验验证质量守恒定律一般应在____容器中进行。
五、计算题
24.化学兴趣小组为测定某铜锌合金中成分金属的含量,称取10g样品放入烧杯中,向其中加入足量稀硫酸,测得反应后烧杯中物质的总质量(m)与反应时间(t)的关系如下表:
反应时间t/s t0 t1 t2 t3 t4 t5
反应后烧杯总质量m/g 110.00 109.94 109.90 109.88 109.80 109.80
请计算:
(1)生成H2的质量为________g;
(2)请计算铜锌合金中铜的质量分数。
25.有一固体为KMnO4和MnO2的混合物,为测定混合物中KMnO4的质量,某同学取样35.0g,对固体充分加热,并在不同时刻测定试管内剩余固体物质的质量(如下表):
反应时间/min 1.0 2.0 3.0 4.0 5.0
剩余固体质量/g 34.2 33.4 32.6 31.8 31.8
分析表中数据,完成下列问题:
(1)反应到___________min时反应完毕。
(2)反应后生成氧气的质量是___________g。
(3)该样品中KMnO4的质量。
参考答案
1.C 2.A 3.D 4.A 5.B 6.D 7.A 8.D 9.B 10.B 11.C 12.C 13.C 14.C 15.C
16.(1) 2HgO 2Hg+O2↑ 分解反应
(2) 4P+5O22P2O5 化合反应
(3)3Fe+2O2Fe3O4
17.(1)35.45 3三
(2) 13 Al3+
(3) 化合
18.(1) NH3 CuSO4
(2) 原子 CO2、MgO 2:1 3:20
19.(1) Al Ca(OH)2 2Na+
(2) 8 阳离子 乙
(3) D 分解反应
20.(1) 高锰酸钾 二氧化锰 二氧化碳
(2) 高锰酸钾锰酸钾+二氧化锰+氧气 分解
(3)碳+氧气二氧化碳
21.H2 2H2O2 2H2O+O2↑ 分解反应 供给呼吸(合理即可)
22.(1) 水槽 锥形瓶
(2) KMnO4K2MnO4+MnO2+O2 H2O2H2O+O2
(3) 防止冷凝水回流,炸裂试管 检查装置的气密性 C
(4) 1:10 氯酸钾没有与二氧化锰充分接触 不是
(5) B A
23.(1) Fe+CuSO4=FeSO4+Cu c
(2) 碳酸钠和盐酸反应生成的二氧化碳气体逸散到空气中 气球中的二氧化碳气体产生了浮力 密闭
24.(1)0.20g(2)35%
解:样品中锌的质量为x
解得x=6.5g
所以铜锌合金中铜的质量分数=
答:铜锌合金中铜的质量分数为35%。
25.(1)40
(2)3.2
(3)解:设样品中高锰酸钾的质量为x
=
x=31.6g
答:样品中高锰酸钾的质量为31.6g。
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
