9.2 溶解度 同步练习(含答案)
图片预览



文档简介
中小学教育资源及组卷应用平台
绝密★启用前
9.2 课题2 溶解度同步练习
人教版初中化学九年级下册
注意:本试卷包含Ⅰ、Ⅱ两卷。第Ⅰ卷 ( http: / / www.21cnjy.com )为选择题,所有答案必须用2B铅笔涂在答题卡中相应的位置。第Ⅱ卷为非选择题,所有答案必须填在答题卷的相应位置。答案写在试卷上均无效,不予记分。www.21-cn-jy.com
一、单选题(本大题共10小题,共20.0分)
1. 下列因素:溶质种类;溶剂种类;溶质质量;溶剂质量;温度;压强;搅拌、振荡.其中与固体溶解度无关的是 21·世纪*教育网
A. B. C. D.
2. 时向一定量不饱和溶液中逐渐加入固体,则下列图象中能正确表示此过程中溶质质量变化规律的是 21*cnjy*com
A. ( http: / / www.21cnjy.com ) B. ( http: / / www.21cnjy.com )
C. ( http: / / www.21cnjy.com ) D. ( http: / / www.21cnjy.com )
3. 甲和乙两种物质的溶解度曲线如图所示 ( http: / / www.21cnjy.com )。下列叙述正确的是
甲的溶解度随温度的升高而增大
时,使甲的饱和溶液析出晶体可用加热升温、冷却降温和蒸发溶剂三种方法
时,向溶质质量分数为的乙溶液中加入乙固体并振荡,有固体不溶解
将相同质量的甲和乙的饱和溶液分别从降温至,甲析出晶体的质量大
A. B. C. D.
4. 如图是甲、乙两种物质的溶解度曲线,下列说法不正确的是
A. 时,甲、乙两 ( http: / / www.21cnjy.com )种物质的溶解度相等
B. 甲物质的溶解度随温度的升高而增大
C. 将时甲、乙两种物质的饱和溶液降温到,溶液仍然饱和
D. 时,将甲物质加入水中,充分搅拌,能得到甲物质的饱和溶液
2-1-c-n-j-y
5. 能溶解在不同浓度的溶液中,其溶解度曲线如图所示。下列叙述错误的是
A. 时,溶液中的溶解度为
B. 时,在溶液中的溶解度大于在溶液中的溶解度
C. 时,在溶液中所溶解的质量,一定小于在溶液中所溶解的质量
D. 时,将溶解在溶液中达到饱和,然后降温至,该过程中一定析出固体
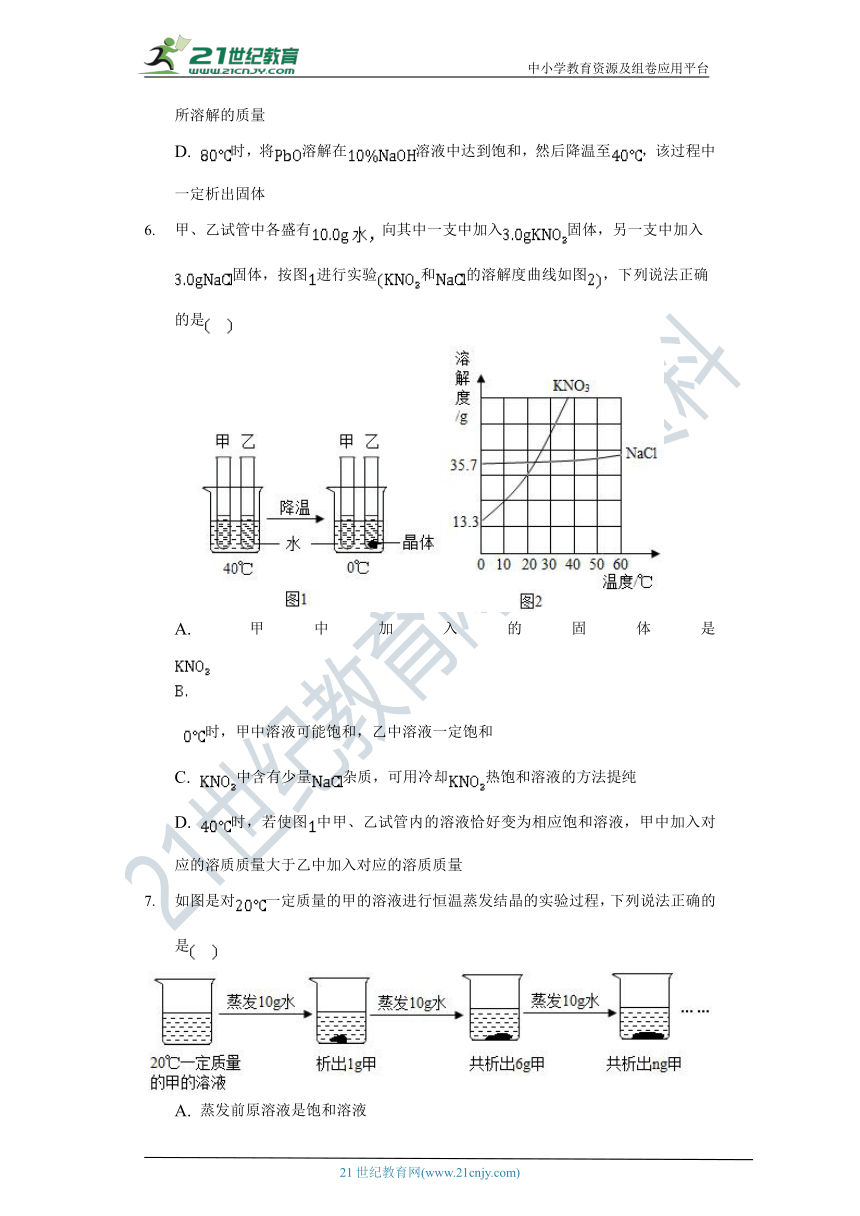
6. 甲、乙试管中各盛有向其中一支中加入固体,另一支中加入固体,按图进行实验和的溶解度曲线如图,下列说法正确的是
A. 甲中加入的固体是 时,甲中溶液可能饱和,乙中溶液一定饱和
C. 中含有少量杂质,可用冷却热饱和溶液的方法提纯
D. 时,若使图中甲、乙试管内的溶液恰好变为相应饱和溶液,甲中加入对应的溶质质量大于乙中加入对应的溶质质量
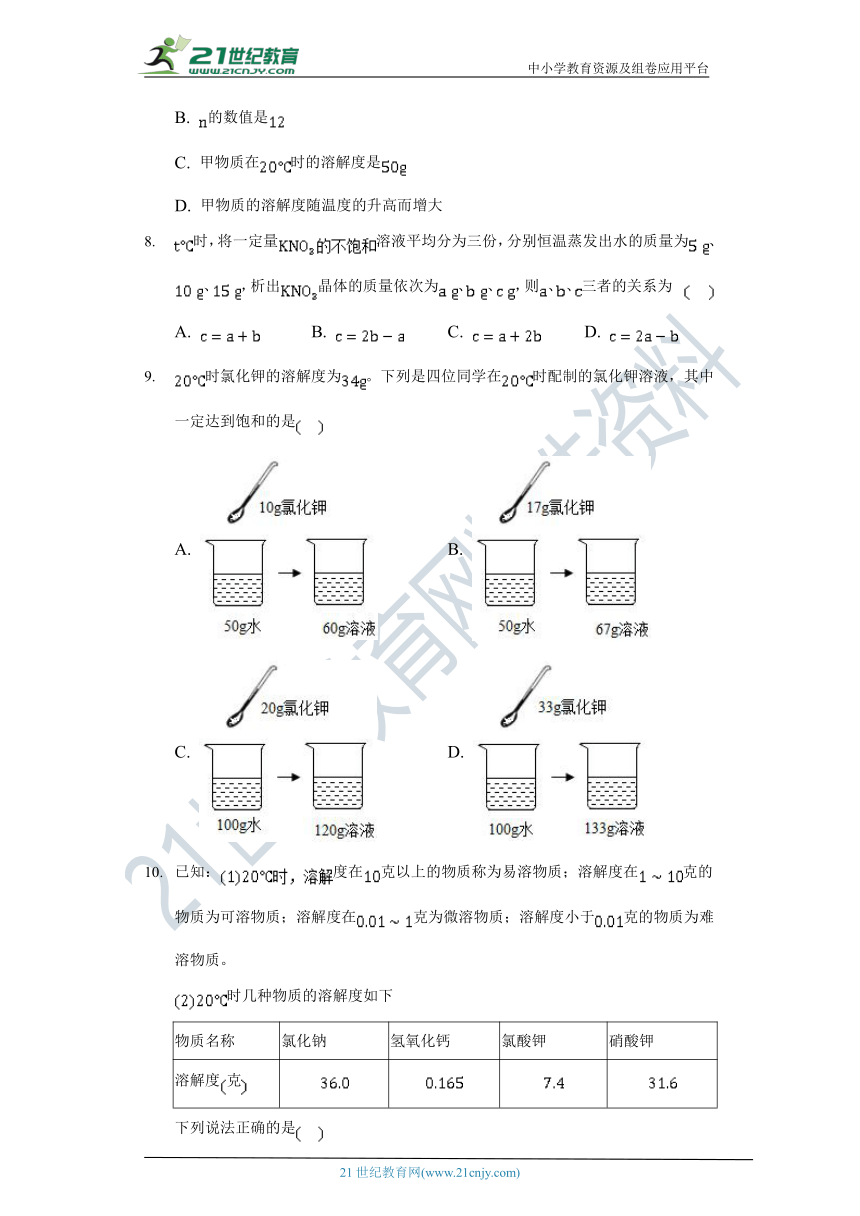
7. 如图是对一定质量的甲的溶液进行恒温蒸发结晶的实验过程,下列说法正确的是
A. 蒸发前原溶液是饱和溶液
B. 的数值是
C. 甲物质在时的溶解度是
D. 甲物质的溶解度随温度的升高而增大
8. 时,将一定量溶液平均分为三份,分别恒温蒸发出水的质量为、、,析出晶体的质量依次为、、,则、、三者的关系为
A. B. C. D.
9. 时氯化钾的溶解度为。下列是四位同学在时配制的氯化钾溶液,其中一定达到饱和的是
A. ( http: / / www.21cnjy.com ) B. ( http: / / www.21cnjy.com )
C. ( http: / / www.21cnjy.com ) D. ( http: / / www.21cnjy.com )
10. 已知:度在克以上的物质称为易溶物质;溶解度在克的物质为可溶物质;溶解度在克为微溶物质;溶解度小于克的物质为难溶物质。
时几种物质的溶解度如下 2·1·c·n·j·y
物质名称 氯化钠 氢氧化钙 氯酸钾 硝酸钾
溶解度克
下列说法正确的是
A. 时氢氧化钙是难溶物质
B. ( http: / / www.21cnjy.com )时可以配制出的硝酸钾溶液
C. 时氯酸钾是易溶物质
D. 时硝酸钾的溶解度比氯化钠大21·cn·jy·com
二、填空题(本大题共4小题,共32.0分)
11. 卤水的主要成分及其溶解度曲线如图 ( http: / / www.21cnjy.com )所示。
时,的溶解度______填“”、“”或“”的溶解度。
将时,、和三种物质的饱和溶液分别升温至时,有晶体析出的是______。
时,水中最多溶解的质量为______。
欲使的饱和溶液变为不饱和溶液,可以采取的措施是______任填一种。
12. 图为氯化钠、碳酸钠在水中的溶解度 ( http: / / www.21cnjy.com )曲线.请回答下列问题:
时,碳酸钠的溶解度为______;
时,氯化钠的溶解度______碳酸钠的溶解度填写“”、“”或“”;
时,向两只盛有水的烧杯中,分别加入氯化钠、碳酸钠两种物质,至不再溶解为止,所得溶液的溶质是______,其中______填溶质质量较大.
将碳酸钠不饱和溶液转化为饱和溶液的方法有______、______至少填两种.
如图所示,时,将盛有饱和碳酸钠溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出.加入的物质可能是______填字母序号.
A.氢氧化钠 氯化钠 硝酸铵.【来源:21·世纪·教育·网】
13. 学习化学知识的目的之一是分析和解决实际问题 ( http: / / www.21cnjy.com ).
甲烷、氢气都是可燃性气体,点燃可燃性气体之前都需要 ______ .
喝了汽水以后,常常会打嗝这说明气体的溶解度与 ______ 有关.
吸烟有害健康香烟烟气中含有几百种对人体有害的物质,如尼古丁、焦油、一氧化碳、二氧化碳等,其中与血红蛋白结合能力强的有毒气体是 ______ .
用洗涤剂清洗油污,是利用了洗涤剂的 ______ 作用.【版权所有:21教育】
14. 根据氯化钠和硝酸钾的溶解度表与溶解度曲线回答下列问题:
温度
溶解度 氯化钠
硝酸钾
时,氯化钠的溶解度 ______硝酸钾的溶解度大于、小于或等于。
图中能表示硝酸钾溶解度曲线的是 ______填“”或“”。
时,将硝酸钾放入水中,所得溶液是 ______溶液填“饱和”或“不饱和”,继续加热至,下列各量一定变大的是 ______填字母序号。
A.溶质质量
B.溶剂质量
C.溶解度
D.溶质的质量分数21教育网
三、推断题(本大题共1小题,共10.0分)
15. 如图是甲、乙两种固体物质的 ( http: / / www.21cnjy.com )溶解度曲线。
由图可获得一条信息是______。
若乙中混有少量甲,提纯乙的方法是______。
时,将不饱和的甲溶液,转化成该温度下的饱和溶液的一种方法是______,变化过程中,溶质的质量分数______选填“增大”、“减少”或“不变”。
将等质量的甲、乙两种物质的溶液由降温至时,析出晶体的质量______。
选序号甲乙 甲乙 无法确定。【出处:21教育名师】
四、实验题(本大题共2小题,共20.0分)
16. 如图所示,在两支试管中进行实验,补全实验方案。
序号 目的 步骤或现象
鉴别溶液和溶液 试管、中分别加入两种溶液;再向两支试管中加入 ______ 。
比较 ______ 试管中加入一粒碘和水;试管中加入一粒碘和汽油。观察到中固体几乎不溶解,中固体全部溶解。
比较锌、铁、铜的金属活动性 试管中加入溶液,试管中加入溶液;
再分别向两支试管中插入铁丝。观察到的现象是 ______ 。
17. 某兴趣小组利用家中的材料研究影响物质溶解性的因素,实验步骤设计如下:
Ⅰ、称取六份冰糖和一份食盐,每为一份,并将其中五份冰糖研磨成粉末。
Ⅱ、按照下表进行实验实验所需仪器略
( http: / / www.21cnjy.com )
请你对他们的实验设计进行分析:
根据上述设计,你认为他们准备 ( http: / / www.21cnjy.com )研究的影响因素是_____________从下列选项中选取,下同,其中不影响物质溶解性的因素是____________。溶质种类溶质颗粒大小实验温度溶剂种类溶剂质量溶质质量。
根据第四组实验与前三组实验的比较,你可以得到的结论是_________________________。21cnjy.com
五、计算题(本大题共1小题,共10.0分)
近期,巴西出现了寨卡病毒疫情。过 ( http: / / www.21cnjy.com )氧乙酸化学式为是常用的一种消毒剂,可用于疫情的消毒。请计算:
过氧乙酸中氢、氧两种元素的质量比是 ______;
多少溶质质量分数为过氧乙酸溶液与多少溶质质量分数为过氧乙酸溶液混合,可以得到的过氧乙酸溶液写计算过程。
18. www-2-1-cnjy-com
答案和解析
1.【答案】
【解析】解:当温度相同时,固体物 ( http: / / www.21cnjy.com )质不同则溶解度不同,如时氯化钠的溶解度为,而硝酸钾的溶解度为,所以溶质种类影响固体物质的溶解度,正确;
溶剂种类能影响固体物质的溶解度,如碘容易溶解在酒精中,不易溶解在水中,故碘在酒精中的溶解度大,正确;
根据溶解度的定义,某物质在溶剂里达到饱和所溶解的溶质的质量,是该温度下的溶解度,故,溶质质量不影响固体物质的溶解度,不对;
根据溶解度的定义,某温度时溶剂中最多溶解的质量为该温度时该物质的溶解度,所以溶剂质量不影响固体物质的溶解度,不对;
大多数固体物质的溶解度随温度的升高而增大,少数物质的溶解度受温度变化影响不大,极少数物质溶解度随温度的升高而减小,即温度影响固体物质的溶解度,正确;
压强的改变不影响固体物质的溶解度,此项不对.
搅拌、振荡的作用是加速固体物质的溶解速率,不会使物质溶解的更多,所以搅拌不影响固体物质的溶解度,不对;
故选C.
物质的溶解度是物质溶解能力的定量表示,溶解能力的大小与溶质和溶剂的种类有关.大多数固体物质的溶解度随温度的升高而增大,所以固体物质的溶解度与温度有关.由溶解度的定义可知,不管溶质或溶剂的量有多少,固体的溶解度都只看在溶剂中达到饱和状态时所能溶解溶质的质量,所以固体物质的溶解度与溶质质量和溶剂质量无关;固体的溶解度与压强无关,搅拌、振荡只能加快溶解的速率,而不能增大溶解的质量,故溶解度与是否搅拌或振荡无关.
该题考查的是影响固体物质溶解度的因素,解答时要结合溶解度的概念,理解溶解度的含义,结合题目中的选项细致分析对溶解度是否产生影响,对”溶剂质量不影响固体物质的溶解度“要加深理解.一般地,影响固体溶解度的因素有三:温度、溶质种类、溶剂种类.
21世纪教育网版权所有
2.【答案】
【解析】解:、不饱和溶液中含有一定量的溶质硝酸钾,不会从开始,故A错误;
B、向一定量不饱和溶液中逐渐加入固体时,硝酸钾能够继续溶解,直到达到饱和状态,故B错误;
C、向一定量不饱和溶液中逐渐加入固体时,硝酸钾能够继续溶解,达到饱和状态时不再溶解,故C正确;
D、在一定温度下,在一定量的溶剂里,硝酸钾不能无限溶解,故D错误。
故选C。
在一定温度下,在一定量的溶剂里,硝酸钾的溶解能力是有一定的限度的。
本题主要考查物质的溶解能力,解答时要注意在一定温度下,在一定量的溶剂里,硝酸钾的溶解能力不是无限的。
21教育名师原创作品
3.【答案】
【解析】
【分析】
本题难度不是很大,主要考查了固 ( http: / / www.21cnjy.com )体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力。
【解答】
通过分析溶解度曲线可知,小于时,甲的溶解度随温度的升高而增大,故错误;
小于时或大于时,甲物质的溶解度随温度的降低、升高时,溶解度都会减少,所以时,使甲的饱和溶液析出晶体可用加热升温、冷却降温和蒸发溶剂三种方法,故正确;
时,乙物质的溶解度是,向溶质质量分数为的乙溶液中含有溶质质量为:,加入乙固体并振荡,有固体不溶解,故正确;
将相同质量的甲和乙的饱和溶液分别从降温至,甲物质的溶解度变化最大,所以甲析出晶体的质量大,故正确。
故选:。
4.【答案】
【解析】解:、通过分析溶 ( http: / / www.21cnjy.com )解度曲线可知,时,甲、乙两种物质的溶解度相等,故A正确;
B、甲物质的溶解度随温度的升高而增大,故B正确;
C、将时甲、乙两种物质的饱和溶液降温到,乙物质的溶解度最大,甲物质的溶解度减小,所以甲物质的溶液仍然饱和,乙物质的溶液不饱和,故C错误;
D、时,甲物质的溶解度是,所以将甲物质加入水中,充分搅拌,能得到甲物质的饱和溶液,故D正确。
故选:。
根据固体的溶解度曲线可以:查出某物质在一定温度下的溶解度,从而确定物质的溶解性,比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的。
本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力。
5.【答案】
【解析】解:、由溶解度曲线可知:时,在溶液中的溶解度为正确,正确但不符合题意,故选项错误;
B、时,在溶液中的溶解度大于在溶液中的溶解度正确,正确但不符合题意,故选项错误;
C、时,在溶液中所溶解的质量,一定小于在溶液中所溶解的质量错误,因为没有指明溶剂的质量,错误符合题意,故选项正确;
D、时,将溶解在溶液中达到饱和,然后降温至,该过程中一定析出固体正确,因为的溶解度随温度的降低而减小,正确但不符合题意,故选项错误。
本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液的变化等,本考点主要出现在选择题和填空题中。
6.【答案】
【解析】
【分析】
本题难度不是很大, ( http: / / www.21cnjy.com )主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力。
【解答】
A、时,氯化钠的溶解度大于,硝酸钾的溶解度小于,甲、乙试管中各盛有水,向其中一支中加入固体,另一支中加入固体,降温到时,乙中有晶体析出,所以乙中加入的固体是,故A错误;
B、时,氯化钠的溶解度大于,硝酸钾的溶解度小于,的水中可以溶解的氯化钠,乙中有晶体析出,所以时,甲中溶液一定不饱和,乙中溶液一定饱和,故B错误;
C、硝酸钾的溶解度受温度变化影响较大,所以中含有少量杂质,可用冷却热饱和溶液的方法提纯,故C正确;
D、时,硝酸钾的溶解度大于氯化钠的溶解度,所以若使图中甲、乙试管内的溶液恰好变为相应饱和溶液,甲中加入对应的溶质质量小于乙中加入对应的溶质质量,故D错误。
故选C。
7.【答案】
【解析】解:、蒸发前的烧杯底部没 ( http: / / www.21cnjy.com )有固体,第一次蒸发水,析出晶体,第二次蒸发水析出晶体,所以蒸发前原溶液是不饱和溶液,错误;
B、蒸发前的烧杯底部没有固体,第一次蒸发水,析出晶体,第二次蒸发水析出晶体,所以第三次蒸发水析出晶体,所以共析出,错误;
C、蒸发水析出晶体,则水中最多能溶解甲,故甲物质在时的溶解度是,正确;
D、题中析出晶体是通过蒸发溶剂得到的,不能判断出温度对溶解度的影响,错误;
故选:。
本题是对物质溶解度、蒸发结晶等知识的考查,解决的重点是能理解溶解度、结晶以及物质溶解度随温度的变化,并能利用相关知识分析并解决问题。
8.【答案】
【解析】
【分析】
本题考查溶液中的相关计算, ( http: / / www.21cnjy.com )解此类题只要善于分解全过程,创设可比中间态,就可以快速求解,大大节约做题时间;当然,只有在做题的过程中,有意识地去使用过程分解法,才能熟练地掌握这种解题技巧。
【解答】
第一份溶液蒸发溶剂,析出晶体后,得到饱和溶液,设为;
第二份溶液析出晶体的过程可以分解为第一步:先蒸发溶剂,析出晶体,得到同于第一份溶液的析晶过程;第二步:对饱和溶液继续处理,再蒸发溶剂,再析出晶体,仍得到饱和溶液,设为,由此可知此温度下该物质饱和溶液中溶质与溶剂的比为;
第三份溶液析出晶体的过程可以分解为第一步:先蒸发溶剂,析出晶体,得到同于第二份溶液的析晶过程;
第二步:对饱和溶液继续处理,再蒸发溶剂,再析出晶体,仍得到饱和溶液;由此可知此温度下该物质饱和溶液中溶质与溶剂的比为;
因为一定温度下饱和溶液中溶质与溶剂的比为一定值,则有,则,或利用水中所含溶质的量作为相等关系得:,整理可得。
故选B。
9.【答案】
【解析】
【分析】
本题难度不大,掌握溶解度的含义 ( http: / / www.21cnjy.com )、饱和溶液的特征等并能灵活运用是正确解答本题的关键。
【解答】
A、时氯化钾的溶解度为,含义是时,水中最多能溶解氯化钾,溶液达到饱和状态,则时,水中最多能溶解氯化钾,溶液达到饱和状态,向水中加入氯化钾,所得溶液是不饱和溶液,故选项错误。
B、向水中加入氯化钾,所得溶液恰好是饱和溶液,故选项正确。
C、时,水中最多能溶解氯化钾,时,向水中加入氯化钾,所得溶液是不饱和溶液,故选项错误。
D、时,向水中加入氯化钾,所得溶液是不饱和溶液,故选项错误。
故选B。 21*cnjy*com
10.【答案】
【解析】解:时氢氧化钙的溶解度是,在之间,属于微溶物质,故A说法不正确;
B、时硝酸钾的溶解度是,饱和溶液的溶质质量分数是:,所以可以配制出的硝酸钾溶液,故B说法正确;
C、时氯酸钾的溶解度是,在之间,属于可溶物质,故C说法不正确;
D、由表中的数据可知,时硝酸钾的溶解度比氯化钠小,故D说法不正确。
故选:。
A、根据在时氢氧化钙的溶解度分析;
B、根据时硝酸钾溶解度、饱和溶液的溶质质量分数分析;
C、根据在时氯酸钾的溶解度分析;
D、根据在时硝酸钾、氯化钠的溶解度分析。
本题难度不是很大,主要考查了固体的溶解度含义,会根据固体的溶解度的含义解决相关的问题,从而培养分析问题、解决问题的能力。
【来源:21cnj*y.co*m】
11.【答案】;
硫酸镁;
;
升高温度。
【解析】解:通过分析溶解度曲线可知 ( http: / / www.21cnjy.com ),时,的溶解度的溶解度;
将时,、和三种物质的饱和溶液分别升温至时,硫酸镁的溶解度减小,氯化镁、氯化钾的溶解度增大,所以有晶体析出的是硫酸镁;
时,氯化镁的溶解度是,所以水中最多溶解的质量为;
氯化镁的溶解度随温度的升高而增大,所以欲使的饱和溶液变为不饱和溶液,可以采取的措施是升高温度。
故答案为:;
硫酸镁;
;
升高温度。
根据固体的溶解度曲线可以:查出某物质在一定温度下的溶解度,从而确定物质的溶解性,比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的。
本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力。
12.【答案】 氯化钠、碳酸钠 氯化钠 加碳酸钠 蒸发水、降温
【解析】解:的溶解度为;
曲线中交点表示该温度时两种物质的溶解度相等,所以时氯化钠和碳酸钠两物质的溶解度相等;
时,碳酸钠的溶解度为,氯化钠的溶解度大于碳酸钠,所以所得溶液中食盐的质量多.
碳酸钠的溶解度随温度升高而增大,将碳酸钠不饱和溶液转化为饱和溶液的方法有加碳酸钠,蒸发水、降温.
由饱和碳酸钠溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出,说明温度降低了,也就是说该物质溶于水是吸热的,所以为硝酸铵.
故答案为:
;
;
氯化钠、碳酸钠;氯化钠;
;
加碳酸钠,蒸发水、降温;
.
根据溶解度曲线的意义解答;
根据曲线中交点的含义考虑;
关键要根据该温度时的溶解度看所加物质是否全部溶解;
根据饱和溶液与不饱和溶液之间的转化方法解答;
物质溶于水吸热和放热情况考虑.
溶解度曲线能定量地表示出溶解度变化的规律.从溶解度曲线可以看出:同一溶质在不同温度下的溶解度;同一温度下,不同溶质的溶解度;温度对不同物质的溶解度影响不同.
13.【答案】验纯 温度 一氧化碳 乳化
【解析】解:可燃性气体点 ( http: / / www.21cnjy.com )燃之前必须验纯,防止不纯点燃发生爆炸.
喝了汽水以后,常常会打嗝,是由于胃内的温度比外界高二氧化碳的溶解度变小而导致的.
当一氧化碳随呼吸进入人体血液后,便于血液中的血红蛋白结合从而使血红蛋白丧失输送氧的能力,导致一氧化碳中毒.
用洗涤剂清洗油污,是利用了洗涤剂的乳化作用;
故答案为:验纯;
温度;
一氧化碳;
乳化.
根据可燃性气体点燃之前必须验纯分析解答;
利用气体的溶解度随温度的升高而降低,随着压强的增大而增大分析;
从一氧化碳中毒的原理分析;
洗涤剂有乳化作用;
学习化学的目的,重要的是善于用化学知识去分析、解决生产生活中的问题.
14.【答案】小于 饱和
【解析】解:中数据可知,时,氯化钠的溶解度小于硝酸钾的溶解度;
由表中的数据可知,硝酸钾的溶解度受温度变化影响较大,所以图中能表示硝酸钾溶解度曲线的是;
在时,硝酸钾的溶解度是,水中最多溶解的硝酸钾,所以时,将硝酸钾固体投入水中,充分溶解后可得到硝酸钾饱和溶液;继续加热至,硝酸钾会继续溶解,溶质质量增加;溶剂质量不变;溶解度会增大;溶质的质量分数变大,故选:。
故答案为:小于;
;
饱和;。
根据固体的溶解度曲线,可以比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小;可以判断物质的溶解度随温度变化的变化情况,从而判断温度改变后,溶液中各种成分的变化程度。
本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力。
15.【答案】时,甲和乙的 ( http: / / www.21cnjy.com )溶解度相等合理均可 蒸发溶剂或蒸发结晶 加入甲物质或恒温蒸发溶剂 增大
【解析】解:由溶解度曲线可 ( http: / / www.21cnjy.com )知:甲、乙两种固体物质的溶解度,都是随温度升高而增大,而甲的溶解度随温度的升高变化比乙大;或时,甲和乙的溶解度相等;故答案为:时,甲和乙的溶解度相等;
若甲中混有少量乙,提纯乙的方法是蒸发结晶或蒸发溶剂,因为甲的溶解度随温度的升高变化较大,而乙的溶解度受温度影响不大;
时,将不饱和的甲溶液转化成该温度下的饱和溶液的一种方法是:加入溶质或恒温蒸发溶剂,温度不变,不能采取降温的方法;
加入溶质,溶质的质量增加,溶剂质量不变,所以溶质质量分数变大;若恒温蒸发溶剂,溶质质量不变,溶剂质量减小,则溶质的质量分数增大;
将等质量的甲、乙两种物质的溶液由降温到,析出晶体的质量无法确定,因为没有指明是否是饱和溶液;
故答案为:时,甲和乙的溶解度相等合理均可; 蒸发溶剂或蒸发结晶; 加入甲物质或恒温蒸发溶剂; 增大; 。
根据题目信息和溶解度曲线可知:甲、乙两种固体物质的溶解度,都是随温度升高而增大,而甲的溶解度随温度的升高变化比乙大;或时,甲和乙的溶解度相等;
若甲中混有少量乙,提纯乙的方法是蒸发结晶或蒸发溶剂;
时,将不饱和的甲溶液转化成该温度下的饱和溶液的一种方法是:加入溶质或恒温蒸发溶剂;并据溶液中溶质、溶剂的质量变化分析溶质质量分数变化情况;
将等质量的甲、乙两种物质的溶液由降温到,析出晶体的质量无法确定,因为没有指明是否是饱和溶液。
本考点考查了主要溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液的结晶方法、饱和溶液与不饱和溶液的转化等,结合相关知识细心分析解答即可。
16.【答案】A.稀盐酸合理即可
B.碘在水和汽油中的溶解性
C.试管中无明显现象,试管中溶液由蓝色变为浅绿色,铁丝表面有红色固体析出
【解析】
【分析】
本题考查物质的鉴别 ( http: / / www.21cnjy.com )、溶解性及金属活动性顺序的比较等,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论。
【解答】
A.鉴别溶液和溶液可选用稀盐酸,能够产生气泡的是碳酸钠溶液,不产生气泡的是氯化钠溶液合理即可。
B.试管中加入一粒碘和水;试管中加入一粒碘和汽油。观察到中固体几乎不溶解,中固体全部溶解,该实验是为了比较碘在水和汽油中的溶解性。
C.金属活动性:锌铁铜,铁与溶液不反应,故试管中无明显现象;铁与溶液反应生成硫酸亚铁和铜,故试管中溶液由蓝色变为浅绿色,铁丝表面有红色固体析出。
17.【答案】;
温度是影响物质溶解性的因素
【解析】
【分析】
本题主要考查了能够影响溶解性的 ( http: / / www.21cnjy.com )因素,解答这类题时要注意尽可能的把题中的能够影响溶解性的因素找出,然后再利用控制变量法来进行判断,最后得出答案。
【解答】
根据上述设计,由第一组的数据分析,实验的温度、固体种类、固体质量、溶剂质量都相同,只有溶剂种类不同,则他们准备研究的影响因素是溶剂种类,由第二组的数据分析,实验的温度、固体种类、固体质量、溶剂质量、溶剂种类都相同,只有冰糖颗粒大小不同,则他们准备研究的影响因素是溶质颗粒大小,由第三组的数据分析,实验的温度、固体质量、溶剂质量、溶剂种类都相同,只有固体种类不同,则他们准备研究的影响因素是溶质种类,由第四组与第三组第一个实验比较可知,他们准备研究的影响因素是实验温度,第一组第一个实验和第三组第一个实验还可以研究影响因素是溶剂质量,溶质的质量并没有变化,所以没有研究它对溶解性的影响,故他们准备研究的影响因素是,其中不影响物质溶解性的因素是,故填:;;
根据第四组实验与前三组实验的比较,可以得到的结论是温度是影响物质溶解性的因素,故填:温度是影响物质溶解性的因素。
18.【答案】:
【解析】解:酸中氢、氧两种元素的质量比是::。
故答案为::。
设需要溶质质量分数为过氧乙酸溶液的质量为,根据溶液稀释前后溶质的质量不变,
则 。
。
答:需要溶质质量分数为过氧乙酸溶液为,需要溶质质量分数为过氧乙酸溶液。
根据化合物中各元素质量比各原子的相对原子质量原子个数之比,进行分析解答。
根据溶液稀释前后溶质的质量不变,进行分析解答。
本题难度不大,掌握溶液稀释前后溶质的质量不变、化学式的有关计算是正确解答此类题的关键所在。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
绝密★启用前
9.2 课题2 溶解度同步练习
人教版初中化学九年级下册
注意:本试卷包含Ⅰ、Ⅱ两卷。第Ⅰ卷 ( http: / / www.21cnjy.com )为选择题,所有答案必须用2B铅笔涂在答题卡中相应的位置。第Ⅱ卷为非选择题,所有答案必须填在答题卷的相应位置。答案写在试卷上均无效,不予记分。www.21-cn-jy.com
一、单选题(本大题共10小题,共20.0分)
1. 下列因素:溶质种类;溶剂种类;溶质质量;溶剂质量;温度;压强;搅拌、振荡.其中与固体溶解度无关的是 21·世纪*教育网
A. B. C. D.
2. 时向一定量不饱和溶液中逐渐加入固体,则下列图象中能正确表示此过程中溶质质量变化规律的是 21*cnjy*com
A. ( http: / / www.21cnjy.com ) B. ( http: / / www.21cnjy.com )
C. ( http: / / www.21cnjy.com ) D. ( http: / / www.21cnjy.com )
3. 甲和乙两种物质的溶解度曲线如图所示 ( http: / / www.21cnjy.com )。下列叙述正确的是
甲的溶解度随温度的升高而增大
时,使甲的饱和溶液析出晶体可用加热升温、冷却降温和蒸发溶剂三种方法
时,向溶质质量分数为的乙溶液中加入乙固体并振荡,有固体不溶解
将相同质量的甲和乙的饱和溶液分别从降温至,甲析出晶体的质量大
A. B. C. D.
4. 如图是甲、乙两种物质的溶解度曲线,下列说法不正确的是
A. 时,甲、乙两 ( http: / / www.21cnjy.com )种物质的溶解度相等
B. 甲物质的溶解度随温度的升高而增大
C. 将时甲、乙两种物质的饱和溶液降温到,溶液仍然饱和
D. 时,将甲物质加入水中,充分搅拌,能得到甲物质的饱和溶液
2-1-c-n-j-y
5. 能溶解在不同浓度的溶液中,其溶解度曲线如图所示。下列叙述错误的是
A. 时,溶液中的溶解度为
B. 时,在溶液中的溶解度大于在溶液中的溶解度
C. 时,在溶液中所溶解的质量,一定小于在溶液中所溶解的质量
D. 时,将溶解在溶液中达到饱和,然后降温至,该过程中一定析出固体
6. 甲、乙试管中各盛有向其中一支中加入固体,另一支中加入固体,按图进行实验和的溶解度曲线如图,下列说法正确的是
A. 甲中加入的固体是 时,甲中溶液可能饱和,乙中溶液一定饱和
C. 中含有少量杂质,可用冷却热饱和溶液的方法提纯
D. 时,若使图中甲、乙试管内的溶液恰好变为相应饱和溶液,甲中加入对应的溶质质量大于乙中加入对应的溶质质量
7. 如图是对一定质量的甲的溶液进行恒温蒸发结晶的实验过程,下列说法正确的是
A. 蒸发前原溶液是饱和溶液
B. 的数值是
C. 甲物质在时的溶解度是
D. 甲物质的溶解度随温度的升高而增大
8. 时,将一定量溶液平均分为三份,分别恒温蒸发出水的质量为、、,析出晶体的质量依次为、、,则、、三者的关系为
A. B. C. D.
9. 时氯化钾的溶解度为。下列是四位同学在时配制的氯化钾溶液,其中一定达到饱和的是
A. ( http: / / www.21cnjy.com ) B. ( http: / / www.21cnjy.com )
C. ( http: / / www.21cnjy.com ) D. ( http: / / www.21cnjy.com )
10. 已知:度在克以上的物质称为易溶物质;溶解度在克的物质为可溶物质;溶解度在克为微溶物质;溶解度小于克的物质为难溶物质。
时几种物质的溶解度如下 2·1·c·n·j·y
物质名称 氯化钠 氢氧化钙 氯酸钾 硝酸钾
溶解度克
下列说法正确的是
A. 时氢氧化钙是难溶物质
B. ( http: / / www.21cnjy.com )时可以配制出的硝酸钾溶液
C. 时氯酸钾是易溶物质
D. 时硝酸钾的溶解度比氯化钠大21·cn·jy·com
二、填空题(本大题共4小题,共32.0分)
11. 卤水的主要成分及其溶解度曲线如图 ( http: / / www.21cnjy.com )所示。
时,的溶解度______填“”、“”或“”的溶解度。
将时,、和三种物质的饱和溶液分别升温至时,有晶体析出的是______。
时,水中最多溶解的质量为______。
欲使的饱和溶液变为不饱和溶液,可以采取的措施是______任填一种。
12. 图为氯化钠、碳酸钠在水中的溶解度 ( http: / / www.21cnjy.com )曲线.请回答下列问题:
时,碳酸钠的溶解度为______;
时,氯化钠的溶解度______碳酸钠的溶解度填写“”、“”或“”;
时,向两只盛有水的烧杯中,分别加入氯化钠、碳酸钠两种物质,至不再溶解为止,所得溶液的溶质是______,其中______填溶质质量较大.
将碳酸钠不饱和溶液转化为饱和溶液的方法有______、______至少填两种.
如图所示,时,将盛有饱和碳酸钠溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出.加入的物质可能是______填字母序号.
A.氢氧化钠 氯化钠 硝酸铵.【来源:21·世纪·教育·网】
13. 学习化学知识的目的之一是分析和解决实际问题 ( http: / / www.21cnjy.com ).
甲烷、氢气都是可燃性气体,点燃可燃性气体之前都需要 ______ .
喝了汽水以后,常常会打嗝这说明气体的溶解度与 ______ 有关.
吸烟有害健康香烟烟气中含有几百种对人体有害的物质,如尼古丁、焦油、一氧化碳、二氧化碳等,其中与血红蛋白结合能力强的有毒气体是 ______ .
用洗涤剂清洗油污,是利用了洗涤剂的 ______ 作用.【版权所有:21教育】
14. 根据氯化钠和硝酸钾的溶解度表与溶解度曲线回答下列问题:
温度
溶解度 氯化钠
硝酸钾
时,氯化钠的溶解度 ______硝酸钾的溶解度大于、小于或等于。
图中能表示硝酸钾溶解度曲线的是 ______填“”或“”。
时,将硝酸钾放入水中,所得溶液是 ______溶液填“饱和”或“不饱和”,继续加热至,下列各量一定变大的是 ______填字母序号。
A.溶质质量
B.溶剂质量
C.溶解度
D.溶质的质量分数21教育网
三、推断题(本大题共1小题,共10.0分)
15. 如图是甲、乙两种固体物质的 ( http: / / www.21cnjy.com )溶解度曲线。
由图可获得一条信息是______。
若乙中混有少量甲,提纯乙的方法是______。
时,将不饱和的甲溶液,转化成该温度下的饱和溶液的一种方法是______,变化过程中,溶质的质量分数______选填“增大”、“减少”或“不变”。
将等质量的甲、乙两种物质的溶液由降温至时,析出晶体的质量______。
选序号甲乙 甲乙 无法确定。【出处:21教育名师】
四、实验题(本大题共2小题,共20.0分)
16. 如图所示,在两支试管中进行实验,补全实验方案。
序号 目的 步骤或现象
鉴别溶液和溶液 试管、中分别加入两种溶液;再向两支试管中加入 ______ 。
比较 ______ 试管中加入一粒碘和水;试管中加入一粒碘和汽油。观察到中固体几乎不溶解,中固体全部溶解。
比较锌、铁、铜的金属活动性 试管中加入溶液,试管中加入溶液;
再分别向两支试管中插入铁丝。观察到的现象是 ______ 。
17. 某兴趣小组利用家中的材料研究影响物质溶解性的因素,实验步骤设计如下:
Ⅰ、称取六份冰糖和一份食盐,每为一份,并将其中五份冰糖研磨成粉末。
Ⅱ、按照下表进行实验实验所需仪器略
( http: / / www.21cnjy.com )
请你对他们的实验设计进行分析:
根据上述设计,你认为他们准备 ( http: / / www.21cnjy.com )研究的影响因素是_____________从下列选项中选取,下同,其中不影响物质溶解性的因素是____________。溶质种类溶质颗粒大小实验温度溶剂种类溶剂质量溶质质量。
根据第四组实验与前三组实验的比较,你可以得到的结论是_________________________。21cnjy.com
五、计算题(本大题共1小题,共10.0分)
近期,巴西出现了寨卡病毒疫情。过 ( http: / / www.21cnjy.com )氧乙酸化学式为是常用的一种消毒剂,可用于疫情的消毒。请计算:
过氧乙酸中氢、氧两种元素的质量比是 ______;
多少溶质质量分数为过氧乙酸溶液与多少溶质质量分数为过氧乙酸溶液混合,可以得到的过氧乙酸溶液写计算过程。
18. www-2-1-cnjy-com
答案和解析
1.【答案】
【解析】解:当温度相同时,固体物 ( http: / / www.21cnjy.com )质不同则溶解度不同,如时氯化钠的溶解度为,而硝酸钾的溶解度为,所以溶质种类影响固体物质的溶解度,正确;
溶剂种类能影响固体物质的溶解度,如碘容易溶解在酒精中,不易溶解在水中,故碘在酒精中的溶解度大,正确;
根据溶解度的定义,某物质在溶剂里达到饱和所溶解的溶质的质量,是该温度下的溶解度,故,溶质质量不影响固体物质的溶解度,不对;
根据溶解度的定义,某温度时溶剂中最多溶解的质量为该温度时该物质的溶解度,所以溶剂质量不影响固体物质的溶解度,不对;
大多数固体物质的溶解度随温度的升高而增大,少数物质的溶解度受温度变化影响不大,极少数物质溶解度随温度的升高而减小,即温度影响固体物质的溶解度,正确;
压强的改变不影响固体物质的溶解度,此项不对.
搅拌、振荡的作用是加速固体物质的溶解速率,不会使物质溶解的更多,所以搅拌不影响固体物质的溶解度,不对;
故选C.
物质的溶解度是物质溶解能力的定量表示,溶解能力的大小与溶质和溶剂的种类有关.大多数固体物质的溶解度随温度的升高而增大,所以固体物质的溶解度与温度有关.由溶解度的定义可知,不管溶质或溶剂的量有多少,固体的溶解度都只看在溶剂中达到饱和状态时所能溶解溶质的质量,所以固体物质的溶解度与溶质质量和溶剂质量无关;固体的溶解度与压强无关,搅拌、振荡只能加快溶解的速率,而不能增大溶解的质量,故溶解度与是否搅拌或振荡无关.
该题考查的是影响固体物质溶解度的因素,解答时要结合溶解度的概念,理解溶解度的含义,结合题目中的选项细致分析对溶解度是否产生影响,对”溶剂质量不影响固体物质的溶解度“要加深理解.一般地,影响固体溶解度的因素有三:温度、溶质种类、溶剂种类.
21世纪教育网版权所有
2.【答案】
【解析】解:、不饱和溶液中含有一定量的溶质硝酸钾,不会从开始,故A错误;
B、向一定量不饱和溶液中逐渐加入固体时,硝酸钾能够继续溶解,直到达到饱和状态,故B错误;
C、向一定量不饱和溶液中逐渐加入固体时,硝酸钾能够继续溶解,达到饱和状态时不再溶解,故C正确;
D、在一定温度下,在一定量的溶剂里,硝酸钾不能无限溶解,故D错误。
故选C。
在一定温度下,在一定量的溶剂里,硝酸钾的溶解能力是有一定的限度的。
本题主要考查物质的溶解能力,解答时要注意在一定温度下,在一定量的溶剂里,硝酸钾的溶解能力不是无限的。
21教育名师原创作品
3.【答案】
【解析】
【分析】
本题难度不是很大,主要考查了固 ( http: / / www.21cnjy.com )体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力。
【解答】
通过分析溶解度曲线可知,小于时,甲的溶解度随温度的升高而增大,故错误;
小于时或大于时,甲物质的溶解度随温度的降低、升高时,溶解度都会减少,所以时,使甲的饱和溶液析出晶体可用加热升温、冷却降温和蒸发溶剂三种方法,故正确;
时,乙物质的溶解度是,向溶质质量分数为的乙溶液中含有溶质质量为:,加入乙固体并振荡,有固体不溶解,故正确;
将相同质量的甲和乙的饱和溶液分别从降温至,甲物质的溶解度变化最大,所以甲析出晶体的质量大,故正确。
故选:。
4.【答案】
【解析】解:、通过分析溶 ( http: / / www.21cnjy.com )解度曲线可知,时,甲、乙两种物质的溶解度相等,故A正确;
B、甲物质的溶解度随温度的升高而增大,故B正确;
C、将时甲、乙两种物质的饱和溶液降温到,乙物质的溶解度最大,甲物质的溶解度减小,所以甲物质的溶液仍然饱和,乙物质的溶液不饱和,故C错误;
D、时,甲物质的溶解度是,所以将甲物质加入水中,充分搅拌,能得到甲物质的饱和溶液,故D正确。
故选:。
根据固体的溶解度曲线可以:查出某物质在一定温度下的溶解度,从而确定物质的溶解性,比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的。
本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力。
5.【答案】
【解析】解:、由溶解度曲线可知:时,在溶液中的溶解度为正确,正确但不符合题意,故选项错误;
B、时,在溶液中的溶解度大于在溶液中的溶解度正确,正确但不符合题意,故选项错误;
C、时,在溶液中所溶解的质量,一定小于在溶液中所溶解的质量错误,因为没有指明溶剂的质量,错误符合题意,故选项正确;
D、时,将溶解在溶液中达到饱和,然后降温至,该过程中一定析出固体正确,因为的溶解度随温度的降低而减小,正确但不符合题意,故选项错误。
本考点考查了溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液的变化等,本考点主要出现在选择题和填空题中。
6.【答案】
【解析】
【分析】
本题难度不是很大, ( http: / / www.21cnjy.com )主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力。
【解答】
A、时,氯化钠的溶解度大于,硝酸钾的溶解度小于,甲、乙试管中各盛有水,向其中一支中加入固体,另一支中加入固体,降温到时,乙中有晶体析出,所以乙中加入的固体是,故A错误;
B、时,氯化钠的溶解度大于,硝酸钾的溶解度小于,的水中可以溶解的氯化钠,乙中有晶体析出,所以时,甲中溶液一定不饱和,乙中溶液一定饱和,故B错误;
C、硝酸钾的溶解度受温度变化影响较大,所以中含有少量杂质,可用冷却热饱和溶液的方法提纯,故C正确;
D、时,硝酸钾的溶解度大于氯化钠的溶解度,所以若使图中甲、乙试管内的溶液恰好变为相应饱和溶液,甲中加入对应的溶质质量小于乙中加入对应的溶质质量,故D错误。
故选C。
7.【答案】
【解析】解:、蒸发前的烧杯底部没 ( http: / / www.21cnjy.com )有固体,第一次蒸发水,析出晶体,第二次蒸发水析出晶体,所以蒸发前原溶液是不饱和溶液,错误;
B、蒸发前的烧杯底部没有固体,第一次蒸发水,析出晶体,第二次蒸发水析出晶体,所以第三次蒸发水析出晶体,所以共析出,错误;
C、蒸发水析出晶体,则水中最多能溶解甲,故甲物质在时的溶解度是,正确;
D、题中析出晶体是通过蒸发溶剂得到的,不能判断出温度对溶解度的影响,错误;
故选:。
本题是对物质溶解度、蒸发结晶等知识的考查,解决的重点是能理解溶解度、结晶以及物质溶解度随温度的变化,并能利用相关知识分析并解决问题。
8.【答案】
【解析】
【分析】
本题考查溶液中的相关计算, ( http: / / www.21cnjy.com )解此类题只要善于分解全过程,创设可比中间态,就可以快速求解,大大节约做题时间;当然,只有在做题的过程中,有意识地去使用过程分解法,才能熟练地掌握这种解题技巧。
【解答】
第一份溶液蒸发溶剂,析出晶体后,得到饱和溶液,设为;
第二份溶液析出晶体的过程可以分解为第一步:先蒸发溶剂,析出晶体,得到同于第一份溶液的析晶过程;第二步:对饱和溶液继续处理,再蒸发溶剂,再析出晶体,仍得到饱和溶液,设为,由此可知此温度下该物质饱和溶液中溶质与溶剂的比为;
第三份溶液析出晶体的过程可以分解为第一步:先蒸发溶剂,析出晶体,得到同于第二份溶液的析晶过程;
第二步:对饱和溶液继续处理,再蒸发溶剂,再析出晶体,仍得到饱和溶液;由此可知此温度下该物质饱和溶液中溶质与溶剂的比为;
因为一定温度下饱和溶液中溶质与溶剂的比为一定值,则有,则,或利用水中所含溶质的量作为相等关系得:,整理可得。
故选B。
9.【答案】
【解析】
【分析】
本题难度不大,掌握溶解度的含义 ( http: / / www.21cnjy.com )、饱和溶液的特征等并能灵活运用是正确解答本题的关键。
【解答】
A、时氯化钾的溶解度为,含义是时,水中最多能溶解氯化钾,溶液达到饱和状态,则时,水中最多能溶解氯化钾,溶液达到饱和状态,向水中加入氯化钾,所得溶液是不饱和溶液,故选项错误。
B、向水中加入氯化钾,所得溶液恰好是饱和溶液,故选项正确。
C、时,水中最多能溶解氯化钾,时,向水中加入氯化钾,所得溶液是不饱和溶液,故选项错误。
D、时,向水中加入氯化钾,所得溶液是不饱和溶液,故选项错误。
故选B。 21*cnjy*com
10.【答案】
【解析】解:时氢氧化钙的溶解度是,在之间,属于微溶物质,故A说法不正确;
B、时硝酸钾的溶解度是,饱和溶液的溶质质量分数是:,所以可以配制出的硝酸钾溶液,故B说法正确;
C、时氯酸钾的溶解度是,在之间,属于可溶物质,故C说法不正确;
D、由表中的数据可知,时硝酸钾的溶解度比氯化钠小,故D说法不正确。
故选:。
A、根据在时氢氧化钙的溶解度分析;
B、根据时硝酸钾溶解度、饱和溶液的溶质质量分数分析;
C、根据在时氯酸钾的溶解度分析;
D、根据在时硝酸钾、氯化钠的溶解度分析。
本题难度不是很大,主要考查了固体的溶解度含义,会根据固体的溶解度的含义解决相关的问题,从而培养分析问题、解决问题的能力。
【来源:21cnj*y.co*m】
11.【答案】;
硫酸镁;
;
升高温度。
【解析】解:通过分析溶解度曲线可知 ( http: / / www.21cnjy.com ),时,的溶解度的溶解度;
将时,、和三种物质的饱和溶液分别升温至时,硫酸镁的溶解度减小,氯化镁、氯化钾的溶解度增大,所以有晶体析出的是硫酸镁;
时,氯化镁的溶解度是,所以水中最多溶解的质量为;
氯化镁的溶解度随温度的升高而增大,所以欲使的饱和溶液变为不饱和溶液,可以采取的措施是升高温度。
故答案为:;
硫酸镁;
;
升高温度。
根据固体的溶解度曲线可以:查出某物质在一定温度下的溶解度,从而确定物质的溶解性,比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的。
本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力。
12.【答案】 氯化钠、碳酸钠 氯化钠 加碳酸钠 蒸发水、降温
【解析】解:的溶解度为;
曲线中交点表示该温度时两种物质的溶解度相等,所以时氯化钠和碳酸钠两物质的溶解度相等;
时,碳酸钠的溶解度为,氯化钠的溶解度大于碳酸钠,所以所得溶液中食盐的质量多.
碳酸钠的溶解度随温度升高而增大,将碳酸钠不饱和溶液转化为饱和溶液的方法有加碳酸钠,蒸发水、降温.
由饱和碳酸钠溶液的小试管放入盛水的烧杯中,向水中加入某物质后,试管中有晶体析出,说明温度降低了,也就是说该物质溶于水是吸热的,所以为硝酸铵.
故答案为:
;
;
氯化钠、碳酸钠;氯化钠;
;
加碳酸钠,蒸发水、降温;
.
根据溶解度曲线的意义解答;
根据曲线中交点的含义考虑;
关键要根据该温度时的溶解度看所加物质是否全部溶解;
根据饱和溶液与不饱和溶液之间的转化方法解答;
物质溶于水吸热和放热情况考虑.
溶解度曲线能定量地表示出溶解度变化的规律.从溶解度曲线可以看出:同一溶质在不同温度下的溶解度;同一温度下,不同溶质的溶解度;温度对不同物质的溶解度影响不同.
13.【答案】验纯 温度 一氧化碳 乳化
【解析】解:可燃性气体点 ( http: / / www.21cnjy.com )燃之前必须验纯,防止不纯点燃发生爆炸.
喝了汽水以后,常常会打嗝,是由于胃内的温度比外界高二氧化碳的溶解度变小而导致的.
当一氧化碳随呼吸进入人体血液后,便于血液中的血红蛋白结合从而使血红蛋白丧失输送氧的能力,导致一氧化碳中毒.
用洗涤剂清洗油污,是利用了洗涤剂的乳化作用;
故答案为:验纯;
温度;
一氧化碳;
乳化.
根据可燃性气体点燃之前必须验纯分析解答;
利用气体的溶解度随温度的升高而降低,随着压强的增大而增大分析;
从一氧化碳中毒的原理分析;
洗涤剂有乳化作用;
学习化学的目的,重要的是善于用化学知识去分析、解决生产生活中的问题.
14.【答案】小于 饱和
【解析】解:中数据可知,时,氯化钠的溶解度小于硝酸钾的溶解度;
由表中的数据可知,硝酸钾的溶解度受温度变化影响较大,所以图中能表示硝酸钾溶解度曲线的是;
在时,硝酸钾的溶解度是,水中最多溶解的硝酸钾,所以时,将硝酸钾固体投入水中,充分溶解后可得到硝酸钾饱和溶液;继续加热至,硝酸钾会继续溶解,溶质质量增加;溶剂质量不变;溶解度会增大;溶质的质量分数变大,故选:。
故答案为:小于;
;
饱和;。
根据固体的溶解度曲线,可以比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小;可以判断物质的溶解度随温度变化的变化情况,从而判断温度改变后,溶液中各种成分的变化程度。
本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力。
15.【答案】时,甲和乙的 ( http: / / www.21cnjy.com )溶解度相等合理均可 蒸发溶剂或蒸发结晶 加入甲物质或恒温蒸发溶剂 增大
【解析】解:由溶解度曲线可 ( http: / / www.21cnjy.com )知:甲、乙两种固体物质的溶解度,都是随温度升高而增大,而甲的溶解度随温度的升高变化比乙大;或时,甲和乙的溶解度相等;故答案为:时,甲和乙的溶解度相等;
若甲中混有少量乙,提纯乙的方法是蒸发结晶或蒸发溶剂,因为甲的溶解度随温度的升高变化较大,而乙的溶解度受温度影响不大;
时,将不饱和的甲溶液转化成该温度下的饱和溶液的一种方法是:加入溶质或恒温蒸发溶剂,温度不变,不能采取降温的方法;
加入溶质,溶质的质量增加,溶剂质量不变,所以溶质质量分数变大;若恒温蒸发溶剂,溶质质量不变,溶剂质量减小,则溶质的质量分数增大;
将等质量的甲、乙两种物质的溶液由降温到,析出晶体的质量无法确定,因为没有指明是否是饱和溶液;
故答案为:时,甲和乙的溶解度相等合理均可; 蒸发溶剂或蒸发结晶; 加入甲物质或恒温蒸发溶剂; 增大; 。
根据题目信息和溶解度曲线可知:甲、乙两种固体物质的溶解度,都是随温度升高而增大,而甲的溶解度随温度的升高变化比乙大;或时,甲和乙的溶解度相等;
若甲中混有少量乙,提纯乙的方法是蒸发结晶或蒸发溶剂;
时,将不饱和的甲溶液转化成该温度下的饱和溶液的一种方法是:加入溶质或恒温蒸发溶剂;并据溶液中溶质、溶剂的质量变化分析溶质质量分数变化情况;
将等质量的甲、乙两种物质的溶液由降温到,析出晶体的质量无法确定,因为没有指明是否是饱和溶液。
本考点考查了主要溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液的结晶方法、饱和溶液与不饱和溶液的转化等,结合相关知识细心分析解答即可。
16.【答案】A.稀盐酸合理即可
B.碘在水和汽油中的溶解性
C.试管中无明显现象,试管中溶液由蓝色变为浅绿色,铁丝表面有红色固体析出
【解析】
【分析】
本题考查物质的鉴别 ( http: / / www.21cnjy.com )、溶解性及金属活动性顺序的比较等,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论。
【解答】
A.鉴别溶液和溶液可选用稀盐酸,能够产生气泡的是碳酸钠溶液,不产生气泡的是氯化钠溶液合理即可。
B.试管中加入一粒碘和水;试管中加入一粒碘和汽油。观察到中固体几乎不溶解,中固体全部溶解,该实验是为了比较碘在水和汽油中的溶解性。
C.金属活动性:锌铁铜,铁与溶液不反应,故试管中无明显现象;铁与溶液反应生成硫酸亚铁和铜,故试管中溶液由蓝色变为浅绿色,铁丝表面有红色固体析出。
17.【答案】;
温度是影响物质溶解性的因素
【解析】
【分析】
本题主要考查了能够影响溶解性的 ( http: / / www.21cnjy.com )因素,解答这类题时要注意尽可能的把题中的能够影响溶解性的因素找出,然后再利用控制变量法来进行判断,最后得出答案。
【解答】
根据上述设计,由第一组的数据分析,实验的温度、固体种类、固体质量、溶剂质量都相同,只有溶剂种类不同,则他们准备研究的影响因素是溶剂种类,由第二组的数据分析,实验的温度、固体种类、固体质量、溶剂质量、溶剂种类都相同,只有冰糖颗粒大小不同,则他们准备研究的影响因素是溶质颗粒大小,由第三组的数据分析,实验的温度、固体质量、溶剂质量、溶剂种类都相同,只有固体种类不同,则他们准备研究的影响因素是溶质种类,由第四组与第三组第一个实验比较可知,他们准备研究的影响因素是实验温度,第一组第一个实验和第三组第一个实验还可以研究影响因素是溶剂质量,溶质的质量并没有变化,所以没有研究它对溶解性的影响,故他们准备研究的影响因素是,其中不影响物质溶解性的因素是,故填:;;
根据第四组实验与前三组实验的比较,可以得到的结论是温度是影响物质溶解性的因素,故填:温度是影响物质溶解性的因素。
18.【答案】:
【解析】解:酸中氢、氧两种元素的质量比是::。
故答案为::。
设需要溶质质量分数为过氧乙酸溶液的质量为,根据溶液稀释前后溶质的质量不变,
则 。
。
答:需要溶质质量分数为过氧乙酸溶液为,需要溶质质量分数为过氧乙酸溶液。
根据化合物中各元素质量比各原子的相对原子质量原子个数之比,进行分析解答。
根据溶液稀释前后溶质的质量不变,进行分析解答。
本题难度不大,掌握溶液稀释前后溶质的质量不变、化学式的有关计算是正确解答此类题的关键所在。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
HYPERLINK "http://21世纪教育网(www.21cnjy.com)
" 21世纪教育网(www.21cnjy.com)
同课章节目录
