人教版九年级化学第7单元 燃料及其利用 单元测试卷(解析版)
文档属性
| 名称 | 人教版九年级化学第7单元 燃料及其利用 单元测试卷(解析版) |

|
|
| 格式 | doc | ||
| 文件大小 | 291.0KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-21 00:00:00 | ||
图片预览




文档简介
人教版九年级上册《第7单元 燃料及其利用》2021年单元测试卷二
一.选择题(共15小题)
1.对下列物质用途的描述,不符合事实的是( )
A.石墨可以制铅笔芯
B.氮气是食品包装袋中的一种防腐剂
C.活性炭可以用于软化硬水
D.二氧化碳可用于人工降雨
2.关于燃烧与灭火,下列说法正确的是( )
A.可燃物燃烧一定会生成二氧化碳
B.家用电器着火时,应立即用水浇灭
C.在加油站使用手机可能引发燃烧、爆炸
D.厨房中天然气泄漏时,可打开抽排油烟机排气
3.我市拥有丰富的页岩气,它与天然气的主要成分都是甲烷(CH4),下列关于页岩气的说法不正确的是( )
A.它是混合物
B.加压使之液化,其分子间的间隔不变
C.它充分燃烧会生成H2O和CO2
D.它与空气混合点燃易发生爆炸
4.下列有关金属和金属材料的说法正确的是( )
A.金属材料包括纯金属和合金
B.铁制品生锈后没有回收价值
C.生铁的含碳量比钢低
D.铝很活泼,所以铝制品在空气中易腐蚀生锈
5.下列做法正确的是( )
A.电器着火用水扑灭
B.室内起火时打开门窗通风
C.油锅着火用锅盖盖灭
D.用明火检查液化气罐是否漏气
6.“纸火锅”(如图所示)是用纸张代替金属材料做容器盛放汤料,当酒精燃烧时纸张不会燃烧.对此现象,下列解释合理的是( )
A.纸张不是可燃物,不能燃烧
B.纸张没有与空气充足接触,不会燃烧
C.纸张被水浸湿,导致纸张的着火点降低
D.锅里的水蒸发时吸收热量,温度达不到纸张的着火点
7.下列关于燃烧与灭火的说法中,正确的是( )
A.蜡烛用嘴一吹即灭,是因为吹出的气体主要是二氧化碳
B.将大块煤粉碎后再燃烧,其目的是延迟煤燃烧的时间
C.如图a,火柴头斜向下时更容易燃烧,是因为降低了火柴梗的着火点
D.由图b的现象可知,金属镁引起的火灾不能用二氧化碳灭火
8.下列实验现象描述正确的是( )
A.红磷在空气中燃烧发出蓝色火焰
B.电解水的实验中正极产生的气体体积是负极产生的气体体积的2倍
C.向硫酸铜溶液中滴加氢氧化钠溶液产生蓝色沉淀
D.做铁钉生锈的对比实验时,最先生锈的是浸没在蒸馏水中的铁钉
9.下列有关燃烧的说法正确的是( )
A.天然气泄漏时,立即打开排气扇电源开关
B.白磷在冷水,通入空气后能燃烧
C.用水灭火,目的是降低可燃物的着火点
D.发生火灾时,应用湿毛巾捂住口鼻,匍匐前进
10.水是重要资源,下列说法正确的是( )
A.过滤或加热均能使硬水转化为软水
B.活性炭的吸附作用可使海水转化为淡水
C.电解水得到的H2和O2质量比为2:1
D.氢气在纯氧中燃烧的实验说明水由氢元素和氧元素组成
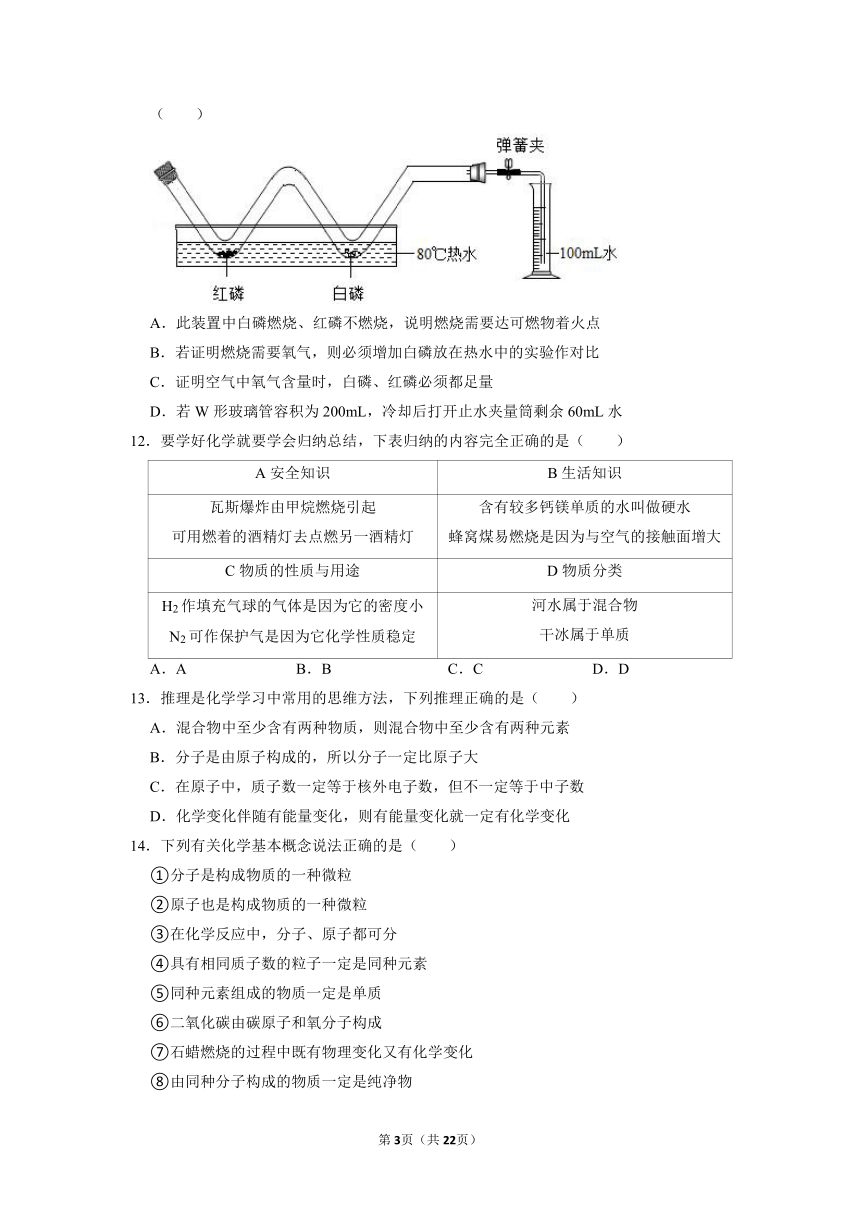
11.化学小组用如图进行实验,探究燃烧条件并测定空气中氧气含量,下列说法错误的是( )
A.此装置中白磷燃烧、红磷不燃烧,说明燃烧需要达可燃物着火点
B.若证明燃烧需要氧气,则必须增加白磷放在热水中的实验作对比
C.证明空气中氧气含量时,白磷、红磷必须都足量
D.若W形玻璃管容积为200mL,冷却后打开止水夹量筒剩余60mL水
12.要学好化学就要学会归纳总结,下表归纳的内容完全正确的是( )
A安全知识 B生活知识
瓦斯爆炸由甲烷燃烧引起可用燃着的酒精灯去点燃另一酒精灯 含有较多钙镁单质的水叫做硬水蜂窝煤易燃烧是因为与空气的接触面增大
C物质的性质与用途 D物质分类
H2作填充气球的气体是因为它的密度小N2可作保护气是因为它化学性质稳定 河水属于混合物干冰属于单质
A.A B.B C.C D.D
13.推理是化学学习中常用的思维方法,下列推理正确的是( )
A.混合物中至少含有两种物质,则混合物中至少含有两种元素
B.分子是由原子构成的,所以分子一定比原子大
C.在原子中,质子数一定等于核外电子数,但不一定等于中子数
D.化学变化伴随有能量变化,则有能量变化就一定有化学变化
14.下列有关化学基本概念说法正确的是( )
①分子是构成物质的一种微粒
②原子也是构成物质的一种微粒
③在化学反应中,分子、原子都可分
④具有相同质子数的粒子一定是同种元素
⑤同种元素组成的物质一定是单质
⑥二氧化碳由碳原子和氧分子构成
⑦石蜡燃烧的过程中既有物理变化又有化学变化
⑧由同种分子构成的物质一定是纯净物
A.①②③④ B.①②⑤⑦ C.①②④⑧ D.①②⑦⑧
15.下列关于碳及其化合物的说法,正确的是( )
A.二氧化碳是导致酸雨的主要气体
B.可以用燃烧法除去二氧化碳中混有的少量一氧化碳
C.中国古代字画经久不褪色,因为常温下碳的化学性质不活泼
D.CO和CO2都是非金属氧化物,都能与NaOH溶液反应
二.填空题(共4小题)
16.在N2、H2、O2、CO、CO2、SO2六种物质中,可用做理想高能燃料,且燃烧产物不污染环境的是 ;能使带火星的木条复燃的是 ;既有可燃性又有还原性的气体化合物是 .
17.随着经济的发展,能源与环境成为人们日益关注的问题.
(1)煤、 和 常称为化石燃料.
(2)燃煤发电时,将煤块粉碎成煤粉,其目的是 .
(3)化石燃料燃烧都会产生二氧化碳,它是空气中含量最多的温室气体为减少它的排放,科学家致力于研究将过多的二氧化碳和氢气在催化剂和加热的条件下反应,转化为水和甲烷.该反应的化学方程式为 .
(4)“绿色化学”的特点之一是“零排放”.一定条件下,二氧化碳和氢气可以按照不同比例反应,生成下列有机物.其中二氧化碳和氢气反应,只生成一种产物就能实现“零排放”,这种产物是 (填字母序号,下同).
A.甲醇(CH4O)
B.甲酸(CH2O2)
C.乙醇(C2H6O)
D.乙酸(C2H4O2)
(5)下列措施中,有利于降低大气中二氧化碳含量的是 .
A.大量使用化石燃料
B.植树造林,增大植被面积
C.将二氧化碳变废为宝,循环利用
18.多角度认识物质的变化,有助于我们更好地理解化学知识.
(1)从微观角度(图 1 为某化学反应的微观示意图,据图回答下列问题.)
①微观上看,该化学变化中发生根本改变的微粒是 (填“原子”或“分子”);
②参加反应的 A2与 B2两种物质的分子个数比为 ;
(2)从物质转化角度(一种物质可通过不同的反应类型生成,以二氧化碳为例)
①能与氧气化合生成二氧化碳的物质是 (填一种物质化学式);
②高温下,石灰石分解生成二氧化碳的化学方程式是 .
(3)从能量变化角度(借用图 2 装置分别进行进行下列实验,认识物质变化中的能量变化)
①往烧杯中加入一定量生石灰会引起白磷燃烧,从燃烧条件分析,此时生石灰的作用是 ,写出生石灰与水反应的化学方程式 ;
②将一定量的下列某物质溶于烧杯中的冷水,其中能引起白磷燃烧的是 (填标号)。
A.氯化钠 B.硝酸铵 C.浓硫酸 D.氢氧化钠
19.化学就在我们身边,与我们的生活有着密切的联系。
(1)“萍水相逢 缘聚天下”。
①萍乡武功山温泉﹣﹣“富硒养生”。其中“硒”指的是 (选填“原子”“离子”或“元素”)。
②莲花的苏轼蜜酒﹣﹣“美酒飘香”。从分子角度解释“美酒飘香”的原因 ;酒中含有乙醇,乙醇燃烧的化学方程式为 。
(2)随着科技进步,人类对能源的需求量日益增长。为了应对能源危机,可以开发和利用新能源,而在各种新能源中, 被认为是最清洁的高能燃料。
三.推断题(共1小题)
20.A~G是初中化学常见的七种物质,且A、B、C、D、E属于单质、氧化物、酸、碱、盐五种不同类别的物质,它们之间的关系如图所示。(“﹣”表示相连的物质能相互反应;“→”表示物质间的转化关系;部分反应物、生成物及反应条件未标出)。已知A物质中含有三种元素;B是使用最广泛的金属单质;物质C的溶液呈蓝色;反应①②的现象相同,都产生白色沉淀;D、G两种物质类别相同,且都易溶于水。试回答:
(1)写出物质C的化学式:C 。
(2)物质E的一种用途是 。
(3)写出D→F的化学方程式 ,写出A与G反应的化学方程式 。
四.实验探究题(共2小题)
21.根据下列实验装置图回答问题。
(1)写出标有字母a的仪器名称: 。
(2)实验室用装置A制取氧气的化学方程式为 。
(3)如图中装置 (填字母)可用来收集氧气。
(4)将反应生成的氧气通入D中,使其接触底部的白磷后,看到的现象是 ,说明可燃物燃烧需要的条件之一是 。
22.化学是一门以实验为基础的学科.根据图1,回答问题.
(1)a仪器的名称为 .
(2)实验室用A装置制O2的化学方程式为 ,选用的收集装置是 (填字母序号).查阅资料后可知,锰酸钾可溶于水,若要从高锰酸钾完全分解后的固体残渣中回收二氧化锰,正确操作的顺序是 (填写选项序号).
a.烘干 b.溶解 c.过滤 d.洗涤
(3)制取CO2用装置F替代装置B的优点是 .通过装置B、E来验证二氧化碳的性质,实验过程中观察到E中有气泡冒出,但澄清的石灰水未变浑浊,试分析其可能的原因 .
(4)氨气是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水.实验室用加热氯化铵和氢氧化钙的固体混合物制取氨气,其发生装置(图2),可选用 (填装置编号),收集氨气时最好选用下列装置中的G装置与 装置相连接(填数字编号).
五.计算题(共2小题)
23.波尔多液是一种农业上常用的杀虫剂,它由硫酸铜、生石灰加水配制而成。
(1)硫酸铜所含阴离子的符号是 ;生石灰属于 (填物质种类),生活中可用于 。
(2)煅烧石灰石(主要成分CaCO3)可制得生石灰(CaO),若要制取11.2t氧化钙,根据化学方程式计算需要碳酸钙的质量是多少?
(3)波尔多液等农药常常配成乳浊液或悬浊液的原因是: 。
24.小丽为探究某石灰石样品中碳酸钙的含量,称取500g样品,磨成粉末后,放在电炉上高温煅烧至质量不再发生变化,称量剩余物质量为302g(假设石灰石样品中杂质不参加反应).据此计算:
(1)生成二氧化碳质量
(2)此石灰石样品中碳酸钙的百分含量.
人教版九年级上册《第7单元 燃料及其利用》2021年单元测试卷二
参考答案与试题解析
一.选择题(共15小题)
1.对下列物质用途的描述,不符合事实的是( )
A.石墨可以制铅笔芯
B.氮气是食品包装袋中的一种防腐剂
C.活性炭可以用于软化硬水
D.二氧化碳可用于人工降雨
【解答】解:A、石墨很软,可用于制铅笔芯,故正确;
B、氮气化学性质稳定,可以做食品包装中的防腐剂,故正确;
C、活性炭具有吸附性,能吸附水中的杂质而不能将将硬水软化,故错误;
D、二氧化碳固体干冰易升华同时吸收大量的热,可用于人工降雨,故正确;
故选:C。
2.关于燃烧与灭火,下列说法正确的是( )
A.可燃物燃烧一定会生成二氧化碳
B.家用电器着火时,应立即用水浇灭
C.在加油站使用手机可能引发燃烧、爆炸
D.厨房中天然气泄漏时,可打开抽排油烟机排气
【解答】解:A.氢气燃烧后只生成水,没有二氧化碳生成,故错误;
B.家用电器着火时,不能用水浇灭,以防触电,故错误;
C.在加油站附近的空气中弥漫着可燃性气体,与空气混合,接打手机产生的电火花可能会引燃甚至引起爆炸,故正确;
D.可燃性气体遇到电火花时可能爆炸,而打开油烟机时产生电火花,故错误。
故选:C。
3.我市拥有丰富的页岩气,它与天然气的主要成分都是甲烷(CH4),下列关于页岩气的说法不正确的是( )
A.它是混合物
B.加压使之液化,其分子间的间隔不变
C.它充分燃烧会生成H2O和CO2
D.它与空气混合点燃易发生爆炸
【解答】解:A、页岩气是甲烷和杂质的混合物,正确但不符合题意,故选项错误;
B、加压使之液化,其分子间的间隔不变错误,分子间隔变小,错误符合题意,故选项正确;
C、甲烷充分燃烧会生成H2O和CO2正确,正确但不符合题意,故选项错误;
D、它与空气混合点燃易发生爆炸正确,因为它具有可燃性,正确但不符合题意,故选项错误;
故选:B。
4.下列有关金属和金属材料的说法正确的是( )
A.金属材料包括纯金属和合金
B.铁制品生锈后没有回收价值
C.生铁的含碳量比钢低
D.铝很活泼,所以铝制品在空气中易腐蚀生锈
【解答】解:A.金属材料包括纯金属和合金,选项说法正确;
B.回收生锈的钢铁既可以节约金属资源,又可以防止环境污染,选项说法错误;
C.生铁中的含碳量为2%~4.3%,钢中的含碳量为0.03%~2%,故生铁的含碳量比钢高,选项说法错误;
D.铝的化学性质较活泼,在空气中易与空气的氧气反应,在铝制品表面形成一层致密的氧化铝保护膜,所以铝制品耐腐蚀,选项说法错误。
故选:A。
5.下列做法正确的是( )
A.电器着火用水扑灭
B.室内起火时打开门窗通风
C.油锅着火用锅盖盖灭
D.用明火检查液化气罐是否漏气
【解答】解:A、电器着火若用水扑灭极易造成电线短路和人体触电,所以电器着火应先切断电源,再灭火;故错;
B、根据燃烧的条件;可燃物燃烧需要与氧气接触,室内失火时,打开门窗,造成空气对流,氧气量充足,使火势加大。故错;
C、用锅盖盖灭,隔绝了氧气使油熄灭;故对;
D、用明火检查液化气罐是否漏气极易引燃液化气而发生火灾;故错。
故选:C。
6.“纸火锅”(如图所示)是用纸张代替金属材料做容器盛放汤料,当酒精燃烧时纸张不会燃烧.对此现象,下列解释合理的是( )
A.纸张不是可燃物,不能燃烧
B.纸张没有与空气充足接触,不会燃烧
C.纸张被水浸湿,导致纸张的着火点降低
D.锅里的水蒸发时吸收热量,温度达不到纸张的着火点
【解答】解:A、纸张具有可燃性,是可燃物,不能燃烧是因为温度没有达到纸张的着火点,故选项解释错误。
B、纸张与空气充分接触,不能燃烧是因为温度没有达到纸张的着火点,故选项解释错误。
C、可燃物的着火点一般是不变的,纸张的着火点一般情况下不能改变,故选项解释错误。
D、水蒸发时吸热,导致温度达不到纸张的着火点,因此纸张不能燃烧,故选项解释正确。
故选:D。
7.下列关于燃烧与灭火的说法中,正确的是( )
A.蜡烛用嘴一吹即灭,是因为吹出的气体主要是二氧化碳
B.将大块煤粉碎后再燃烧,其目的是延迟煤燃烧的时间
C.如图a,火柴头斜向下时更容易燃烧,是因为降低了火柴梗的着火点
D.由图b的现象可知,金属镁引起的火灾不能用二氧化碳灭火
【解答】解:A.蜡烛用嘴一吹即灭,是因为空气流通带走热量,造成蜡烛温度低于其着火点而灭火,故错误;
B.将大块煤粉碎后再燃烧,其目的是增大与氧气的接触面积,促进燃烧,故错误;
C.如图a,火柴头斜向下时更容易燃烧,是因为火柴梗的温度更容易达到其着火点,故错误;
D.镁条能在二氧化碳中燃烧,所以金属镁引起的火灾不能用二氧化碳灭火,故正确;
故选:D。
8.下列实验现象描述正确的是( )
A.红磷在空气中燃烧发出蓝色火焰
B.电解水的实验中正极产生的气体体积是负极产生的气体体积的2倍
C.向硫酸铜溶液中滴加氢氧化钠溶液产生蓝色沉淀
D.做铁钉生锈的对比实验时,最先生锈的是浸没在蒸馏水中的铁钉
【解答】解:A、红磷在空气中燃烧,发出黄色火焰,产生大量的白烟,故选项说法错误.
B、电解水时,可观察到:与电源正极相连的试管内产生的气体体积少,与电源负极相连的试管内的气体体积多,且两者的体积之比大约是1:2,故选项说法错误。
C、氢氧化钠溶液与硫酸铜溶液反应生成氢氧化铜蓝色沉淀和硫酸钠,产生蓝色沉淀,故选项说法正确。
D、做铁钉生锈的对比实验时,最先生锈的不是浸没在蒸馏水中的铁钉,浸没在蒸馏水中的铁钉不能与氧气接触,不会生锈,故选项说法错误。
故选:C。
9.下列有关燃烧的说法正确的是( )
A.天然气泄漏时,立即打开排气扇电源开关
B.白磷在冷水,通入空气后能燃烧
C.用水灭火,目的是降低可燃物的着火点
D.发生火灾时,应用湿毛巾捂住口鼻,匍匐前进
【解答】解:A、发现煤气泄漏时,打开排气扇电源开关时产生的明火会点燃煤气,故A不正确;
B、白磷在冷水中,通入空气后也不能燃烧,因为冷水不能使温度达到白磷的着火点,故B不正确;
C、用水能够灭火,是因为水蒸发时吸收热量,能使温度降低到可燃物的着火点以下,而不是降低可燃物的着火点。故C错误;
D、由于发生火灾时,有害气体漂在上面,所以要匍匐前进,用湿毛巾捂住口鼻,可利用水吸收一部分有害气体;故D正确;
故选:D。
10.水是重要资源,下列说法正确的是( )
A.过滤或加热均能使硬水转化为软水
B.活性炭的吸附作用可使海水转化为淡水
C.电解水得到的H2和O2质量比为2:1
D.氢气在纯氧中燃烧的实验说明水由氢元素和氧元素组成
【解答】解:A、加热、蒸馏可使硬水软化,过滤时除去不溶性杂质,不能使硬水软化,故A错误;
B、活性炭具有吸附性,能吸附色素和异味,但不能使海水淡化,故B错误。
C、电解水得到的H2和O2体积比为2:1,故C错误;
D、氢气在氧气中燃烧生成水,氢气是由氢元素组成的,氧气是由氧元素组成的,则说明水是由氢元素和氧元素组成的;故D正确;
故选:D。
11.化学小组用如图进行实验,探究燃烧条件并测定空气中氧气含量,下列说法错误的是( )
A.此装置中白磷燃烧、红磷不燃烧,说明燃烧需要达可燃物着火点
B.若证明燃烧需要氧气,则必须增加白磷放在热水中的实验作对比
C.证明空气中氧气含量时,白磷、红磷必须都足量
D.若W形玻璃管容积为200mL,冷却后打开止水夹量筒剩余60mL水
【解答】解:A.装置中的白磷和红磷均与氧气接触,但实验中红磷没有燃烧,白磷发生燃烧,对比可知,燃烧需要达可燃物着火点,选项说法正确;
B.若证明燃烧需要氧气,则必须增加白磷放在热水中的实验作对比,装置内的白磷燃烧,而热水中的白磷没有燃烧,对比可知,燃烧需要氧气,选项说法正确;
C.因为该实验中,红磷没有燃烧,所以证明空气中氧气含量时,白磷必须都足量,而红磷无需过量,选项说法错误;
D.因为氧气约占空气体积的五分之一,所以足量的白磷燃烧所消耗的氧气体积为:200mL×=40mL,则冷却后打开止水夹量筒剩余水的体积为100mL﹣40mL=60mL,选项说法正确。
故选:C。
12.要学好化学就要学会归纳总结,下表归纳的内容完全正确的是( )
A安全知识 B生活知识
瓦斯爆炸由甲烷燃烧引起可用燃着的酒精灯去点燃另一酒精灯 含有较多钙镁单质的水叫做硬水蜂窝煤易燃烧是因为与空气的接触面增大
C物质的性质与用途 D物质分类
H2作填充气球的气体是因为它的密度小N2可作保护气是因为它化学性质稳定 河水属于混合物干冰属于单质
A.A B.B C.C D.D
【解答】解:A、不可用燃着的酒精灯去点燃另一酒精灯,会引起火灾,错误;
B、硬水是含有较多钙、镁化合物的水,错误;
C、H2作填充气球的气体是因为它的密度小,N2可作保护气是因为它化学性质稳定,正确;
D、干冰属于化合物,错误;
故选:C。
13.推理是化学学习中常用的思维方法,下列推理正确的是( )
A.混合物中至少含有两种物质,则混合物中至少含有两种元素
B.分子是由原子构成的,所以分子一定比原子大
C.在原子中,质子数一定等于核外电子数,但不一定等于中子数
D.化学变化伴随有能量变化,则有能量变化就一定有化学变化
【解答】解:A.混合物是由两种或两种以上的物质组成的,但是混合物中不一定含有多种元素,如氧气和臭氧组成的混合物中只含一种元素,故错误;
B.分子是由原子构成的,由原子构成的分子要比构成它的原子大,但是笼统的说分子一定比原子大,是错误的,有的原子要比有的分子大,分子和原子是不能比较大小的,故错误;
C.在原子中,质子数=核外电子数,但是不一定等于中子数,故正确;
D.灯泡通电后发光放热,有能量的变化,但是属于物理变化,故错误。
故选:C。
14.下列有关化学基本概念说法正确的是( )
①分子是构成物质的一种微粒
②原子也是构成物质的一种微粒
③在化学反应中,分子、原子都可分
④具有相同质子数的粒子一定是同种元素
⑤同种元素组成的物质一定是单质
⑥二氧化碳由碳原子和氧分子构成
⑦石蜡燃烧的过程中既有物理变化又有化学变化
⑧由同种分子构成的物质一定是纯净物
A.①②③④ B.①②⑤⑦ C.①②④⑧ D.①②⑦⑧
【解答】解:①构成物质的微粒有:分子、原子和离子,故①正确;
②构成物质的微粒有:分子、原子和离子,故②正确;
③在化学反应中分子分成原子,原子再重新组合成新的分子,所以化学反应中原子不能再分,故③错误;
④具有相同质子数的粒子不一定是同种元素,例如水分子和氖原子质子数都是10,故④错;
⑤单质是指由一种元素组成的纯净物,同种元素组成的物质不一定是纯净物,故⑤错误;
⑥二氧化碳由二氧化碳分子构成,故⑥错误;
⑦化学变化中一定存在物理变化,石蜡燃烧的过程中既有物理变化又有化学变化,故⑦正确;
⑧由分子构成的物质中,由同种分子构成的物质一定是纯净物,故⑧正确。
故选:D。
15.下列关于碳及其化合物的说法,正确的是( )
A.二氧化碳是导致酸雨的主要气体
B.可以用燃烧法除去二氧化碳中混有的少量一氧化碳
C.中国古代字画经久不褪色,因为常温下碳的化学性质不活泼
D.CO和CO2都是非金属氧化物,都能与NaOH溶液反应
【解答】解:A、导致酸雨的气体是二氧化硫,不是二氧化碳,故说法错误;
B、虽然一氧化碳能燃烧,但二氧化碳气体中混有少量一氧化碳,二氧化碳不支持燃烧,所以根本就不能点燃一氧化碳,故说法错误;
C、碳在常温下的化学性质不活泼,所以古代字画会久不褪色,故说法正确;
D、CO与NaOH溶液不反应,故说法错误。
故选:C。
二.填空题(共4小题)
16.在N2、H2、O2、CO、CO2、SO2六种物质中,可用做理想高能燃料,且燃烧产物不污染环境的是 H2 ;能使带火星的木条复燃的是 O2 ;既有可燃性又有还原性的气体化合物是 CO .
【解答】解:氢气具有可燃烧性,在燃烧时放出大量的热,且生成水,所以可以作为高能燃料;而氧气具有支持燃烧的性质,能够使带火星的木条复燃;一氧化碳和氢气具有可燃性和还原性,但是氢气是单质,而一氧化碳是化合物.
故答案为:H2;O2;CO.
17.随着经济的发展,能源与环境成为人们日益关注的问题.
(1)煤、 石油 和 天然气 常称为化石燃料.
(2)燃煤发电时,将煤块粉碎成煤粉,其目的是 增大与氧气的接触面积,使燃烧更充分 .
(3)化石燃料燃烧都会产生二氧化碳,它是空气中含量最多的温室气体为减少它的排放,科学家致力于研究将过多的二氧化碳和氢气在催化剂和加热的条件下反应,转化为水和甲烷.该反应的化学方程式为 CO2+4H22H2O+CH4 .
(4)“绿色化学”的特点之一是“零排放”.一定条件下,二氧化碳和氢气可以按照不同比例反应,生成下列有机物.其中二氧化碳和氢气反应,只生成一种产物就能实现“零排放”,这种产物是 (填字母序号,下同).
A.甲醇(CH4O)
B.甲酸(CH2O2)
C.乙醇(C2H6O)
D.乙酸(C2H4O2)
(5)下列措施中,有利于降低大气中二氧化碳含量的是 BC .
A.大量使用化石燃料
B.植树造林,增大植被面积
C.将二氧化碳变废为宝,循环利用
【解答】解:(1)煤、石油和天然气常称为化石燃料,故填:石油,天然气.
(2)燃煤发电时,将煤块粉碎成煤粉,其目的是增大与氧气的接触面积,使燃烧更充分,故答案为:增大与氧气的接触面积,使燃烧更充分;
(3)二氧化碳和氢气在催化剂和加热的条件下反应,转化为水和甲烷,故填:CO2+4H22H2O+CH4;
(4)零排放就是反应物的原子全部转化到生成物中,则二氧化碳与氢气发生的是化合反应,只有生成的甲酸符合此反应,故填:B;
(5)降低二氧化碳的含量就是减少二氧化碳的排放或增大二氧化碳的吸收,故填:B C.
18.多角度认识物质的变化,有助于我们更好地理解化学知识.
(1)从微观角度(图 1 为某化学反应的微观示意图,据图回答下列问题.)
①微观上看,该化学变化中发生根本改变的微粒是 分子 (填“原子”或“分子”);
②参加反应的 A2与 B2两种物质的分子个数比为 1:1 ;
(2)从物质转化角度(一种物质可通过不同的反应类型生成,以二氧化碳为例)
①能与氧气化合生成二氧化碳的物质是 C(或CO) (填一种物质化学式);
②高温下,石灰石分解生成二氧化碳的化学方程式是 CaCO3CaO+CO2↑ .
(3)从能量变化角度(借用图 2 装置分别进行进行下列实验,认识物质变化中的能量变化)
①往烧杯中加入一定量生石灰会引起白磷燃烧,从燃烧条件分析,此时生石灰的作用是 生石灰与水反应放出大量的热,水温升高,达到了白磷的着火点 ,写出生石灰与水反应的化学方程式 CaO+H2O═Ca(OH)2 ;
②将一定量的下列某物质溶于烧杯中的冷水,其中能引起白磷燃烧的是 CD (填标号)。
A.氯化钠 B.硝酸铵 C.浓硫酸 D.氢氧化钠
【解答】解:(1)①微观上看,由微粒的变化可知,该化学变化中发生根本改变的微粒是分子;
②由微粒的变化可知,有一个B2分子未参加反应,参加反应的A2与B2两种物质的分子个数比为 1:1.
(2)①能与氧气化合生成二氧化碳的物质是碳和一氧化碳,化学式分别是:C、CO.
②高温下,石灰石分解生成氧化钙和二氧化碳的化学方程式是:CaCO3CaO+CO2↑;
(3)①往烧杯中加入一定量生石灰会引起白磷燃烧,从燃烧条件分析,此时生石灰的作用是:生石灰与水反应放出大量的热,水温升高,达到了白磷的着火点.生石灰与水反应的化学方程式是:CaO+H2O═Ca(OH)2.
②将一定量的下列某物质溶于烧杯中的冷水,能引起白磷燃烧,说明了物质在溶于水时能放出热量,浓硫酸、氢氧化钠在溶于水时能放出热量,能使溶液的温度升高.
故答为:(1)①分子,②1:1.(2)①C(或CO).②CaCO3CaO+CO2↑;③Fe.(3)①生石灰与水反应放出大量的热,水温升高,达到了白磷的着火点,CaO+H2O═Ca(OH)2;②CD
19.化学就在我们身边,与我们的生活有着密切的联系。
(1)“萍水相逢 缘聚天下”。
①萍乡武功山温泉﹣﹣“富硒养生”。其中“硒”指的是 元素 (选填“原子”“离子”或“元素”)。
②莲花的苏轼蜜酒﹣﹣“美酒飘香”。从分子角度解释“美酒飘香”的原因 分子在不断运动 ;酒中含有乙醇,乙醇燃烧的化学方程式为 C2H5OH+3O22CO2+3H2O 。
(2)随着科技进步,人类对能源的需求量日益增长。为了应对能源危机,可以开发和利用新能源,而在各种新能源中, 氢气 被认为是最清洁的高能燃料。
【解答】解:(1)①物质是由元素组成的,所以其中“硒”指的是元素;故填:元素;
②分子在不断运动,所以在远处就可以闻到酒的香味,在点燃的条件下,乙醇与氧气反应生成二氧化碳和水,化学方程式为:C2H5OH+3O22CO2+3H2O;故填:分子在不断运动;C2H5OH+3O22CO2+3H2O;
(2)氢气的热值高,制备原料来源广泛,燃烧产物只有水,不会对环境造成任何污染,所以被认为氢气是最清洁的高能燃料;故填:氢气。
三.推断题(共1小题)
20.A~G是初中化学常见的七种物质,且A、B、C、D、E属于单质、氧化物、酸、碱、盐五种不同类别的物质,它们之间的关系如图所示。(“﹣”表示相连的物质能相互反应;“→”表示物质间的转化关系;部分反应物、生成物及反应条件未标出)。已知A物质中含有三种元素;B是使用最广泛的金属单质;物质C的溶液呈蓝色;反应①②的现象相同,都产生白色沉淀;D、G两种物质类别相同,且都易溶于水。试回答:
(1)写出物质C的化学式:C CuSO4 。
(2)物质E的一种用途是 灭火、制碳酸饮料、气体肥料、制冷剂(任写一个) 。
(3)写出D→F的化学方程式 2NaOH+CO2═Na2CO3+H2O ,写出A与G反应的化学方程式 H2SO4+Ba(OH)2═BaSO4↓+2H2O 。
【解答】解:(1)B是使用最广泛的金属单质,则B为铁,物质C的溶液呈蓝色,则C为硫酸铜,A物质中含有三种元素,且能和铁发生反应,则A为硫酸,则D、E的物质类别为碱和氧化物,且D为可溶性碱,如氢氧化钠,由于D和E能相互反应,则E为二氧化碳,F能生成二氧化碳,则F为碳酸盐,如碳酸钠,D、G两种物质类别相同,则G也是一种碱,反应①②的现象相同,都产生白色沉淀,则G为氢氧化钡;
故填:CuSO4;
(2)物质E为二氧化碳,可用于灭火、制碳酸饮料、气体肥料、制冷剂等;
故填:灭火、制碳酸饮料、气体肥料、制冷剂(任写一个);
(3)D→F的化学方程式为:2NaOH+CO2═Na2CO3+H2O,A与G反应的化学方程式为:H2SO4 +Ba(OH)2 ═BaSO4 ↓+2H2O;
故填:2NaOH+CO2═Na2CO3+H2O;
H2SO4 +Ba(OH)2 ═BaSO4 ↓+2H2O。
四.实验探究题(共2小题)
21.根据下列实验装置图回答问题。
(1)写出标有字母a的仪器名称: 集气瓶 。
(2)实验室用装置A制取氧气的化学方程式为 2H2O22H2O+O2↑ 。
(3)如图中装置 (填字母)可用来收集氧气。
(4)将反应生成的氧气通入D中,使其接触底部的白磷后,看到的现象是 白磷燃烧 ,说明可燃物燃烧需要的条件之一是 与氧气接触 。
【解答】解:(1)标有字母a的仪器名称是集气瓶;故填:集气瓶;
(2)装置A适用于固液常温下制取气体,若制取氧气则为过氧化氢在二氧化锰的催化作用下分解为水和氧气,化学方程式为2H2O22H2O+O2↑;故填:2H2O22H2O+O2↑;
(3)氧气的密度比空气大,不易溶于水,可用向上排空气法或排水法来收集氧气;故填:B;
(4)D中的白磷温度达到了着火点,但是没有发生燃烧,若将反应生成的氧气通入D中,使其接触底部的白磷后,看到白磷燃烧,说明可燃物燃烧需要的条件之一是与氧气接触;故填:白磷燃烧;与氧气接触。
22.化学是一门以实验为基础的学科.根据图1,回答问题.
(1)a仪器的名称为 长颈漏斗 .
(2)实验室用A装置制O2的化学方程式为 2KClO32KCl+3O2↑ ,选用的收集装置是 C (填字母序号).查阅资料后可知,锰酸钾可溶于水,若要从高锰酸钾完全分解后的固体残渣中回收二氧化锰,正确操作的顺序是 bcda (填写选项序号).
a.烘干 b.溶解 c.过滤 d.洗涤
(3)制取CO2用装置F替代装置B的优点是 可以控制反应的发生和停止 .通过装置B、E来验证二氧化碳的性质,实验过程中观察到E中有气泡冒出,但澄清的石灰水未变浑浊,试分析其可能的原因 二氧化碳中混有氯化氢气体 .
(4)氨气是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水.实验室用加热氯化铵和氢氧化钙的固体混合物制取氨气,其发生装置(图2),可选用 A (填装置编号),收集氨气时最好选用下列装置中的G装置与 ② 装置相连接(填数字编号).
【解答】解:(1)长颈漏斗方便加液体药品,故答案为:长颈漏斗;
(2)氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,配平即可;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;查阅资料后可知,锰酸钾可溶于水,若要从高锰酸钾完全分解后的固体残渣中回收二氧化锰,正确操作的顺序是:溶解、过滤、洗涤、干燥;故答案为:2KClO32KCl+3O2↑;C;bcda;
(3)制取CO2用装置F替代装置B的优点是:可以控制反应的发生和停止;通过装置B、E来验证二氧化碳的性质,实验过程中观察到E中有气泡冒出,但澄清的石灰水未变浑浊,试分析其可能的原因:二氧化碳中混有氯化氢气体;故答案为:可以控制反应的发生和停止;二氧化碳中混有氯化氢气体;
(4)实验室用加热氯化铵和氢氧化钙的固体混合物制取氨气,因此需要加热;收集氨气时最好选用下列装置中的G装置与②装置相连接,防止氨气污染空气;故答案为:A;②;
五.计算题(共2小题)
23.波尔多液是一种农业上常用的杀虫剂,它由硫酸铜、生石灰加水配制而成。
(1)硫酸铜所含阴离子的符号是 SO42﹣ ;生石灰属于 氧化物 (填物质种类),生活中可用于 干燥剂 。
(2)煅烧石灰石(主要成分CaCO3)可制得生石灰(CaO),若要制取11.2t氧化钙,根据化学方程式计算需要碳酸钙的质量是多少?
(3)波尔多液等农药常常配成乳浊液或悬浊液的原因是: 常温条件下直接用硫酸铜和氢氧化钙配制成的波尔多液是一种具有暂时灭菌效力的悬浊液形式,为了更好在植物表面吸附和渗透,通常都会在波尔多标准配方里加入适量阴离子或者非离子表面活性剂乳化来显著降低张力获得更好药效 。
【解答】解:(1)解:(1)硫酸铜中所含阴离子是硫酸根离子,其离子符号为SO42﹣;生石灰中含有两种元素,其中一种是氧元素,所以生石灰属于氧化物,其和水反应生成氢氧化钙,生活中可用于干燥剂;
(2)设需要碳酸钙的质量是x。
CaCO3CaO+CO2↑
100 56
x 11.2t
x=20t
答:需要碳酸钙的质量是20t;
(3)波尔多液等农药常常配成乳浊液或悬浊液的原因是:常温条件下直接用硫酸铜和氢氧化钙配制成的波尔多液是一种具有暂时灭菌效力的悬浊液形式,为了更好在植物表面吸附和渗透,通常都会在波尔多标准配方里加入适量阴离子或者非离子表面活性剂乳化来显著降低张力获得更好药效。
故答案为:
(1)SO42﹣;氧化物;干燥剂;
(2)20t;
(3)波尔多液等农药常常配成乳浊液或悬浊液的原因是:常温条件下直接用硫酸铜和氢氧化钙配制成的波尔多液是一种具有暂时灭菌效力的悬浊液形式,为了更好在植物表面吸附和渗透,通常都会在波尔多标准配方里加入适量阴离子或者非离子表面活性剂乳化来显著降低张力获得更好药效。
24.小丽为探究某石灰石样品中碳酸钙的含量,称取500g样品,磨成粉末后,放在电炉上高温煅烧至质量不再发生变化,称量剩余物质量为302g(假设石灰石样品中杂质不参加反应).据此计算:
(1)生成二氧化碳质量
(2)此石灰石样品中碳酸钙的百分含量.
【解答】解:(1)根据质量守恒定律,二氧化碳的质量为:500g﹣302g=198g
(2)设500g石灰石样品中碳酸钙的质量为x.
CaCO3CaO+CO2↑
100 44
x 198g
解得:x=450g
此石灰石样品中碳酸钙的质量分数为:%=90%
答:(1)生成二氧化碳的质量为198g.(2)此石灰石样品中碳酸钙的质量分数为90%.
声明:试题解析著作权属所有,未经书面同意,不得复制发布
日期:2021/11/19 17:59:19;用户:2548256485;邮箱:2548256485@;学号:19601098
第1页(共3页)
一.选择题(共15小题)
1.对下列物质用途的描述,不符合事实的是( )
A.石墨可以制铅笔芯
B.氮气是食品包装袋中的一种防腐剂
C.活性炭可以用于软化硬水
D.二氧化碳可用于人工降雨
2.关于燃烧与灭火,下列说法正确的是( )
A.可燃物燃烧一定会生成二氧化碳
B.家用电器着火时,应立即用水浇灭
C.在加油站使用手机可能引发燃烧、爆炸
D.厨房中天然气泄漏时,可打开抽排油烟机排气
3.我市拥有丰富的页岩气,它与天然气的主要成分都是甲烷(CH4),下列关于页岩气的说法不正确的是( )
A.它是混合物
B.加压使之液化,其分子间的间隔不变
C.它充分燃烧会生成H2O和CO2
D.它与空气混合点燃易发生爆炸
4.下列有关金属和金属材料的说法正确的是( )
A.金属材料包括纯金属和合金
B.铁制品生锈后没有回收价值
C.生铁的含碳量比钢低
D.铝很活泼,所以铝制品在空气中易腐蚀生锈
5.下列做法正确的是( )
A.电器着火用水扑灭
B.室内起火时打开门窗通风
C.油锅着火用锅盖盖灭
D.用明火检查液化气罐是否漏气
6.“纸火锅”(如图所示)是用纸张代替金属材料做容器盛放汤料,当酒精燃烧时纸张不会燃烧.对此现象,下列解释合理的是( )
A.纸张不是可燃物,不能燃烧
B.纸张没有与空气充足接触,不会燃烧
C.纸张被水浸湿,导致纸张的着火点降低
D.锅里的水蒸发时吸收热量,温度达不到纸张的着火点
7.下列关于燃烧与灭火的说法中,正确的是( )
A.蜡烛用嘴一吹即灭,是因为吹出的气体主要是二氧化碳
B.将大块煤粉碎后再燃烧,其目的是延迟煤燃烧的时间
C.如图a,火柴头斜向下时更容易燃烧,是因为降低了火柴梗的着火点
D.由图b的现象可知,金属镁引起的火灾不能用二氧化碳灭火
8.下列实验现象描述正确的是( )
A.红磷在空气中燃烧发出蓝色火焰
B.电解水的实验中正极产生的气体体积是负极产生的气体体积的2倍
C.向硫酸铜溶液中滴加氢氧化钠溶液产生蓝色沉淀
D.做铁钉生锈的对比实验时,最先生锈的是浸没在蒸馏水中的铁钉
9.下列有关燃烧的说法正确的是( )
A.天然气泄漏时,立即打开排气扇电源开关
B.白磷在冷水,通入空气后能燃烧
C.用水灭火,目的是降低可燃物的着火点
D.发生火灾时,应用湿毛巾捂住口鼻,匍匐前进
10.水是重要资源,下列说法正确的是( )
A.过滤或加热均能使硬水转化为软水
B.活性炭的吸附作用可使海水转化为淡水
C.电解水得到的H2和O2质量比为2:1
D.氢气在纯氧中燃烧的实验说明水由氢元素和氧元素组成
11.化学小组用如图进行实验,探究燃烧条件并测定空气中氧气含量,下列说法错误的是( )
A.此装置中白磷燃烧、红磷不燃烧,说明燃烧需要达可燃物着火点
B.若证明燃烧需要氧气,则必须增加白磷放在热水中的实验作对比
C.证明空气中氧气含量时,白磷、红磷必须都足量
D.若W形玻璃管容积为200mL,冷却后打开止水夹量筒剩余60mL水
12.要学好化学就要学会归纳总结,下表归纳的内容完全正确的是( )
A安全知识 B生活知识
瓦斯爆炸由甲烷燃烧引起可用燃着的酒精灯去点燃另一酒精灯 含有较多钙镁单质的水叫做硬水蜂窝煤易燃烧是因为与空气的接触面增大
C物质的性质与用途 D物质分类
H2作填充气球的气体是因为它的密度小N2可作保护气是因为它化学性质稳定 河水属于混合物干冰属于单质
A.A B.B C.C D.D
13.推理是化学学习中常用的思维方法,下列推理正确的是( )
A.混合物中至少含有两种物质,则混合物中至少含有两种元素
B.分子是由原子构成的,所以分子一定比原子大
C.在原子中,质子数一定等于核外电子数,但不一定等于中子数
D.化学变化伴随有能量变化,则有能量变化就一定有化学变化
14.下列有关化学基本概念说法正确的是( )
①分子是构成物质的一种微粒
②原子也是构成物质的一种微粒
③在化学反应中,分子、原子都可分
④具有相同质子数的粒子一定是同种元素
⑤同种元素组成的物质一定是单质
⑥二氧化碳由碳原子和氧分子构成
⑦石蜡燃烧的过程中既有物理变化又有化学变化
⑧由同种分子构成的物质一定是纯净物
A.①②③④ B.①②⑤⑦ C.①②④⑧ D.①②⑦⑧
15.下列关于碳及其化合物的说法,正确的是( )
A.二氧化碳是导致酸雨的主要气体
B.可以用燃烧法除去二氧化碳中混有的少量一氧化碳
C.中国古代字画经久不褪色,因为常温下碳的化学性质不活泼
D.CO和CO2都是非金属氧化物,都能与NaOH溶液反应
二.填空题(共4小题)
16.在N2、H2、O2、CO、CO2、SO2六种物质中,可用做理想高能燃料,且燃烧产物不污染环境的是 ;能使带火星的木条复燃的是 ;既有可燃性又有还原性的气体化合物是 .
17.随着经济的发展,能源与环境成为人们日益关注的问题.
(1)煤、 和 常称为化石燃料.
(2)燃煤发电时,将煤块粉碎成煤粉,其目的是 .
(3)化石燃料燃烧都会产生二氧化碳,它是空气中含量最多的温室气体为减少它的排放,科学家致力于研究将过多的二氧化碳和氢气在催化剂和加热的条件下反应,转化为水和甲烷.该反应的化学方程式为 .
(4)“绿色化学”的特点之一是“零排放”.一定条件下,二氧化碳和氢气可以按照不同比例反应,生成下列有机物.其中二氧化碳和氢气反应,只生成一种产物就能实现“零排放”,这种产物是 (填字母序号,下同).
A.甲醇(CH4O)
B.甲酸(CH2O2)
C.乙醇(C2H6O)
D.乙酸(C2H4O2)
(5)下列措施中,有利于降低大气中二氧化碳含量的是 .
A.大量使用化石燃料
B.植树造林,增大植被面积
C.将二氧化碳变废为宝,循环利用
18.多角度认识物质的变化,有助于我们更好地理解化学知识.
(1)从微观角度(图 1 为某化学反应的微观示意图,据图回答下列问题.)
①微观上看,该化学变化中发生根本改变的微粒是 (填“原子”或“分子”);
②参加反应的 A2与 B2两种物质的分子个数比为 ;
(2)从物质转化角度(一种物质可通过不同的反应类型生成,以二氧化碳为例)
①能与氧气化合生成二氧化碳的物质是 (填一种物质化学式);
②高温下,石灰石分解生成二氧化碳的化学方程式是 .
(3)从能量变化角度(借用图 2 装置分别进行进行下列实验,认识物质变化中的能量变化)
①往烧杯中加入一定量生石灰会引起白磷燃烧,从燃烧条件分析,此时生石灰的作用是 ,写出生石灰与水反应的化学方程式 ;
②将一定量的下列某物质溶于烧杯中的冷水,其中能引起白磷燃烧的是 (填标号)。
A.氯化钠 B.硝酸铵 C.浓硫酸 D.氢氧化钠
19.化学就在我们身边,与我们的生活有着密切的联系。
(1)“萍水相逢 缘聚天下”。
①萍乡武功山温泉﹣﹣“富硒养生”。其中“硒”指的是 (选填“原子”“离子”或“元素”)。
②莲花的苏轼蜜酒﹣﹣“美酒飘香”。从分子角度解释“美酒飘香”的原因 ;酒中含有乙醇,乙醇燃烧的化学方程式为 。
(2)随着科技进步,人类对能源的需求量日益增长。为了应对能源危机,可以开发和利用新能源,而在各种新能源中, 被认为是最清洁的高能燃料。
三.推断题(共1小题)
20.A~G是初中化学常见的七种物质,且A、B、C、D、E属于单质、氧化物、酸、碱、盐五种不同类别的物质,它们之间的关系如图所示。(“﹣”表示相连的物质能相互反应;“→”表示物质间的转化关系;部分反应物、生成物及反应条件未标出)。已知A物质中含有三种元素;B是使用最广泛的金属单质;物质C的溶液呈蓝色;反应①②的现象相同,都产生白色沉淀;D、G两种物质类别相同,且都易溶于水。试回答:
(1)写出物质C的化学式:C 。
(2)物质E的一种用途是 。
(3)写出D→F的化学方程式 ,写出A与G反应的化学方程式 。
四.实验探究题(共2小题)
21.根据下列实验装置图回答问题。
(1)写出标有字母a的仪器名称: 。
(2)实验室用装置A制取氧气的化学方程式为 。
(3)如图中装置 (填字母)可用来收集氧气。
(4)将反应生成的氧气通入D中,使其接触底部的白磷后,看到的现象是 ,说明可燃物燃烧需要的条件之一是 。
22.化学是一门以实验为基础的学科.根据图1,回答问题.
(1)a仪器的名称为 .
(2)实验室用A装置制O2的化学方程式为 ,选用的收集装置是 (填字母序号).查阅资料后可知,锰酸钾可溶于水,若要从高锰酸钾完全分解后的固体残渣中回收二氧化锰,正确操作的顺序是 (填写选项序号).
a.烘干 b.溶解 c.过滤 d.洗涤
(3)制取CO2用装置F替代装置B的优点是 .通过装置B、E来验证二氧化碳的性质,实验过程中观察到E中有气泡冒出,但澄清的石灰水未变浑浊,试分析其可能的原因 .
(4)氨气是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水.实验室用加热氯化铵和氢氧化钙的固体混合物制取氨气,其发生装置(图2),可选用 (填装置编号),收集氨气时最好选用下列装置中的G装置与 装置相连接(填数字编号).
五.计算题(共2小题)
23.波尔多液是一种农业上常用的杀虫剂,它由硫酸铜、生石灰加水配制而成。
(1)硫酸铜所含阴离子的符号是 ;生石灰属于 (填物质种类),生活中可用于 。
(2)煅烧石灰石(主要成分CaCO3)可制得生石灰(CaO),若要制取11.2t氧化钙,根据化学方程式计算需要碳酸钙的质量是多少?
(3)波尔多液等农药常常配成乳浊液或悬浊液的原因是: 。
24.小丽为探究某石灰石样品中碳酸钙的含量,称取500g样品,磨成粉末后,放在电炉上高温煅烧至质量不再发生变化,称量剩余物质量为302g(假设石灰石样品中杂质不参加反应).据此计算:
(1)生成二氧化碳质量
(2)此石灰石样品中碳酸钙的百分含量.
人教版九年级上册《第7单元 燃料及其利用》2021年单元测试卷二
参考答案与试题解析
一.选择题(共15小题)
1.对下列物质用途的描述,不符合事实的是( )
A.石墨可以制铅笔芯
B.氮气是食品包装袋中的一种防腐剂
C.活性炭可以用于软化硬水
D.二氧化碳可用于人工降雨
【解答】解:A、石墨很软,可用于制铅笔芯,故正确;
B、氮气化学性质稳定,可以做食品包装中的防腐剂,故正确;
C、活性炭具有吸附性,能吸附水中的杂质而不能将将硬水软化,故错误;
D、二氧化碳固体干冰易升华同时吸收大量的热,可用于人工降雨,故正确;
故选:C。
2.关于燃烧与灭火,下列说法正确的是( )
A.可燃物燃烧一定会生成二氧化碳
B.家用电器着火时,应立即用水浇灭
C.在加油站使用手机可能引发燃烧、爆炸
D.厨房中天然气泄漏时,可打开抽排油烟机排气
【解答】解:A.氢气燃烧后只生成水,没有二氧化碳生成,故错误;
B.家用电器着火时,不能用水浇灭,以防触电,故错误;
C.在加油站附近的空气中弥漫着可燃性气体,与空气混合,接打手机产生的电火花可能会引燃甚至引起爆炸,故正确;
D.可燃性气体遇到电火花时可能爆炸,而打开油烟机时产生电火花,故错误。
故选:C。
3.我市拥有丰富的页岩气,它与天然气的主要成分都是甲烷(CH4),下列关于页岩气的说法不正确的是( )
A.它是混合物
B.加压使之液化,其分子间的间隔不变
C.它充分燃烧会生成H2O和CO2
D.它与空气混合点燃易发生爆炸
【解答】解:A、页岩气是甲烷和杂质的混合物,正确但不符合题意,故选项错误;
B、加压使之液化,其分子间的间隔不变错误,分子间隔变小,错误符合题意,故选项正确;
C、甲烷充分燃烧会生成H2O和CO2正确,正确但不符合题意,故选项错误;
D、它与空气混合点燃易发生爆炸正确,因为它具有可燃性,正确但不符合题意,故选项错误;
故选:B。
4.下列有关金属和金属材料的说法正确的是( )
A.金属材料包括纯金属和合金
B.铁制品生锈后没有回收价值
C.生铁的含碳量比钢低
D.铝很活泼,所以铝制品在空气中易腐蚀生锈
【解答】解:A.金属材料包括纯金属和合金,选项说法正确;
B.回收生锈的钢铁既可以节约金属资源,又可以防止环境污染,选项说法错误;
C.生铁中的含碳量为2%~4.3%,钢中的含碳量为0.03%~2%,故生铁的含碳量比钢高,选项说法错误;
D.铝的化学性质较活泼,在空气中易与空气的氧气反应,在铝制品表面形成一层致密的氧化铝保护膜,所以铝制品耐腐蚀,选项说法错误。
故选:A。
5.下列做法正确的是( )
A.电器着火用水扑灭
B.室内起火时打开门窗通风
C.油锅着火用锅盖盖灭
D.用明火检查液化气罐是否漏气
【解答】解:A、电器着火若用水扑灭极易造成电线短路和人体触电,所以电器着火应先切断电源,再灭火;故错;
B、根据燃烧的条件;可燃物燃烧需要与氧气接触,室内失火时,打开门窗,造成空气对流,氧气量充足,使火势加大。故错;
C、用锅盖盖灭,隔绝了氧气使油熄灭;故对;
D、用明火检查液化气罐是否漏气极易引燃液化气而发生火灾;故错。
故选:C。
6.“纸火锅”(如图所示)是用纸张代替金属材料做容器盛放汤料,当酒精燃烧时纸张不会燃烧.对此现象,下列解释合理的是( )
A.纸张不是可燃物,不能燃烧
B.纸张没有与空气充足接触,不会燃烧
C.纸张被水浸湿,导致纸张的着火点降低
D.锅里的水蒸发时吸收热量,温度达不到纸张的着火点
【解答】解:A、纸张具有可燃性,是可燃物,不能燃烧是因为温度没有达到纸张的着火点,故选项解释错误。
B、纸张与空气充分接触,不能燃烧是因为温度没有达到纸张的着火点,故选项解释错误。
C、可燃物的着火点一般是不变的,纸张的着火点一般情况下不能改变,故选项解释错误。
D、水蒸发时吸热,导致温度达不到纸张的着火点,因此纸张不能燃烧,故选项解释正确。
故选:D。
7.下列关于燃烧与灭火的说法中,正确的是( )
A.蜡烛用嘴一吹即灭,是因为吹出的气体主要是二氧化碳
B.将大块煤粉碎后再燃烧,其目的是延迟煤燃烧的时间
C.如图a,火柴头斜向下时更容易燃烧,是因为降低了火柴梗的着火点
D.由图b的现象可知,金属镁引起的火灾不能用二氧化碳灭火
【解答】解:A.蜡烛用嘴一吹即灭,是因为空气流通带走热量,造成蜡烛温度低于其着火点而灭火,故错误;
B.将大块煤粉碎后再燃烧,其目的是增大与氧气的接触面积,促进燃烧,故错误;
C.如图a,火柴头斜向下时更容易燃烧,是因为火柴梗的温度更容易达到其着火点,故错误;
D.镁条能在二氧化碳中燃烧,所以金属镁引起的火灾不能用二氧化碳灭火,故正确;
故选:D。
8.下列实验现象描述正确的是( )
A.红磷在空气中燃烧发出蓝色火焰
B.电解水的实验中正极产生的气体体积是负极产生的气体体积的2倍
C.向硫酸铜溶液中滴加氢氧化钠溶液产生蓝色沉淀
D.做铁钉生锈的对比实验时,最先生锈的是浸没在蒸馏水中的铁钉
【解答】解:A、红磷在空气中燃烧,发出黄色火焰,产生大量的白烟,故选项说法错误.
B、电解水时,可观察到:与电源正极相连的试管内产生的气体体积少,与电源负极相连的试管内的气体体积多,且两者的体积之比大约是1:2,故选项说法错误。
C、氢氧化钠溶液与硫酸铜溶液反应生成氢氧化铜蓝色沉淀和硫酸钠,产生蓝色沉淀,故选项说法正确。
D、做铁钉生锈的对比实验时,最先生锈的不是浸没在蒸馏水中的铁钉,浸没在蒸馏水中的铁钉不能与氧气接触,不会生锈,故选项说法错误。
故选:C。
9.下列有关燃烧的说法正确的是( )
A.天然气泄漏时,立即打开排气扇电源开关
B.白磷在冷水,通入空气后能燃烧
C.用水灭火,目的是降低可燃物的着火点
D.发生火灾时,应用湿毛巾捂住口鼻,匍匐前进
【解答】解:A、发现煤气泄漏时,打开排气扇电源开关时产生的明火会点燃煤气,故A不正确;
B、白磷在冷水中,通入空气后也不能燃烧,因为冷水不能使温度达到白磷的着火点,故B不正确;
C、用水能够灭火,是因为水蒸发时吸收热量,能使温度降低到可燃物的着火点以下,而不是降低可燃物的着火点。故C错误;
D、由于发生火灾时,有害气体漂在上面,所以要匍匐前进,用湿毛巾捂住口鼻,可利用水吸收一部分有害气体;故D正确;
故选:D。
10.水是重要资源,下列说法正确的是( )
A.过滤或加热均能使硬水转化为软水
B.活性炭的吸附作用可使海水转化为淡水
C.电解水得到的H2和O2质量比为2:1
D.氢气在纯氧中燃烧的实验说明水由氢元素和氧元素组成
【解答】解:A、加热、蒸馏可使硬水软化,过滤时除去不溶性杂质,不能使硬水软化,故A错误;
B、活性炭具有吸附性,能吸附色素和异味,但不能使海水淡化,故B错误。
C、电解水得到的H2和O2体积比为2:1,故C错误;
D、氢气在氧气中燃烧生成水,氢气是由氢元素组成的,氧气是由氧元素组成的,则说明水是由氢元素和氧元素组成的;故D正确;
故选:D。
11.化学小组用如图进行实验,探究燃烧条件并测定空气中氧气含量,下列说法错误的是( )
A.此装置中白磷燃烧、红磷不燃烧,说明燃烧需要达可燃物着火点
B.若证明燃烧需要氧气,则必须增加白磷放在热水中的实验作对比
C.证明空气中氧气含量时,白磷、红磷必须都足量
D.若W形玻璃管容积为200mL,冷却后打开止水夹量筒剩余60mL水
【解答】解:A.装置中的白磷和红磷均与氧气接触,但实验中红磷没有燃烧,白磷发生燃烧,对比可知,燃烧需要达可燃物着火点,选项说法正确;
B.若证明燃烧需要氧气,则必须增加白磷放在热水中的实验作对比,装置内的白磷燃烧,而热水中的白磷没有燃烧,对比可知,燃烧需要氧气,选项说法正确;
C.因为该实验中,红磷没有燃烧,所以证明空气中氧气含量时,白磷必须都足量,而红磷无需过量,选项说法错误;
D.因为氧气约占空气体积的五分之一,所以足量的白磷燃烧所消耗的氧气体积为:200mL×=40mL,则冷却后打开止水夹量筒剩余水的体积为100mL﹣40mL=60mL,选项说法正确。
故选:C。
12.要学好化学就要学会归纳总结,下表归纳的内容完全正确的是( )
A安全知识 B生活知识
瓦斯爆炸由甲烷燃烧引起可用燃着的酒精灯去点燃另一酒精灯 含有较多钙镁单质的水叫做硬水蜂窝煤易燃烧是因为与空气的接触面增大
C物质的性质与用途 D物质分类
H2作填充气球的气体是因为它的密度小N2可作保护气是因为它化学性质稳定 河水属于混合物干冰属于单质
A.A B.B C.C D.D
【解答】解:A、不可用燃着的酒精灯去点燃另一酒精灯,会引起火灾,错误;
B、硬水是含有较多钙、镁化合物的水,错误;
C、H2作填充气球的气体是因为它的密度小,N2可作保护气是因为它化学性质稳定,正确;
D、干冰属于化合物,错误;
故选:C。
13.推理是化学学习中常用的思维方法,下列推理正确的是( )
A.混合物中至少含有两种物质,则混合物中至少含有两种元素
B.分子是由原子构成的,所以分子一定比原子大
C.在原子中,质子数一定等于核外电子数,但不一定等于中子数
D.化学变化伴随有能量变化,则有能量变化就一定有化学变化
【解答】解:A.混合物是由两种或两种以上的物质组成的,但是混合物中不一定含有多种元素,如氧气和臭氧组成的混合物中只含一种元素,故错误;
B.分子是由原子构成的,由原子构成的分子要比构成它的原子大,但是笼统的说分子一定比原子大,是错误的,有的原子要比有的分子大,分子和原子是不能比较大小的,故错误;
C.在原子中,质子数=核外电子数,但是不一定等于中子数,故正确;
D.灯泡通电后发光放热,有能量的变化,但是属于物理变化,故错误。
故选:C。
14.下列有关化学基本概念说法正确的是( )
①分子是构成物质的一种微粒
②原子也是构成物质的一种微粒
③在化学反应中,分子、原子都可分
④具有相同质子数的粒子一定是同种元素
⑤同种元素组成的物质一定是单质
⑥二氧化碳由碳原子和氧分子构成
⑦石蜡燃烧的过程中既有物理变化又有化学变化
⑧由同种分子构成的物质一定是纯净物
A.①②③④ B.①②⑤⑦ C.①②④⑧ D.①②⑦⑧
【解答】解:①构成物质的微粒有:分子、原子和离子,故①正确;
②构成物质的微粒有:分子、原子和离子,故②正确;
③在化学反应中分子分成原子,原子再重新组合成新的分子,所以化学反应中原子不能再分,故③错误;
④具有相同质子数的粒子不一定是同种元素,例如水分子和氖原子质子数都是10,故④错;
⑤单质是指由一种元素组成的纯净物,同种元素组成的物质不一定是纯净物,故⑤错误;
⑥二氧化碳由二氧化碳分子构成,故⑥错误;
⑦化学变化中一定存在物理变化,石蜡燃烧的过程中既有物理变化又有化学变化,故⑦正确;
⑧由分子构成的物质中,由同种分子构成的物质一定是纯净物,故⑧正确。
故选:D。
15.下列关于碳及其化合物的说法,正确的是( )
A.二氧化碳是导致酸雨的主要气体
B.可以用燃烧法除去二氧化碳中混有的少量一氧化碳
C.中国古代字画经久不褪色,因为常温下碳的化学性质不活泼
D.CO和CO2都是非金属氧化物,都能与NaOH溶液反应
【解答】解:A、导致酸雨的气体是二氧化硫,不是二氧化碳,故说法错误;
B、虽然一氧化碳能燃烧,但二氧化碳气体中混有少量一氧化碳,二氧化碳不支持燃烧,所以根本就不能点燃一氧化碳,故说法错误;
C、碳在常温下的化学性质不活泼,所以古代字画会久不褪色,故说法正确;
D、CO与NaOH溶液不反应,故说法错误。
故选:C。
二.填空题(共4小题)
16.在N2、H2、O2、CO、CO2、SO2六种物质中,可用做理想高能燃料,且燃烧产物不污染环境的是 H2 ;能使带火星的木条复燃的是 O2 ;既有可燃性又有还原性的气体化合物是 CO .
【解答】解:氢气具有可燃烧性,在燃烧时放出大量的热,且生成水,所以可以作为高能燃料;而氧气具有支持燃烧的性质,能够使带火星的木条复燃;一氧化碳和氢气具有可燃性和还原性,但是氢气是单质,而一氧化碳是化合物.
故答案为:H2;O2;CO.
17.随着经济的发展,能源与环境成为人们日益关注的问题.
(1)煤、 石油 和 天然气 常称为化石燃料.
(2)燃煤发电时,将煤块粉碎成煤粉,其目的是 增大与氧气的接触面积,使燃烧更充分 .
(3)化石燃料燃烧都会产生二氧化碳,它是空气中含量最多的温室气体为减少它的排放,科学家致力于研究将过多的二氧化碳和氢气在催化剂和加热的条件下反应,转化为水和甲烷.该反应的化学方程式为 CO2+4H22H2O+CH4 .
(4)“绿色化学”的特点之一是“零排放”.一定条件下,二氧化碳和氢气可以按照不同比例反应,生成下列有机物.其中二氧化碳和氢气反应,只生成一种产物就能实现“零排放”,这种产物是 (填字母序号,下同).
A.甲醇(CH4O)
B.甲酸(CH2O2)
C.乙醇(C2H6O)
D.乙酸(C2H4O2)
(5)下列措施中,有利于降低大气中二氧化碳含量的是 BC .
A.大量使用化石燃料
B.植树造林,增大植被面积
C.将二氧化碳变废为宝,循环利用
【解答】解:(1)煤、石油和天然气常称为化石燃料,故填:石油,天然气.
(2)燃煤发电时,将煤块粉碎成煤粉,其目的是增大与氧气的接触面积,使燃烧更充分,故答案为:增大与氧气的接触面积,使燃烧更充分;
(3)二氧化碳和氢气在催化剂和加热的条件下反应,转化为水和甲烷,故填:CO2+4H22H2O+CH4;
(4)零排放就是反应物的原子全部转化到生成物中,则二氧化碳与氢气发生的是化合反应,只有生成的甲酸符合此反应,故填:B;
(5)降低二氧化碳的含量就是减少二氧化碳的排放或增大二氧化碳的吸收,故填:B C.
18.多角度认识物质的变化,有助于我们更好地理解化学知识.
(1)从微观角度(图 1 为某化学反应的微观示意图,据图回答下列问题.)
①微观上看,该化学变化中发生根本改变的微粒是 分子 (填“原子”或“分子”);
②参加反应的 A2与 B2两种物质的分子个数比为 1:1 ;
(2)从物质转化角度(一种物质可通过不同的反应类型生成,以二氧化碳为例)
①能与氧气化合生成二氧化碳的物质是 C(或CO) (填一种物质化学式);
②高温下,石灰石分解生成二氧化碳的化学方程式是 CaCO3CaO+CO2↑ .
(3)从能量变化角度(借用图 2 装置分别进行进行下列实验,认识物质变化中的能量变化)
①往烧杯中加入一定量生石灰会引起白磷燃烧,从燃烧条件分析,此时生石灰的作用是 生石灰与水反应放出大量的热,水温升高,达到了白磷的着火点 ,写出生石灰与水反应的化学方程式 CaO+H2O═Ca(OH)2 ;
②将一定量的下列某物质溶于烧杯中的冷水,其中能引起白磷燃烧的是 CD (填标号)。
A.氯化钠 B.硝酸铵 C.浓硫酸 D.氢氧化钠
【解答】解:(1)①微观上看,由微粒的变化可知,该化学变化中发生根本改变的微粒是分子;
②由微粒的变化可知,有一个B2分子未参加反应,参加反应的A2与B2两种物质的分子个数比为 1:1.
(2)①能与氧气化合生成二氧化碳的物质是碳和一氧化碳,化学式分别是:C、CO.
②高温下,石灰石分解生成氧化钙和二氧化碳的化学方程式是:CaCO3CaO+CO2↑;
(3)①往烧杯中加入一定量生石灰会引起白磷燃烧,从燃烧条件分析,此时生石灰的作用是:生石灰与水反应放出大量的热,水温升高,达到了白磷的着火点.生石灰与水反应的化学方程式是:CaO+H2O═Ca(OH)2.
②将一定量的下列某物质溶于烧杯中的冷水,能引起白磷燃烧,说明了物质在溶于水时能放出热量,浓硫酸、氢氧化钠在溶于水时能放出热量,能使溶液的温度升高.
故答为:(1)①分子,②1:1.(2)①C(或CO).②CaCO3CaO+CO2↑;③Fe.(3)①生石灰与水反应放出大量的热,水温升高,达到了白磷的着火点,CaO+H2O═Ca(OH)2;②CD
19.化学就在我们身边,与我们的生活有着密切的联系。
(1)“萍水相逢 缘聚天下”。
①萍乡武功山温泉﹣﹣“富硒养生”。其中“硒”指的是 元素 (选填“原子”“离子”或“元素”)。
②莲花的苏轼蜜酒﹣﹣“美酒飘香”。从分子角度解释“美酒飘香”的原因 分子在不断运动 ;酒中含有乙醇,乙醇燃烧的化学方程式为 C2H5OH+3O22CO2+3H2O 。
(2)随着科技进步,人类对能源的需求量日益增长。为了应对能源危机,可以开发和利用新能源,而在各种新能源中, 氢气 被认为是最清洁的高能燃料。
【解答】解:(1)①物质是由元素组成的,所以其中“硒”指的是元素;故填:元素;
②分子在不断运动,所以在远处就可以闻到酒的香味,在点燃的条件下,乙醇与氧气反应生成二氧化碳和水,化学方程式为:C2H5OH+3O22CO2+3H2O;故填:分子在不断运动;C2H5OH+3O22CO2+3H2O;
(2)氢气的热值高,制备原料来源广泛,燃烧产物只有水,不会对环境造成任何污染,所以被认为氢气是最清洁的高能燃料;故填:氢气。
三.推断题(共1小题)
20.A~G是初中化学常见的七种物质,且A、B、C、D、E属于单质、氧化物、酸、碱、盐五种不同类别的物质,它们之间的关系如图所示。(“﹣”表示相连的物质能相互反应;“→”表示物质间的转化关系;部分反应物、生成物及反应条件未标出)。已知A物质中含有三种元素;B是使用最广泛的金属单质;物质C的溶液呈蓝色;反应①②的现象相同,都产生白色沉淀;D、G两种物质类别相同,且都易溶于水。试回答:
(1)写出物质C的化学式:C CuSO4 。
(2)物质E的一种用途是 灭火、制碳酸饮料、气体肥料、制冷剂(任写一个) 。
(3)写出D→F的化学方程式 2NaOH+CO2═Na2CO3+H2O ,写出A与G反应的化学方程式 H2SO4+Ba(OH)2═BaSO4↓+2H2O 。
【解答】解:(1)B是使用最广泛的金属单质,则B为铁,物质C的溶液呈蓝色,则C为硫酸铜,A物质中含有三种元素,且能和铁发生反应,则A为硫酸,则D、E的物质类别为碱和氧化物,且D为可溶性碱,如氢氧化钠,由于D和E能相互反应,则E为二氧化碳,F能生成二氧化碳,则F为碳酸盐,如碳酸钠,D、G两种物质类别相同,则G也是一种碱,反应①②的现象相同,都产生白色沉淀,则G为氢氧化钡;
故填:CuSO4;
(2)物质E为二氧化碳,可用于灭火、制碳酸饮料、气体肥料、制冷剂等;
故填:灭火、制碳酸饮料、气体肥料、制冷剂(任写一个);
(3)D→F的化学方程式为:2NaOH+CO2═Na2CO3+H2O,A与G反应的化学方程式为:H2SO4 +Ba(OH)2 ═BaSO4 ↓+2H2O;
故填:2NaOH+CO2═Na2CO3+H2O;
H2SO4 +Ba(OH)2 ═BaSO4 ↓+2H2O。
四.实验探究题(共2小题)
21.根据下列实验装置图回答问题。
(1)写出标有字母a的仪器名称: 集气瓶 。
(2)实验室用装置A制取氧气的化学方程式为 2H2O22H2O+O2↑ 。
(3)如图中装置 (填字母)可用来收集氧气。
(4)将反应生成的氧气通入D中,使其接触底部的白磷后,看到的现象是 白磷燃烧 ,说明可燃物燃烧需要的条件之一是 与氧气接触 。
【解答】解:(1)标有字母a的仪器名称是集气瓶;故填:集气瓶;
(2)装置A适用于固液常温下制取气体,若制取氧气则为过氧化氢在二氧化锰的催化作用下分解为水和氧气,化学方程式为2H2O22H2O+O2↑;故填:2H2O22H2O+O2↑;
(3)氧气的密度比空气大,不易溶于水,可用向上排空气法或排水法来收集氧气;故填:B;
(4)D中的白磷温度达到了着火点,但是没有发生燃烧,若将反应生成的氧气通入D中,使其接触底部的白磷后,看到白磷燃烧,说明可燃物燃烧需要的条件之一是与氧气接触;故填:白磷燃烧;与氧气接触。
22.化学是一门以实验为基础的学科.根据图1,回答问题.
(1)a仪器的名称为 长颈漏斗 .
(2)实验室用A装置制O2的化学方程式为 2KClO32KCl+3O2↑ ,选用的收集装置是 C (填字母序号).查阅资料后可知,锰酸钾可溶于水,若要从高锰酸钾完全分解后的固体残渣中回收二氧化锰,正确操作的顺序是 bcda (填写选项序号).
a.烘干 b.溶解 c.过滤 d.洗涤
(3)制取CO2用装置F替代装置B的优点是 可以控制反应的发生和停止 .通过装置B、E来验证二氧化碳的性质,实验过程中观察到E中有气泡冒出,但澄清的石灰水未变浑浊,试分析其可能的原因 二氧化碳中混有氯化氢气体 .
(4)氨气是一种无色、有刺激性气味的气体,密度比空气小,极易溶于水.实验室用加热氯化铵和氢氧化钙的固体混合物制取氨气,其发生装置(图2),可选用 A (填装置编号),收集氨气时最好选用下列装置中的G装置与 ② 装置相连接(填数字编号).
【解答】解:(1)长颈漏斗方便加液体药品,故答案为:长颈漏斗;
(2)氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,配平即可;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;查阅资料后可知,锰酸钾可溶于水,若要从高锰酸钾完全分解后的固体残渣中回收二氧化锰,正确操作的顺序是:溶解、过滤、洗涤、干燥;故答案为:2KClO32KCl+3O2↑;C;bcda;
(3)制取CO2用装置F替代装置B的优点是:可以控制反应的发生和停止;通过装置B、E来验证二氧化碳的性质,实验过程中观察到E中有气泡冒出,但澄清的石灰水未变浑浊,试分析其可能的原因:二氧化碳中混有氯化氢气体;故答案为:可以控制反应的发生和停止;二氧化碳中混有氯化氢气体;
(4)实验室用加热氯化铵和氢氧化钙的固体混合物制取氨气,因此需要加热;收集氨气时最好选用下列装置中的G装置与②装置相连接,防止氨气污染空气;故答案为:A;②;
五.计算题(共2小题)
23.波尔多液是一种农业上常用的杀虫剂,它由硫酸铜、生石灰加水配制而成。
(1)硫酸铜所含阴离子的符号是 SO42﹣ ;生石灰属于 氧化物 (填物质种类),生活中可用于 干燥剂 。
(2)煅烧石灰石(主要成分CaCO3)可制得生石灰(CaO),若要制取11.2t氧化钙,根据化学方程式计算需要碳酸钙的质量是多少?
(3)波尔多液等农药常常配成乳浊液或悬浊液的原因是: 常温条件下直接用硫酸铜和氢氧化钙配制成的波尔多液是一种具有暂时灭菌效力的悬浊液形式,为了更好在植物表面吸附和渗透,通常都会在波尔多标准配方里加入适量阴离子或者非离子表面活性剂乳化来显著降低张力获得更好药效 。
【解答】解:(1)解:(1)硫酸铜中所含阴离子是硫酸根离子,其离子符号为SO42﹣;生石灰中含有两种元素,其中一种是氧元素,所以生石灰属于氧化物,其和水反应生成氢氧化钙,生活中可用于干燥剂;
(2)设需要碳酸钙的质量是x。
CaCO3CaO+CO2↑
100 56
x 11.2t
x=20t
答:需要碳酸钙的质量是20t;
(3)波尔多液等农药常常配成乳浊液或悬浊液的原因是:常温条件下直接用硫酸铜和氢氧化钙配制成的波尔多液是一种具有暂时灭菌效力的悬浊液形式,为了更好在植物表面吸附和渗透,通常都会在波尔多标准配方里加入适量阴离子或者非离子表面活性剂乳化来显著降低张力获得更好药效。
故答案为:
(1)SO42﹣;氧化物;干燥剂;
(2)20t;
(3)波尔多液等农药常常配成乳浊液或悬浊液的原因是:常温条件下直接用硫酸铜和氢氧化钙配制成的波尔多液是一种具有暂时灭菌效力的悬浊液形式,为了更好在植物表面吸附和渗透,通常都会在波尔多标准配方里加入适量阴离子或者非离子表面活性剂乳化来显著降低张力获得更好药效。
24.小丽为探究某石灰石样品中碳酸钙的含量,称取500g样品,磨成粉末后,放在电炉上高温煅烧至质量不再发生变化,称量剩余物质量为302g(假设石灰石样品中杂质不参加反应).据此计算:
(1)生成二氧化碳质量
(2)此石灰石样品中碳酸钙的百分含量.
【解答】解:(1)根据质量守恒定律,二氧化碳的质量为:500g﹣302g=198g
(2)设500g石灰石样品中碳酸钙的质量为x.
CaCO3CaO+CO2↑
100 44
x 198g
解得:x=450g
此石灰石样品中碳酸钙的质量分数为:%=90%
答:(1)生成二氧化碳的质量为198g.(2)此石灰石样品中碳酸钙的质量分数为90%.
声明:试题解析著作权属所有,未经书面同意,不得复制发布
日期:2021/11/19 17:59:19;用户:2548256485;邮箱:2548256485@;学号:19601098
第1页(共3页)
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
