第六单元 燃烧与燃料 测试题—2021-2022学年九年级化学鲁教版上册(Word版含答案)
文档属性
| 名称 | 第六单元 燃烧与燃料 测试题—2021-2022学年九年级化学鲁教版上册(Word版含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 106.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-20 00:00:00 | ||
图片预览




文档简介
第六单元《燃烧与燃料》测试题
一、单选题
1.在一定条件下,木炭、一氧化碳、氢气都能与氧化铜发生反应,下列叙述正确的是
A.反应后生成的气体都有毒 B.反应类型都是化合反应
C.反应后都能生成红色固体 D.反应前后各元的化合价都发生了变化
2.下列物质的用途主要由其化学性质决定的是
A.石墨作电极 B.干冰作制冷剂 C.氢气作燃料 D.金刚石切割玻璃
3.下列实验方法不正确的是
A.用肥皂水区分硬水和软水 B.用观察固体颜色区分氧化铜和二氧化锰
C.用燃着的木条区分氧气和二氧化碳 D.用澄清石灰水区分氮气和二氧化碳
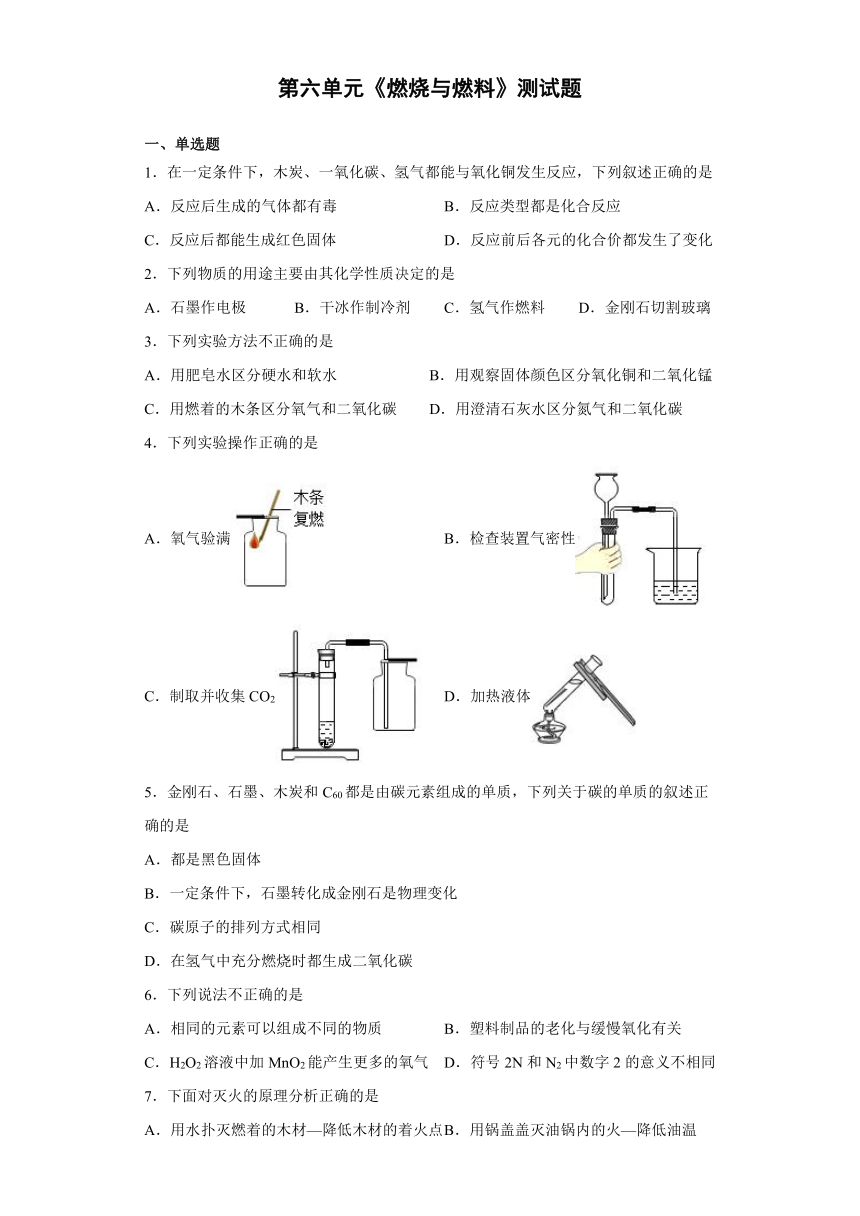
4.下列实验操作正确的是
A.氧气验满 B.检查装置气密性
C.制取并收集CO2 D.加热液体
5.金刚石、石墨、木炭和C60都是由碳元素组成的单质,下列关于碳的单质的叙述正确的是
A.都是黑色固体
B.一定条件下,石墨转化成金刚石是物理变化
C.碳原子的排列方式相同
D.在氢气中充分燃烧时都生成二氧化碳
6.下列说法不正确的是
A.相同的元素可以组成不同的物质 B.塑料制品的老化与缓慢氧化有关
C.H2O2溶液中加MnO2能产生更多的氧气 D.符号2N和N2中数字2的意义不相同
7.下面对灭火的原理分析正确的是
A.用水扑灭燃着的木材—降低木材的着火点 B.用锅盖盖灭油锅内的火—降低油温
C.砍掉大火蔓延路线前的树木—清除可燃物 D.用扇子扇灭烛火--隔离空气
8.推理是学习化学的一种常用方法,下列推理正确的是
A.阴离子带负电荷,则带负电荷的粒子一定是阴离子
B.单质只含一种元素,则只含一种元素的物质一定是单质
C.元素的种类是由质子数决定的,则质子数相同的原子一定属于同种元素
D.化学反应一定伴随着能量变化,则伴随能量变化的一定是化学反应
9.比较推理是化学学习中常用的思维方法,下列推理正确的是
A.燃烧过程中伴随着发光放热,所以有发光放热现象的变化都是燃烧
B.分子可以构成物质,所以物质都是由分子构成的
C.单质只含一种元素,所以含一种元素的物质都是单质
D.物理变化没有其他物质生成,所以没有生成其他物质的变化叫做物理变化
10.2021年世界环境日中国主题是“人与自然和谐共生”下列做法不符合该主题的是
A.长江沿线十年禁止捕鱼 B.生活中出行多乘坐轻轨
C.冬天用天然气炉替代碳炉生火取暖 D.朋友聚餐鼓励使用公筷
11.下列鉴别物质的方法错误的是
A.用加热的方法鉴别碳酸氢铵和食盐 B.用燃着的木条鉴别氮气和二氧化碳
C.用肥皂水鉴别蒸馏水和澄清石灰水 D.用二氧化锰鉴别蒸馏水和双氧水
12.对下列事实的解释合理的是
A.医用口罩能有效阻隔病毒—其阻隔原理与过滤类似
B.干冰能营造云雾缭绕效果—干冰升华形成白色气体
C.水电解能生成氢气和氧气—水是由氢气和氧气组成
D.分离液态空气可得到氧气—液氧沸点比液氮沸点低
13.下列实验方案,不能达到实验目的的是
选项 实验目的 实验方案
A 鉴别软水和硬水 用肥皂水
B 鉴别氧气和二氧化碳 分别加入澄清石灰水
C 鉴别水和白醋 闻气味
D 鉴别空气和氮气 用带火星的木条
A.A B.B C.C D.D
14.某兴趣小组为探究影响化学反应速率的因素,使用等量的同种钙片和白醋开展四组实验,分别测得产生的二氧化碳体积分数随时间的变化曲线如图所示。
选取CO2的体积分数从0-8%为研究对象,下列实验结果的分析,不正确的是
A.对比①③,温度越高,反应速率越快
B.对比②③,反应物接触面积越小,反应速率越慢
C.对比③④,反应物接触面积越大,反应速率越快
D.对比①②③④,④的反应速率最慢
15.化学反应之间、化学物质之间具有包含、并列、交叉等关系。下表中X、Y符合下图所示关系的是
A B C D
X 燃烧 化合反应 纯净物 化合反应
Y 氧化反应 分解反应 混合物 氧化反应
A.A B.B C.C D.D
二、填空题
16.2020年9月,中国向世界宣布了2030年前实现碳达峰、2060年前实现碳中和。
(1)为减缓大气中二氧化碳含量的增加,下列措施可行的是 (填字母代号);
A.植树造林,开发和利用太阳能、水能、风能等新能源
B.禁止使用煤、石油、天然气等化石燃料
(2)绿色植物通过光合作用吸收二氧化碳,生成葡萄糖并放出氧气,其反应的化学方程式:,则葡萄糖的化学式为 。(填字母)
A.CH6O B.C6H12 C.C6H12O6
(3)近年我国科学家合成了一种新型催化剂,可将二氧化碳和氢气转化为清洁的液体燃料甲醇(CH3OH)和水,该反应的化学方程式为____________。
17.现有两瓶气体:CO2和O2.可以用下列方法来区别它们:
往两个集气瓶中分别滴入紫色石蕊溶液;
(1)_______;
(2)_______。(只写方法即可)
18.水与人类的生活和生产密切相关。
(1)在自来水生产的过程中,未涉及的净水方法是_____(填序号)。
A.吸附 B.沉淀 C.过滤 D.蒸馏
(2)利用活性炭生产自来水时,利用了活性炭的__________性质(填“物理”或“化学”)。
(3)人们常用_____检验地下水是硬水还是软水。生活中可用_____的方法降低水的硬度。
三、推断题
19.有A、B、C、D、E五种物质,A是无色无味的气体;B在A中燃烧有蓝紫色火焰并生成能造成空气污染的气体C;D是黑色固体,在A中燃烧生成气体E; E能使澄清的石灰水变浑浊。请根据以上所述回答下列问题:
(1)A是________;B是_______;C是________;D是_______;E是_______。
(2)B与A发生反应的文字表达式是:__________;属于________反应。D与A发生反应的文字表达式是:___________。
20.如图中A、B、C、D、E是初中化学中常见的五种物质,在通常情况下,A为黑色固体,B、C、E均为无色无味的气体,D为不溶于水的白色固体,在实验室常用含D的物质与稀盐酸反应制取C,单质E是组成空气的主要成分之一。它们之间的关系如图所示,请回答下列问题:
(1)A的化学式是____________。
(2)写出B→C的化学方程式____________。
(3)写出C→D的化学方程式____________。
四、实验题
21.实验是进行科学探究的重要手段。根据如图实验回答下列问题。
(1)如图一所示。
Ⅰ.1号瓶中加入红磷,2号瓶中加入白磷,3号瓶中加少量白磷并注满水。把三个玻璃瓶同时放进盛有80℃热水的大烧杯中。
Ⅱ.用注射器向2号瓶中注入适量的水。
Ⅲ.用注射器把3号瓶中水抽出发现3号瓶中的白磷燃烧起来。
①写出步骤Ⅰ中三个玻璃瓶中的现象_______。
②步骤Ⅲ中,3号瓶中白磷燃烧的原因是_______。
(2)用图二所示装置来测定空气中氧气含量。
①该实验涉及的反应属于_______(填“化合”或“分解”)反应。
②完成下表(不考虑两支注射器中间连接部分的容积)。
左侧注射器中气体体积 右侧注射器中气体体积 结论
实验前 5 mL 10mL 氧气约占空气总体积的20%
完全冷却后 0 _______mL
22.根据下列实验装置,请回答:
(1)仪器a的名称是_______________。
(2)检查装置A气密性的方法是:夹紧止水夹,_______________,则气密性良好;
(3)实验室里用H2O2制取氧气,选择的发生装置为_______________(填字母),反应的化学方程式为_______________。
(4)用装置F和另一仪器(除导管外)收集并测量O2体积,另一仪器名称为_______________,在F中,气体应从导管_______________(填“b”或“c”)端通入;
(5)实验室制取二氧化碳选用的发生装置与收集装置为_______和________,不选择E装置收集二氧化碳的原因是_______________。
(6)实验室里,常用加热无水醋酸钠和碱石灰固体混合物的方法,制备甲烷:
①选择的发生装置为_______________(填字母),用装置E收集甲烷,利用了甲烷_______________的物理性质;用装置C而不用装置D收集甲烷,原因是_______________。
②甲烷是一种可燃性气体,点燃前应该进行的操作是_______________。
五、计算题
23.足量稀盐酸与125克纯度为80%的石灰石反应,生成二氧化碳的质量是多少?
24.小东从海边捡来一些嵌有砂砾的贝壳(主要成分是CaCO3),他做了如下实验:首先称取50g贝壳样品,然后将150mL的盐酸分5次加入(假设其余杂质均不与盐酸反应),实验过程中的数据记录如下:
实验次数 第一次 第二次 第三次 第四次 第五次
稀盐酸的体积 30mL 30mL 30mL 30mL 30mL
剩余固体质量 40.0g X 20.0g 10.0g 5.0g
(1)X=______g;
(2)求充分反应后,最终产生二氧化碳的质量。
参考答案
1.C 2.C 3.B 4.C 5.D 6.C 7.C 8.C 9.D 10.D 11.B 12.A 13.D 14.B 15.D
16.(1)A(2)C(3)
17.(1)往两个集气瓶中分别滴入澄清石灰水
(2)往两个集气瓶中分别伸入带火星的木条
18.(1)D
(2)物理
(3) 肥皂水 煮沸
19.(1) 氧气(或O2) 硫(或S) 二氧化硫(或SO2) 碳(或C) 二氧化碳(或CO2)
(2)
化合
20.(1)C
(2)
(3)
21.(1) 2号瓶中的白磷燃烧产生大量白烟,1号、3号瓶无明显现象 将瓶中水抽出,白磷与氧气(或空气)接触,且温度达到了着火点
(2) 化合 12
22.(1)锥形瓶
(2)从长颈漏斗中倒入水至淹没下端管口,使长颈漏斗中形成一段水柱,一段时间后,水柱液面不下降
(3) A
(4) 量筒 c
(5) A D 二氧化碳可溶于水
(6) B 不易溶于水 密度比空气小 验纯
23.解:m(碳酸钙)=125g×80%=100g
设生成二氧化碳的质量为 x
x = 44g
答:生成二氧化碳的质量为 44g。
24.(1)30g (2)19.8g
一、单选题
1.在一定条件下,木炭、一氧化碳、氢气都能与氧化铜发生反应,下列叙述正确的是
A.反应后生成的气体都有毒 B.反应类型都是化合反应
C.反应后都能生成红色固体 D.反应前后各元的化合价都发生了变化
2.下列物质的用途主要由其化学性质决定的是
A.石墨作电极 B.干冰作制冷剂 C.氢气作燃料 D.金刚石切割玻璃
3.下列实验方法不正确的是
A.用肥皂水区分硬水和软水 B.用观察固体颜色区分氧化铜和二氧化锰
C.用燃着的木条区分氧气和二氧化碳 D.用澄清石灰水区分氮气和二氧化碳
4.下列实验操作正确的是
A.氧气验满 B.检查装置气密性
C.制取并收集CO2 D.加热液体
5.金刚石、石墨、木炭和C60都是由碳元素组成的单质,下列关于碳的单质的叙述正确的是
A.都是黑色固体
B.一定条件下,石墨转化成金刚石是物理变化
C.碳原子的排列方式相同
D.在氢气中充分燃烧时都生成二氧化碳
6.下列说法不正确的是
A.相同的元素可以组成不同的物质 B.塑料制品的老化与缓慢氧化有关
C.H2O2溶液中加MnO2能产生更多的氧气 D.符号2N和N2中数字2的意义不相同
7.下面对灭火的原理分析正确的是
A.用水扑灭燃着的木材—降低木材的着火点 B.用锅盖盖灭油锅内的火—降低油温
C.砍掉大火蔓延路线前的树木—清除可燃物 D.用扇子扇灭烛火--隔离空气
8.推理是学习化学的一种常用方法,下列推理正确的是
A.阴离子带负电荷,则带负电荷的粒子一定是阴离子
B.单质只含一种元素,则只含一种元素的物质一定是单质
C.元素的种类是由质子数决定的,则质子数相同的原子一定属于同种元素
D.化学反应一定伴随着能量变化,则伴随能量变化的一定是化学反应
9.比较推理是化学学习中常用的思维方法,下列推理正确的是
A.燃烧过程中伴随着发光放热,所以有发光放热现象的变化都是燃烧
B.分子可以构成物质,所以物质都是由分子构成的
C.单质只含一种元素,所以含一种元素的物质都是单质
D.物理变化没有其他物质生成,所以没有生成其他物质的变化叫做物理变化
10.2021年世界环境日中国主题是“人与自然和谐共生”下列做法不符合该主题的是
A.长江沿线十年禁止捕鱼 B.生活中出行多乘坐轻轨
C.冬天用天然气炉替代碳炉生火取暖 D.朋友聚餐鼓励使用公筷
11.下列鉴别物质的方法错误的是
A.用加热的方法鉴别碳酸氢铵和食盐 B.用燃着的木条鉴别氮气和二氧化碳
C.用肥皂水鉴别蒸馏水和澄清石灰水 D.用二氧化锰鉴别蒸馏水和双氧水
12.对下列事实的解释合理的是
A.医用口罩能有效阻隔病毒—其阻隔原理与过滤类似
B.干冰能营造云雾缭绕效果—干冰升华形成白色气体
C.水电解能生成氢气和氧气—水是由氢气和氧气组成
D.分离液态空气可得到氧气—液氧沸点比液氮沸点低
13.下列实验方案,不能达到实验目的的是
选项 实验目的 实验方案
A 鉴别软水和硬水 用肥皂水
B 鉴别氧气和二氧化碳 分别加入澄清石灰水
C 鉴别水和白醋 闻气味
D 鉴别空气和氮气 用带火星的木条
A.A B.B C.C D.D
14.某兴趣小组为探究影响化学反应速率的因素,使用等量的同种钙片和白醋开展四组实验,分别测得产生的二氧化碳体积分数随时间的变化曲线如图所示。
选取CO2的体积分数从0-8%为研究对象,下列实验结果的分析,不正确的是
A.对比①③,温度越高,反应速率越快
B.对比②③,反应物接触面积越小,反应速率越慢
C.对比③④,反应物接触面积越大,反应速率越快
D.对比①②③④,④的反应速率最慢
15.化学反应之间、化学物质之间具有包含、并列、交叉等关系。下表中X、Y符合下图所示关系的是
A B C D
X 燃烧 化合反应 纯净物 化合反应
Y 氧化反应 分解反应 混合物 氧化反应
A.A B.B C.C D.D
二、填空题
16.2020年9月,中国向世界宣布了2030年前实现碳达峰、2060年前实现碳中和。
(1)为减缓大气中二氧化碳含量的增加,下列措施可行的是 (填字母代号);
A.植树造林,开发和利用太阳能、水能、风能等新能源
B.禁止使用煤、石油、天然气等化石燃料
(2)绿色植物通过光合作用吸收二氧化碳,生成葡萄糖并放出氧气,其反应的化学方程式:,则葡萄糖的化学式为 。(填字母)
A.CH6O B.C6H12 C.C6H12O6
(3)近年我国科学家合成了一种新型催化剂,可将二氧化碳和氢气转化为清洁的液体燃料甲醇(CH3OH)和水,该反应的化学方程式为____________。
17.现有两瓶气体:CO2和O2.可以用下列方法来区别它们:
往两个集气瓶中分别滴入紫色石蕊溶液;
(1)_______;
(2)_______。(只写方法即可)
18.水与人类的生活和生产密切相关。
(1)在自来水生产的过程中,未涉及的净水方法是_____(填序号)。
A.吸附 B.沉淀 C.过滤 D.蒸馏
(2)利用活性炭生产自来水时,利用了活性炭的__________性质(填“物理”或“化学”)。
(3)人们常用_____检验地下水是硬水还是软水。生活中可用_____的方法降低水的硬度。
三、推断题
19.有A、B、C、D、E五种物质,A是无色无味的气体;B在A中燃烧有蓝紫色火焰并生成能造成空气污染的气体C;D是黑色固体,在A中燃烧生成气体E; E能使澄清的石灰水变浑浊。请根据以上所述回答下列问题:
(1)A是________;B是_______;C是________;D是_______;E是_______。
(2)B与A发生反应的文字表达式是:__________;属于________反应。D与A发生反应的文字表达式是:___________。
20.如图中A、B、C、D、E是初中化学中常见的五种物质,在通常情况下,A为黑色固体,B、C、E均为无色无味的气体,D为不溶于水的白色固体,在实验室常用含D的物质与稀盐酸反应制取C,单质E是组成空气的主要成分之一。它们之间的关系如图所示,请回答下列问题:
(1)A的化学式是____________。
(2)写出B→C的化学方程式____________。
(3)写出C→D的化学方程式____________。
四、实验题
21.实验是进行科学探究的重要手段。根据如图实验回答下列问题。
(1)如图一所示。
Ⅰ.1号瓶中加入红磷,2号瓶中加入白磷,3号瓶中加少量白磷并注满水。把三个玻璃瓶同时放进盛有80℃热水的大烧杯中。
Ⅱ.用注射器向2号瓶中注入适量的水。
Ⅲ.用注射器把3号瓶中水抽出发现3号瓶中的白磷燃烧起来。
①写出步骤Ⅰ中三个玻璃瓶中的现象_______。
②步骤Ⅲ中,3号瓶中白磷燃烧的原因是_______。
(2)用图二所示装置来测定空气中氧气含量。
①该实验涉及的反应属于_______(填“化合”或“分解”)反应。
②完成下表(不考虑两支注射器中间连接部分的容积)。
左侧注射器中气体体积 右侧注射器中气体体积 结论
实验前 5 mL 10mL 氧气约占空气总体积的20%
完全冷却后 0 _______mL
22.根据下列实验装置,请回答:
(1)仪器a的名称是_______________。
(2)检查装置A气密性的方法是:夹紧止水夹,_______________,则气密性良好;
(3)实验室里用H2O2制取氧气,选择的发生装置为_______________(填字母),反应的化学方程式为_______________。
(4)用装置F和另一仪器(除导管外)收集并测量O2体积,另一仪器名称为_______________,在F中,气体应从导管_______________(填“b”或“c”)端通入;
(5)实验室制取二氧化碳选用的发生装置与收集装置为_______和________,不选择E装置收集二氧化碳的原因是_______________。
(6)实验室里,常用加热无水醋酸钠和碱石灰固体混合物的方法,制备甲烷:
①选择的发生装置为_______________(填字母),用装置E收集甲烷,利用了甲烷_______________的物理性质;用装置C而不用装置D收集甲烷,原因是_______________。
②甲烷是一种可燃性气体,点燃前应该进行的操作是_______________。
五、计算题
23.足量稀盐酸与125克纯度为80%的石灰石反应,生成二氧化碳的质量是多少?
24.小东从海边捡来一些嵌有砂砾的贝壳(主要成分是CaCO3),他做了如下实验:首先称取50g贝壳样品,然后将150mL的盐酸分5次加入(假设其余杂质均不与盐酸反应),实验过程中的数据记录如下:
实验次数 第一次 第二次 第三次 第四次 第五次
稀盐酸的体积 30mL 30mL 30mL 30mL 30mL
剩余固体质量 40.0g X 20.0g 10.0g 5.0g
(1)X=______g;
(2)求充分反应后,最终产生二氧化碳的质量。
参考答案
1.C 2.C 3.B 4.C 5.D 6.C 7.C 8.C 9.D 10.D 11.B 12.A 13.D 14.B 15.D
16.(1)A(2)C(3)
17.(1)往两个集气瓶中分别滴入澄清石灰水
(2)往两个集气瓶中分别伸入带火星的木条
18.(1)D
(2)物理
(3) 肥皂水 煮沸
19.(1) 氧气(或O2) 硫(或S) 二氧化硫(或SO2) 碳(或C) 二氧化碳(或CO2)
(2)
化合
20.(1)C
(2)
(3)
21.(1) 2号瓶中的白磷燃烧产生大量白烟,1号、3号瓶无明显现象 将瓶中水抽出,白磷与氧气(或空气)接触,且温度达到了着火点
(2) 化合 12
22.(1)锥形瓶
(2)从长颈漏斗中倒入水至淹没下端管口,使长颈漏斗中形成一段水柱,一段时间后,水柱液面不下降
(3) A
(4) 量筒 c
(5) A D 二氧化碳可溶于水
(6) B 不易溶于水 密度比空气小 验纯
23.解:m(碳酸钙)=125g×80%=100g
设生成二氧化碳的质量为 x
x = 44g
答:生成二氧化碳的质量为 44g。
24.(1)30g (2)19.8g
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
