四川省绵阳市第一高级中学2021-2022学年高一上学期期中教学质量测试化学试卷(Word版含答案)
文档属性
| 名称 | 四川省绵阳市第一高级中学2021-2022学年高一上学期期中教学质量测试化学试卷(Word版含答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 197.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-22 00:00:00 | ||
图片预览


文档简介
秘密 ★ 启用前 【考试时间:2021年11月4日10:30—11:50】
绵阳市第一高级中学2021-2022学年高一上学期期中教学质量测试
化学
本试卷分为试题卷和答题卡两部分,其中试题卷由第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)组成,共x页;答题卡共x页。满分100分,考试时间80分钟。
注意事项:
1. 答题前,考生务必将自己的学校、班级、姓名用0.5毫米黑色签字笔填写清楚,同时用2B铅笔将考号准确填涂在“准考证号”栏目内。
2. 选择题使用2B铅笔填涂在答题卡对应题目标号的位置上,如需改动,用橡皮擦擦干净后再选涂其它答案;非选择题用0.5毫米黑色签字笔书写在答题卡的对应框内,超出答题区域书写的答案无效;在草稿纸、试题卷上答题无效。
3. 考试结束后将答题卡收回。
可能用到的相对原子质量:H 1 C 12 O 16 Na 23 S 32
第Ⅰ卷(选择题,共51分)
一、选择题(本题包括14小题,每小题3分,共42分。每小题只有一个选项符合题意)
1.下列物质与危险化学品标志的对应关系错误的是( )
A B C D
砒霜 NaCl 乙醇 浓硫酸
2.下列关于古籍中的记载说法不正确的是( )
A.《天工开物》中“凡石灰,经火焚炼为用”涉及的反应类型是分解反应
B.“朝坛雾卷,曙岭烟沉”中的雾是一种气溶胶,能产生丁达尔效应
C.“熬胆矾铁釜,久之亦化为铜”,该过程发生了氧化还原反应
D.“丹砂(HgS)烧之成水银,积变又还成丹砂”,该过程中不涉及氧化还原反应
3.下列实验操作完全正确的是( )
编号 实 验 操 作
A 用浓硫酸配制一定浓度的稀硫酸 用量筒准确量取一定体积的浓硫酸,将浓硫酸溶于水后,立刻转移到容量瓶中。
B 量取盐酸溶液 用10 mL量筒量取4.0 mol/L的盐酸5.62 mL
C 除去BaSO4中的少量BaCO3 加入足量稀盐酸,充分反应后,过滤、洗涤、干燥
D 取出分液漏斗中所需的上层液体 下层液体从分液漏斗下口放出,关闭活塞,换一个接收容器,上层液体继续从分液漏斗下口放出
4.用胆矾配制的硫酸铜溶液,下列操作正确的是( )
A.取25 g胆矾溶于1 L水中
B.取16 g胆矾溶于水配成1 L溶液
C.取25 g胆矾溶于水配成1 L溶液
D.将胆矾加热除去结晶水,再取16 g硫酸铜溶于1 L水中
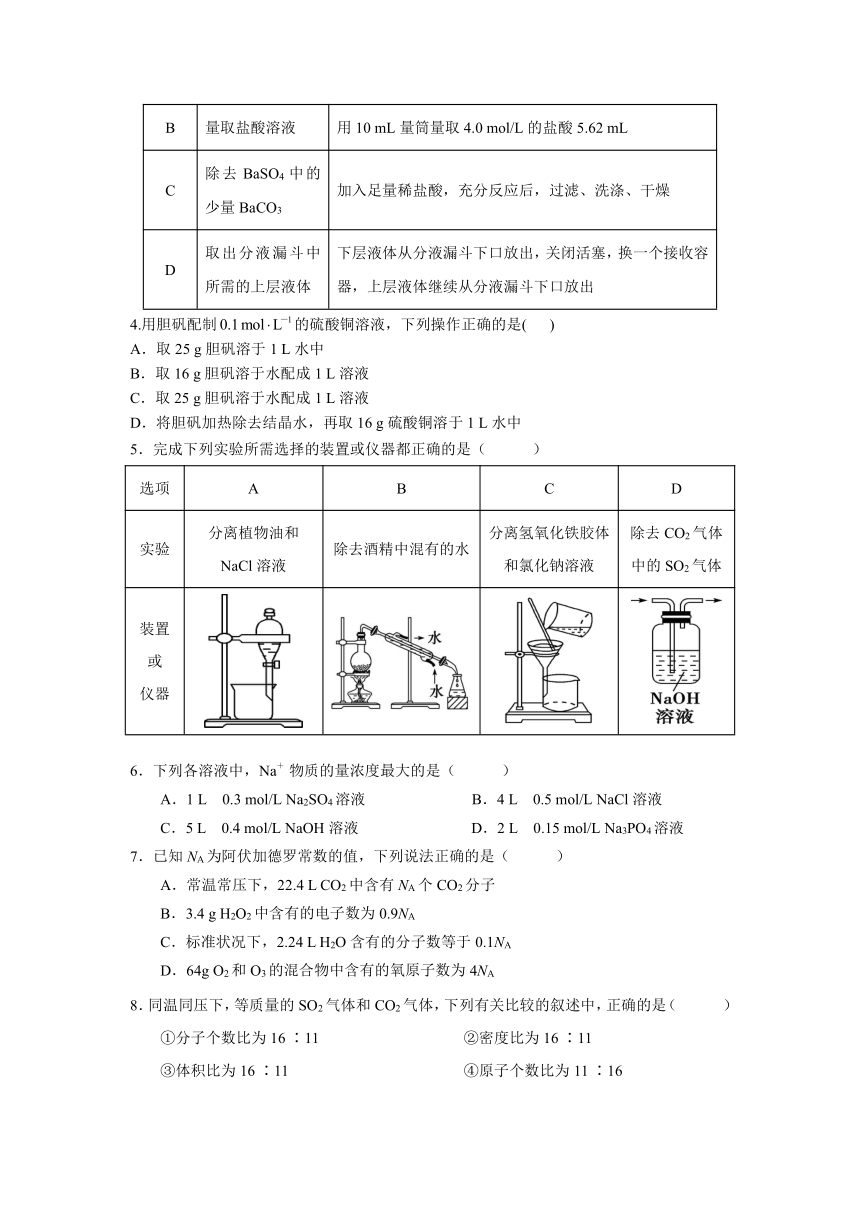
5.完成下列实验所需选择的装置或仪器都正确的是( )
选项 A B C D
实验 分离植物油和NaCl溶液 除去酒精中混有的水 分离氢氧化铁胶体和氯化钠溶液 除去CO2气体中的SO2气体
装置或仪器
6.下列各溶液中,Na+ 物质的量浓度最大的是( )
A.1 L 0.3 mol/L Na2SO4溶液 B.4 L 0.5 mol/L NaCl溶液
C.5 L 0.4 mol/L NaOH溶液 D.2 L 0.15 mol/L Na3PO4溶液
7.已知NA为阿伏加德罗常数的值,下列说法正确的是( )
A.常温常压下,22.4 L CO2中含有NA个CO2分子
B.3.4 g H2O2中含有的电子数为0.9NA
C.标准状况下,2.24 L H2O含有的分子数等于0.1NA
D.64g O2和O3的混合物中含有的氧原子数为4NA
8.同温同压下,等质量的SO2气体和CO2气体,下列有关比较的叙述中,正确的是( )
①分子个数比为16 ∶11 ②密度比为16 ∶11
③体积比为16 ∶11 ④原子个数比为11 ∶16
A.①③ B. ①④ C. ②③ D. ②④
9.下列物质的分类正确的组合是( )
电解质 非电解质 酸 盐 碱性氧化物
A H2SO4 干冰 硫酸 小苏打 Al2O3
B KCl SO2 盐酸 食盐 Na2O
C HCl NH3 CH3COOH CuSO4·5H2O 生石灰
D Na2O 酒精 HNO3 碳酸钙 Na2O2
10.下列关于胶体的叙述中,不正确的是( )
A.豆腐的制作是利用了胶体的聚沉
B.胶体与其他分散系的本质区别是分散质粒子的直径大小
C.利用丁达尔效应可以区分溶液和胶体
D.胶体能发生电泳现象是因为胶体带电
11.甲、乙两种溶液中分别含有大量的Cu2+、K+、H+、Cl-、CO32-、OH-这6种离子中的3种(两种溶液中的离子不重复),已知甲溶液呈蓝色,则乙溶液中大量存在的离子是( )
A.Cu2+、H+、Cl- B.K+、OH-、CO32-
C.CO32-、OH-、Cl- D.K+、H+、Cl-
12.亚硝酸钠可将人体血红蛋白中的离子转化为离子,生成高铁血红蛋白而丧失与氧气结合的能力。误食亚硝酸钠中毒,可服维生素C缓解,则亚硝酸钠和维生素C分别表现出的性质是( )
A.氧化性、酸性 B.还原性、氧化性
C.氧化性、还原性 D.还原性、碱性
13.提纯下列物质除去其中的杂质(括号中为杂质),所用试剂和方法一定正确的是( )
A.:溶液、过滤 B.:过量溶液、过滤
C.:盐酸、过滤 D.:加少量水、过滤
14.下列变化中,必须加入还原剂才可以实现的是( )
A.KC1→C12 B.KMnO4→MnO2 C.Fe2(SO4)3→FeSO4 D.CaO→Ca(OH)2
15.下列离子方程式书写正确的是( )
A.过氧化钠与水反应:2O22- + 2H2O == 4OH- + O2↑
B.将金属钠投入硫酸铜溶液中:Na + Cu2+ == Na+ + Cu
C.实验室制备氢氧化铝:Al3+ + 3NH3·H2O == Al(OH)3↓ + 3NH4+
D.盐酸与氢氧化镁中和:H+ + OH- == H2O
16.反应①、②分别是从海藻灰和某种矿石中提取碘的主要反应:
①2NaI + MnO2 + 3H2SO4 =2NaHSO4 + MnSO4 + 2H2O + I2
②2NaIO3 + 5NaHSO3 = 2Na2SO4 + 3NaHSO4 + H2O + I2。下列说法中正确的是( )
A.两个反应中硫元素均被氧化
B.碘元素在反应①中被还原,在反应②中被氧化
C.反应①、②中生成等质量的I2时,转移电子数之比为1:5
D.氧化性:MnO2 > I2 >IO3- > SO42-
17.R2O82-离子在一定条件下可以把Mn2+离子氧化,若反应后R2O82-离子变为RO42-离子,又知反应中氧化剂和还原剂的物质的量之比为5︰2,Mn2+离子被氧化后的化合价为( )
A.+4 B.+5 C.+6 D.+7
第Ⅱ卷(非选择题,共49分)
18.(10分)有下列物质:①氢氧化钡固体 ②KHSO4 ③HNO3 ④稀硫酸 ⑤二氧化碳气体 ⑥铜 ⑦碳酸钠粉末 ⑧蔗糖晶体 ⑨熔融氯化钠 ⑩CuSO4·5H2O晶体。请用序号填空:
(1)上述状态下可导电的是 。
(2)属于电解质的是 。
(3)属于非电解质的是 。
(4)②在水溶液中的电离方程式为 ,过量的④与⑦在溶液中反应的离子方程式为 。
19.(14分)高铁酸钾(K2FeO4)是一种绿色氧化剂,具有高效的杀菌消毒作用,常用于饮水处理,在许多领域展现出广阔的应用前景。制备高铁酸钾有下列两种方法:
方法一:Fe2O3 + KNO3 + KOH== K2FeO4 + KNO2 + H2O (未配平)
方法二:2Fe(OH)3+3KClO+4KOH=2K2FeO4+3KCl+ 5H2O
(1)配平方法一的化学方程式,并用双线桥标明电子转移的方向和数目:
Fe2O3 + KNO3 + KOH == K2FeO4 + KNO2 + H2O
(2)方法二中的还原产物为 (写化学式),将方法二的化学方程式改写为离子方程式 ,根据反应方程式判断,氧化性:KClO K2FeO4(填“>”、“<”或“=”);
(3)利用方法二制备K2FeO4,若有0.5mol K2FeO4生成,转移的电子数为 ;
(4)已知反应:①Cl2+2KBr=2KCl+Br2,②2KMnO4+16HCl(浓) =2KCl + 2MnCl2+ 5Cl2↑+8H2O,③Br2+K2S=2KBr+S。下列说法正确的是__________。
A.上述三个反应都有单质生成,所以都是置换反应
B.氧化性由强到弱顺序为KMnO4>Cl2>Br2>S
C.反应②中氧化剂与还原剂的物质的量之比为1:8
D.反应③中1mol还原剂被氧化则转移电子的物质的量为2mol
20.(12分)化学是以实验为基础的科学。下列是中学化学中一些常见的实验装置,按要求回答下列问题:
① ② ③ ④
(1)写出仪器名称:B ;D ;
(2)指出装置①中的一处错误 。
(3)分离下列混合物的操作中,用到装置②的是 ,用到装置③的是 (填字母)。
A.水和泥沙的混合物 B.水和酒精的混合物
C.水和四氯化碳的混合物 D.淀粉胶体和氯化钠溶液
E.固体氯化钠和碘单质 F.碳酸钙和碳酸钠粉末
(4)装置②可用于CCl4萃取碘水中的碘,实验现象是 。
21.(13分)已知某工业废水中含有大量FeSO4,较多的Cu2+, 以及部分污泥,通过下列流程可从该废水中回收FeSO4·7H2O晶体及金属Cu。
(1)步骤1的主要操作是 (填操作名称),需用到的玻璃仪器除烧杯外还有 、 。
(2)步骤2中发生反应的离子方程式为_____________________________________。
(3)步骤3中发生反应的化学方程式为_____________________________________。
(4)步骤4中涉及的操作是:蒸发浓缩、____________、过滤、洗涤、烘干。
绵阳一中高2020级第一学期半期考试
化学参考答案及评分标准
第Ⅰ卷(选择题,共51分)
一、选择题(本题包括14小题,每小题3分,共42分。每小题只有一个选项符合题意)
1. B 2. D 3. C 4.C 5. A 6. A 7. D 8.D 9.C 10. D 11. B 12.C 13.C 14. C 15. C 16. C 17. D
第Ⅱ卷(非选择题,共49分)
18.(10分,每空2分)(1)④⑥⑨; (2)①②③⑦⑨⑩; (3)⑤⑧;
(4)KHSO4 = K+ + H+ + SO42-;2H+ + CO32- = CO2 ↑ + H2O
19.(14分)(1) 1 Fe2O3 + 3 KNO3 + 4 KOH == 2 K2FeO4 + 3 KNO2 + 2 H2O(4分,其中
配平2分,双线桥2分); (2)KCl;2Fe(OH)3+3ClO-+4OH- =2FeO42-+3Cl- + 5H2O > (6分,每空2分); (3)1.5NA(2分); (4)BD(2分)
20.(12分,每空2分)(1)冷凝管;分液漏斗; (2)冷凝水的进出口反了;
(3)C; AF; (4)上下分层,上层几乎无色,下层为紫红色
21.(13分,)(1)过滤;玻璃棒、漏斗; (2) Fe + Cu2+ = Cu + Fe2+(此空3分)
(3)Fe + H2SO4 = FeSO4 + H2↑; (4)冷却结晶(答结晶也可)
失去6e-
得到6e-
绵阳市第一高级中学2021-2022学年高一上学期期中教学质量测试
化学
本试卷分为试题卷和答题卡两部分,其中试题卷由第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)组成,共x页;答题卡共x页。满分100分,考试时间80分钟。
注意事项:
1. 答题前,考生务必将自己的学校、班级、姓名用0.5毫米黑色签字笔填写清楚,同时用2B铅笔将考号准确填涂在“准考证号”栏目内。
2. 选择题使用2B铅笔填涂在答题卡对应题目标号的位置上,如需改动,用橡皮擦擦干净后再选涂其它答案;非选择题用0.5毫米黑色签字笔书写在答题卡的对应框内,超出答题区域书写的答案无效;在草稿纸、试题卷上答题无效。
3. 考试结束后将答题卡收回。
可能用到的相对原子质量:H 1 C 12 O 16 Na 23 S 32
第Ⅰ卷(选择题,共51分)
一、选择题(本题包括14小题,每小题3分,共42分。每小题只有一个选项符合题意)
1.下列物质与危险化学品标志的对应关系错误的是( )
A B C D
砒霜 NaCl 乙醇 浓硫酸
2.下列关于古籍中的记载说法不正确的是( )
A.《天工开物》中“凡石灰,经火焚炼为用”涉及的反应类型是分解反应
B.“朝坛雾卷,曙岭烟沉”中的雾是一种气溶胶,能产生丁达尔效应
C.“熬胆矾铁釜,久之亦化为铜”,该过程发生了氧化还原反应
D.“丹砂(HgS)烧之成水银,积变又还成丹砂”,该过程中不涉及氧化还原反应
3.下列实验操作完全正确的是( )
编号 实 验 操 作
A 用浓硫酸配制一定浓度的稀硫酸 用量筒准确量取一定体积的浓硫酸,将浓硫酸溶于水后,立刻转移到容量瓶中。
B 量取盐酸溶液 用10 mL量筒量取4.0 mol/L的盐酸5.62 mL
C 除去BaSO4中的少量BaCO3 加入足量稀盐酸,充分反应后,过滤、洗涤、干燥
D 取出分液漏斗中所需的上层液体 下层液体从分液漏斗下口放出,关闭活塞,换一个接收容器,上层液体继续从分液漏斗下口放出
4.用胆矾配制的硫酸铜溶液,下列操作正确的是( )
A.取25 g胆矾溶于1 L水中
B.取16 g胆矾溶于水配成1 L溶液
C.取25 g胆矾溶于水配成1 L溶液
D.将胆矾加热除去结晶水,再取16 g硫酸铜溶于1 L水中
5.完成下列实验所需选择的装置或仪器都正确的是( )
选项 A B C D
实验 分离植物油和NaCl溶液 除去酒精中混有的水 分离氢氧化铁胶体和氯化钠溶液 除去CO2气体中的SO2气体
装置或仪器
6.下列各溶液中,Na+ 物质的量浓度最大的是( )
A.1 L 0.3 mol/L Na2SO4溶液 B.4 L 0.5 mol/L NaCl溶液
C.5 L 0.4 mol/L NaOH溶液 D.2 L 0.15 mol/L Na3PO4溶液
7.已知NA为阿伏加德罗常数的值,下列说法正确的是( )
A.常温常压下,22.4 L CO2中含有NA个CO2分子
B.3.4 g H2O2中含有的电子数为0.9NA
C.标准状况下,2.24 L H2O含有的分子数等于0.1NA
D.64g O2和O3的混合物中含有的氧原子数为4NA
8.同温同压下,等质量的SO2气体和CO2气体,下列有关比较的叙述中,正确的是( )
①分子个数比为16 ∶11 ②密度比为16 ∶11
③体积比为16 ∶11 ④原子个数比为11 ∶16
A.①③ B. ①④ C. ②③ D. ②④
9.下列物质的分类正确的组合是( )
电解质 非电解质 酸 盐 碱性氧化物
A H2SO4 干冰 硫酸 小苏打 Al2O3
B KCl SO2 盐酸 食盐 Na2O
C HCl NH3 CH3COOH CuSO4·5H2O 生石灰
D Na2O 酒精 HNO3 碳酸钙 Na2O2
10.下列关于胶体的叙述中,不正确的是( )
A.豆腐的制作是利用了胶体的聚沉
B.胶体与其他分散系的本质区别是分散质粒子的直径大小
C.利用丁达尔效应可以区分溶液和胶体
D.胶体能发生电泳现象是因为胶体带电
11.甲、乙两种溶液中分别含有大量的Cu2+、K+、H+、Cl-、CO32-、OH-这6种离子中的3种(两种溶液中的离子不重复),已知甲溶液呈蓝色,则乙溶液中大量存在的离子是( )
A.Cu2+、H+、Cl- B.K+、OH-、CO32-
C.CO32-、OH-、Cl- D.K+、H+、Cl-
12.亚硝酸钠可将人体血红蛋白中的离子转化为离子,生成高铁血红蛋白而丧失与氧气结合的能力。误食亚硝酸钠中毒,可服维生素C缓解,则亚硝酸钠和维生素C分别表现出的性质是( )
A.氧化性、酸性 B.还原性、氧化性
C.氧化性、还原性 D.还原性、碱性
13.提纯下列物质除去其中的杂质(括号中为杂质),所用试剂和方法一定正确的是( )
A.:溶液、过滤 B.:过量溶液、过滤
C.:盐酸、过滤 D.:加少量水、过滤
14.下列变化中,必须加入还原剂才可以实现的是( )
A.KC1→C12 B.KMnO4→MnO2 C.Fe2(SO4)3→FeSO4 D.CaO→Ca(OH)2
15.下列离子方程式书写正确的是( )
A.过氧化钠与水反应:2O22- + 2H2O == 4OH- + O2↑
B.将金属钠投入硫酸铜溶液中:Na + Cu2+ == Na+ + Cu
C.实验室制备氢氧化铝:Al3+ + 3NH3·H2O == Al(OH)3↓ + 3NH4+
D.盐酸与氢氧化镁中和:H+ + OH- == H2O
16.反应①、②分别是从海藻灰和某种矿石中提取碘的主要反应:
①2NaI + MnO2 + 3H2SO4 =2NaHSO4 + MnSO4 + 2H2O + I2
②2NaIO3 + 5NaHSO3 = 2Na2SO4 + 3NaHSO4 + H2O + I2。下列说法中正确的是( )
A.两个反应中硫元素均被氧化
B.碘元素在反应①中被还原,在反应②中被氧化
C.反应①、②中生成等质量的I2时,转移电子数之比为1:5
D.氧化性:MnO2 > I2 >IO3- > SO42-
17.R2O82-离子在一定条件下可以把Mn2+离子氧化,若反应后R2O82-离子变为RO42-离子,又知反应中氧化剂和还原剂的物质的量之比为5︰2,Mn2+离子被氧化后的化合价为( )
A.+4 B.+5 C.+6 D.+7
第Ⅱ卷(非选择题,共49分)
18.(10分)有下列物质:①氢氧化钡固体 ②KHSO4 ③HNO3 ④稀硫酸 ⑤二氧化碳气体 ⑥铜 ⑦碳酸钠粉末 ⑧蔗糖晶体 ⑨熔融氯化钠 ⑩CuSO4·5H2O晶体。请用序号填空:
(1)上述状态下可导电的是 。
(2)属于电解质的是 。
(3)属于非电解质的是 。
(4)②在水溶液中的电离方程式为 ,过量的④与⑦在溶液中反应的离子方程式为 。
19.(14分)高铁酸钾(K2FeO4)是一种绿色氧化剂,具有高效的杀菌消毒作用,常用于饮水处理,在许多领域展现出广阔的应用前景。制备高铁酸钾有下列两种方法:
方法一:Fe2O3 + KNO3 + KOH== K2FeO4 + KNO2 + H2O (未配平)
方法二:2Fe(OH)3+3KClO+4KOH=2K2FeO4+3KCl+ 5H2O
(1)配平方法一的化学方程式,并用双线桥标明电子转移的方向和数目:
Fe2O3 + KNO3 + KOH == K2FeO4 + KNO2 + H2O
(2)方法二中的还原产物为 (写化学式),将方法二的化学方程式改写为离子方程式 ,根据反应方程式判断,氧化性:KClO K2FeO4(填“>”、“<”或“=”);
(3)利用方法二制备K2FeO4,若有0.5mol K2FeO4生成,转移的电子数为 ;
(4)已知反应:①Cl2+2KBr=2KCl+Br2,②2KMnO4+16HCl(浓) =2KCl + 2MnCl2+ 5Cl2↑+8H2O,③Br2+K2S=2KBr+S。下列说法正确的是__________。
A.上述三个反应都有单质生成,所以都是置换反应
B.氧化性由强到弱顺序为KMnO4>Cl2>Br2>S
C.反应②中氧化剂与还原剂的物质的量之比为1:8
D.反应③中1mol还原剂被氧化则转移电子的物质的量为2mol
20.(12分)化学是以实验为基础的科学。下列是中学化学中一些常见的实验装置,按要求回答下列问题:
① ② ③ ④
(1)写出仪器名称:B ;D ;
(2)指出装置①中的一处错误 。
(3)分离下列混合物的操作中,用到装置②的是 ,用到装置③的是 (填字母)。
A.水和泥沙的混合物 B.水和酒精的混合物
C.水和四氯化碳的混合物 D.淀粉胶体和氯化钠溶液
E.固体氯化钠和碘单质 F.碳酸钙和碳酸钠粉末
(4)装置②可用于CCl4萃取碘水中的碘,实验现象是 。
21.(13分)已知某工业废水中含有大量FeSO4,较多的Cu2+, 以及部分污泥,通过下列流程可从该废水中回收FeSO4·7H2O晶体及金属Cu。
(1)步骤1的主要操作是 (填操作名称),需用到的玻璃仪器除烧杯外还有 、 。
(2)步骤2中发生反应的离子方程式为_____________________________________。
(3)步骤3中发生反应的化学方程式为_____________________________________。
(4)步骤4中涉及的操作是:蒸发浓缩、____________、过滤、洗涤、烘干。
绵阳一中高2020级第一学期半期考试
化学参考答案及评分标准
第Ⅰ卷(选择题,共51分)
一、选择题(本题包括14小题,每小题3分,共42分。每小题只有一个选项符合题意)
1. B 2. D 3. C 4.C 5. A 6. A 7. D 8.D 9.C 10. D 11. B 12.C 13.C 14. C 15. C 16. C 17. D
第Ⅱ卷(非选择题,共49分)
18.(10分,每空2分)(1)④⑥⑨; (2)①②③⑦⑨⑩; (3)⑤⑧;
(4)KHSO4 = K+ + H+ + SO42-;2H+ + CO32- = CO2 ↑ + H2O
19.(14分)(1) 1 Fe2O3 + 3 KNO3 + 4 KOH == 2 K2FeO4 + 3 KNO2 + 2 H2O(4分,其中
配平2分,双线桥2分); (2)KCl;2Fe(OH)3+3ClO-+4OH- =2FeO42-+3Cl- + 5H2O > (6分,每空2分); (3)1.5NA(2分); (4)BD(2分)
20.(12分,每空2分)(1)冷凝管;分液漏斗; (2)冷凝水的进出口反了;
(3)C; AF; (4)上下分层,上层几乎无色,下层为紫红色
21.(13分,)(1)过滤;玻璃棒、漏斗; (2) Fe + Cu2+ = Cu + Fe2+(此空3分)
(3)Fe + H2SO4 = FeSO4 + H2↑; (4)冷却结晶(答结晶也可)
失去6e-
得到6e-
同课章节目录
