第4章 认识化学变化测试卷—2021-2022学年九年级化学沪教版(全国)上册(无答案)
文档属性
| 名称 | 第4章 认识化学变化测试卷—2021-2022学年九年级化学沪教版(全国)上册(无答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 317.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-11-21 00:00:00 | ||
图片预览



文档简介
第4章《认识化学变化》测试卷
(满分:100分 时间:45分钟)
可能用到的相对原子质量:H-1 B-11 O-16 Mg-24 Al-27 P-31 Mn-55
一、选择题(每小题只有一个正确答案。每小题2分,共40分)
1.不适宜用质量守恒定律解释的现象是 ( )
A.煤炭燃烧后变成煤灰,质量变小了
B.樟脑球放在衣柜中一段时间后变小了
C.镁带燃烧后生成的固体质量增加
D.高锰酸钾受热,其固体的总质量逐渐减小
2.小华在一次探究实验中将一小粒金属钠投入盛有蒸水的烧杯中,发现反应剧烈并生成大量气体,则该气体可能是 ( )
A. H2 B.CH4 C. He D. NH3
3.如图所示,2个甲分子反应生成1个丙分子和3个乙分子。下列判断错误的是 ( )
A.该反应的基本反应类型为分解反应
B.该化学反应中原子的种类发生了改变
C.根据质量守恒定律可推知,1个乙分子中含有2个A原子
D.参加反应的甲物质属于化合物
4.煤油中含有噻吩,噻吩(用X表示)有令人不愉快的气味,其燃烧的化学方程式可表示为
X + 6O24CO2 + SO2 + 2H2O,则X的化学式为 ( )
A.CH4S B.C2H6S C.C4H4S D.C6H6S
5.已知化学方程式X + 2O2CO2 + 2H2O,下列对X的判断正确的是( )
A.X中一定含碳、氢元素,可能含氧元素
B.X中一定含碳、氢、氧三种元素
C.X中碳、氢元素的质量比为1:4
D.X的化学式是CH4
6.煤的气化是提高煤的利用率、减少环境污染的有效措施。煤的气化过程中发生了化学反应
C + H2O(气) H2 + CO,反应前后,发生了变化的是( )
A.元素的种类 B.碳、氢元素的化合价
C.原子的数目 D.物质的总质量
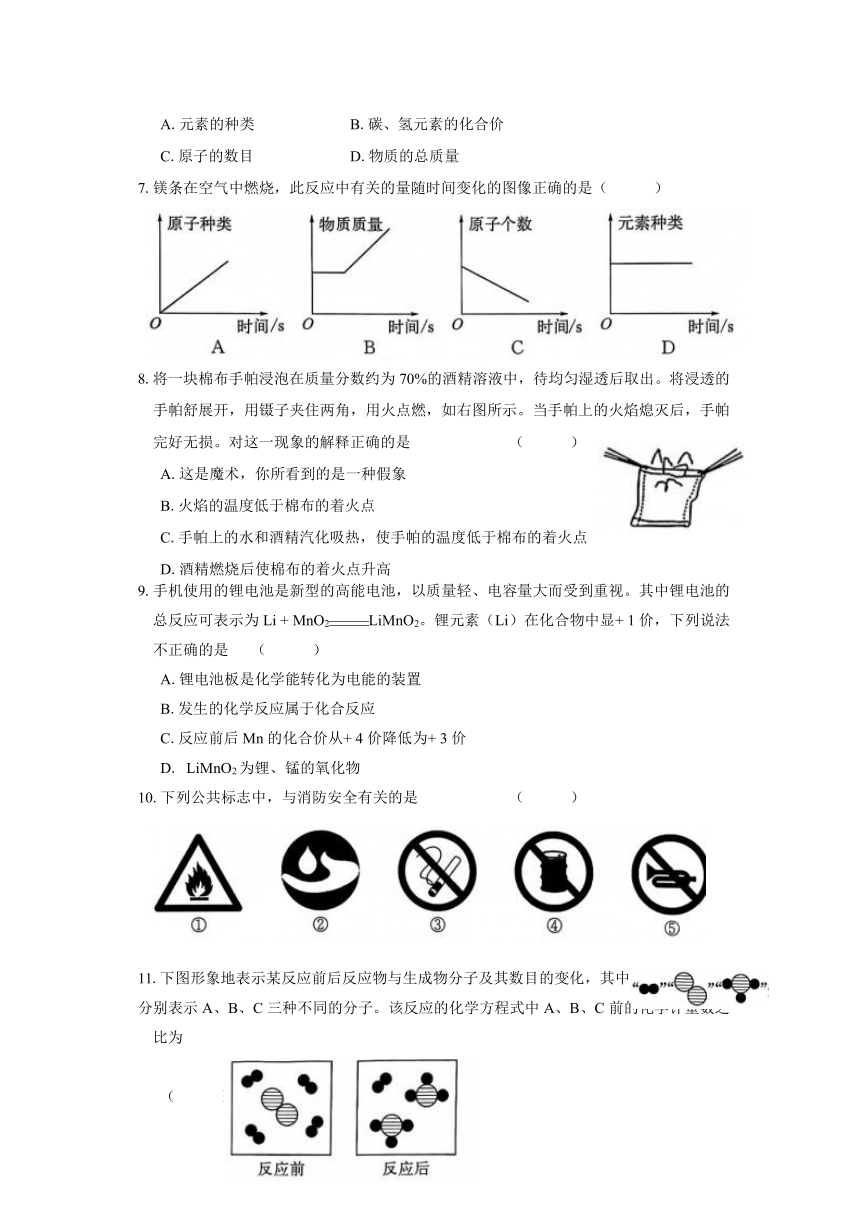
7.镁条在空气中燃烧,此反应中有关的量随时间变化的图像正确的是( )
8.将一块棉布手帕浸泡在质量分数约为70%的酒精溶液中,待均匀湿透后取出。将浸透的手帕舒展开,用镊子夹住两角,用火点燃,如右图所示。当手帕上的火焰熄灭后,手帕完好无损。对这一现象的解释正确的是 ( )
A.这是魔术,你所看到的是一种假象
B.火焰的温度低于棉布的着火点
C.手帕上的水和酒精汽化吸热,使手帕的温度低于棉布的着火点
D.酒精燃烧后使棉布的着火点升高
9.手机使用的锂电池是新型的高能电池,以质量轻、电容量大而受到重视。其中锂电池的总反应可表示为Li + MnO2LiMnO2。锂元素(Li)在化合物中显+ 1价,下列说法不正确的是 ( )
A.锂电池板是化学能转化为电能的装置
B.发生的化学反应属于化合反应
C.反应前后Mn的化合价从+ 4价降低为+ 3价
D. LiMnO2为锂、锰的氧化物
10.下列公共标志中,与消防安全有关的是 ( )
A.①②③④⑤ B.②③④ C.③④⑤ D.①③④
11.下图形象地表示某反应前后反应物与生成物分子及其数目的变化,其中
分别表示A、B、C三种不同的分子。该反应的化学方程式中A、B、C前的化学计量数之比为
( )
A.4:1:3 B.3:1:2 C.4:1:2 D.3:1:3
12.下列有关化学方程式2CO + O22CO2的叙述错误的是( )
A.一氧化碳和氧气在点燃条件下反应生成二氧化碳
B.每2个一氧化碳分子与1个氧分子在点燃条件下结合成2个二氧化碳分子
C.每2份质量的一氧化碳和1份质量的氧气通过点燃生成2份质量的二氧化碳
D.每56份质量的一氧化碳与32份质量的氧气在点燃条件下反应生成88份质量的二氧化碳
13.一定质量的某化合物完全燃烧,需要3.2 g氧气,生成4.4 g二氧化碳和1.8 g水。下列判断错误的是 ( )
A.该化合物的质量为3.0 g
B.该化合物一定含有碳、氢、氧三种元素
C.该化合物中碳、氢、氧的原子个数比为2:4:1
D.该化合物中碳元素的质量分数是40%
4.铝在氧气中燃烧生成氧化铝,在这个反应中,铝、氧气、氧化铝的质量比为( )
A.27:32:102 B.27:24:13
C.4:3:2 D.108:96:204
15.下列关于化学反应X2 + 3Y22Z的叙述错误的是 ( )
A.Z的化学式为XY3
B.若mgX2和ngY2恰好完全反应,则生成Z的质量一定是(m + n)g
C.若X2和Y2的相对分子质量分别为M和N,则Z的相对分子质量为(M + N)
D.若a g X2完全反应生成b g Z,则同时消耗(b - a)gY2
16.下列区别CO和CO2的最好方法是 ( )
A.用动物试验它们的毒性 B.看其能否使带火星的木条复燃
C.通入澄清石灰水中 D.观察它们在水中的溶解性
17.类推是化学学习中常用的方法。下列的类推结果正确的是 ( )
A.氧化物都含有氧元素,但含有氧元素的化合物不一定是氧化物
B.火药爆炸是化学变化,所以爆炸一定是化学变化
C.燃烧一般都伴随发光、放热现象,所以有发光、放热现象的一定是燃烧
D.煤、石油、天然气等化石燃料的使用会对环境造成污染,所以应禁止使用化石燃料
18.下列叙述中正确的是 ( )
A.因为“质量守恒”,所以镁带完全燃烧后生成白色固体的质量一定等于镁带的质量
B.铁丝在氧气中完全燃烧后,生成物比铁丝质量增加了
C.大理石和稀盐酸反应后剩余物的总质量小于反应前混合物的总质量,不符合质量守
恒定律
D.水蒸发变成水蒸气的质量等于水的质量,符合质量守恒定律
19.加热63.2g KMnO4,当得到6 g氧气时,剩余固体的成分是 ( )
A.K2MnO4 和 MnO2 B.KMnO4和K2MnO4
C.KMnO4、K2MnO4和MnO2 D.KMnO4和MnO2
20.三种物质在密闭容器中发生反应,反应前后质量比例的变化关系如图所示,下列说法正确的是 ( )
A.反应中CaO为催化剂
B.该反应是分解反应
C.反应后容器中固体质量增加
D.反应后容器中氧元素质量分数增大
二、非选择题(共60分)
21.(10分)完成下列化学实验中相关变化的化学方程式,并按要求填空。
(1)碳在氧气中不完全燃烧: ,该反应属于(选填“放热”或“吸热”)反应。
(2)加热高锰酸钾制取氧气: ,其基本反应类型是 _________ 。
(3)镁条在氧气中燃烧: ,该反应的现象是 。
(4)实验室制备二氧化碳气体: ,检验二氧化碳气体的试剂是 。
(5)电解水: ,与电源正、负极相连的玻璃管内生成气体的体积之比约为 。
22.(4分)一定质量的某物质在空气中完全燃烧后,生成8.8 g二氧化碳和5.4 g水,在①CH4、②C2H2、③C2H6、④C2H5OH四种物质中符合上述条件的是 _________ (填序号)。写出所选物质燃烧的化学方程式: 。
23.(6分)把4 g硫粉放在给定质量的氧气中燃烧,有关实验数据如下表所示。
请回答下列问题。
第一次 第二次 第三次
O2质量/g 3 4 6
SO2质量/g 6
(1)第一次实验中,参加反应的S的质量、O2的质量与生成的SO2的质量比是 _________ 。
(2)请你通过计算求出第二次实验生成二氧化硫的质量为 _________ ;第三次实验生成二氧化硫的质量为 _________ 。
24.(6分)构建和谐社会,建设社会主义新农村的目标之一是让农民饮用清洁的自来水。ClO2是新一代饮用水的消毒剂,我国成功研制出制取ClO2的新方法,其反应的微观示意图如下图所示。
试回答:
(1)ClO2叫作 _________ ,其中氯元素的化合价为 _________ 。
(2)根据反应的微观示意图写出反应的化学方程式: _________ 。
(3)制取13.5g ClO2至少需要NaClO2质量为 _________ 。
25.(4分)高级汽车中常配置有一种汽车安全气囊,内部储存有硝酸铵。当汽车高速行驶中受到猛烈撞击时,硝酸铵迅速分解产生大量一氧化二氮(N2O)气体和另一种氧化物充满气袋,填补在乘员与挡风玻璃、方向盘之间,防止乘员受伤。
(1)硝酸铵受撞击发生分解反应的化学方程式是 _________ 。
(2)此反应中反应物和生成物中氮元素的化合价从左到右依次为 _________ 。
26.(4分)为测定空气中氧气所占的体积分数,某同学设计了如右
图所示实验。在一个耐热活塞的底部放一小块白磷(足量),然
后迅速将活塞下压,可以观察到的现象为 _________ ;冷却至原
来温度时,慢慢松开手,活塞最终将回到刻度 _________ 处,白
磷燃烧的原因是 _________ 。
27.(9分)探究化学反应前后,反应物与生成物之间的质量关系,三位同学分别做了这样三个实验:
实验一:称量镁条,点燃,待反应结束后再称量。
实验二:将装有稀盐酸的小试管放入装有锌粒的烧杯中称量,然后使盐酸与锌粒接触,过一会儿再称量。
实验三:将装有氢氧化钠溶液的试管放入盛有硫酸铜溶液的烧杯中,称量,然后设法使两种溶液接触,过一会儿再称量。数据见下表[锌与盐酸反应的化学方程式为Zn + 2HCl ZnCl2 + H2↑;氢氧化钠溶液与硫酸铜溶液混合反应的化学方程式为2NaOH + CuSO4 Na2SO4 + Cu(OH)2↓]。
(1)从表面上看,这三个实验过程中,反应后的剩余物质的质量变化是实验一 _________ ,实验二 _________ ,实验三 _________ 。(均选填“减小”“增大”或“不变”)
(2)这三个实验中,实验 _________ 正确地反映了反应物与生成物之间的质量关系。造成其他两个实验结果错误的原因分别是 。
(3)从不能正确反映反应物和生成物之间质量关系的实验中,选一例提出改进思路: 。
(4)由此可以得出,探究有气体参加或生成的化学反应前后反应物与生成物质量关系的实验,必须在 体系中进行。
28.(7分)硼及其化合物在现代工农业、医学、国防中有着重要的应用价值。利用硼镁矿可制备硼,工艺流程如图所示。请回答下列问题。
(1)B2O3中B元素的化合价为 _________ 。
(2)为加快硼镁矿石与浓NaOH溶液的反应速率,可采取的措施是 。
(3)已知H3BO3加热分解只生成两种氧化物,则流程②的化学反应方程式为 。
(4)根据流程③的化学反应方程式:B2O3 + 3Mg2B + 3MgO,理论上制备1.1 t的硼,需消耗镁多少吨(写出计算过程)
29.(10分)小强同学前往当地的石灰石矿区进行调查,他取回了若干块矿石样品,对样品中碳酸钙的质量分数进行检测,采用了以下方法:取8 g石灰石样品,将40 g稀盐酸分四次加入,测量过程所得数据见下表(已知石灰石样品中含有的杂质不溶于水,不与盐酸反应)。请计算:
(1)表格中m的值为 _________ 。
(2)样品中碳酸钙的质量分数是 _________ 。
(3)实验结束一共生成二氧化碳的质量是 _________ g。
1
(满分:100分 时间:45分钟)
可能用到的相对原子质量:H-1 B-11 O-16 Mg-24 Al-27 P-31 Mn-55
一、选择题(每小题只有一个正确答案。每小题2分,共40分)
1.不适宜用质量守恒定律解释的现象是 ( )
A.煤炭燃烧后变成煤灰,质量变小了
B.樟脑球放在衣柜中一段时间后变小了
C.镁带燃烧后生成的固体质量增加
D.高锰酸钾受热,其固体的总质量逐渐减小
2.小华在一次探究实验中将一小粒金属钠投入盛有蒸水的烧杯中,发现反应剧烈并生成大量气体,则该气体可能是 ( )
A. H2 B.CH4 C. He D. NH3
3.如图所示,2个甲分子反应生成1个丙分子和3个乙分子。下列判断错误的是 ( )
A.该反应的基本反应类型为分解反应
B.该化学反应中原子的种类发生了改变
C.根据质量守恒定律可推知,1个乙分子中含有2个A原子
D.参加反应的甲物质属于化合物
4.煤油中含有噻吩,噻吩(用X表示)有令人不愉快的气味,其燃烧的化学方程式可表示为
X + 6O24CO2 + SO2 + 2H2O,则X的化学式为 ( )
A.CH4S B.C2H6S C.C4H4S D.C6H6S
5.已知化学方程式X + 2O2CO2 + 2H2O,下列对X的判断正确的是( )
A.X中一定含碳、氢元素,可能含氧元素
B.X中一定含碳、氢、氧三种元素
C.X中碳、氢元素的质量比为1:4
D.X的化学式是CH4
6.煤的气化是提高煤的利用率、减少环境污染的有效措施。煤的气化过程中发生了化学反应
C + H2O(气) H2 + CO,反应前后,发生了变化的是( )
A.元素的种类 B.碳、氢元素的化合价
C.原子的数目 D.物质的总质量
7.镁条在空气中燃烧,此反应中有关的量随时间变化的图像正确的是( )
8.将一块棉布手帕浸泡在质量分数约为70%的酒精溶液中,待均匀湿透后取出。将浸透的手帕舒展开,用镊子夹住两角,用火点燃,如右图所示。当手帕上的火焰熄灭后,手帕完好无损。对这一现象的解释正确的是 ( )
A.这是魔术,你所看到的是一种假象
B.火焰的温度低于棉布的着火点
C.手帕上的水和酒精汽化吸热,使手帕的温度低于棉布的着火点
D.酒精燃烧后使棉布的着火点升高
9.手机使用的锂电池是新型的高能电池,以质量轻、电容量大而受到重视。其中锂电池的总反应可表示为Li + MnO2LiMnO2。锂元素(Li)在化合物中显+ 1价,下列说法不正确的是 ( )
A.锂电池板是化学能转化为电能的装置
B.发生的化学反应属于化合反应
C.反应前后Mn的化合价从+ 4价降低为+ 3价
D. LiMnO2为锂、锰的氧化物
10.下列公共标志中,与消防安全有关的是 ( )
A.①②③④⑤ B.②③④ C.③④⑤ D.①③④
11.下图形象地表示某反应前后反应物与生成物分子及其数目的变化,其中
分别表示A、B、C三种不同的分子。该反应的化学方程式中A、B、C前的化学计量数之比为
( )
A.4:1:3 B.3:1:2 C.4:1:2 D.3:1:3
12.下列有关化学方程式2CO + O22CO2的叙述错误的是( )
A.一氧化碳和氧气在点燃条件下反应生成二氧化碳
B.每2个一氧化碳分子与1个氧分子在点燃条件下结合成2个二氧化碳分子
C.每2份质量的一氧化碳和1份质量的氧气通过点燃生成2份质量的二氧化碳
D.每56份质量的一氧化碳与32份质量的氧气在点燃条件下反应生成88份质量的二氧化碳
13.一定质量的某化合物完全燃烧,需要3.2 g氧气,生成4.4 g二氧化碳和1.8 g水。下列判断错误的是 ( )
A.该化合物的质量为3.0 g
B.该化合物一定含有碳、氢、氧三种元素
C.该化合物中碳、氢、氧的原子个数比为2:4:1
D.该化合物中碳元素的质量分数是40%
4.铝在氧气中燃烧生成氧化铝,在这个反应中,铝、氧气、氧化铝的质量比为( )
A.27:32:102 B.27:24:13
C.4:3:2 D.108:96:204
15.下列关于化学反应X2 + 3Y22Z的叙述错误的是 ( )
A.Z的化学式为XY3
B.若mgX2和ngY2恰好完全反应,则生成Z的质量一定是(m + n)g
C.若X2和Y2的相对分子质量分别为M和N,则Z的相对分子质量为(M + N)
D.若a g X2完全反应生成b g Z,则同时消耗(b - a)gY2
16.下列区别CO和CO2的最好方法是 ( )
A.用动物试验它们的毒性 B.看其能否使带火星的木条复燃
C.通入澄清石灰水中 D.观察它们在水中的溶解性
17.类推是化学学习中常用的方法。下列的类推结果正确的是 ( )
A.氧化物都含有氧元素,但含有氧元素的化合物不一定是氧化物
B.火药爆炸是化学变化,所以爆炸一定是化学变化
C.燃烧一般都伴随发光、放热现象,所以有发光、放热现象的一定是燃烧
D.煤、石油、天然气等化石燃料的使用会对环境造成污染,所以应禁止使用化石燃料
18.下列叙述中正确的是 ( )
A.因为“质量守恒”,所以镁带完全燃烧后生成白色固体的质量一定等于镁带的质量
B.铁丝在氧气中完全燃烧后,生成物比铁丝质量增加了
C.大理石和稀盐酸反应后剩余物的总质量小于反应前混合物的总质量,不符合质量守
恒定律
D.水蒸发变成水蒸气的质量等于水的质量,符合质量守恒定律
19.加热63.2g KMnO4,当得到6 g氧气时,剩余固体的成分是 ( )
A.K2MnO4 和 MnO2 B.KMnO4和K2MnO4
C.KMnO4、K2MnO4和MnO2 D.KMnO4和MnO2
20.三种物质在密闭容器中发生反应,反应前后质量比例的变化关系如图所示,下列说法正确的是 ( )
A.反应中CaO为催化剂
B.该反应是分解反应
C.反应后容器中固体质量增加
D.反应后容器中氧元素质量分数增大
二、非选择题(共60分)
21.(10分)完成下列化学实验中相关变化的化学方程式,并按要求填空。
(1)碳在氧气中不完全燃烧: ,该反应属于(选填“放热”或“吸热”)反应。
(2)加热高锰酸钾制取氧气: ,其基本反应类型是 _________ 。
(3)镁条在氧气中燃烧: ,该反应的现象是 。
(4)实验室制备二氧化碳气体: ,检验二氧化碳气体的试剂是 。
(5)电解水: ,与电源正、负极相连的玻璃管内生成气体的体积之比约为 。
22.(4分)一定质量的某物质在空气中完全燃烧后,生成8.8 g二氧化碳和5.4 g水,在①CH4、②C2H2、③C2H6、④C2H5OH四种物质中符合上述条件的是 _________ (填序号)。写出所选物质燃烧的化学方程式: 。
23.(6分)把4 g硫粉放在给定质量的氧气中燃烧,有关实验数据如下表所示。
请回答下列问题。
第一次 第二次 第三次
O2质量/g 3 4 6
SO2质量/g 6
(1)第一次实验中,参加反应的S的质量、O2的质量与生成的SO2的质量比是 _________ 。
(2)请你通过计算求出第二次实验生成二氧化硫的质量为 _________ ;第三次实验生成二氧化硫的质量为 _________ 。
24.(6分)构建和谐社会,建设社会主义新农村的目标之一是让农民饮用清洁的自来水。ClO2是新一代饮用水的消毒剂,我国成功研制出制取ClO2的新方法,其反应的微观示意图如下图所示。
试回答:
(1)ClO2叫作 _________ ,其中氯元素的化合价为 _________ 。
(2)根据反应的微观示意图写出反应的化学方程式: _________ 。
(3)制取13.5g ClO2至少需要NaClO2质量为 _________ 。
25.(4分)高级汽车中常配置有一种汽车安全气囊,内部储存有硝酸铵。当汽车高速行驶中受到猛烈撞击时,硝酸铵迅速分解产生大量一氧化二氮(N2O)气体和另一种氧化物充满气袋,填补在乘员与挡风玻璃、方向盘之间,防止乘员受伤。
(1)硝酸铵受撞击发生分解反应的化学方程式是 _________ 。
(2)此反应中反应物和生成物中氮元素的化合价从左到右依次为 _________ 。
26.(4分)为测定空气中氧气所占的体积分数,某同学设计了如右
图所示实验。在一个耐热活塞的底部放一小块白磷(足量),然
后迅速将活塞下压,可以观察到的现象为 _________ ;冷却至原
来温度时,慢慢松开手,活塞最终将回到刻度 _________ 处,白
磷燃烧的原因是 _________ 。
27.(9分)探究化学反应前后,反应物与生成物之间的质量关系,三位同学分别做了这样三个实验:
实验一:称量镁条,点燃,待反应结束后再称量。
实验二:将装有稀盐酸的小试管放入装有锌粒的烧杯中称量,然后使盐酸与锌粒接触,过一会儿再称量。
实验三:将装有氢氧化钠溶液的试管放入盛有硫酸铜溶液的烧杯中,称量,然后设法使两种溶液接触,过一会儿再称量。数据见下表[锌与盐酸反应的化学方程式为Zn + 2HCl ZnCl2 + H2↑;氢氧化钠溶液与硫酸铜溶液混合反应的化学方程式为2NaOH + CuSO4 Na2SO4 + Cu(OH)2↓]。
(1)从表面上看,这三个实验过程中,反应后的剩余物质的质量变化是实验一 _________ ,实验二 _________ ,实验三 _________ 。(均选填“减小”“增大”或“不变”)
(2)这三个实验中,实验 _________ 正确地反映了反应物与生成物之间的质量关系。造成其他两个实验结果错误的原因分别是 。
(3)从不能正确反映反应物和生成物之间质量关系的实验中,选一例提出改进思路: 。
(4)由此可以得出,探究有气体参加或生成的化学反应前后反应物与生成物质量关系的实验,必须在 体系中进行。
28.(7分)硼及其化合物在现代工农业、医学、国防中有着重要的应用价值。利用硼镁矿可制备硼,工艺流程如图所示。请回答下列问题。
(1)B2O3中B元素的化合价为 _________ 。
(2)为加快硼镁矿石与浓NaOH溶液的反应速率,可采取的措施是 。
(3)已知H3BO3加热分解只生成两种氧化物,则流程②的化学反应方程式为 。
(4)根据流程③的化学反应方程式:B2O3 + 3Mg2B + 3MgO,理论上制备1.1 t的硼,需消耗镁多少吨(写出计算过程)
29.(10分)小强同学前往当地的石灰石矿区进行调查,他取回了若干块矿石样品,对样品中碳酸钙的质量分数进行检测,采用了以下方法:取8 g石灰石样品,将40 g稀盐酸分四次加入,测量过程所得数据见下表(已知石灰石样品中含有的杂质不溶于水,不与盐酸反应)。请计算:
(1)表格中m的值为 _________ 。
(2)样品中碳酸钙的质量分数是 _________ 。
(3)实验结束一共生成二氧化碳的质量是 _________ g。
1
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
