课题3 制取氧气
图片预览






文档简介
(共16张PPT)
课题3 制取氧气
石家庄外国语学校初二化学组 何晓丽
项目目标:
2.认识催化剂及催化作用。
1.了解实验室制取氧气的主要方法和原理。
3.自主探究二氧化锰是过氧化氢分解的
催化剂
我们如何得到氧气呢?
集思广益
比一比
哪个小组办法多
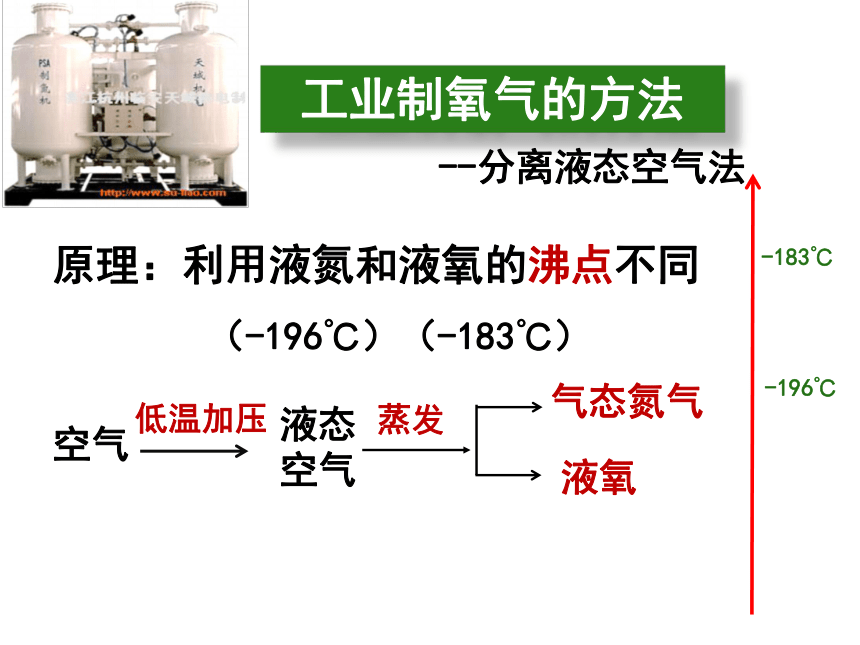
--分离液态空气法
低温加压
蒸发
气态氮气
液氧
-196℃
-183℃
空气
液态空气
工业制氧气的方法
原理:利用液氮和液氧的沸点不同
(-196℃)(-183℃)
实验室制取氧气的方法
1、分解过氧化氢溶液;
2、加热氯酸钾固体;
3、加热高锰酸钾固体。
分解过氧化氢溶液
预习检测
1.药品:
2.反应原理:
过氧化氢 水+氧气
二氧化锰
过氧化氢 二氧化锰
MnO2
H2O2 H2O+O2
在化学反应里能改变其他物质的化学反应速率,而本身质量和化学性质在化学反应前后都没有发生变化的物质。(又叫触媒)
一变:改变其他物质的化学反应速率
二不变:本身质量和化学性质不变
2.催化剂的特点:
1.催化剂:
请你根据催化剂的特点设计实验
探究二氧化锰是过氧化氢溶液分解的催化剂
小组讨论:
改变 ≠加快
交流展示环节
每个小组选一名代表,简述实验设计方案
探究方案设计
要求:
组长做好分工,注意组内音。
3、5号同学作好记录。
3.注意节约药品
步骤一:在常温下,把带火星的木条伸入盛有过氧化氢溶液的试管中,观察木条是否复燃。
实验 现象 结论
1
2
带火星的木条不复燃
常温下,过氧化氢溶液放出氧气量少
产生大量气泡,带火星的木条复燃
常温下二氧化锰加快了过氧化氢产生氧气的速率
步骤二:向上述试管中,加入少量二氧化锰,再将带火星的木条伸入试管中,观察发生的现象。
探究方案设计
说明二氧化锰可重复使用,在反应前后它的化学性质没有改变。
现象 结论
木条复燃了
步骤三:反应停止后,重新加入过氧化氢溶液,把带火星的木条伸入试管。观察发生的现象。
二氧化锰仍然起作用
不能。催化剂改变的是反应速率,与生成物
质量无关。
能,催化剂不能控制反应的发生或停止
不对,催化剂是针对具体反应而言的,具有选择性。并且二氧化锰并不是在任何情况下都是催化剂。
思考
1.催化剂是否可以使生成物质量增加呢?
2.没有催化剂反应能否进行呢?
3.二氧化锰就是催化剂,这种说法对吗?
4、催化剂的性质在化学反应前后保持不变,对吗?
不对,物理性质有可能改变。
5.是否可用其它物质代替二氧化锰作为过氧化氢分解的催化剂?
可以,比如硫酸铜,土豆片等。
试试看!验证一下土豆片的催化效果吧
1.下列物质中含有氧气的是( )
A.二氧化锰 B.过氧化氢 C.空气 D.氧化镁
2.有关催化剂的说法正确的是( )
A.在化学反应前后其质量减少了
B.催化剂可以重复使用
C.反应前后催化剂的性质没有发生变化
D.任何反应都需要加催化剂
C
B
巩固练习
感受成功
学完本课你收获了什么
完成项目书32页巩固练习
(除2、8、9题)
作业来啦!
小知识:
食用油里加入0.01%~0.02%的没食子酸正丙脂可以减慢油脂与氧气的化学反应速率,有效的防止酸败。
课题3 制取氧气
石家庄外国语学校初二化学组 何晓丽
项目目标:
2.认识催化剂及催化作用。
1.了解实验室制取氧气的主要方法和原理。
3.自主探究二氧化锰是过氧化氢分解的
催化剂
我们如何得到氧气呢?
集思广益
比一比
哪个小组办法多
--分离液态空气法
低温加压
蒸发
气态氮气
液氧
-196℃
-183℃
空气
液态空气
工业制氧气的方法
原理:利用液氮和液氧的沸点不同
(-196℃)(-183℃)
实验室制取氧气的方法
1、分解过氧化氢溶液;
2、加热氯酸钾固体;
3、加热高锰酸钾固体。
分解过氧化氢溶液
预习检测
1.药品:
2.反应原理:
过氧化氢 水+氧气
二氧化锰
过氧化氢 二氧化锰
MnO2
H2O2 H2O+O2
在化学反应里能改变其他物质的化学反应速率,而本身质量和化学性质在化学反应前后都没有发生变化的物质。(又叫触媒)
一变:改变其他物质的化学反应速率
二不变:本身质量和化学性质不变
2.催化剂的特点:
1.催化剂:
请你根据催化剂的特点设计实验
探究二氧化锰是过氧化氢溶液分解的催化剂
小组讨论:
改变 ≠加快
交流展示环节
每个小组选一名代表,简述实验设计方案
探究方案设计
要求:
组长做好分工,注意组内音。
3、5号同学作好记录。
3.注意节约药品
步骤一:在常温下,把带火星的木条伸入盛有过氧化氢溶液的试管中,观察木条是否复燃。
实验 现象 结论
1
2
带火星的木条不复燃
常温下,过氧化氢溶液放出氧气量少
产生大量气泡,带火星的木条复燃
常温下二氧化锰加快了过氧化氢产生氧气的速率
步骤二:向上述试管中,加入少量二氧化锰,再将带火星的木条伸入试管中,观察发生的现象。
探究方案设计
说明二氧化锰可重复使用,在反应前后它的化学性质没有改变。
现象 结论
木条复燃了
步骤三:反应停止后,重新加入过氧化氢溶液,把带火星的木条伸入试管。观察发生的现象。
二氧化锰仍然起作用
不能。催化剂改变的是反应速率,与生成物
质量无关。
能,催化剂不能控制反应的发生或停止
不对,催化剂是针对具体反应而言的,具有选择性。并且二氧化锰并不是在任何情况下都是催化剂。
思考
1.催化剂是否可以使生成物质量增加呢?
2.没有催化剂反应能否进行呢?
3.二氧化锰就是催化剂,这种说法对吗?
4、催化剂的性质在化学反应前后保持不变,对吗?
不对,物理性质有可能改变。
5.是否可用其它物质代替二氧化锰作为过氧化氢分解的催化剂?
可以,比如硫酸铜,土豆片等。
试试看!验证一下土豆片的催化效果吧
1.下列物质中含有氧气的是( )
A.二氧化锰 B.过氧化氢 C.空气 D.氧化镁
2.有关催化剂的说法正确的是( )
A.在化学反应前后其质量减少了
B.催化剂可以重复使用
C.反应前后催化剂的性质没有发生变化
D.任何反应都需要加催化剂
C
B
巩固练习
感受成功
学完本课你收获了什么
完成项目书32页巩固练习
(除2、8、9题)
作业来啦!
小知识:
食用油里加入0.01%~0.02%的没食子酸正丙脂可以减慢油脂与氧气的化学反应速率,有效的防止酸败。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
